血清25-羟基维生素D、胱抑素C与脑白质疏松严重程度的相关性研究
李 博,张 琰,雷 娜, 文微微
脑白质疏松(Leukoaraiosis,LA)即皮质下或脑室周围的脑白质出现斑片状、斑点状改变,主要病变表现为神经系统发生脱髓鞘改变。LA是导致老年人自理能力降低的重要因素,且与卒中发病密切相关[1]。有学者发现,LA可致患者出现抑郁、焦虑等情绪[2]。该病发病机制复杂,临床认为可能与炎症、饮酒、动脉粥样硬化等存在关联[3]。近年来,研究提示,肾功能受损可能与LA病变有关[4]。胱抑素C(Cys-C)在评估肾功能中应用广泛,它被证实是脑血管病发生的危险因素,其异常变化可能促进、加重脑血管病变[5]。此外,维生素D可保护血管内皮细胞,对血管平滑肌增殖存在抑制作用。25-羟基维生素D[25(OH)D]可反映机体维生素D水平的变化,在炎症介导影响下,可致维生素D含量下降,削弱其对内皮细胞的保护作用,引起LA病变[6]。LA病变严重度对其预后影响非常大,本研究主要观察血清25(OH)D与Cys-C是否与LA病变程度存在关联,为该病治疗提供依据,报道如下。
1 资料与方法
1.1 一般资料 纳入我院2018年2月-2020年2月收治的LA患者130例,根据患者的LA严重度,分成轻度组(n=43)、中度组(n=45)以及重度组(n=42)。纳入同期于我院体检的健康体检者40例作为对照组。LA严重度评价[7]:参考Fazekas标准进行评估,脑白质表现为局灶性受损为轻度,计1分;早期融合性病灶为中度,计2分;弥漫性融合性病灶为重度,计3分。研究方案获伦理委员会批准,4组基线资料比较无差异(P>0.05)(见表1)。
1.2 纳入与排除标准
1.2.1 纳入标准 (1)LA患者:①行头部MRI、CT检查,提示存在LA病变;②皮质下或脑室周围的脑白质出现斑片状、斑点状改变,病灶直径≥5 mm;③意识清醒,具备一定认知功能;④签署知情同意书。(2)对照组:①性别、年龄等基线资料与LA患者匹配;②经体检提示身体健康状况良好;③签署知情同意书。
1.2.2 排除标准 (1)患佝偻病、甲状腺异常等代谢性疾病;(2)患重症肌无力、红斑狼疮等自身免疫性疾病;(3)近期有钙剂、维生素制剂应用史;(4)患脑梗死等其他神经系统病;(5)重度感染;(6)患恶性肿瘤;(7)心、肺等脏器严重受损;(8)既往有精神病史。
1.3 方法 所有纳入者在就诊或体检当日,采集3 ml空腹静脉血,在受检者空腹状态操作,行离心处理,时间为15 min,转速为3500 r/min,分离血清,存放于低温冰箱等待测定,离心半径=10 cm。经酶联免疫吸附法测定血清25(OH)D水平,试剂盒购自上海江莱生物科技有限公司。经免疫比浊法检测血清Cys-C水平,试剂盒由赛默飞世尔公司提供。比较4组受检者的血清25(OH)D、Cys-C水平,分析二者间的相关性。经蒙特利尔认知评价量表(MoCA)评价LA患者的认知功能,分析血清25(OH)D、Cys-C与MoCA评分的相关性以及血清25(OH)D、Cys-C与LA严重程度的相关性。MoCA量表评分[8]:包括延迟回忆、语言、视空间与执行力、定向力、抽象思维、注意力、命名7个项目,共计30分。若总分<26分,则提示存在认知障碍;≥26分提示无认知障碍。如果受检者受教育时间不超过12 y,则总分需加1分,校正偏倚。
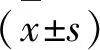
2 结 果
2.1 4组血清25(OH)D、Cys-C水平比较 轻度、中度、重度组的血清25(OH)D均低于对照组,且重度组低于中度、轻度组;中度组低于轻度组(P<0.05)。轻度、中度、重度组的血清Cys-C均高于对照组,且重度组高于中度、轻度组;中度组高于轻度组(P<0.05)(见表2)。
2.2 LA患者血清25(OH)D与Cys-C的相关性 在130例LA患者中,平均血清25(OH)D为(50.93±19.76)nmol/L,平均血清Cys-C为(1.58±0.56)mg/L。经Pearson线性相关分析提示,血清25(OH)D与Cys-C呈负相关(r=-0.767,P<0.05)。
2.3 血清25(OH)D、Cys-C与MoCA评分的相关性 在130例患者中,平均MoCA评分为(26.92±4.34)分。经Pearson线性相关分析提示,血清25(OH)D与MoCA评分呈正相关(r=0.588,P<0.05),血清Cys-C与MoCA评分呈负相关(r=-0.694,P<0.05)。
2.4 血清25(OH)D、Cys-C对LA加重的评估价值 将中、重度患者视为LA加重,平均血清25(OH)D、Cys-C分别为(45.32±3.04)nmol/L、(1.55±0.14)mg/L。血清25(OH)D、Cys-C评估LA加重的AUC分别为0.760(标准误=0.043,P<0.001,95%CI0.674~0.845,最佳界值=47.500 nmol/L,敏感度=75.50%,特异性=76.50%)、0.749(标准误=0.749,P<0.001,95%CI0.659~0.839,最佳界值=1.408 mg/L,敏感度=75.50%,特异性=72.00%)。ROC曲线(见图1、图2)。
2.5 LA加重的危险因素分析 以表3中各变量为自变量X,以LA是否加重作为因变量Y,经Logistic回归模型行量化赋值,其中两项血清指标以上述得出的最佳界值为界进行赋值。结果显示,血清Cys-C增高、血清25(OH)D减低是LA加重的危险因素(P<0.05)(见表3)。
2.6 血清25(OH)D、Cys-C与LA程度的相关性 利用Fazekas评分标准反映LA程度,与血清25(OH)D、Cys-C进行相关性分析。经Pearson线性相关分析提示,血清25(OH)D与LA病变程度呈负相关(r=-0.666,P<0.05),血清Cys-C与LA病变程度呈正相关(r=0.840,P<0.05)。

表1 4组基线资料比较

表2 4组血清25(OH)D、Cys-C水平比较

表3 LA加重的危险因素分析
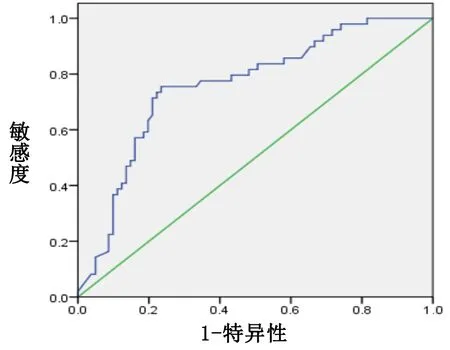
图1 血清25(OH)D评估LA加重的ROC曲线
图2 血清Cys-C评估LA加重的ROC曲线
3 讨 论
LA发病隐匿,其被认为与步态、认知障碍、卒中等存在关联,可导致痴呆发生风险增高,在脑白质缺血非常严重的情况下,可能引起抑郁、尿便障碍等表现,对其生活质量影响较大[9]。由于该病早期缺乏典型症状,为了尽早确诊,临床需寻求敏感性、特异性高的指标对其进行评估,了解LA发病与进展情况,为临床治疗提供依据。维生素D对钙磷代谢有调节作用,可对骨质代谢进行调节,此外,其还对内皮细胞生成存在抑制作用,能导致肾素-血管紧张素降低,从而对血管病变状态产生影响[10]。Cys-C在正常生理状态下非常稳定,炎症也不易对其产生影响。目前,有研究发现,Cys-C与动脉粥样硬化存在关联,且参与了脑血管病变[11]。
本次结果显示,与健康者相比,LA患者的血清Cys-C均增高,而血清25(OH)D均下降,且随着患者LA程度越重,血清Cys-C水平越高,25(OH)D水平越低。25(OH)D能促进内皮细胞功能改善,其能反映维生素D含量的变化,当机体内维生素D水平低下时,可增加内皮细胞功能受损风险,为脑小血管病的发生提供条件,导致LA发病风险增加[12]。Cys-C被证实可导致血管壁受损,一旦其表达失衡,则会诱发或加重动脉粥样硬化,从而促进LA发生[13]。LA患者血脑屏障受损,导致脑脊液内Cys-C释放入血,上调血清Cys-C水平。而血清Cys-C越高,越可能将凝血级联反应激活,致小血管受损,增加血脑屏障损害程度,形成恶性循环,最终致LA进展加速。因此,血清Cys-C增高与25(OH)D的缺失能增加LA发生与进展风险。
本研究显示,血清25(OH)D与Cys-C为负相关,表明随着25(OH)D含量越低,Cys-C含量越高。血清25(OH)D对炎症通路有阻断作用,且能对淋巴细胞增殖进行有效抑制,促使炎症因子生成减少,降低脑损伤程度[14]。当25(OH)D含量下降后,促炎因子含量上调,导致血管内皮受损,血脑屏障完整性则被破坏。而Cys-C在血清中的表达上调,也会导致血脑屏障受损,或加重局部组织受损程度[15]。基于上述机制,可推测在血清25(OH)D降低与Cys-C增高的共同作用下,导致患者血脑屏障进一步受到破坏,使血浆内大分子物质到达脑组织,诱发脑血管病变,致LA进展风险增加。
认知功能损害在LA患者中常见,其机制在于LA可将与认知功能相关的神经纤维联络途径阻断[16]。本研究利用MoCA评分对患者认知功能进行评价,该量表可靠性高,结果显示血清25(OH)D与其呈正相关,血清Cys-C与之呈负相关,即血清25(OH)D越高,认知功能越好,而血清Cys-C越高,患者认知功能越差。Cys-C增高可促进淀粉样斑块形成,为神经细胞变性、凋亡提供条件,这提示其表达含量的变化与认知障碍密切相关[17]。25(OH)D严重缺乏时,可增加脑血管病风险,对认知功能也有一定影响[18]。二者共同作用,在异常表达下能促进认知功能损害。
本结果显示,血清25(OH)D、Cys-C对LA加重具有良好的评估作用,AUC均超过0.70,且二者为LA加重的危险因素,进一步证实二者与LA病变程度存在关联。25(OH)D与Cys-C对内皮细胞的影响机制完全不同,前者可保护内皮细胞,而后者可导致内皮细胞受损。25(OH)D的低表达与Cys-C高表达能共同致内皮细胞损害,削弱大脑调节功能,破坏血脑屏障,导致LA进展。本研究最终证实,血清25(OH)D、Cys-C与LA程度有相关性,随着25(OH)D表达越低,Cys-C表达越高,LA病变程度越重。这主要的机制在于,Cys-C能引起炎症反应,且可促进血管变性,导致微小栓子生成,增加毒素释放量,致血脑屏障损害,反复循环导致LA进展[19]。而25(OH)D减低可削弱其对内皮细胞的保护功能,促进血脑屏障受损,也为了LA进展提供了条件[20]。二者相互影响,在共同作用下加重LA病变严重度。因此,临床可考虑针对这类患者补充维生素D,并给予药物治疗抑制Cys-C水平,改善病情。
综上,血清25(OH)D、Cys-C水平与LA进展密切相关,其中25(OH)D减低、Cys-C增高会促进LA加重,在这种情况下,二者相互作用,通过影响血脑屏障功能,致LA病变进一步进展。

