围手术期膈肌超声评估术后肌松残余的可行性
郎珈馨,易 杰
中国医学科学院 北京协和医学院 北京协和医院麻醉科,北京 100730
麻醉恢复期肌松残余可引起拔管后呼吸功能恢复不全、呼吸道梗阻、术后低氧甚至拔管后再次插管等问题,导致恢复室滞留时间延长,增加围手术期呼吸系统并发症[1]。在我国肌松残余的发生率较高[2]。肌松残余通常采用四个成串刺激(train of four ratio,TOFr)拇内收肌的运动比例进行判断[3]。TOFr<90%提示存在肌松残余。但由于目前国内肌松监测尚未能常规开展[2],对肌松残余的判断主要依靠临床经验,临床指标判断肌松残余灵敏度和特异性均较低。临床亟待寻找较为客观的指标作为判断肌松残余的辅助手段。近年来,超声在麻醉科的应用越来越广。文献报道超声测量膈肌厚度变化率和膈肌运动幅度与跨膈压相关,证实膈肌超声指标可反应膈肌肌力[4]。膈肌超声在重症医学科(intensive care unit,ICU)指导带管患者脱机拔管[5- 6]和评估神经肌肉病患者呼吸肌受累情况[7- 8]等方面均有应用,但在麻醉患者围手术期肌松恢复过程的研究较少[9],因此,本研究旨在运用膈肌超声评估全麻插管患者术后肌松残余的可行性,试图探索新的客观指标判断临床肌松残余。
对象和方法
对象本研究为前瞻性观察性临床研究,经研究单位伦理委员会批准(批准号:ZS- 1984)并与患者签订研究知情同意书。于2019年8至10月随机纳入北京协和医院拟行非胸腹部手术全麻插管的患者75例,美国麻醉医师协会分级 Ⅰ~Ⅱ级,年龄18~65岁,性别不限。排除标准为:(1)明确膈肌功能异常或神经肌肉疾病(重症肌无力、肌无力综合征、肌萎缩侧索硬化和格林巴利综合征等疾病);(2)存在胸廓畸形或既往胸腹部手术史;(3)术前肺功能检查异常;(4)肝肾功能不全;(5)有原因导致无法监测TOFr;(6)妊娠;(7)急诊手术;(8)参与其他临床试验等。
麻醉方法患者入手术室后开放静脉补液通路,常规监测无创血压、心率及脉搏氧饱和度。诱导采用丙泊酚(阿斯利康公司,进口药品注册证号:H20100646)1.5~2 mg/kg;芬太尼(宜昌人福药业有限责任公司,国药准字:H42022076)1~2 μg/kg,待患者意识消失,给予罗库溴铵(荷兰欧加农公司,进口药品注册证号:H20140847)0.6~0.9 mg/kg,2 min后行气管插管。术中维持采用七氟烷(上海百特医疗用品有限公司,进口药品注册证号:H20110142)及N2O/O2,维持最小肺泡浓度 0.9~1.2,瑞芬太尼(宜昌人福药业有限责任公司,国药准字:H20030197)持续输注0.05~0.25 g·kg-1·min-1,根据手术进展按需追加芬太尼50~100 μg及罗库溴铵10 mg。预计手术结束前30 min停止追加肌松药,预计结束前10 min给予肌松拮抗(阿托品1 mg及新斯的明2 mg)。麻醉医生按常规通过判断患者意识、肌力及自主呼吸恢复,认为符合拔管指征后即可拔出气管插管,同时记录此时的醒觉镇静评分(observer assessment of alertness and sedation,O/AAS),生命体征稳定后转入恢复室观察,拔管后20 min记录改良Aldrete评分,如Aldrete评分>9分可出室,评分未达标者继续观察至达标。
肌松监测肌松监测采用迈瑞肌加速度仪监护模块(深圳迈瑞生物医疗电子股份有限公司,型号:BeneVision N12),TOFr模式,由独立研究人员实施完成,主麻医生不参与肌松监测,避免知晓肌松监测数据影响拔管决策。肌松监测数据独立录入数据库。诱导前将患者前臂外展,将两枚电极放置在尺神经位置的两侧,远端电极置于前臂尺侧腕屈肌桡侧缘与近端腕横纹交点,与远端电极相距3 cm处固定近端电极,肌松换能器放置于同侧拇指远端平坦处,垂直于移动方向,避免影响拇指活动。当患者意识消失后,进行刺激定标,使T4/T1在0.95~1.05。校准完毕后给予肌松药。术中采用TOFr模式,频率2 Hz 波宽200 μs,测定时间间隔为15 min,过程中避免触碰监测侧手臂,同时注意手臂皮肤保温,预计手术结束前10 min调整TOFr监测间隔为30 s,记录拮抗前、拔管前即刻TOFr值。
膈肌超声采用wisonic超声机(深圳华声医疗技术股份有限公司,型号:指南针),由熟悉膈肌超声操作的独立医师完成膈肌超声检查,同时避免知晓肌松监测结果。分别在麻醉诱导前和拔管后即刻进行膈肌超声检查。采用高频探头(4~15 MHz)置于右侧腋前线和腋中线间第8或第9肋间隙,测量平静(quiet breathing,QB)及用力深呼吸(deep breathing,DB)时吸气末和呼气末膈肌厚度,并计算膈肌厚度变化率(diaphragmatic thickness fraction,DTF),即吸气末膈肌厚度与呼气末膈肌厚度差值/呼气末膈肌厚度,可分别计算出平静呼吸(DTF-QB)及深呼吸膈肌厚度变化率(DTF-DB)。采用低频探头(1~5 MHz)于右侧锁骨中线肋缘,以肝为声窗,找到同时存在肝、膈肌和下腔静脉切面,切换M模式,取样线与膈肌垂直,分别测量平静呼吸和用力深呼吸时膈肌在吸气相与呼气相垂直运动的距离为膈肌移动度(diaphragmatic excursion,DE)。深呼吸膈肌厚度变化率差异(△DTF-DB)定义为术后DTF-DB与术前的差值。深呼吸膈肌移动度差异(△DE-DB)定义为术后DE-DB与术前的差值。
本研究主要观察指标:平静呼吸及用力深呼吸膈肌移动度和膈肌厚度及其变化率;拔管时TOFr等。次要观察指标:拔管后O/ASS评分,呼吸并发症(气道痉挛、气道梗阻、反流误吸、非计划返ICU、二次插管、肺炎和支气管扩张等)发生率等。
统计学处理用SPSS 17.0统计软件进行分析。正态分布的计量资料以均数±标准差表示。根据TOFr是否大于0.9进行分组,TOFr≥0.9定义为无肌松残余组,TOFr<0.9定义为肌松残余组,两组间参数进行比较。正态分布两独立样本组间比较采用t检验,非正态分布两独立样本组间比较应用Mann-Whitney秩和检验,同一指标前后比较成对样本t检验,计数资料采用χ2检验,正态分布变量相关分析应用Pearson相关分析,非正态分布应用Spearman相关分析。P<0.05为差异有统计学意义。
结 果
一般情况符合纳入标准的患者共86例,剔除11例(2例术前肺功能存在异常、3例有胸腹部手术史、3例患者拒绝参与研究、2例术前超声评估存在困难、1例肌松监测反复校准后未在达标范围),最终实际纳入75例,手术种类包括:甲状腺切除术、下肢骨折内固定和支撑喉镜下喉肿物切除术等。根据拔管前TOFr分组,<0.9为肌松残余组,≥0.9为无残余组,两组患者年龄、ASA分级、体质量指数、术中应用芬太尼总量、罗库溴铵/体重剂量、拔管时O/AAS镇静程度评分差异均无统计学意义(P均>0.05)(表1)。
术前膈肌超声两组平静呼吸膈肌移动度(DE-QB)、深呼吸膈肌移动度(DE-DB)、平静呼吸膈肌厚度变化率(DTF-QB)和深呼吸膈肌厚度变化率(DTF-DB)差异均无统计学意义(P均>0.05)(表2)。
肌松监测结果拔管时平均TOFr 为(74.2±28.4)%,以拔管时TOFr<0.9定义肌松残余,肌松残余发生率为54.7%。拮抗前和拔管前肌松残余组TOFr均显著低于无肌松残余组(P均<0.001)(表3)。
术后膈肌超声结果平静呼吸DTF-QB、DE-QB两组比较差异无统计学意义(P=0.643,P=0.867)。而肌松残余组拔管后深呼吸DTF-DB和DE-DB均显著低于无肌松残余组(P=0.045,P<0.001)(表4)。Spearman相关分析显示拔管即刻DTF-DB(r=0.351,P=0.002)与拔管时TOFr显著相关,Pearson相关分析显示拔管后DE-DB(r=0.580,P<0.001)与拔管时TOFr显著相关。肌松残余组改良Aldrete评分较低 [8(7,9)比10(9,10),P<0.001]。所有患者术后均未出现气道痉挛、气道梗阻、反流误吸、非计划返ICU、二次插管、肺炎和支气管扩张等情况。

表1 两组患者一般资料
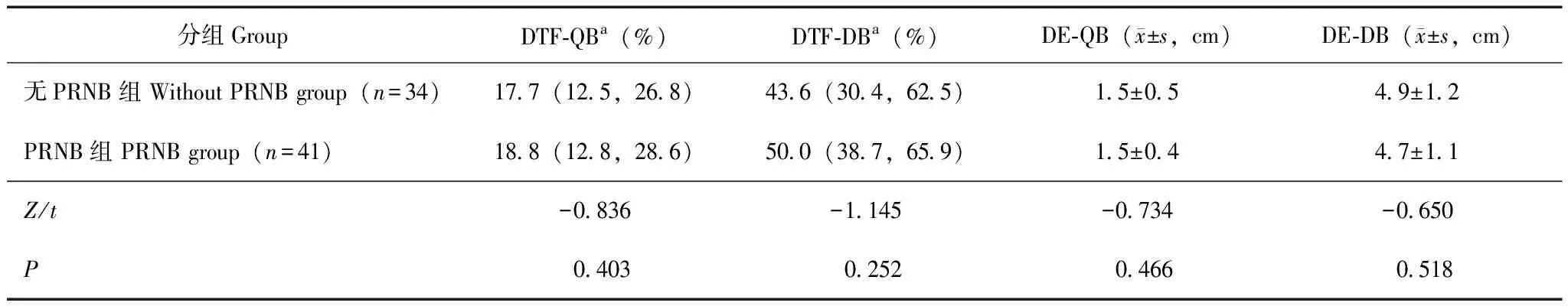
表2 两组患者术前膈肌超声

表3 两组患者不同时间肌松监测结果

表4 两组患者术后膈肌超声
讨 论
全身麻醉患者恢复期肌松残余仍是临床中常见问题,既往研究显示在未拮抗肌松药物情况下,肌松残余发生率可达37%~82%,应用拮抗药物情况下恢复室肌松残余的发生率仍在20%~40%[10- 11]。本研究监测术后肌松残余发生率54.6%,与既往文献[1]水平基本一致。监测过程由独立人员进行,监测数据避免麻醉医师及超声医师知晓,以保证研究客观及准确性。尽管大量指南均建议对应用非去极化肌松药的患者进行全程肌松监测,但由于肌松监测操作复杂,测量干扰较多,监测过程存在一定不适,在美国、欧洲其应用率仅在30%,在我国也尚未普及和常规应用,因此探究评估肌松残余的其他方法具有一定临床价值。
超声作为一种安全、无创、可视的方法,监测膈肌厚度变化率和移动度简便易行。对健康受试者和ICU患者的观察显示,其可重复性达94%~96%[12- 13]。自主呼吸受试者中膈肌移动度及膈肌厚度变化率均与跨膈压存在相关性,提示膈肌超声可反映膈肌肌力[14],给本研究提供一定理论支持。由于右侧膈肌超声显示比左侧更为清晰,可重复性强,既往文献亦认为仅在考虑存在单侧膈肌麻痹时方有必要进行双侧膈肌超声检查[13],因此,本研究仅评估了右侧膈肌运动情况。另外,由于带管状态进行膈肌超声检查会给患者带来一定不适,容易出现呛咳,同时,呼吸管路过滤器等也会造成额外阻力,影响膈肌超声的准确性,因此本研究选择在拔管后即刻,而非拔管前进行右侧膈肌超声检查,可获得较为全面观察指标,同时避免呛咳对超声监测的干扰,提高患者舒适度。为避免肌松监测结果与膈肌超声结果不匹配,本研究两者获取时间尽量接近,TOFr获取在拔管前1 min以内,膈肌超声监测在拔管后即刻完成。
既往文献显示,膈肌厚度及移动度个体差异较大,正常膈肌移动度为1.9~9.0 cm,膈肌厚度变化率为28%~96%[13,15],与性别、年龄、体质量指数、肺功能等相关,本研究膈肌移动度基线指标略低于国外研究水平,与国内研究一致[16],这种差异可能与人种和体型相关。另外,既往ICU研究将膈肌厚度变化率>20%作为成功脱机拔管预测指标[17]。本研究患者术后平静姑息膈肌厚度变化率略低于20%,可能与麻醉后轻度镇静状态有一定关系[18],但两组患者术后深呼吸膈肌厚度变化率分别为38.5(26.6,53.9)%和31.3(21.1,45.0)%,均高于临界值,提示呼吸储备功能可以满足氧供需平衡,与本研究所有患者均无二次插管和术后呼吸系统并发症,随访结果一致。目前尚无研究显示阿片类药物对膈肌超声指标存在影响,但鉴于阿片类药物的呼吸抑制作用,为排除阿片类药物影响,本研究两组患者阿片类药物用量无差异,同时所用患者拔管时呼吸频率均达到拔管标准。
本研究肌松残余组拔管时深呼吸膈肌厚度变化率和运动幅度均较术前基线下降,对监测肌松残余有一定提示意义。通过直接评估拔管时深呼吸膈肌厚度变化率及运动幅度在两组中的差异,发现肌松残余组显著低于无肌松残余组。因此,尽管膈肌对肌松药相对不敏感,肌力恢复较快,但本研究结果显示肌松残余患者膈肌功能不全仍然存在。因此,即使在术前未获取超声基线指标时,直接测量拔管时深呼吸膈肌移动度及膈肌厚度变化率对判断肌松残余仍有一定的提示意义,而且膈肌超声检查不会使清醒患者感到不适,可作为一种恢复室辅助判断术后肌松残余及呼吸恢复情况的简便舒适的新方法。
本研究仍存在一定不足。首先,熟练掌握膈肌超声需要经过培训和练习[12,19],测量结果的质量与操作者对超声的熟悉程度有关。另外,胸腹部手术切口疼痛可导致患者浅快呼吸,切口位置可能会与测量位置重叠,因此,本研究排除胸腹部手术患者。对于胸腹部手术患者,膈肌超声是否能够用于评估肌松残余仍有待于进一步探究。最后,咽喉肌群对于维持上呼吸道开放具有重要意义,其功能恢复对呼吸功能有很大影响,膈肌超声对此预测能力受限,因此,本研究也未予涉及。
综上,临床中肌松残余的发生率仍较高,膈肌超声提示肌松残余患者深呼吸膈肌厚度变化率与膈肌移动度较低,且与TOFr显著相关,因此,麻醉恢复期采用膈肌超声评估辅助判断肌松残余具有一定的可行性,对临床有参考价值。

