血液透析患者血镁水平与死亡的相关分析
林莹莹 汪年松 尹建永 王 锋
镁不仅参与其他离子的跨膜转运,还作为辅因子参与300多个酶促反应,对调节机体的神经肌肉兴奋性、骨代谢、心血管功能等具有重要的作用[1]。近年来研究发现,血镁浓度的轻度升高与血液透析患者全因死亡及心血管死亡的降低有显著关联,尽管过低或过高的血镁浓度依然增加患者的死亡风险[2,3]。与此同时,也有研究指出低镁血症常伴随营养不良、炎症、多并发症的情况,校正此类混杂因素后,血镁的保护作用则失去了显著性[4,5]。因此,伴随死亡风险升高的同时,低血镁究竟是“始作俑者”还是“旁观者”的争论引发了学界的兴趣。目前,多数研究主要集中在基于患者随访起始的基线镁离子浓度的生存分析,却极少关注患者在血液透析过程中的血镁动态变化以及生命末期的血镁水平。因此,本研究旨在分析终末期肾脏病患者血液透析治疗后血镁水平变化及其与患者全因死亡的关系。
对象与方法
1.研究对象:回顾性分析2016年1月1日~2019年7月31日在上海交通大学附属第六人民医院行维持性血液透析(MHD)治疗的终末期肾脏病患者。入选标准:年龄≥18岁,病情稳定行门诊透析治疗至少3个月。排除标准:①重症感染、腹泻,活动性出血;②合并恶性肿瘤;③联合腹膜透析;④肾移植;⑤转院;⑥病史资料及关键化验指标缺失。所有入选患者透析方案为:每周2~3次,每次4h,透析液钙离子浓度为1.25~1.50mmol/L,镁离子浓度为0.5mmol/L,钾离子浓度为2mmol/L。
2.方法:经电子病历系统查阅患者年龄、性别、透析龄、原发病、合并症及临床转归时间。详细记录所有患者最近1次(以2019年7月为观测终止日期)血液透析前电解质及相关生化检验,如:血镁、血磷、血钾、血钙、血红蛋白、白蛋白、血清高敏C反应蛋白、血尿酸、肌酐、尿素氮、血清全段甲状旁腺素等,并计算尿素清除指数(spKt/V)、尿素下降率(URR)。此外,为了观察患者最近3年的血镁变化,本研究每6个月记录1次患者的血镁水平,共记录6次,按检测时间先后依次记为mg1、mg2、mg3、mg4、mg5、mg6。

结 果
1.患者基线人口学特征:纳入2016年1月~2019年7月于上海市第六人民医院行维特性血液透析治疗3个月以上的门诊患者。经纳入排除标准筛选后,共262例患者入选,其中已死亡患者67例。该研究人群平均年龄为65.86±12.84岁,中位透析龄为31(14.5,55.0)个月,其中男性183例(69.8%),平均血镁浓度1.07±0.15mmol/L,原发病包括:糖尿病肾病(93例)、原发性肾小球疾病(79例)、高血压肾病(41例)、多囊肾(16例)、肾结石(6例)、无记录或不明原因(27例)。基于笔者医院血镁浓度参考范围为0.65~1.05mmol/L,低镁血症发生率为0,高镁血症发生率为52.7%(138例)。
2.血镁四分位分组及组间变量比较:本研究人群中位血镁水平为1.06mmol/L,按四分位数分组如下:第一分位:<0.97mmol/L,第二分位:0.97~1.05mmol/L,第三分位:1.06~1.15mmol/L,第四分位:>1.15mmol/L。4组患者性别构成及合并糖尿病、高血压、心脑血管疾病的比例差异均无统计学意义。高血镁组,既第三、四分位组较第一、二分位组年龄轻、病死率低、血清白蛋白及血红蛋白浓度高。不同组间血钾、血磷、肌酐、尿素氮、尿酸、尿素、甲状旁腺激素、血清高敏C反应蛋白(hsCRP)、血清铁蛋白比较,差异均有统计学意义,脂质代谢相关指标、血液透析充分性指标(spKt/V、URR)比较,差异无统计学意义(表1)。
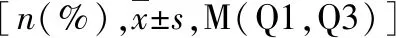
表1 依据末次透析前血镁水平分组后各组患者临床及实验室参数比较
3. 维持性血液透析患者血镁动态变化:本研究共有128例透析龄达2.5年以上并完整记录6次血镁浓度的患者。存活患者血镁水平总体高于死亡患者,但仅mg1、mg3、mg6 3个时点差异有统计学意义(P值分别为0.002、0.008、0.000)。由于所有存活患者每次检测的时间相近(2017年1月~2019年7月),因此呈现出明显的季节波动,即冬季高于夏季;而死亡患者由于转归时间随机,故而没有了季节影响,可见平均血镁水平基本稳定,仅在末次测量时急转直下。此外,由标准差曲线范围可见死亡患者组个体间的血镁变异较大,血镁浓度分布范围更广,尤其在mg4、mg5时点(图1)。
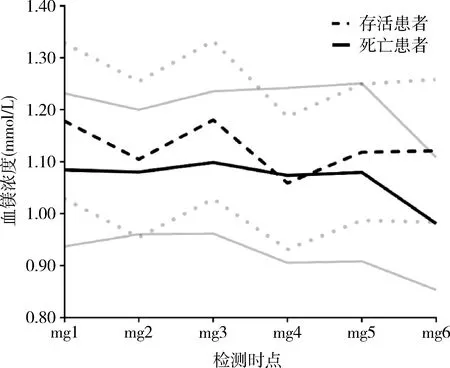
图1 存活和死亡患者透前血镁动态变化图血镁浓度以均数±标准差表示,其中黑线代表均值,灰线区域内代表±1个标准差范围
4.血镁与各临床生化指标的相关性:血镁除了与总蛋白、血清白蛋白、血红蛋白等营养状况指标呈正相关,与肌酐、尿素、血钾、血磷也同样呈显著正相关,并且该相关关系不随死亡患者的剔除而发生显著变化(表2)。其次,血镁随着年龄增长而降低(r=-0.181,P=0.003)。炎性指标血清高敏C反应蛋白(hsCRP)水平在不同组间差异有统计学意义,hsCRP显著上升的病例多分布于血镁较低的第一、二分位组。然而,除去死亡患者后不同组间的hsCRP水平差异无统计学意义(图2)。
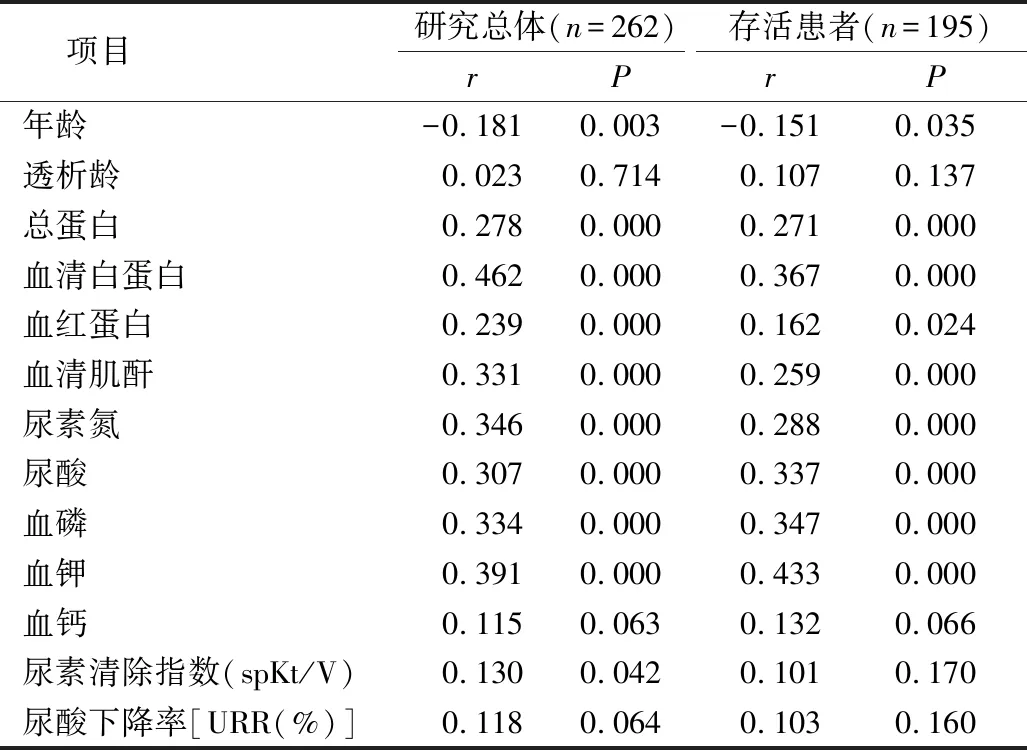
表2 血镁与各临床指标的相关分析

图2 依据末次血镁水平分组的组间hsCRP水平比较A.研究总体B.存活患者。组间两两比较,经Bonferroni法校正,以P<0.0083为差异有统计学意义
讨 论
与既往的报道类似,本研究发现低镁血症在维持性血液透析患者的发生率极低(<1%),高镁血症较为常见且存活患者高血镁发生的比例远高于死亡患者(61.5% vs 26.8%)[6]。经四分位数分组比较发现,血镁升高与MHD患者全因死亡风险的降低有显著关联。此外,笔者同样发现长期使用0.5mmol/L镁离子透析液使得患者血镁浓度略微降低[7]。然而,临床实践中对于透析患者是否应当提高透析液镁离子浓度或应用含镁制剂等依然存在争论。
自2007年以来陆续有报道指出,低血镁不仅是非心血管死亡的预测因子,也与猝死、血管钙化等心血管事件有关[8,9]。然而,部分研究者认为,血镁与死亡风险的负相关关系很可能是因为低血镁通常与营养不良-炎性综合征相关造成的[10,11]。一项随访长达5年的大型观察性研究表明,仅当血清白蛋白<35g/L时,低血镁(≤0.82mmol/L)才会额外增加患者的死亡风险,但是当患者血清白蛋白≥35g/L时,低血镁与高血镁(>0.82mmol/L)患者的死亡风险没有差别[4]。而最近国内的一项研究表明,将血清白蛋白<38g/L联合血镁≥0.95mmol/L 作为参照,也没有发现血清白蛋白<38g/L联合血镁<0.95mmol/L的患者全因死亡风险有进一步增加[12]。
在本研究中,血镁与其他生化指标尤其是营养-代谢产物相关指标的关系似乎也支持了这一论点。尤其是低蛋白血症往往表明机体处于营养不良或炎症的高分解代谢状态,其本身是透析患者死亡的独立危险因素[13]。而血镁水平与血清白蛋白的关联,一方面反映了患者总体营养摄入的水平,另一方面也是由于吉布斯-唐南效应,使得低蛋白血症的透析患者,更容易发生低镁血症[14]。
另一方面,支持高血镁作为主动保护因素的理论依据之一是大量的体内外实验表明血镁具有抗炎、抗氧化的作用[15]。然而,本研究分析发现尽管血镁第一、二分位组炎性指标hsCRP水平显著高于第三、四分位组,但在除外死亡后的稳定透析患者中,血镁水平与hsCRP水平没有显著关联(r=-0.138,P=0.057)。再者,血镁的动态变化规律显示死亡患者即使在终末2~3年内,血镁依然大体保持稳定,最终的衰竭死亡可能是导致血镁急剧降低的直接原因,这似乎也验证了低血镁作为被动反映机体营养状况指标的合理性。但仍然值得注意的是,死亡患者的基线血镁水平确实低于存活患者,一方面这可能是由于死亡患者组年龄偏大造成的,另一方面也不能完全排除长期相对低血镁引发不良结局的可能。
虽然本研究为回顾性的观察研究,无法做出有力的病因推断,但通过一系列的横向和纵向的比较,为剖析轻度高血镁在降低患者死亡风险中的角色提供了一定的线索。首先,不仅横向比较了死亡和存活患者的血镁水平差距,也纵向观察了血镁的动态变化。其次,通过比较剔除死亡患者前后血镁与各临床生化指标的相关关系,发现了血镁与其他变量的相关规律。但本研究尚存在以下不足:(1)由于单中心、样本量有限导致血镁极端观测值的缺失,因此血镁的作用和影响很可能在本研究中被大大掩盖。(2)由于透析液种类单一,无法比较不同镁离子浓度透析液对透析患者血镁水平的影响,也无法调查不同透析方案下患者全因死亡风险的差异。
综上所述,本研究主要讨论了血镁与维持性血透患者全因死亡的相关关系,尽管上述分析显示血镁更像是一个“旁观者”而非真正的“始作俑者”,但是由于观察性研究的局限性,很难做出有力的推论,因此要了解血镁的真实效应还需在控制营养因素的干扰下进行更为严格的随机对照临床试验研究。

