深在性囊性胃炎1例
张洪文,荣亚梅,张毅宏
深在性囊性胃炎(gastritis cystic profunda, GCP)是一种罕见的胃黏膜下病变,最早由Lettler等[1]在1972年首次发现并报道。1981年,Franzin等[2]将其正式命名为深在性囊性胃炎(GCP),至今,国内共报道约两百例。现将天津北辰医院消化科收治的1例GCP病例报道如下,并复习相关文献,以期提高对该病的认识。
1 病历资料
患者女性,57岁,因反酸、烧心、腹胀不适就诊于我院门诊,行胃镜检查提示:胃窦前壁近幽门处见一黏膜下隆起,大小约1.5 cm×1.0 cm,局部可见发红和凹陷(图1)。患者为行内镜下胃隆起切除治疗于2020年9月9日入住我科。入院后完善相关检查,血常规提示血红蛋白112 g/L,血生化检查及肿瘤标志物检查未见明显异常。腹部CT提示十二指肠球结节,考虑良性;肝右叶S8、左叶S3小血管瘤;肝囊肿;左肾小囊肿(图2)。超声胃镜提示胃窦前壁可见一不均匀低回声,其内局部可见无回声区,来源于胃固有肌层,大小约1.3 cm×0.6 cm(图3)。征得患者及家属同意后行内镜黏膜下剥离术(endoscopic submucosal dissection,ESD)切除,术后未发生出血及穿孔。术后病理:(胃窦)黏膜慢性炎症,黏膜下层见较多黏液腺,部分腺体扩张,个别腺体肠化,考虑GCP(图4)。术后随访患者恢复良好。
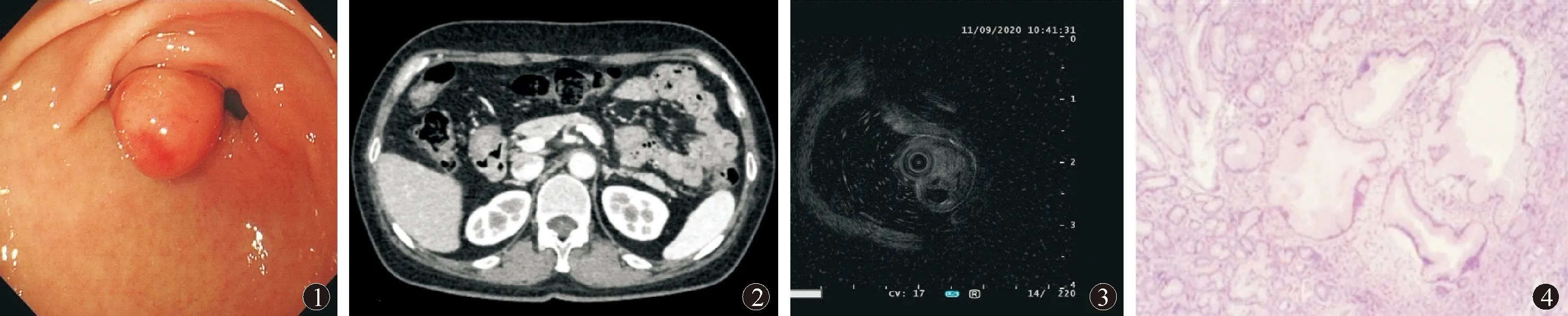
图1 胃镜提示胃窦隆起病变 图2 腹部CT提示十二指肠良性结节,考虑为胃窦隆起脱落至十二指肠 图3 超声胃镜提示肿物为低回声病灶,来源于胃窦固有肌层 图4 病理提示黏膜下层腺体扩张(HE, ×40)
2 讨论
GCP患者临床表现缺乏特异性,部分患者无任何消化道症状,部分患者表现为腹部不适,如腹痛、腹胀、恶心、纳差、反酸、消瘦等,严重者可出现消化道出血或幽门梗阻。腹部CT可表现为胃壁增厚或囊性低密度肿块形成。超声胃镜特异性表现为深达黏膜下层或固有肌层的低回声区伴无回声囊腔。GCP需与间质瘤、异位胰腺、淋巴瘤等鉴别。EUS引导下细针抽吸术(FNA)有助于鉴别诊断及病灶评估[3]。典型的GCP病理表现为胃腺体呈囊状扩张,不同程度扩张的胃体腺、幽门腺或化生性腺体向黏膜深层及黏膜下浸润,腺体组织形态多较规则、完整[4]。本例患者临床表现无特异性,行胃镜常规检查时发现病变,进一步行超声胃镜检查考虑此诊断,后经ESD切除后依据病理确诊。
GCP是良性病变,但部分文献认为其有癌变风险,Choi等[5]发现10 728例胃癌患者中,161例(1.5%)合并GCP;龚帅等[4]回顾性研究了40例GCP患者,22例(55%)合并瘤变或腺癌。另外,研究提示GCP患者p53、p21、ki-67基因高表达[6-7],KCNE2基因低表达[8]。故GCP与胃癌之间存在一定的相关性,GCP可能是胃癌发生过程中的一个环节,但相关证据及机制仍需进一步研究探讨。临床工作中,必需高度警惕GCP与胃癌的鉴别。GCP发病机制尚未明确。最初报道的GCP病例多为胃手术后患者[1,9],认为胃手术损伤黏膜,进而导致GCP发生。随着胃镜及内镜下操作技术的成熟,越来越多无手术史的GCP病例被发现[10-12],推翻了上述结论。目前认为,胃的胆汁反流[13]、幽门螺杆菌感染[14]、EB病毒感染[5,15]等均可导致GCP发生。本例患者无手术史,无明确炎症刺激病史,其发病原因及预后仍需进一步随访观察。因GCP有癌变风险,临床上多采取积极治疗,可行内镜下切除或外科手术切除。内镜下治疗创伤小、并发症少、无复发、预后良好[16-19]。Xu G等[18]经内镜治疗了34例GCP患者,2例患者手术时合并出血,合并瘤变或黏膜内癌的比例为14.7%(5/34),随访23个月,所有患者预后良好;朱博群等[19]回顾性分析了40例确诊的GCP患者,合并黏膜内癌的比例为12.5%(5/40),所有患者均行内镜下治疗,仅1例出现迟发性出血,余患者随访39个月预后良好。但GCP合并癌变且侵及固有肌层及以下组织,或者GCP合并癌变且存在淋巴结转移或远处转移时,外科手术则为首选治疗方案。目前,关于GCP的研究仍较少,尚需大样本、多中心研究及长时间随访以明确其发病机制、诊治方案等。

