替诺福韦单一用药预防肝移植术后乙肝复发的疗效分析
姜晓青,解曼,张群,孔心涓,饶伟〔.潍坊市益都中心医院消化内科,山东 潍坊 6000;.青岛大学附属医院消化内科,山东 青岛 66000;.青岛大学附属医院器官移植中心(肝脏移植科),青岛大学附属医院肝脏病中心(肝脏内科),青岛大学移植医学研究所,山东 青岛 66000〕
2018 年中国肝移植注册系统显示,乙肝在我国成人肝移植(liver transplantation,LT)病因中居首位(占72.27%),患者术后如不采取有效措施,乙型肝炎病毒(hepatitis B virus,HBV)复发率可超过90%[1-2]。核苷(酸)类似物〔nucleos(t)ide analogs,NAs〕联合低剂量乙肝免疫球蛋白(hepatitis B hyper-immune globulin,HBIG)是目前公认有效的方案[1,3],但HBIG 价格昂贵、长期注射患者依从性差,所以随着TDF等新一代更加高效安全且具有高耐药屏障的NAs出现,LT 后预防HBV 复发有了新的方向。本研究旨在探究HBV 相关术后停用HBIG,单用TDF 预防HBV 复发的有效性、安全性及经济性。
1 资料方法
1.1 临床资料:研究对象为青岛大学附属医院HBV 相关LT 患者,患者术后常规给予HBIG 联合TDF 或ETV。将患者分为单药组和联用组,单药组停用HBIG 改TDF 单药,联用组给予HBIG 联合ETV,收集患者临床及实验室数据。所有患者均对该研究过程及风险知情并签署同意书,符合世界医学会赫尔辛基宣言伦理要求,通过我院伦理学委员会审批。
1.2 纳入及排除标准:纳入标准为① 年龄满18 岁;② 首次LT;③ 移植前均明确有HBV 感染(HBsAg及HBV-DNA 均为阳性)且无合并丙肝或HIV 感染;④ 随访开始前患者血HBsAg 及HBV-DNA均为阴性(我院血HBV-DNA 检测最低限为1×102U/ml,试剂盒为中山大学达安基因股份有限公司HBV DNA 荧光定量PCR 试剂);⑤ 随访开始前患者肝肾功能稳定,无肾功能衰竭〔定义为eGFR <30 ml/ (min·1.73m2〕。排除标准:① 年龄未满18 岁;② 二次LT 或联合其他实体器官移植;③ 患者一般情况较差,预期存活时间不超过1 年;④ 随访开始前已有HBV 复发。
1.3 观测指标:患者年龄,性别,乙肝病史,化验指标包括HBsAg、HBV-DNA、丙氨酸转氨酶(alanine aminotransferase,ALT)、天冬氨酸转氨酶(aspartate aminotransferase,AST)、 尿 素 氮(urea nitrogen,BUN)、肌酐(creatinine,Cr)、估算肾小球滤过率(eGFR,按MRDR 简易公式计算),LT时间及年龄,抗排斥反应用药,抗HBV 用药。
1.4 具体方案:患者术后均给予HBIG 联合TDF或ETV,具体用药剂量为ETV 口服0.5 mg/(次·d),TDF 口服300 mg/(次·d),HBIG 无肝期开始使用,具体用量以乙肝表面抗体(抗- HBs)滴度为准:术后1 周内升至1000 U/L;3 个月内不低于500 U/L;3 ~ 6 个 月 不 低 于200 U/L;6 个 月 以 上 不 低 于100 U/L。2018 年4 月1 日起将符合纳入标准的患者分为单药组和联用组:单药组停用HBIG 改TDF单药;联用组给予HBIG(抗-HBs 滴度不低于100 U/ L)联合ETV。每3 个月复查HBsAg、HBVDNA、ALT、AST、BUN、Cr,电话随访患者有无不良反应及费用。
1.5 术后抗排斥反应方案:术后抗排斥反应方案由他克莫司、环孢素或西罗莫司组成,可同时联合霉酚酸酯、皮质类固醇。
1.6 随访终点:① 出现HBV 复发,连续两次检测血HBsAg 或HBV-DNA 阳性;② 患者出现严重不良反应或死亡;③ 随访日期到2019 年6 月30 日。1.7 统计方法:用SPSS 22 软件进行统计分析。计量资料用均数±标准差(±s)表示,精确到小数点后两位,组间比较用独立样本t 检验或秩和检验;计数资料用频数和百分比表示,组间比较用χ2检验;多因素分析用二分类Logistic 回归法。P ≤0.05为差异有统计意义。
2 结 果
2.1 患者特征:本研究自2018 年4 月1 日— 2018 年10 月30 日共纳入符合标准的患者42 例,平均年龄52(37 ~66)岁;男性37 例(88.10%);LT 前患者平均抗HBV 治疗5.09 年(0 ~30 年);移植前34 例(80.95%)HBsAg 阳性,11 例(26.19%)HBV-DNA 阳性;4 例(9.52%)出现NAs 耐药(变异位点检测阳性,详见表1);肝脏原发病方面,以肝癌合并乙肝最多(23/42,54.76%);平均移植年龄49.5 岁(35 ~63 岁);入组前4 例(9.52%)为TDF 联合HBIG,38 例(90.48%)为ETV 联合HIBG;从LT 到入组前的平均时间为17.12 个月(0 ~91 个月,见表2)。

表 1 耐药变异位点检测情况

表2 患者基本信息(n =42)
2.2 随访结果:随访开始后单药组因个人原因及药物可疑不良反应剔除4 例(见表3),最终单药组共纳入10 例,联用组28 例不变。截止到2019 年6 月30 日,单药组和联用组分别平均随访13.50 个月和13.03 个月(P =0.651);两组平均年龄52 岁;单药组全为男性,联用组24 例(85.71%)男性(P =0.556);平均移植年龄分别为49 岁和50 岁(P =0.673);入组前单药组4 例(40.00%)为TDF 联合HBIG,6 例(60.00%)为ETV 联合HBIG,联用组28 例(100.00%)均为ETV 联合HBIG(P =0.003);单药组入组前联合用药时间(27.40 个月)明显多于联用组(12.57 个月,P =0.05),详情见表4。
2.2.1 乙肝复发情况:入组前两组患者HBsAg 和HBV-DNA 均为阴性,至随访结束共有3 例(7.89%)出现HBsAg 阳性复发,单药组1 例(10.00%),联用组2 例(7.14%,P =1.000),HBV-DNA 在LT后始终保持阴性(见表5)。
2.2.2 HBV 复发相关危险因素:本研究中HBV 复发组3 例,HBV 未复发组35 例,复发组平均年龄(42 岁比53 岁,P =0.022)及移植平均年龄(41 岁比50 岁,P =0.039)均小于未复发组,多因素分析显示,这两个因素均不与HBV 复发独立相关;性别(P =1.000)、家族史(P =1.000)、耐药史(P =1.000)、术前肝癌史(P =1.000)、术前HBVsAg 阳性(P =1.000)及HBV-DNA 阳性(P =1.000)等均无统计差异;术后肝癌复发率(P =0.224)、入组前抗HBV 治疗时间 (P =0.350)及用药方案(P =1.000)也无统计差异。两组随访时间相近 (13.00 个月比13.20 个月,P =0.906),复发组1 例(33.33%)为TDF 单药,未复发组9 例(25.71%)为TDF 单药(P =1.000),详见表6。2.2.3 安全性:研究期间未发现与治疗相关的重大不良事件。单药组1 例术后转氨酶长期高于正常水平,考虑为术后出现胆道并发症所致,联用组1 例术后转氨酶恢复正常后又逐渐升高考虑为肝癌复发所致,其余患者术后转氨酶回落至正常且保持稳定,两组转氨酶水平无明显差异;患者术后肌酐有不同程度升高,单药组eGFR 均维持在59 ml/(min·1.73m2)以 上,联用组部分患者术 后eGFR <60 ml/(min·1.73m2) 但 维 持 在30 ml/(min·1.73m2)以上,两组肌酐和eGFR水平及变化值无明显差异(见表4,表7)。本研究中患者均未调整抗HBV 药量,部分eGFR <60 ml/(min·1.73m2)的患者于肾病科门诊随诊并加用保肾药物,肾功稳定。
不良反应方面,单药组2 例因可疑TDF 不良反应退出研究:1 例患者服用TDF 2 个月后出现蛋白尿(不排除其他药物影响),改回ETV 联合HBIG 并定期肾病科随诊药物治疗,蛋白尿情况较前明显改善;1 例患者服用TDF 5 个月后出现失眠,改回ETV 联合HBIG,症状较前改善。至随访结束单药组另有2 例出现TDF 相关不良反应:1 例服用TDF 3 个月后出现腹泻,未经治疗症状自行改善,用药无改动;1 例服用TDF 3 个月后出现高尿酸血症,患者继续服用TDF 并加用降尿酸药物,尿酸较前下降。联用组未发现明显ETV 相关不良反应。
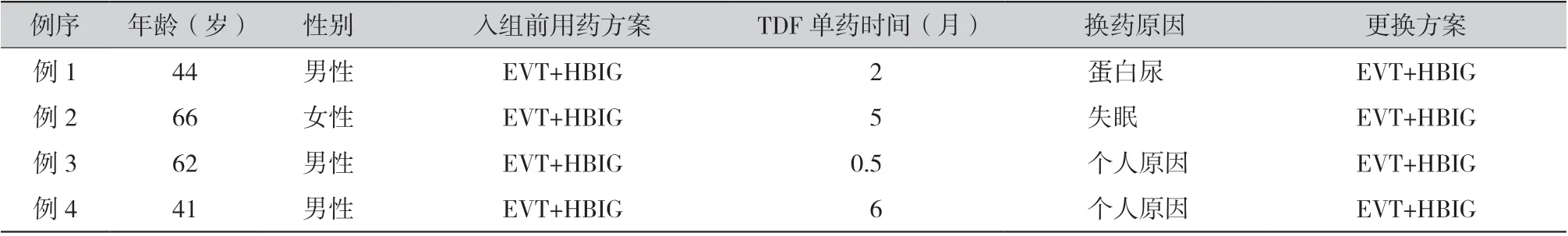
表3 剔除患者情况
2.2.4 肿瘤复发及生存情况:至随访结束,单药组和联用组分别有1 例(10.00%)和3 例(10.71%)出现肝癌复发,其中1 例同时有HBV 复发,其发现肝癌复发时间为2019 年1 月9 日,HBsAg 转阳时间为2019 年1 月12 日。联用组1 例(3.57%)因术后发现肺转移癌合并严重肺部感染死亡。
2.2.5 药物花费:根据医院药物价格,患者入组前均为联合用药,平均花费基本接近(2073.23 元/月比1952.55 元/ 月,P =0.976),随 访 开 始 后 单药组停用HBIG 改TDF 单药花费明显低于联用组(490 元/月比1952.55 元/月,P <0.001),见表4。
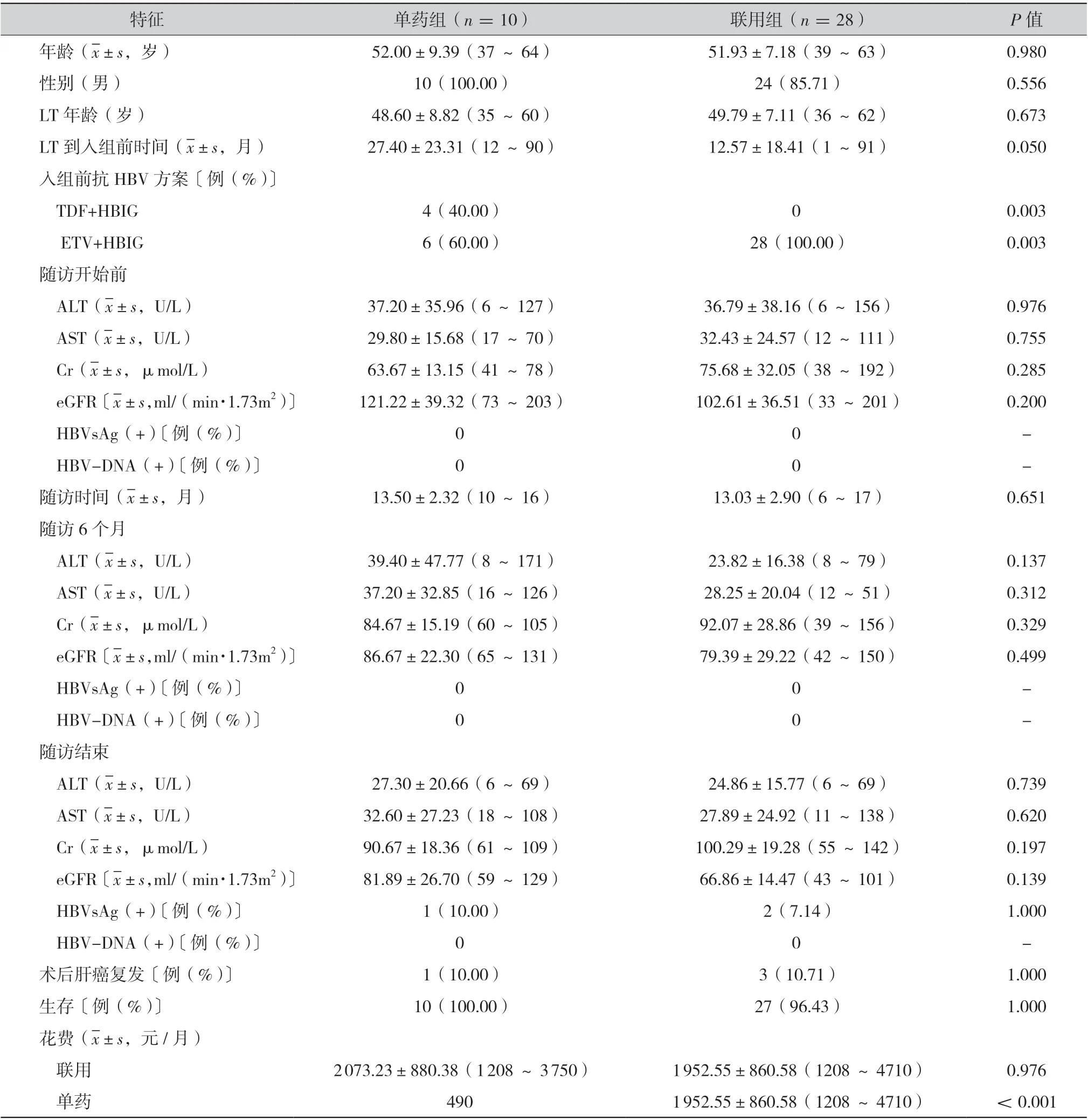
表4 两组患者随访情况
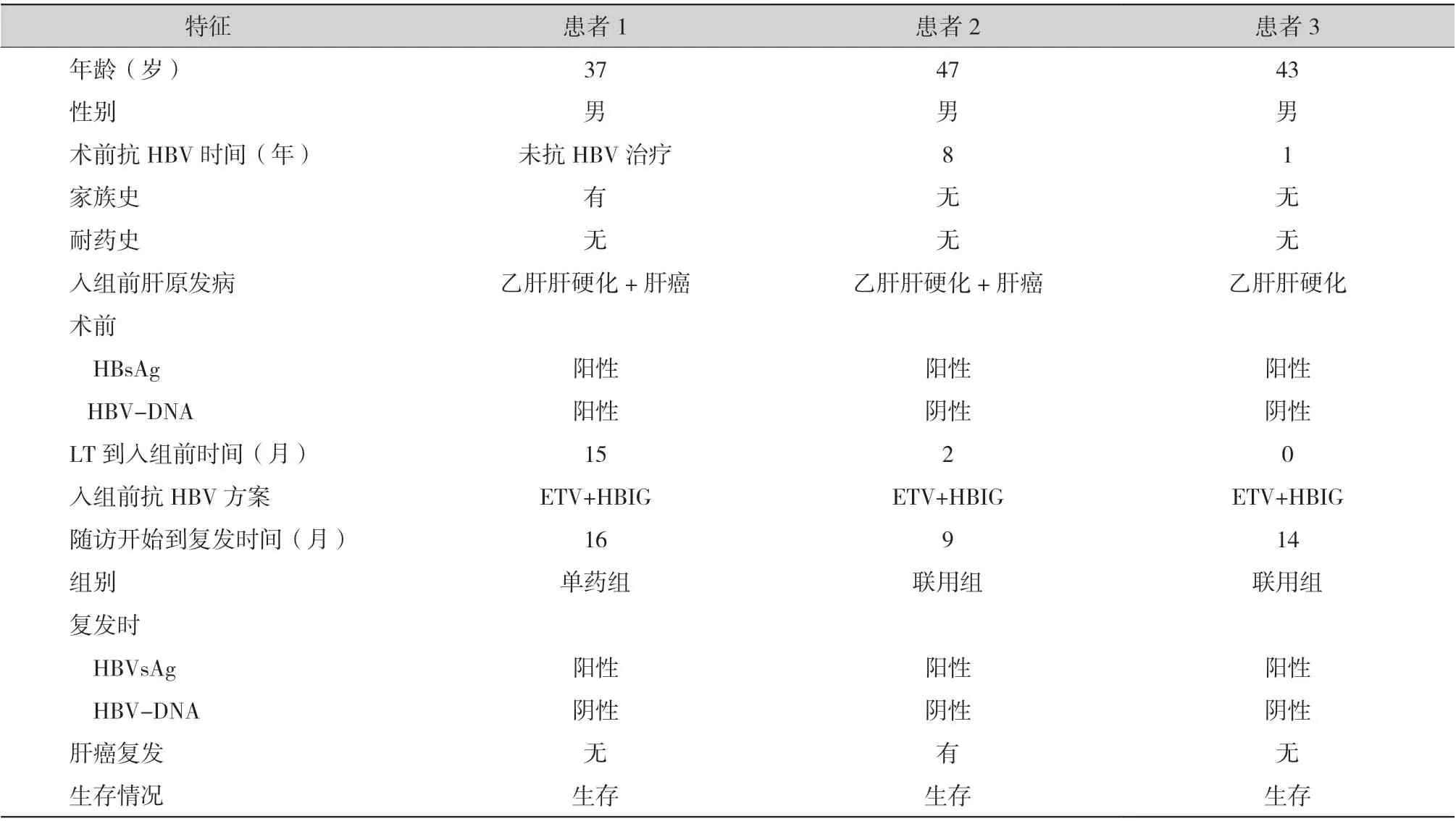
表5 HBV 复发患者基本信息
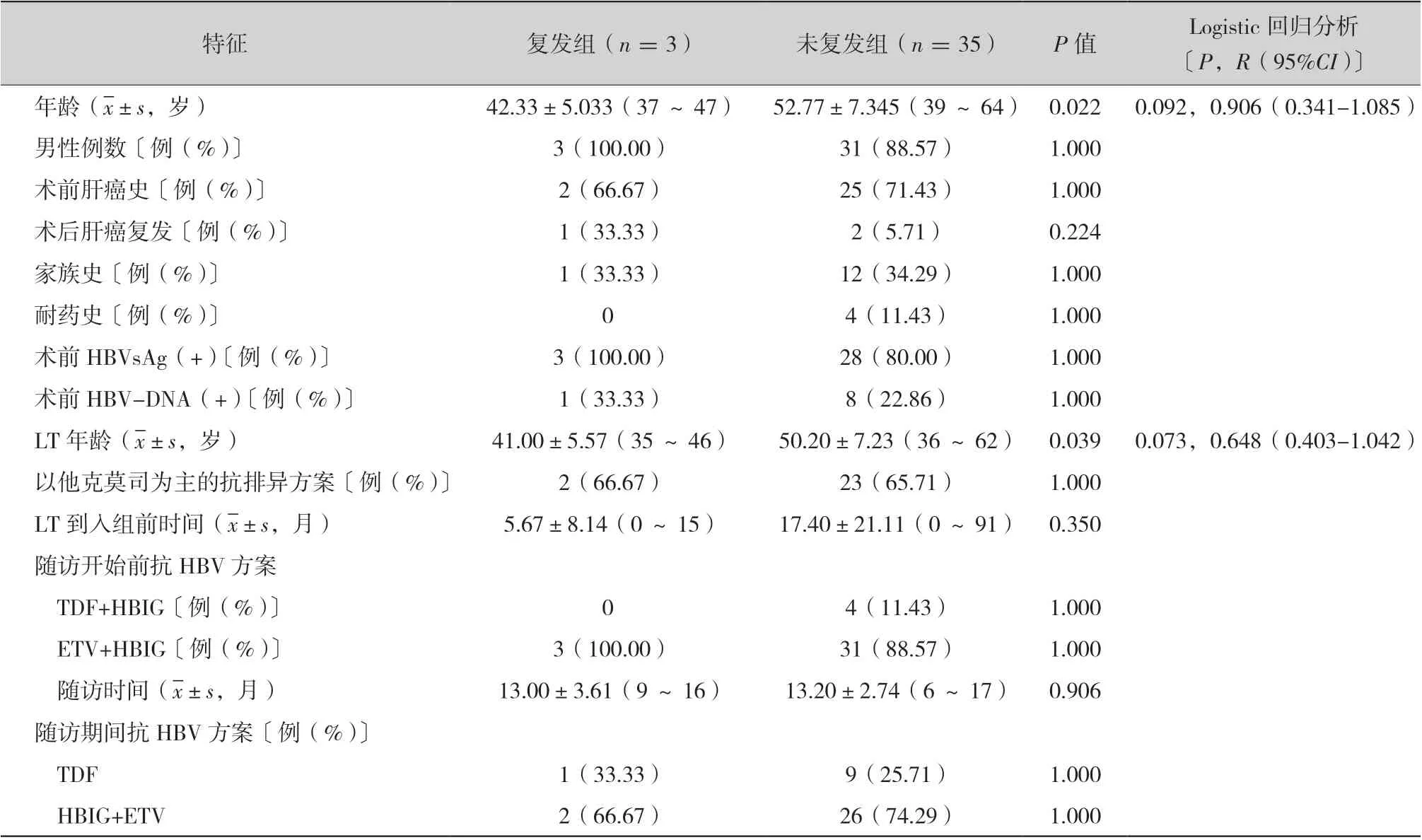
表6 HBV 复发患者特征对比
表7 两组患者随访后比较(±s)

表7 两组患者随访后比较(±s)
时间 单药组(n =10) 联合组(n =28) P 值随访后肌酐变化值(μmol/L)随访6 个月 21.56±12.81(2 ~45) 16.39±23.21(-36 ~70) 0.407随访1 年 27.56±11.71(6 ~46) 24.61±23.89(-78 ~59) 0.724随访后eGFR 变化值〔ml/(min·1.73m2)〕随访6 个月 -34.00±27.12(-73 ~1) -23.21±35.51(-141 ~29) 0.410随访1 年 -38.78±24.07(-75 ~-3) -35.75±29.73(-133 ~27) 0.783
3 讨 论
3.1 有效性:本研究中单药组术后27.4 个月(最少12 个月)后停用HBIG 改TDF 单药,单药组和联用组平均随访13.50 个月和13.03 个月,分别有1 例(10%)和2 例 (7.14%)出现HBsAg 阳性复发(P =1.000),HBV-DNA 术后始终为阴性。目前,临床上HBV 相关LT 后预防HBV 复发的方案主要包括注射HBV 疫苗、单用HBIG、NAs 联合HBIG及单用NAs 4 种。LT 患者乙肝疫苗成功接种率低[1,4]且成功接种后易因免疫逃逸复发[1,5-7];单一注射HBIG 可将复发率降至36%[8]; HBIG 联合NAs 是目前公认有效的方案[1,3],有效率可达90%[3,9],高耐药屏障NAs 联合HBIG 可将复发率降至1.0%[10]。由于HBIG 花费高且需长期注射,研究者们尝试术后停用HBIG 改高耐药屏障NAs单药预防HBV 复发(复发率为0 ~11%[4-5,9-20])。Tanaka 等[17]的回顾研究纳入132 例LT 患者,术后12 个月停用HBIG 改NAs 单药,5 年HBV 复发率为8.6%。Manini 等[11]的前瞻研究在LT 后至 少6 个 月 停 用HBIG 改 为TDF 或EVT 单 药,69 例HBV 感染患者5 年HBsAg 阳性复发率为9%,HBV-DNA 始终阴性。Radhakrishnan 等[13]的前瞻研究纳入42 例HBV 相关LT 患者,移植5 d 后停用HBIG 改单用TDF 或EVT,5 年HBsAg 和HBV DNA 阳性复发率分别为2.9%和3.3%。
本研究中复发组平均年龄以及移植年龄明显小于未复发组,多因素分析后这两个因素不与HBV 复发独立相关。许多研究表明,LT 后HBV 复发的影响因素有更高的移植年龄[11]、移植 后 肝 癌 复 发[4,20]、拉 米 呋 定 耐 药 史[4],而HBIG[4,10-11]是否停用不影响HBV 复发。Lens等[4]的回顾研究显示术后肝癌复发(P <0.001)和拉米呋定耐药史(P <0.001)是HBV 复发的独立影响因素,术后是否停用HBIG 不影响HBV 复发(P =0.9)。这可能是肝癌复发可导致病毒在癌细胞中复制增加,拉米呋定耐药可促进耐药突变进一步产生进而增加HBV 的复发风险。本研究中1 例HBV 复发患者HBsAg 转阳时间与肝癌复发时间大致相当,其肝癌复发或可增加HBV 复发风险,但此结果也受到复查时间间隔的限制。
3.2 安全性:本研究中,大部分患者术后转氨酶稳步回落至正常范围;患者术后eGFR 均稍有下降,原因包括长期服用免疫抑制剂、术中血流动力学变化、并发症(高血压、糖尿病等)、高龄等,但两组患者术后肾功及变化值无明显差异。本研究中单药组TDF 可疑不良反应包括蛋白尿、腹泻、高尿酸血症、失眠,患者经更改NAs 种类或对症治疗后症状均得到改善;联用组未发现ETV 相关药物不良反应,考虑大部分患者术前长期服用ETV,对ETV 耐受性好且联用组移植时间较单药组短。
既往研究中,TDF 不良反应包括胃肠反应[21]、肾损害[21-22]、低磷性骨质疏松[22]等,其中肾损害是临床最为关注的问题。目前研究中HBV 相关LT 患者采用TDF 单药后肾功监测结果普遍较为理想[10-11,19],且TDF 与ETV 对肾功影响并无统计差异[11,19]。Cholongitas 等[10]的系统回顾分析纳入7 项研究,6 项研究结果显示使用TDF 或ETV平均24 个月后患者肾功没有显著改变,仅1 项均使用TDF 的研究中14%(3/21)的患者出现可逆性急性肾功能衰竭。值得一提的是,替诺福韦阿拉酚胺(tenofovir alafenamide,TAF)作为TDF 的一种口服药,于2016 年被美国FDA 批准用于治疗成人乙肝[23]。《2017 年欧洲肝病学会临床实践指南:HBV 感染的管理》[24]也首次将TAF 与ETV、TDF 并列为治疗慢性乙肝的首选药物。TAF 在使用剂量低于TDF 十分之一时即可获得相同疗效。2 项国际临床Ⅲ期试验[25-26]显示使用TAF 的患者肾功能及骨骼指标都明显优于服用TDF 的患者。TAF 或可为LT 患者进一步减少不良反应提供更好的选择。
本研究中仅1 例因为肺转移癌合并肺部严重感染死亡(无HBV 复发)。目前几项研究中,患者LT 后停用HBIG 改NAs 单药的生存率为82%~100%[4,11-14,16-19],但HBV 复发并不是影响患者生存的因素[4,17,20]。Lens 等[4]的回顾研究中患者5 年生存率为82%,术前出现急性爆发性肝衰竭(P <0.001)、合并丙肝感染(P <0.001)、术后肝癌复发(P <0.001)与患者生存独立相关,而HBV 复发(P =0.71)不影响患者生存。Tanaka 等[17]的回顾研究中患者第1、5、10 年的生存率分别为93.9%、86.9%、84.1%,所有死亡患者均无HBV 复发。
3.3 经济性:根据医院药品定价,由于HBIG 费用明显高于ETV 和TDF,停用HBIG 前两组花费基本接近,停用HBIG 后单药组花费明显低于联用组(490 元/月比1952.55 元/月,P <0.001)。
4 小 结
本研究结果显示与EVT 联合HBIG 相比,LT超过1 年后停用HBIG 改用TDF 单药可有效预防HBV 复发,且TDF 单药有着良好的安全性,在减轻患者注射痛苦同时减轻经济负担。本研究创新性将药物花费纳入统计,为临床实践提供更加具有现实意义的参考资料。希望以后有更多前瞻性大样本多中心临床数据完善此方面研究。

