生物炭与粘土材料对水体中铅的吸附研究
徐若琳 刘人荣 谭丽亚,2 ANNA Kerkula 王 海
(1.绍兴文理学院 生命科学学院,浙江 绍兴 312000;2.绍兴文理学院 土木工程学院,浙江 绍兴 312000)
0 引言
近年来,随着我国经济工业化快速发展,周围环境质量逐渐开始衰退,各种污染问题越来越严重[1],而其中污染物的不合理排放与处置,使重金属进入水体和土壤中富集,严重危害到生态环境和人类健康.当重金属与环境中离子发生结合后, 难以被自然界的生物体吸收、排出或是降解, 从而引起生物体的病变, 产生严重的危害[2-4]. 其中铅污染最为常见;当过量的铅
(Pb(II))在人体内富集,导致生殖系统障碍,器官损害以及大脑损伤.因此,加强重金属污染治理刻不容缓,寻求高效,低成本的治理途径是实现工农业健康可持续发展的关键之一[5-7].
吸附法是利用生物炭等固体吸附剂将水样中的一种或数种组分吸附于表面,再用适宜溶剂,加热或吹气等方法将预测组分解吸附,达到分离和富集的目的,其效率高,操作便捷,成本低廉,可循环利用以及较好特向性等优点已经成为目前吸附重金属废水的一种重要处理方法[8].而生物炭是废弃的生物质材料经过完全无氧或缺氧条件下进行高温热解,炭化形成的固态生物燃料.其具有较大的比表面积,疏松多孔,含有羟基、羧基等活性官能团[9],对水中的重金属等的去除有着良好的效果[10-15].因此,生物炭吸附法成为去除污水重金属热门研究方向[16-19].目前重金属吸附研究中,由不同原料和热解温度下制备而成的生物炭,其结构表征存在明显差别,以及在不同反应条件下[20-24](溶液初始pH,接触时间和溶液初始浓度等),对重金属铅的吸附能力也存在显著差异[25],有待进一步研究.
本研究以花生壳为原料, 在热解温度为250 ℃制备生成生物炭,选择常见的粘土材料(蒙脱土和高岭土)做对比,利用比表面积和孔径分析法(BET)、扫描电镜法(SEM)、电镜能谱分析法(EDS)和傅里叶红外吸收光谱法(FTIR)对吸附材料进行结构表征;同时综合考虑溶液初始pH值,接触时间和溶液初始浓度等外界因素对吸附反应的影响,进一步通过吸附动力学与吸附热力学探讨吸附材料对重金属铅的吸附机理.
1 材料与方法
1.1 材料的制备与结构表征
选择花生壳作为原料,经2500C粉碎机粉碎,于WRN-120箱式电阻马弗炉中250 ℃限氧高温热解2 h,自然冷却后过100目筛后得到生物炭.
生物炭与粘土材料(高岭土和蒙脱土)的结构表征通过比表面积和孔径分析法(N2-BET)测定比表面积和微孔结构;扫描电镜法(SEM)观察材料的表面形貌;电镜能谱分析法(EDS)测定吸附材料内部的组成元素种类及含量;傅里叶红外吸收光谱法(FTIR)定性确定表面官能团等组成.
1.2 试剂与仪器
本实验所用试剂:37%浓盐酸,氢氧化钠,8-羟基喹啉,乙醇,四(3,5-二溴-4-羟基苯基)卟啉,NN-二甲基酰胺(DMF),辛基酚聚氯乙烯醚,亚硫酸钠和氯化铅均为分析纯;实验用水均为去离子水.
实验所用仪器有2500C粉碎机;WRN-120箱式电阻马弗炉;JJ124BC电子分析天平;FE20精密pH计;BSW-200B恒温振荡器;752N紫外可见分光光度计;OKP-S220S超低有机型纯水机;KQ5200超声波清洗器;全自动比面积及孔隙度分析仪;扫描电镜仪;X-射线能谱仪;红外光谱仪等.
1.3 静态吸附实验
Pb(II)的测定方法:取1 mL样品,用0.45 um水系滤膜过滤,置于50 mL比色管中,依次加入1.5 mL 2% HOz,1.0 mL 2 mol/L NaOH, 2.0 mL 2% Na2SO3和2.0 mL 0.04% T(DBHP)P溶液.静置3 min,加入2.5 mL 6%乳化剂OP,加去离子水稀释至刻度,摇匀.待测液装入1 cm比色皿,以相应的试剂空白为参照,在波长为479 nm处,测定吸光度.
标准曲线测定:0.671 g PbCl2与去离子水在500 mL容量瓶中制备浓度为1.342 g/L的PbCl2标准溶液.分别取0 mL,1 mL,2 mL,3 mL,4 mL,5 mL,6 mL,7 mL和8 mL标准溶液于50 mL比色管中进行测定.从测得的吸光度经空白校正后,以吸光度为横坐标,以含铅量为纵坐标作图,绘制吸光度对铅含量的标准曲线.
单一影响因素:为了确定吸附材料的最佳反应条件,通过研究溶液初始pH,接触时间和初始浓度对吸附反应的影响.分别称取0.05 g吸附材料加入100 mL 50 mg/L的Pb(II)溶液中, 溶液初始pH用0.1M-10.0M HCl/NaOH调节至4.0~8.0;接触时间选择为0 min,5 min,10 min,15 min,20 min,30 min, 40 min, 60 min和90 min进行定点取样测定;初始浓度为30 mg/L,40 mg/L,50 mg/L,60 mg/L和70 mg/L.
机理分析:实验数据分别与吸附动力学(准一级吸附动力学方程和准二级吸附动力学方程)和吸附热力学(Freundlich模型和Langmuir模型)拟合,进一步探讨吸附材料对水中重金属铅的吸附机理.
为了避免实验误差以及保证实验数据的科学性,所有实验均重复3次,以平均值表示实验结果.采用Microsoft Excel 2007和Origin 2017软件进行数据处理及图表制作.
2 结果与讨论
2.1 吸附材料的结构表征
3种吸附材料的比表面积和微孔结构如表1所示.
由表1可知,粘土材料中蒙脱土的比表面积和外表面积明显最大,生物炭的最小.而微孔表面积生物炭最大,高岭土的最小.吸附材料的较大比表面积以及丰富的孔隙,能够为重金属提供更多的吸附位点,从而提高其对水体重金属的吸附能力[25].
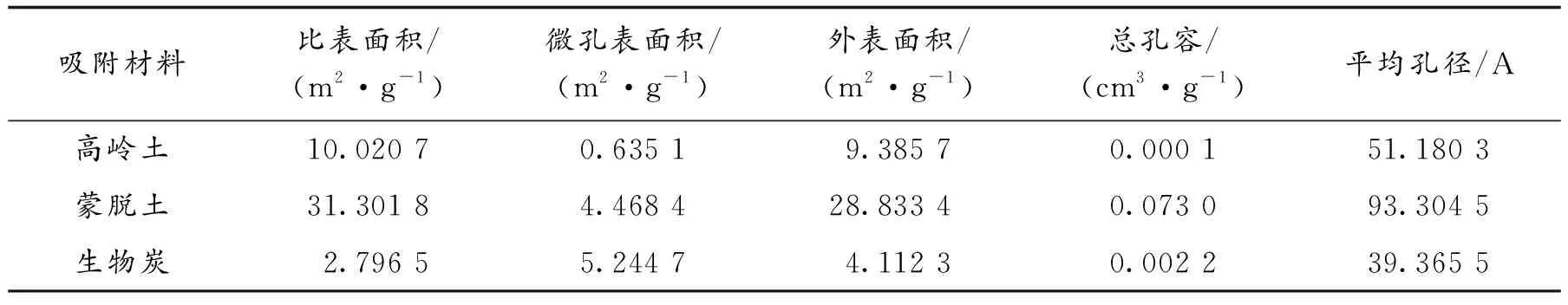
表1 3种材料的表面结构特征
3种材料的SEM图和EDS图如图1所示.可以看出高岭土表面分布许多分散的小颗粒,主要呈絮状;蒙脱土与生物炭两者均有着较大的平滑表面,在一定程度上提高其对重金属铅的吸附能力.在EDS图中可以看出,3种吸附材料的元素组成及含量明显不同.其中蒙脱土含有大量的金属元素,推测Fe的氧化物会与水中Pb(II)生成沉淀物[26].
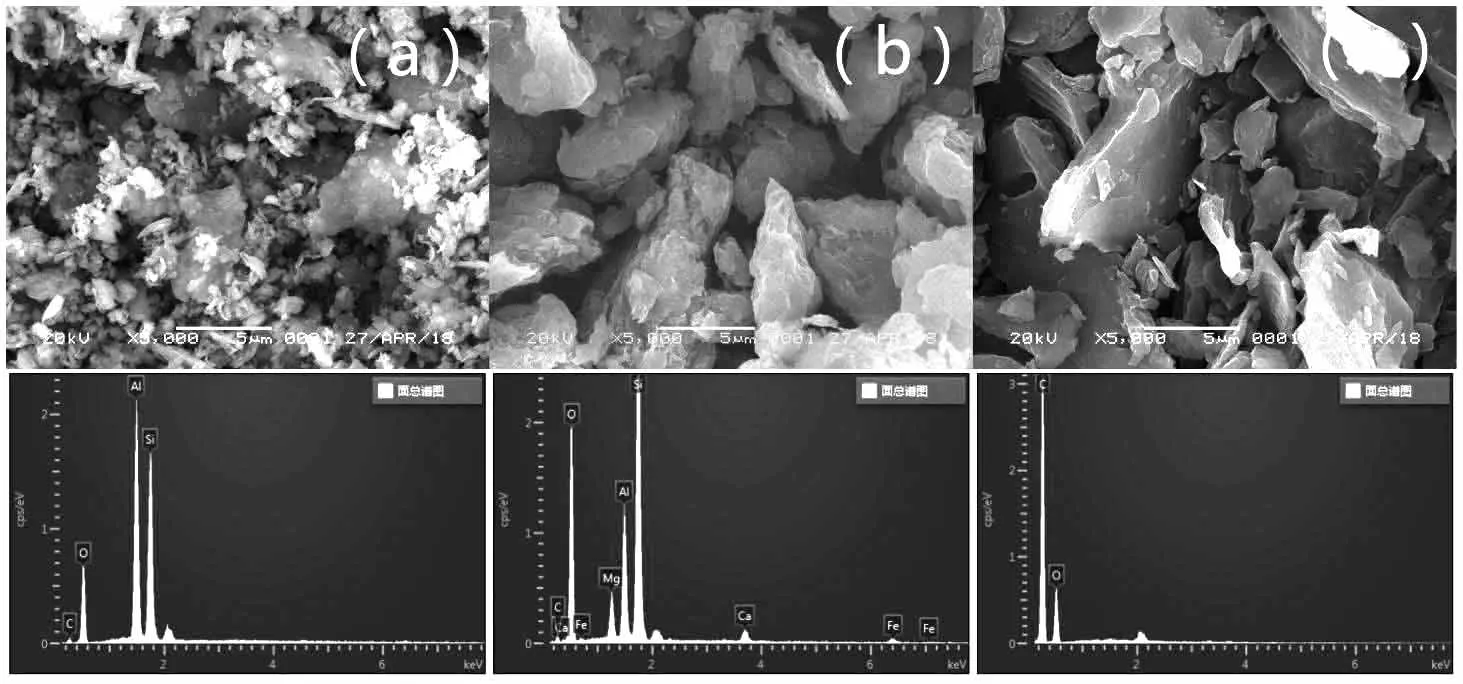
(a)高岭土 (b)蒙脱土 (c)生物炭
3种吸附材料中所含基团种类及含量如图2所示. 吸收特征峰在3 500~3 700 cm-1附近为缔合-OH的伸缩振动峰; 吸收特征峰在1 650 cm-1附近为-COOH伸缩振动; 吸收特征峰在1 410 cm-1附近为C-H伸缩振动; 吸收特征峰在1 100 cm-1附近为C-O伸缩振动. 3种吸附材料中, 蒙脱土所含基团含量最高. 吸附材料主要通过自身中的-COOH和-OH基团吸附水中重金属铅, 可以用以下两个反应方程表示[3,27-28]:
nC-COOH + Pb2++H2O → nC-COOPb++H3O+
nC-OH + Pb2++H2O → nC-OPb++H3O+
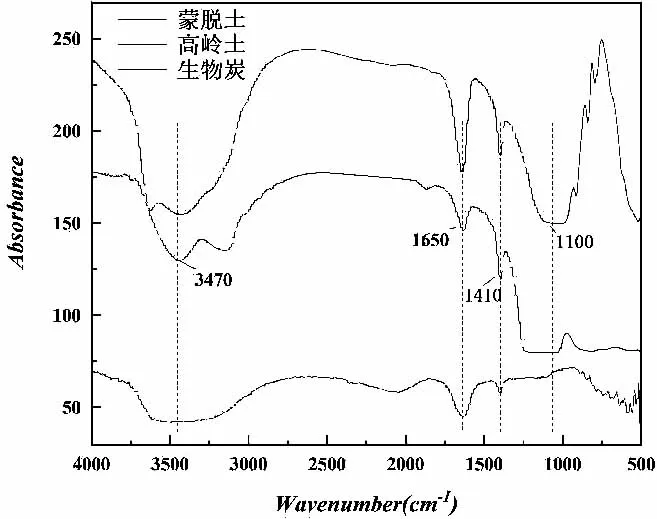
图2 3种吸附材料的红外吸收光谱图
2.2 溶液初始pH对材料吸附性能的影响
溶液初始pH值是影响重金属离子吸附的重要因素.在酸性条件下,大量的氢离子可以抑制生物炭对Pb(Ⅱ)的吸附. 一旦pH>6.0, Pb(Ⅱ)在水中的存在形式转化为Pb(OH)2,从离子状态到胶体状态.图3结果表明在溶液初始pH=5.0~6.0时,3种材料对Pb(Ⅱ)的去除率最佳,这也与已有研究结论一致[29-30]. 由于原溶液初始pH=5.0时吸附效果最佳,故后续实验中溶液初始pH设定为5.0.
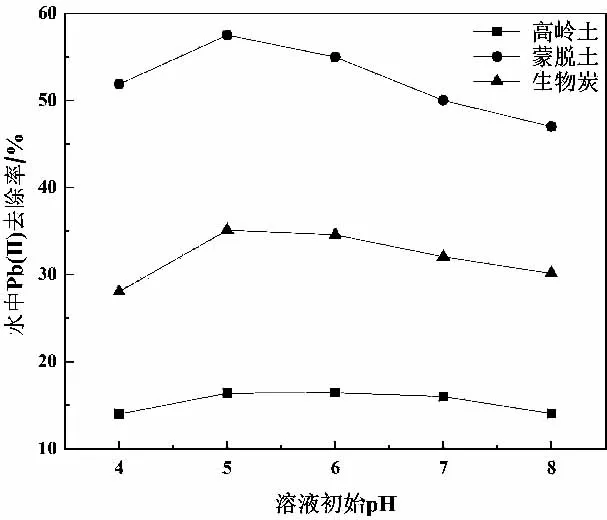
图3 3种吸附材料在不同溶液初始pH下对Pb(Ⅱ)的去除率
2.3 接触时间对材料吸附性能的影响
3种吸附材料对水中重金属Pb(Ⅱ)的吸附平衡与接触时间关系如图4所示,该吸附平衡曲线表明高岭土在20 min内达到吸附平衡;而生物炭和蒙脱土在40 min内达到吸附平衡.随着吸附材料与重金属的接触时间延长,水中重金属Pb(Ⅱ)浓度逐渐趋于稳定.

图4 3种吸附材料的吸附平衡曲线
2.4 吸附动力学模型分析
3种吸附材料的实验数据分别用准一级吸附动力学方程式(1)和准二级吸附动力学方程式(2)进行拟合,拟合参数如表2所示.
qt=qe(1-e-k1t)
(1)
(2)
其中t为吸附时间(min);k1为准一级吸附动力学方程速率常数(min-1);k2为准二级吸附动力学方程(min-1);qt和qe分别为在t时刻,吸附材料对Pb(Ⅱ)的吸附量(mg·g-1),以及吸附反应达到平衡时,吸附材料对Pb(Ⅱ)的最大吸附容量(mg·g-1).
根据表2结果可知,3种吸附材料的吸附动力学更符合准二级吸附动力学方程(R2均为0.999),这说明3种材料对Pb(II)的吸附主要以化学吸附为主[31].通过准二级吸附动力学方程拟合计算所得最大吸附容量值(qe)与实验值(qe,exp)非常接近. 最大吸附量为: 蒙脱土(56.454 mg·g-1)>生物炭(35.530 mg·g-1)>高岭土(16.583 mg·g-1).
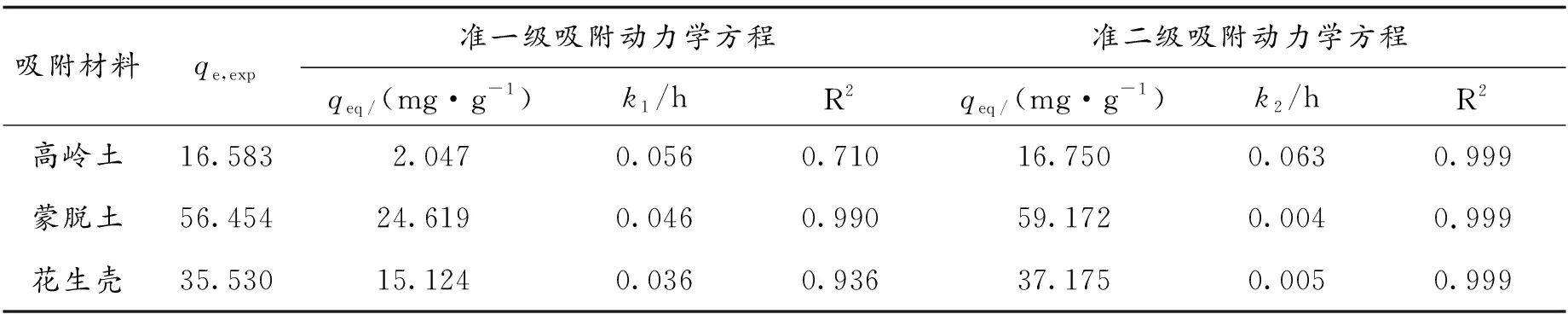
表2 吸附动力学方程拟合参数
2.5 吸附热力学模型分析
3种吸附材料的实验数据分别用Langmuir模型式(3)和Freundich模型式(4)吸附热力学模型进行拟合,拟合参数如表3所示.
(3)
(4)
其中Ce为吸附反应达到吸附平衡时溶液浓度(mg/L);qe为吸附反应达到平衡时,吸附材料对Pb(Ⅱ)的最大吸附容量(mg·g-1);qm为吸附剂对Pb(Ⅱ)的最大吸附量(mg/g);kL为Langmuir平衡常数(L·mg-1);KF为与吸附剂吸附能力有关的Freundich常数,mg1-n·Ln·g-1;n为与吸附材料和吸附质表面相互作用强度有关的参数.
根据表3拟合参数结果表明,Langmuir模型(R2=0.924~0.972)比Freundlich模型具有更高的R2值(R2=0.649~0.937),3种材料的吸附热力学更符合Langmuir模型[32].这表明3种材料对重金属Pb(Ⅱ)的吸附反应属于单分子吸附.Langmuir模型中,吸附反应达到吸附平衡后,3种材料对Pb(Ⅱ)的最大吸附量(qm)接近于实验值(qe,exp).同时根据Freundlich模型中,1/n的值在0~1(1/n=0.316~0.615)之间,表明Pb(Ⅱ)易于被3种吸附材料吸附.
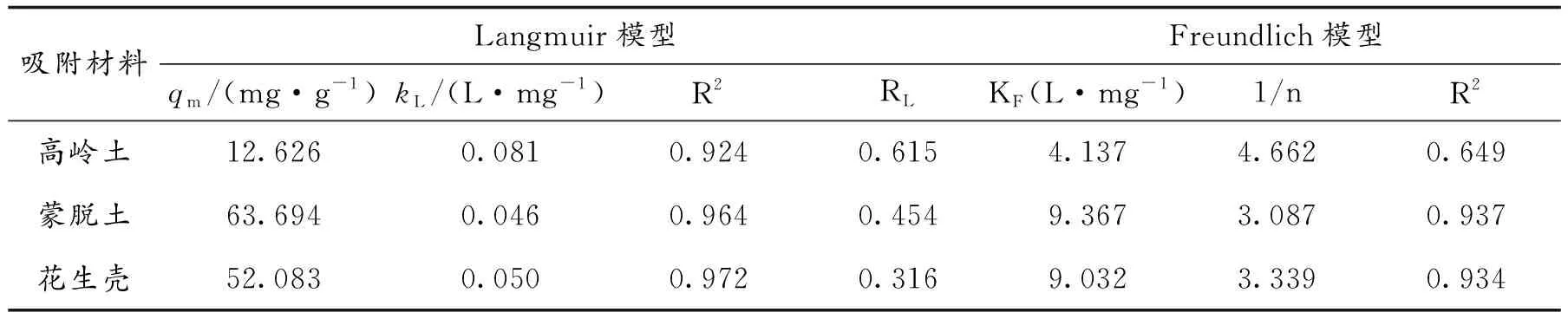
表3 Langmuir和Freundlich模型拟合参数
4 结论
研究结果表明:
(1)从BET,SEM,EDS和FTIR中可知,蒙脱土具有较大比表面积和孔隙,丰富的金属元素以及含氧官能团,能够为重金属提供更多的吸附位点,从而提高其对水体重金属铅的吸附能力.
(2)溶液初始pH=5.0时,3种材料对重金属Pb(Ⅱ)的去除率最佳.同时吸附材料的吸附平衡时间不同,高岭土在20 min内达到吸附平衡;而生物炭和蒙脱土在40 min内达到吸附平衡.
(3)3种吸附材料对重金属Pb(Ⅱ)的吸附动力学更符合准二级动力学方程,表明该吸附反应以化学吸附为主;吸附热力学均更符合Langmuir模型,表明3种材料对重金属Pb(Ⅱ)的吸附反应为单分子吸附.
总之,蒙脱土对水体重金属Pb(Ⅱ)的吸附效果最好,具有较好的应用潜力与发展前景.生物炭与粘土复合材料的性能有待进一步研究.

