3D胸腔镜肺叶切除术治疗原发性肺癌的疗效分析
万志华 吴瑞锋 刘伟明 蔡艳 刘博 于宁 姚轶超
肺癌预后不佳,手术切除是获得良好生存质量的治疗方案,电视胸腔镜辅助肺叶切除术逐渐受到临床医生青睐[1]。电视胸腔镜辅助肺叶切除术微创、术后恢复快,在胸外科领域中运用较广[2]。二维(2D)胸腔镜肺叶切除术是肺癌微创手术代表,其临床疗效受到临床肯定,然而2D胸腔镜肺叶切除术手术视野容易失真、术中器械操作角度受限、操作技术较复杂。三维(3D)胸腔镜肺叶切除术是2D胸腔镜肺叶切除术改良版,作为解剖性术式重点在于立体性、层次感,继承了传统开胸手术手术视野,便于手术操作者充分观察病灶,保障术中精准性、精细性和安全性,提高手术效果[3-4],有效弥补了2D胸腔镜肺叶切除术的不足。本研究将3D胸腔镜肺叶切除术用于原发性肺癌的治疗,对手术情况、淋巴结清扫数目和术后外科病理分期、肺功能指标、疼痛情况、并发症情况等进行分析。
对象与方法
一、对象
2018年10月~2020年2月我院收治的原发性肺癌病人120例。纳入标准:(1)符合《肺癌诊断治疗学(精)》诊断标准,临床分期为Ⅰ~ⅢA 期,经病理检查确诊[5];(2)肿瘤直径<6 cm,且无肺部、纵隔淋巴结转移;(3)符合胸腔镜肺叶切除术指征,且对手术可耐受;(4)预计生存时间超过半年;(5)病人及家属知情并签署知情同意书。排除标准:有放化疗治疗史;影像学检查证实肿瘤已侵犯周边器官;合并其他恶性肿瘤;存在心、肝、肾等器质性病变。根据手术方式不同分为观察组和对照组,观察组67例,男36例,女31例,年龄45~75岁,平均年龄(61.69±8.65)岁,肿瘤直径25~46 mm,平均直径(37.22±7.89)mm;病变部位:右肺上叶22例、右肺中叶9例、右肺下叶20例、左肺上叶11例、左肺下叶5例;病理分期:ⅠA 16例,ⅠB 18例,ⅡA 13例,ⅡB 9例,ⅢA 11例。对照组53例,男27例,女26例,年龄46~76岁,平均年龄(61.71±8.80)岁,肿瘤直径25~47 mm,平均直径(35.69±7.74)mm;病变部位:右肺上叶21例、右肺中叶9例、右肺下叶13例、左肺上叶7例、左肺下叶3例;病理分期:ⅠA 16例,ⅠB 14例,ⅡA 7例,ⅡB 9例,ⅢA 7例。两组一般资料比较差异无统计学意义(P>0.05)。本研究经医院医学伦理委员会批准。
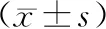
表1 两组手术情况比较
二、方法
1.手术方法:两组病人均由同一组医护人员完成手术,病人行全麻,将管插入双腔气管,实行单肺通气;取健侧卧位,垫高腋窝以下胸部,常规消毒。对照组为2D胸腔镜肺叶切除术,采用2D电视胸腔镜系统(德国 Karl Storz GmbH& Co.KG公司)确定病灶,切口位置选择第4和第5肋间,光源口选择第7和第8肋间,辅助操作口选择第7和第8肋间肩胛下角线1.5 cm,切口长度4 cm。依次游离下肺韧带、肺静脉,充分显示肺动脉主干及其分支,切割叶间裂、肺动静脉,将支气管夹闭,手术复位后进行膨肺,在肺复张较好,无漏气情况下切断支气管,不采用肋骨开胸器,保护切口,系统性清扫淋巴结,避免伤害膈神经、迷走神经。观察组为3D胸腔镜肺叶切除术,采用全高清3D电视胸腔镜系统(德国 Karl Storz GmbH& Co.KG公司),手术操作者佩戴3D眼镜,切口位置选择腋前线第4肋间,切口长度4 cm,也是观察孔和操作孔,手术操作者和扶镜助手站在腹侧处,进入操作孔,合理调整镜头角度,便于直线切割缝合器通过操作孔;手术操作者佩戴3D偏振眼镜,在3D电视上显示手术画面,通过立体定位胸腔镜观察胸腔,其余操作同对照组。
2.观察指标:(1)手术情况:记录手术时间、术中出血量、术后24小时引流量、术后引流管留置时间、术后住院时间。(2)淋巴结清扫数目和术后外科病理分期:病理分期参照《肺癌诊断治疗学(精)》[5]。(3)肺功能指标:术前和术后3个月采用多肺功能检测仪[老优(上海)仪器设备有限公司,BTL)]检测用力呼气肺活量(forced expiratory vital capacity,FVC)、用力呼气肺活量1秒量(forced expiratory volume 1 second,FEV1)、一氧化碳弥散量(diffusingcapacity for carbon monoxide,DLCO)。(4)疼痛情况:术后及术后3个月采用视觉模拟疼痛评分(visual analogue score,VAS)[6],其中轻度疼痛为0~3分,可忍受;中度疼痛为4~6分,疼痛较强影响休息,但可以忍受;重度疼痛为7~10分,病人疼痛加强,无法忍受。(5)并发症:包括肺部感染、肺不张、心律失常等方面。
三、统计学方法

结果
1.两组手术情况比较见表1。结果表明,观察组手术时间、术后引流管留置时间、术后住院时间均短于对照组,术中出血量、术后24小时引流量低于对照组,差异有统计学意义(P<0.05)。
2.两组淋巴结清扫数目和术后外科病理分期比较见表2。结果表明,两组淋巴结清扫数目和术后外科病理分期比较,差异无统计学意义(P>0.05)。
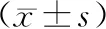
表2 两组淋巴结清扫数目和术后外科病理分期比较
3.两组肺功能指标比较见表3。结果表明,两组术前FVC、FEV1、DLCO比较,差异无统计学意义(P>0.05);术后3个月,两组FVC、FEV1、DLCO改善,且观察组FEV1优于对照组,差异有统计学意义(P<0.05)。
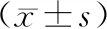
表3 两组肺功能指标比较
4.两组VAS评分比较见表4。结果表明,术后两组VAS评分比较,差异无统计学意义(P>0.05);术后3个月两组VAS评分均减小,且观察组小于对照组,差异有统计学意义(P<0.05)。
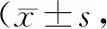
表4 两组VAS评分比较分)
5.两组并发症比较见表5。结果表明,观察组并发症发生率(5.97%)低于对照组(18.87)%,差异有统计学意义(P<0.05)。
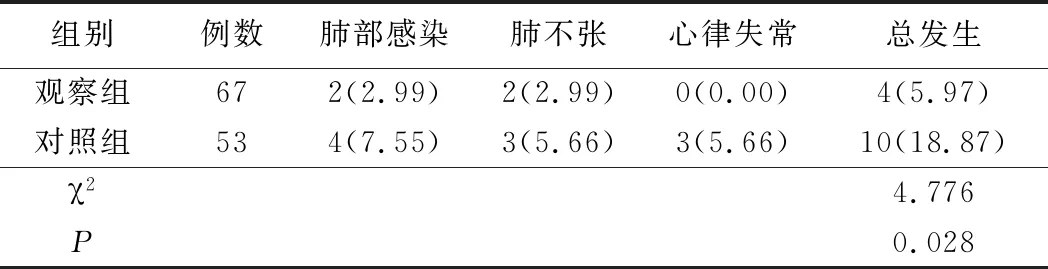
表5 两组并发症比较(例,%)
讨论
近年来,原发性肺癌发病率呈上升趋势。临床治疗主要采用手术切除肿瘤,防止肺癌转移、复发[7]。随着医疗技术进步,胸腔镜发展日趋成熟,为原发性肺癌提供了更加安全的治疗手段。2D胸腔镜肺叶切除术属于微创手术,切口相对传统开胸手术较小、疼痛较轻,且安全性好。但2D胸腔镜肺叶切除术在空间感、深度感方面存在一定局限性,手术误伤风险及手术操作难度增加[8-9]。3D胸腔镜肺叶切除术是在2D胸腔镜肺叶切除改良得到,是集3D仿真视野、高清立体成像、精准定位病变位置、高适应性于一体的手术方式。术中操作者佩戴3D 眼镜可清晰观察病灶周围血管、神经组织等3D 立体结构,防止手术误伤,简化手术操作步骤[10-11]。
本研究结果表示,观察组手术时间、术后引流管留置时间、术后住院时间均短于对照组,术中出血量、术后24小时引流量低于对照组。与2D胸腔镜肺叶切除术比较,3D胸腔镜肺叶切除术手术效果更好。3D胸腔镜肺叶切除术手术具有较好的纵深效果,20倍放大视觉效果能够帮助手术操作者更加直观清晰观察病灶组织及淋巴结,降低误伤风险。3D胸腔镜肺叶切除术手术比2D胸腔镜肺叶切除术更容易操作,原因在于在初次操作腔镜器械时也能较好地进行抓持、分离、切割操作,减少了学习曲线,增强了眼手操作协调性,降低血管出血及肺组织撕裂风险,便于对目标组织自由控制缝合[12-13]。3D胸腔镜肺叶切除术空间深度信息及空间比例均优于2D胸腔镜肺叶切除术,能适当扩宽手术适应证,增加手术安全性[14]。有研究表示,胸腔镜手术时间较传统开胸手术短,且全胸腔镜手术与传统开胸手术在淋巴结清扫方面无明显差异[15]。结果表示,两组淋巴结清扫数目和术后外科病理分期比较无明显差异。提示3D胸腔镜肺叶切除术入路不影响手术效果,与上述研究结果一致。3D胸腔镜肺叶切除术会影响肺功能,但安全性较高,检查FVC可观察病人肺部通气功能障碍程度,DLCO能反映肺功能异常情况,两者联合FEVI可较好地反映肺损伤[16]。有研究表示,传统开胸手术对肺功能影响较大,会降低肺功能,而3D胸腔镜肺叶切除术通过特殊操作孔,对肺功能影响较小[17]。本研究结果表示,观察组术后3个月FEVI优于对照组,而两组FVC与DLCO无明显差异。提示3D胸腔镜肺叶切除术对肺功能影响较小。有研究表示,3D胸腔镜肺叶切除术优势在于手术视野较广、解剖层次清晰、纵深感和立体感均较强,更利于手术操作者找到手术解剖层面,评估周围组织,减少术中出血,进而提高手术安全性[18-19]。本研究结果表示,观察组术后3个月VAS小于对照组,并发症发生率明显低于对照组。提示3D胸腔镜肺叶切除术可明显较少原发性肺癌病人术后疼痛,降低并发症发生率。
综上所述,3D胸腔镜肺叶切除术治疗原发性肺癌可缩短手术时间、术后引流管留置时间、术后住院时间,减少术中出血量、术后24小时引流量,改善肺功能,减少疼痛,且并发症发生率较低。

