中药“药效基团-功效假说”及其应用
张文晋,曹 也,常丽坤,王 升,康传志,周 利,郭兰萍
·专 论·
中药“药效基团-功效假说”及其应用
张文晋1,曹 也2,常丽坤3,王 升1,康传志1,周 利1,郭兰萍1*
1. 中国中医科学院 中药资源中心,北京 100700 2. 安徽中医药大学药学院,安徽 合肥 230012 3. 广东药科大学中药学院,广东 广州 510006
中药现代化应是在继承传统理论和经验的基础上,利用现代科学技术,加以研究、提高和发展。随着药效团虚拟筛选技术在计算机辅助药物设计方面应用的日趋成熟,该技术在中药现代化研究中的应用已成为可能。从中药“药效团药性假说”出发,分析“药效团”的科学内涵,提出适用于中药现代化研究的“药效基团-功效假说”。
药效团;药效基团-功效假说;药效成分辨识;ADME-Tox;靶标搜寻
中药基本是以混合物的作用为一个功效单位。这些混合物中,有的为同类化合物,如基本母核(分子骨架)一致或基本基团一致。这些化合物根据相同结构母核可分为苯丙素类、醌类、黄酮类、鞣质类、萜类、甾体及其苷类、生物碱类7大类[1]。研究表明相同类型的化合物往往具有某些相近的药理作用,只是作用程度有所不同[2];但是属于同一类的化合物又可能具有不同的药理活性,如分子结构完全相同的光学异构体具有不同的药理作用;中药的药效物质一部分是其原型成分,一部分是原型成分在体内的代谢产物[3],因为缺乏对中药体内代谢的系统研究,对于一味中药而言,其药效物质是以何种形式发挥药效并不清楚。另一方面,中药中有效成分的含量一般很低,而中药多数以口服为主,进入体内后血药浓度往往很低,中药为什么还能产生药效?针对此类问题,学者提出了以下几种理论假说:(1)疾病缩减效应假说[4],认为单味中药的有效成分结构往往相似,从构效关系上看,其作用靶点即病理环节可能大致相同,在治疗上存在疗效叠加效应或竞争拮抗效应。(2)中药显效理论[3,5],认为中药药效物质“显效形式”的集合或叠加是药效的核心物质基础;中药中各药效物质(显效型)在各个单靶点上的“叠加作用”以及各靶点之间多成分的协同作用,共同构成了中药发挥药效的药理作用机制。而产生“叠加作用”的前提是上述各化合物具有相同的药效基团(化合物骨架的一部分或取代基等),可产生相同的生理/药理效应[3,5]。(3)分子药性假说。中药化学、中药药理学及临床实践证明中药中的化学物质(蛋白质、糖类、生物碱、黄酮、萜类等)是其药效物质基础。中药有效成分在体内的分布是归经的基础,归经的物质基础则是受体(核酸、酶、受体等生物大分子)。据此,李石生等[2]提出了中药“分子药性假说”,认为中药的性味是由中药所含有的化学物质所决定的。(4)药效团药性假说。一味中药所含有的全部化合物分子中,不是所有分子都是有效成分,往往是其中一些具有一定骨架的化合物或不同骨架化合物组成的分子群具有特定的生理活性或治疗作用。在此基础上,李爱秀提出了“药效团药性假说”[6],认为药物分子的药性蕴含在药物分子的特定结构中,这里的“特定结构”指的是药物分子与某个受体产生相互作用时所具有的“药效团”。该理论中的药效团指的是化合物微观的三维结构,药效团理论从分子水平上揭示了中药药效物质起效的作用机制。然而,中药药性理论体系复杂,基于化学特性的中药药性辨识技术研究至今仍未取得突破性进展。
中药功效是联系中药药理与临床实践的枢纽,中药功效本身也具有较强的组学性质,如活血化瘀与现代医学的多种疾病(如冠心病、心绞痛、脑出血、肿瘤及呼吸衰竭等)相关联;而中药的临床功效又是以中药药理活性为基础的,中药功效与多种药理活性相对应,如清热解毒与解热、抗病毒、抗菌、抗炎等药理活性相对应,二者之间具有较强的对应关系[7]。疗效是中医药的生命力,合理诠释中药功效的科学内涵有助于科学指导中药新药研发和中医临床实践。本文从中药“药效团药性假说”出发,分析“药效团”的科学内涵,提出适用于中药现代化研究的“药效基团-功效假说”。
1 中药药性物质基础
中药药性是指导中医药临床应用的重要依据。现代研究表明,辛温药有效成分以挥发油为主[8],甘平药有效成分以多糖类成分为主,酸味药有效成分多以酚酸、鞣质等成分为主,苦寒药有效成分为生物碱、苷类等,咸类药以无机盐或有机盐类等为其主要活性物质[9]。继而发现中药化学成分中分子结构与药性相关,即中药所含化合物分子中一类或一群基团作用于人体后产生相似的作用,而且,这种相同类型的化合物(有效部位)临床效果良好,且作用缓和持久[2]。药物分子的基本母核(分子骨架)一致的化合物,或者是基本基团一致的化合物,与中药药性密切相关,且具有一定的规律,特定骨架的分子具有一定的生理活性,可能特定骨架的分子或分子群具有一定的性味和归经[10]。归经主要是药物作用所及或药物效应的定向、定位,即药物作用的区域性和选择性,是空间和功能的综合。在回顾当前中药药性理论研究现状的基础上,张冰等[11]提出了“药性三要素”假说,即应从药性与化学成分、机体状态以及生物学效应这3要素及其之间的关联关系进行整体、系统探讨中药药性。
2 中药“分子药性假说”
结合中药化学和中药药理学的研究成果,有学者认为,各种化学物质(蛋白质、糖类、生物碱、黄酮、萜类等)的存在是中药性味的物质基础,每味中药都是一个大型的天然分子库;受体(核酸、酶、受体等生物大分子)是归经的物质基础。基于此,李石生等[2]最先提出“中药理论体系——分子药性学假说”,其中分子是指一定骨架的同类化合物群体或不同类型化合物组成的分子群,即中药中包含的有效成分。该假说认为中药性味取决于其所含的化学成分,有共同物质基础属性则会有相同药性,如解表药多数味辛、归肺经,挥发油是其共同的物质基础[12]。中药药性的多样性本质上是由中药化学成分的分子多样性决定的,中药对机体的多靶点作用机制由组成中药的分子多样性及其药性的多样性决定。刘培勋等[13]提出“中药药性物组学”的概念,认为中药药性在时间维和空间三维中对特定生物体的作用是中药中发挥特定药性作用的分子集合,该集合被称为“中药药性物质组”。而匡海学等[14]提出的“中药性味的可拆分性、可组合性”也是建立在中药诸多化学成分各自承载的分子药性的基础之上。因此,抽象的中药药性是具有物质基础的,是中药所含化学成分的高度概括。“分子药性假说”在分子水平上研究传统中药药性理论中性味与归经之间的关系,即中药中特定分子骨架的有效成分(药物小分子)与受体(生物大分子)之间的关系,但“分子药性假说”中的“分子骨架”和“特定骨架分子”等概念并不明确。
3 药效团
药物的化学结构与其生物活性(包括药理和毒理作用)之间的关系密切,即构效关系在现代药理学中已经被揭示。早在1909年,Ehrlich就提出了“pharmacophore(药效团、药效基团、药效结构)”的概念,认为药物的药理作用或毒性归属于某些特定的化学活性基团或毒性团(toxicophore)[15]。此概念可以解释为何结构相似的化合物具有相近的药理作用,但对于某些化学结构微小的变化就可以导致完全不同的生物活性,而某些化学结构完全不同的化合物又会显示出相同或相近的生物活性这一问题很难作出解释。药效团的现代定义最初是由Kier于1967年提出的,并于1971年首次出现在出版物中[16]。其定义不再是“化学基团”,而是“抽象特征”。药效团被国际纯粹与应用化学联合会(International Union of Pure and Applied Chemistry,IUPAC)定义为空间和电子特性的集合,是确保与特定生物靶点的最佳超分子相互作用并触发(或阻断)其生物反应所必需的[17]。药效团并不代表分子或功能基团的真正结合,而是一个纯粹的抽象概念,表征一组化合物对其目标结构的共同分子相互作用能力。该定义摒弃了药物化学中常见的一种“误用”,即把简单的化学功能命名为药效团,如胍、磺酰胺或二氢咪唑等,或典型的结构骨架,如黄酮、吩噻嗪、前列腺素或类固醇等。这种“误用”可能更符合药效团的原始含义。如今在进行药效团建模时,普遍利用“抽象特征”(如氢键受体、亲水中心等)以及特定“化学基团”(如羰基氧)的组合,并定义它们的3D关系。
药效团是一组活性分子所共有的分子相互作用特征的最大公分母,是负责生物效应的分子特征的模式。药效团模型既利用了分子拓扑学相似性又利用了基团的功能相似性,运用了生物电子等排体(bioisosterism)的概念使得模型更加可靠。药效团模型的生成是为了更好地理解大分子靶点(如受体、酶或离子通道)与小分子配体的相互作用,分子中的每一种原子或基团如果表现出与分子识别有关的某些性质,就可以归结为药效团特征。这些分子模式包括氢键供体(hydrogen bond donor,HBD)、氢键受体(hydrogen bond acceptor,HBA)、疏水相互作用(hydrophobic interactions,H)、芳香环系统(ring aromatic,RA)、正电离基团(positive ionization,PI)和负电离功能(negative ionization,NI)以及任何可能的组合(图1)。郭亦然[18]认为,药效团是化合物产生药效的关键特征的集合,是药效结构的共同属性,是有效成分结构的更高层次,将中药的主要成分群以药效团的形式进行回归和分析,是从还原论研究结果向系统论回归的一条有效途径。
尽管人们对药效团的内涵基本已达成共识,但许多药物化学家仍然认为药效团为某些特定的功能群,因为通常它们与生物活性有关。药物化学家认为药效团包含2种不同的含义,即“赋予活性的分子片段,通常也称为优势结构”[19]和“一组具有相似药理特征并被靶蛋白的相同位点识别的分子的最高共同特征”。功能性分子片段包含药物产生生物活性所必须的结构单元,是对负责生物效应的“化学基团”这一术语的传统定义。代表性的优势结构有芳基乙胺(包括吲哚基乙胺)、二苯甲烷衍生物、三环精神药物和磺酰胺、二氢吡啶[20]、苯并二氮杂䓬[21]、-芳基哌嗪、联苯、哒嗪等。例如,呋喃酮是一类具有多种药理活性的杂环化合物,多年来,含呋喃酮环系统的化合物在药物发现、设计和开发大量药理活性部分方面发挥了重要作用,被认为是生物活性物质的药效团之一[21]。喹唑啉是药物研究中最常见的杂环核心,是因为其具有广泛的药理潜力且其大量衍生物被认为是许多生理相关性和药物应用的显著结构合成子[22]。药效团第2种含义通过理性的计算机辅助推理来进行药物设计。主要涵盖3个方面:(1)建立相关的药效团模型,该模型可通过构象搜索和分子叠合模拟配体分子的活性构象,据此来推断和解释受体与配体分子之间可能的作用模式;(2)药效团模型可用于分子结构的辅助改造,对于复杂分子可以通过保留药效团结构进行结构简化的同时保持生物活性;(3)药效团最直接的用途是判断一个分子是否具有某一类药效特征。基于药效团的虚拟筛选技术已成为先导化合物发现、优化和药物分子设计的重要辅助手段[23-25]。将药效团技术应用到中药研究中,可提高有效成分辨识的速度和成功率,且在保持中医药的特色与优势下,可为现代中药研究提供一种新的思路和方法[26-28]。
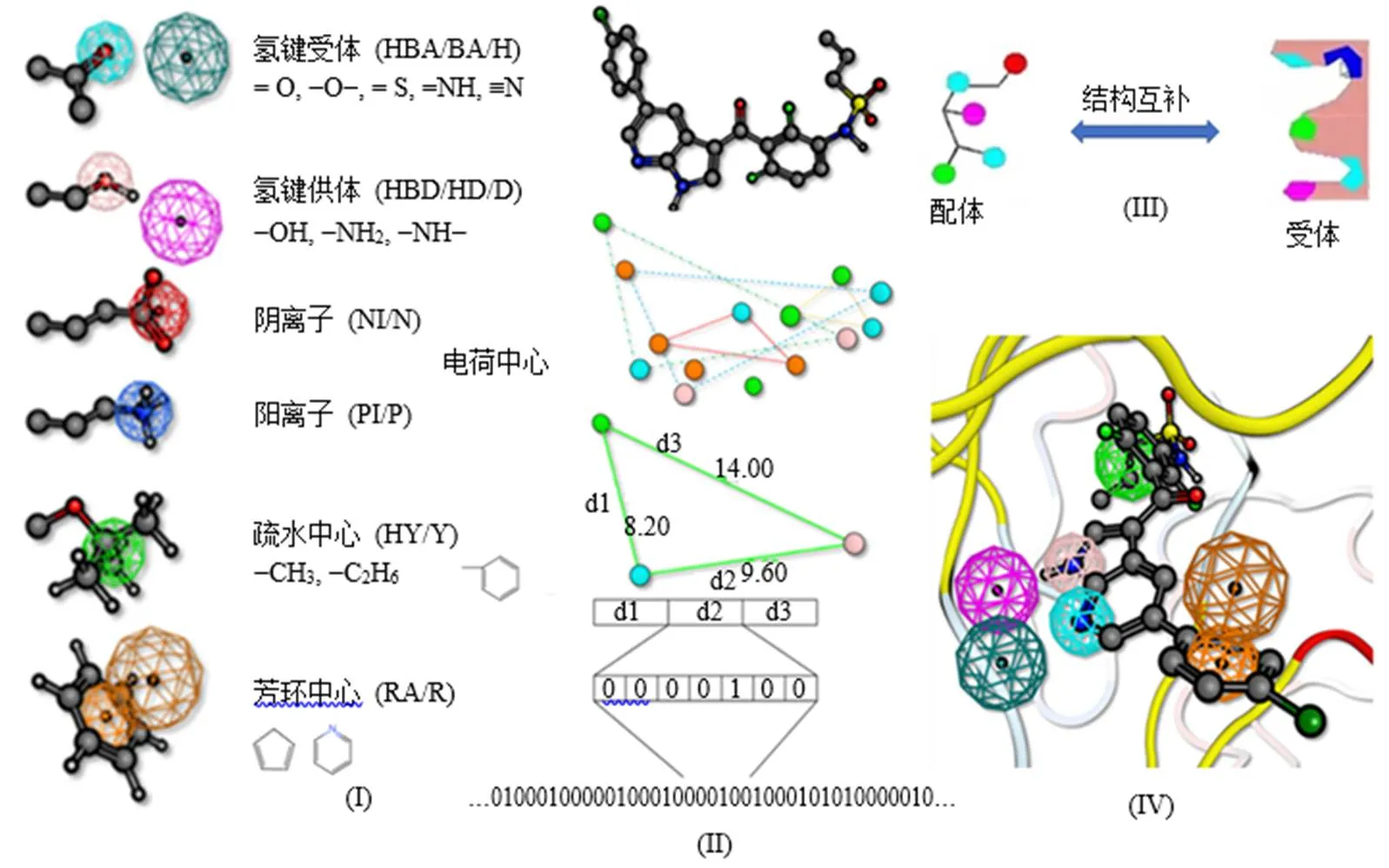
图1 常见的药效团特征(I)、药效团表示方法(II)、配体与受体结构互补性结合(III)、配体受体结合的三维构象(IV)
4 中药“药效团药性假说”
结合现代药理学理论和药效团理论,李爱秀[6]认为“分子药性假说”中的“分子骨架”和“特定骨架分子”应该是“药效团”和“具有特定药效团的分子”,基于此,提出了“药效团药性假说”:(1)分子具有药性,其药性是有规律的。药物分子的药性蕴含在与某个受体产生相互作用时所具有的药效团中。(2)中药有效成分具有化学成分和药效团多样性的特点。作用相同或相近的化学成分具有相同的药效团,反之亦然,化学成分多样性是药效团多样性的前提。(3)中药有效成分所含药效团的多样性,决定中药药性的多样性;中药药性的多样性,决定中药对机体的多靶点作用机制。该假说将药物的微观三维分子结构特征与其分子作用机制对应起来,利用现代科学新知识和新理论,从分子水平揭示中药物质基础产生疗效的作用机制。在此基础上,张燕玲等[29]提出了“物质决定药性,物质基础共同属性与药性之间存在内在相关性”这一假说,建立了中药药性与中药药理作用的数据库,并利用中药有效成分族辨识技术,以活血化瘀药为研究对象,初步探讨了以药效团为物质基础共同属性与中药药性的内在相关性。
综上所述,基于中药药性-化学成分结构关系的规律研究认为,分子药性蕴含在药物分子的特定结构中,从化合物结构特征出发,挖掘对药物活性、药动学-毒性反应过程(吸收、分布、代谢、排泄、毒性反应,absorption,distribution,metabolism,excretion,toxicity,ADME-Tox)起决定作用的药效、药动和毒性基团或骨架,可为研究分子药性规律提供依据[30]。盛良[31-32]采用广义酸碱原则和电子得失解释中药的“四气五味”,并利用青黛有效成分靛玉红分子结构中药效团为给电子体的特征,判断出其味辛、咸,性寒,与其临床功效符合。Zhang等[33]借助中药有效成分族辨识技术,以活血化瘀中药为研究对象,以血管紧张素转换酶(angiotensin converting enzyme,ACE)、血小板活化因子(platelet activating factor,PAF)、血管紧张素II(angiotensin II,Ang II)和5-羟色胺2A(5-hydroxytryptamine 2A,5-HT2A)4个受体为载体,初步探讨了药效团与中药药性的内在关联。张亚超等[34]利用定量构效关系(quantitative structure-activity relationship,QSAR)研究技术对代表性平性中药中的有效成分的化学结构进行数字化处理,选取17种典型分子骨架特征和官能团用于表征各种有效成分的结构信息,利用支持向量机分类,发现黄酮类成分最能显示出平性与非平性药的差异。中药药性理论体系的复杂性,同时由于技术条件的限制中药药性辨识技术的研究至今仍未取得突破性进展。笔者认为,单纯从化学成分角度本身不足以解释中药的药性,如一些有效成分比较明确的中药,也无法用这些有效成分表征其药性。中药药性来自药物自身所含的有效成分、生物活性及其药理作用,与其品种、产地和自然环境等多种因素有关。中药性能的认识和论定,是对中药各种性质和作用特征的高度概括。
5 中药“药效基团-功效假说”
中药临床应用是多样的,中药功效涵盖其对不同的中医证候及中医证候群的作用,具有较强的组学性质,如活血化瘀与现代医学的多种疾病如脑出血、冠心病、心绞痛、肿瘤及呼吸衰竭等相关联。中药的临床功效又是以中药药理活性为基础的,中药功效与多种药理活性相对应,如清热解毒与抗菌、抗病毒、解热、抗炎等药理活性相对应[7]。可见中药功效是联系中药药理与临床实践的枢纽。现代药理学认为药物分子与受体靶点结合时,为了要与靶点之间产生更好的几何匹配和能量匹配,会采用特定的构象,也就是所说的活性构象。研究发现药物分子中的基团对于活性的影响不同,具有相同活性的分子往往具有相同的某些特征。药效团就更好地说明了那些对活性有重要贡献的特征。最初药效团是指具有活性必需特征的原子的分子框架,后来进一步明确为“分子中的一组能够识别受体,并能形成分子生物活性的结构特征”[1]。虽然之后对药效团的定义表述方法略有不同,但对其基本内涵的认知已达成共识,即药物分子中对活性起重要作用的结构特征的空间排列形式[2]。西方医学与中医药在理论、方法大相径庭,但均以疗效作为“金标准”。与其“原理之争”,不如聚焦共性,守正创新。基于此,笔者提出中药“药效基团-功效假说”(图2),主要包括以下内容:(1)物质决定活性,物质基础共同属性与活性之间存在内在相关性,活性与功效相关。(2)药效基团是用以表征具有相同功效的有效成分的共性化学特征,是对有效成分活性特征的抽象与简化;是以计算辅助药物设计中抽象的“药效团”概念为基础,同时也重视药物化学中具体的“活性基团”,在具体的应用过程中注重二者的有机结合。(3)功效的产生是同一靶点上共性显效型药效基团的“叠加效应”及在此基础上多靶点协同效应的共同作用。在药物分子少、靶点分子多的情况下,不同的显效型分子可相继与靶点分子结合,发生叠加作用,当“靶点充分占位”时,药效开始启动,既有浓度上的叠加作用又有时间段先后的叠加作用,使得药效得以持久[3]。
图2 中药“药效基团-功效假说”示意图
中药“药效基团-功效假说”与中药“药效团药性假说”不同,单纯从化学物质角度不足以或不适宜诠释中药药性,相反的,有效成分是药理作用的物质基础,药理作用直接与功效相关联,中药功效直接反映中药疗效,而疗效是所有医学的共同语言,抽象的“药效团”理论基于现代药理的受体-配体理论。中药产生药效或不良反应是一系列复杂过程的综合和宏观表现,本质上是“显效物质”同机体内生物大分子靶点之间产生特异性相互作用引发的。分子间的相互识别与结合是发生相互作用的前提,相互作用的强弱程度又取决于二者之间物化性质和化学结构间的适配程度,适配程度和适配分子的“叠加效应”就决定了药物药效和毒副作用的高低。此互作效应是在三维空间进行的,一方面,作用于同一受体的分子化学结构微小变化可能导致完全不能结合,有着严格的空间分子识别作用;另一方面,化学结构完全不同的化合物又可能与同一受体结合,有着类似的生物活性。因此,化合物的化学类别和其二维结构不能说明其与受体的作用方式。换言之,三维药效团模型是研究中药药效物质基础及其作用机制的有益策略。而具体的“优势结构”或“活性基团”来源于药物化学领域实际的活性验证,二者均具有借鉴价值。基于化学信息学和知识发现的活性表征方法很大程度上依赖于计算机平台的虚拟设计和公开的实测数据。
6 中药“药效基团-功效假说”的应用
与“药效团”模型在中药领域的应用相似,“药效基团-功效假说”可用于中药药效物质基础的辨识及其ADME-Tox、中药作用靶标搜寻等方面。目前中国已建立了中药有效成分三维结构数据库、中国天然产物数据库及中药化学数据库(TCMD)等适用于中药研究的数据库。美国伊利诺斯大学建立了世界上较大的天然产物数据库NAPRALERT(Narural Produets Alert);Tsai等[35]构建了TCM Database@Taiwan数据库以及对该数据库进行基于云计算系统的智能筛选网络平台(iScreen);通过蛋白质数据库(PDB,http//:www.pdb.org)可公开获取与药理相关大分子结合的有机小分子的三维结构;Discovery Studio(DS)、MOE、LigandScout、Phase和Sybyl等商业平台系统整合了的药效团自动生成和分析模块。这为中药药效成分的筛选与辨识、中药作用靶点研究等奠定了基础。在基于“药效团”模型的虚拟筛选过程中,“药效基团-功效假说”强调重视“优势结构”和“活性基团”的重要性,具体在预过滤过程中兼顾类药性的同时需重点考虑这类特殊结构,并且在活性验证的基础上辅以“活性基团”验证,这将有助于进一步提高中药有效成分或靶标辨识的成功率,在保持中医药的特色与优势下,可为现代中药研究提供一种新的思路和方法。在此基础上开展候选药物的结构修饰,将有针对性地提高化合物合成效率和生物活性。
7 结语
本文在中药“药效团药性假说”的基础上提出了中药“药效基团-功效假说”,并论证了其合理性和可行性。不同于以前提出的“分子药性假说”和“药效团药性假说”,中药“药效基团-功效假说”将简单抽象的“药效团”与药物化学中具体的“活性基团”结合,既适合高效的计算机处理,也容易被药物化学家理解。大数据时代的到来,为如何实现中医药现代化,如何以中医药为灵感开发新药提供了思路,现代科研手段必须要同传统中医药理论相结合,多学科共容,协调发展,以期突破和超越传统理论,从而让中药药性理论在日常的医疗实践中,在中医药现代化的发展过程中,更好地发挥把握方向、统领全局的指导作用。后续笔者将从“药效团”模型的研究方法出发,对其在中药有效成分的辨识及其ADME-Tox、中药作用靶标搜寻等方面的应用技术及其不足进行系统总结和概述。
利益冲突 所有作者均声明不存在利益冲突
[1] 魏雄辉, 张建斌. 天然药物化学 [M]. 北京: 北京大学出版社, 2013: 6-18.
[2] 李石生, 邓京振, 赵守训, 等. 中药现代化研究的关键在于建立科学的现代中药理论体系: 分子药性假说的提出 [J]. 中国中西医结合杂志, 2000, 20(2): 83-84.
[3] 徐风, 杨东辉, 尚明英, 等. 中药药效物质的“显效形式”、“叠加作用”和“毒性分散效应”: 由中药体内代谢研究引发的思考 [J]. 世界科学技术—中医药现代化, 2014, 16(4): 688-703.
[4] 吴水生. 疾病缩减效应假说在中药复方作用机制阐述上的应用 [J]. 中国中医药科技, 2006, 13(1): 44-45.
[5] 蔡少青, 王璇, 尚明英, 等. 中药“显效理论”或有助于阐释并弘扬中药特色优势 [J]. 中国中药杂志, 2015, 40(17): 3435-3443.
[6] 李爱秀. 中药“药效团药性假说”的提出 [J]. 天津药学, 2007, 19(2): 41-44.
[7] 李寒冰, 吴宿慧, 牛明, 等. 中药品质生物评价的历史与发展 [J]. 中草药, 2017, 48(14): 2809-2816.
[8] 周复辉, 易增兴, 罗亨凡. 辛味中药化学成分的分析 [J]. 安徽农业科学, 2006, 34(12): 2760.
[9] 刘群, 杨晓农. 中药四气五味的现代认识 [J]. 西南民族大学学报:自然科学版, 2006, 32(5): 981-985.
[10] 王米渠, 许锦文. 中药分子药性学的进展 [J]. 世界科学技术, 2002, 4(6): 51-54.
[11] 张冰, 林志健, 翟华强, 等. 基于“三要素”假说研究中药药性的设想 [J]. 中国中药杂志, 2008, 33(2): 221-223.
[12] 黄明进, 郭刚, 徐立军, 等. 解表药药性与挥发油成分相关性研究 [J]. 北京中医药大学学报, 2009, 32(2): 101-103.
[13] 刘培勋, 龙伟. 中药药性与中药药性物组学 [J]. 中国中药杂志, 2008, 33(14): 1769-1771.
[14] 匡海学, 程伟. 中药性味的可拆分性、可组合性研究: 中药性味理论新假说与研究方法的探索 [J]. 世界科学技术—中医药现代化, 2009, 11(6): 768-771.
[15] Ehrlich P. Über den jetzigen Stand der Chemotherapie [J]., 1960:150-170.
[16] Drie J H V. Monty Kier and the origin of the pharmacophore concept [J]., 2012, 11(1): 271-279.
[17] Wermuth C G, Ganellin C R, Lindberg P,. Glossary of terms used in medicinal chemistry (IUPAC Recommendations 1998) [J]., 1998, 70(5): 1129-1143.
[18] 郭亦然. 基于三维数据库搜寻的中药信息学研究 [D]. 北京: 北京中医药大学, 2006.
[19] Evans B E, Rittle K E, Bock M G,. Methods for drug discovery: Development of potent, selective, orally effective cholecystokinin antagonists [J]., 1988, 31(12): 2235-2246.
[20] Husain A, Khan S A, Iram F,. Insights into the chemistry and therapeutic potential of furanones: A versatile pharmacophore [J]., 2019, 171: 66-92.
[21] Thompson L A, Ellman J A. ChemInform abstract: Synthesis and applications of small molecule libraries [J]., 2010, 27(22): 555-600.
[22] Ajani O O, Aderohunmu D V, Umeokoro E N,. Quinazoline pharmacophore in therapeutic medicine [J]., 2016, 11(3): 716.
[23] Ryu K, Kim N D, Choi S I,. Identification of novel inhibitors of HCV RNA-dependent RNA polymerase by pharmacophore-based virtual screening andevaluation [J]., 2009, 17(8): 2975-2982.
[24] Madzhidov T I, Rakhimbekova A, Kutlushuna A,. Probabilistic approach for virtual screening based on multiple pharmacophores [J]., 2020, 25(2): E385.
[25] Liu C S, Yin J H, Yao J Q,. Pharmacophore-based virtual screening toward the discovery of novel anti-echinococcal compounds [J]., 2020, 10: 118.
[26] 邵欣欣, 陈聪, 王振国, 等. 靶向5-LOX中药黄酮类化合物的活性筛选及其作用方式和共性规律研究 [J]. 天然产物研究与开发, 2019, 31(9): 1506-1514.
[27] 谷宇, 张栩, 陈艳昆, 等. 基于分子模拟技术筛选大黄、羌活、秦艽的5-LOX、LTA4H抑制剂 [J]. 中国中药杂志, 2017, 42(23): 4494-4502.
[28] 刘傲雪, 王晶娟. 基于反向找靶当归补血汤的药效成分研究初探 [A] //第五届全国中药商品学术大会论文集 [C]. 哈尔滨: 中国商品学会, 2017: 466-469.
[29] 张燕玲,王耘,乔延江. 基于药效团的药性物质基础研究 [J]. 世界科学技术—中医药现代化, 2009, 11(5): 735-738.
[30] 陶丽, 陆茵, 王爱云, 等. 试论组分中药的药性配伍 [J]. 中草药, 2012, 43(11): 2107-2110.
[31] 盛良. 中药四气五味和化学成分的关系 [J]. 现代中西医结合杂志, 2004, 13(21): 2804-2806.
[32] 盛良. 论中药四气五味的宏观化学成分说 [J]. 上海中医药杂志, 2008, 42(7): 63-67.
[33] Zhang Y L, Wang Y, Qiao Y J. Research on material base of TCM property based on pharmacophore [J]., 2009, 11(5): 735-738.
[34] 张亚超, 李梦龙, 郭延芝, 等. 平性药有效成分与药性相关性研究 [J]. 化学研究与应用, 2010, 22(1): 67-72.
[35] Tsai T Y, Chang K W, Chen C Y. iScreen: world's first cloud-computing web server for virtual screening anddrug design based on TCM database@Taiwan [J]., 2011, 25(6): 525-531.
“Pharmacophore-efficacy hypothesis” of traditional Chinese medicine and its application
ZHANG Wen-jin1, CAO Ye2, CHANG Li-kun3, WANG Sheng1, KANG Chuan-zhi1, ZHOU Li1, GUO Lan-ping1
1. Chinese Medicine Resource Center, China Academy of Chinese Medical Sciences, Beijing 100700, China 2. School of Medicine, Anhui University of Chinese Medicine, Hefei 230012, China 3. School of Traditional Chinese Medicine, Guangdong Pharmaceutical University, Guangzhou 510006, China
Based on the inheritance of traditional theories and experience, modern science and technology was used for research, improvement, and development of the modernization of traditional Chinese medicine. With the increasing maturity of pharmacophore virtual screening technology in computer-aided drug design, it has become possible to apply this technology in the modernization of traditional Chinese medicine. This article starts from the “pharmacophore hypothesis” of traditional Chinese medicine, analyzes the scientific connotation of “pharmacophore”, and proposes a “pharmacophore-efficacy hypothesis” suitable for modernization research of traditional Chinese medicine.
pharmacophore; pharmacophore-efficacy hypothesis; pharmacodynamic component identification; ADME-Tox; target search
R285
A
0253 - 2670(2021)07 - 1865 - 07
10.7501/j.issn.0253-2670.2021.07.001
2020-11-13
国家自然科学基金重大项目(81891014)
张文晋,博士研究生,研究方向为中药资源与质量评价。E-mail: glzwj625@163.com
郭兰萍,研究员。E-mail: glp01@126.com
[责任编辑 潘明佳]

