中药治疗缺血性脑卒中致多器官损伤的研究进展
龙 宇,张羽璐,万金艳,刘松雨,倪 丽,李 楠, 杨 明
·综 述·
中药治疗缺血性脑卒中致多器官损伤的研究进展
龙 宇1,张羽璐1,万金艳1,刘松雨1,倪 丽1,李 楠1*, 杨 明2*
1. 成都中医药大学药学院,四川 成都 611137 2. 江西中医药大学药学院,江西 南昌 330004
缺血性脑卒中(cerebral ischemic stroke,CIS)可引发包括心、肝、脾、肺、肾在内的多个器官损伤,该类疾病是由多个病理环节组成,具有复杂的发病机制及高发病率、高致残率和高死亡率的特点,严重者可形成多器官功能障碍综合征(multiple organ dysfunction syndromes,MODS)。目前任何针对单一环节、单一靶点的治疗都不足以应对这一问题。研究发现中药可经多途径、多靶点,参与疾病的多个环节干预疾病。中药通过抗氧化作用、抑制炎症反应、调节能量代谢等对CIS引发的多器官损伤具有明显的保护作用。对中药及其有效成分对CIS后引起的多器官损伤及其相关机制进行了综述,以期更大程度地发挥祖国医学的治疗作用和治疗范围,为中药临床干预脑血管类合并多器官损伤类疾病提供科学依据和参考。
中药;多靶点;缺血性脑卒中;多器官损伤;多器官功能障碍综合征
据《中国卒中报告2019》报道,我国卒中的死亡人数约占全球卒中死亡人数的1/3,中国已经成为卒中终身风险最高和疾病负担最重的国家[1]。缺血性脑卒中(cerebral ischemic stroke,CIS)是指因脑血管闭塞或狭窄,导致血流通行不畅而使脑组织缺血缺氧、软化甚至坏死,脑血管功能障碍,引起相关症状的疾病[2],约占卒中类疾病的3/4。据临床发现,急性脑血管病可导致多器官损伤,如继发心肌损伤、肝脏损伤、肺水肿、肾功能衰竭及代谢紊乱等。由CIS引起的多器官损伤是CIS疾病病程中最常见的并发症之一。传统中医理论认为,人体作为一个整体,脑与五脏具有密切的联系,脑若受难必将影响包括心、肝、脾、肺、肾在内的多个脏器的正常功能。现代研究发现,CIS病程进展中所产生的有害物质聚集在血液中可被送往机体的其他重要脏器,对相关器官功能产生损伤的级联反应,继而引起对心、肝、脾、肺、肾等多器官损伤及微循环障碍(multiple organ dysfunction syndrome,MODS)[3]。MODS是指原无器官功能障碍的患者在遭受严重创伤、感染、休克、大手术及急性中毒等致病因素急性损害24 h后,同时或序贯性出现≥2个的器官功能障碍以致机体内环境的稳定必须靠临床干预才能维持的综合征[4],在临床上是急性脑血管类疾病常见的高致残率、高病死率的并发症,严重威胁着人体健康,故积极寻找干预CIS所致MODS的疗法具有重要的社会意义。
临床上常用化学药作为治疗CIS所致多器官损伤及MODS的基础药物,但在病程中常涉及包括炎症、氧化应激等在内的多个病理机制,化学药发挥作用时多作用于单一靶点,且部分药物具有肝肾毒性[5]。而中药具有多成分、多靶点、不良反应小的特点,且分布范围较广,来源丰富,具有悠久的药用历史,在临床使用范围较广,对CIS致MODS具有积极的治疗意义,是临床治疗多器官损伤的有力药物。
1 理论研究
1.1 传统理论对中药治疗CIS致多器官损伤的认知
中医理论认为,人体作为一个整体,各个脏腑之间具有紧密的联系。脑作为元神之府,具有协调五脏六腑功能的作用,可通过经脉的络属关系与五脏六腑发生联系,也可通过脑髓发出的脑气筋散布脑气入脏腑发挥支配脏腑运动与感觉的作用。脑的生成、濡养离不开五脏六腑化生输布气血津液的作用,而脑又对五脏六腑化生输布气血津液起着协调和支配作用。若脑部发生病变,则精血津液髓运行失常,可导致五脏六腑功能异常。中风(卒中)病位在脑髓血脉,脑络受损,神机失用,可导致多脏腑如心、肝、脾、肺、肾等功能紊乱,具体症状体现在临床相关症状上。而中药由于其成分复杂,性味归经较多的特点,或可同时作用于多个脏腑。因此中药在治疗中风的同时对五脏功能异常亦有调节作用,同时中医理论亦强调脑之为病可从脏腑论治。故传统中医理论证明了中药治疗CIS致MODS具有科学性与可行性。
1.2 现代理论对中药治疗CIS致多器官损伤的认知
CIS可导致多器官损伤,引起的损伤是复杂的病理生理过程相互作用的结果,常呈现为级联反应,涉及到炎症反应、氧化应激、兴奋性氨基酸释放、细胞内钙稳态、自由基生成、凋亡基因激活、能量代谢紊乱、自噬等多个环节,线粒体功能障碍、梗死周围去极化、内质网应激、基质金属蛋白酶激活、血脑屏障受损等[6]。
目前,关于MODS发病机制多集中于全身炎症反应综合征(systemic inflammatory response syndrome,SIRS)学说、微循环障碍学说、代谢障碍学说、神经内分泌学说等[7]。脑在病理状态下交感-肾上腺系统受到一定程度影响,机体神经体液调节功能紊乱;下丘脑等调节中枢受损,导致对人体活动调节功能紊乱;CIS将进一步触发炎症级联的激活,导致全身炎症反应。在CIS后由循环活性氧和促炎性细胞因子引起的环境中,包括心、肝、肺、肾脏等在内的多个器官会受损,导致MODS[8]。现行研究主要分为临床研究和实验研究,即通过收集筛选临床符合条件的患者及实验室内采用动物模型进行分析探讨。现有研究证明,中药成分丰富,药理作用广泛,针对CIS后发生的多器官损伤病理机制较多的特征,可通过抗氧化作用、抑制炎症反应、调节能量代谢等进行多靶点干预。故现代医学理论亦为中药治疗CIS致MODS提供了理论依据。CIS及其致MODS的现代病理机制见图1。
2 中药治疗CIS致相关器官损伤
2.1 心脏损伤
对于脑心关系的认识,传统医学与现代医学基本达到统一[9]。中医理论认为,脑与心脏是一个有机整体,二者之间经脉相连、气血相通、神明贯通,具体关系可概括为“心脑相关”。心功能的正常是脑正常运行的前提条件,同时又依赖于脑对其的协调作用,心与脑在生理上相互依赖,病理上相互影响。中医理论认为“中风”与心病(胸痹、心悸)有着相同的病因病机,其病机均为本虚标实。脑心同病的发病机制是多种因素诱发中风后痰瘀阻络,气机失和,气血运行不畅,心脉失养,或痰火扰心,心神不宁,从而出现心悸、胸痹等[10]。心脑相关理论的现代机制则主要体现在“神经-内分泌-免疫网络”学说、“络病”学说[11]。脑作为神经系统的高级中枢,可支配包括心脏在内的各个器官。脑对心的影响,临床上最为典型的表现为脑心综合征(cerebral cardiac syndrome,CCS)的发生,CCS指急性脑血管疾病常继发心肌损伤,其定义范围为急性脑血管循环障碍及急性颅脑外伤等后产生的心肌缺血、心律失常、急性心肌梗死或心力衰竭的一组症状。在临床上,以急性脑卒中并CCS最多见[12]。
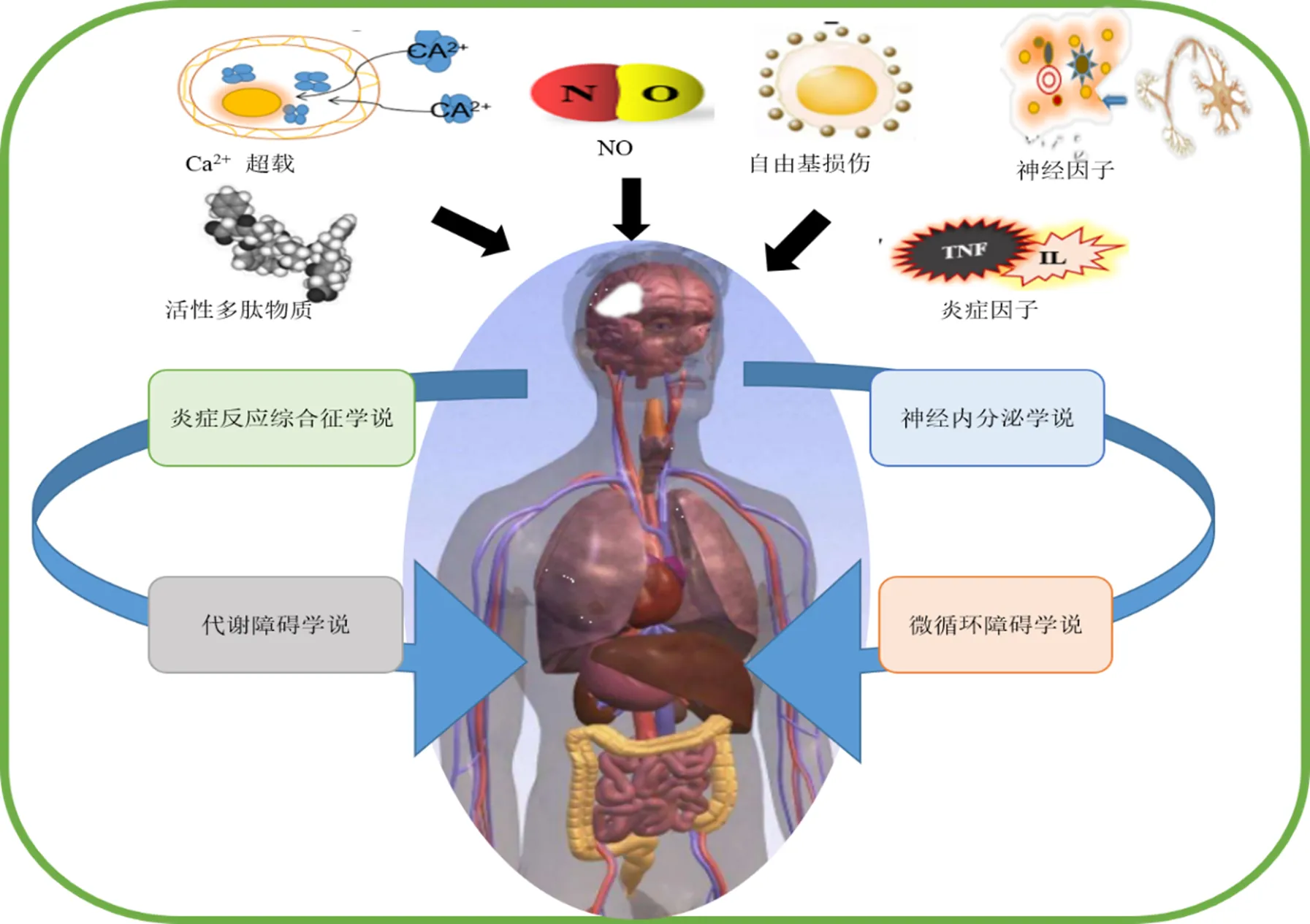
图1 CIS及其致MODS的现代病理机制
现代理论认为CCS形成的机制主要为CIS导致中央自主神经网络和下丘脑-垂体-肾上腺轴的激活或失调,其分泌的儿茶酚胺等神经体液因子的过度释放可对心肌细胞和(微)血管造成损伤[13-14];CIS后,机体释放多种促炎细胞因子,通过血脑屏障进入循环系统,诱发SIRS,使心脏损伤,出现微循环障碍[15];氧自由基生成增加,使心肌细胞受到损伤;当脑卒中发生于脑支配心脏交感与副交感神经的中枢及神经传导途径的部位时,可引起心脏损伤;低钾、低钠、低氯的电解质平衡失调,使得心肌细胞的应激性下降;中枢及外在神经肽Y可能参与脑心综合征的发生发展[16];脑-心血管存在共同的病理基础,CIS或可诱发、加重心脏病变[17]。研究发现中药可通过改善氧化应激、调节神经递质紊乱、降低心电图异常率等作用进行干预,应用中药、中药联合化学药等手段治疗CIS并CCS,可取得较好疗效。见表1。
2.2 肝脏损伤
中医关于肝的理论有明确的形态基础,肝位于腹部,在肋之内,与现代医学所述基本相同[38]。传统医学认为,肝与脑的关系表现为肝脑相维,肝主疏泄,又主藏血,亦可调畅气机,若疏泄失常,情志失调,清窍不通,痰瘀内生,血溢于脑,导致中风。痰瘀内生后,进一步阻滞气机,可影响肝脏正常运行,由此形成恶性循环。肝脏与急性缺血性中风关系较密切的证候有脉弦、胁痛胁胀、急躁易怒,且急性缺血性中风所表现的临床证候皆以肝脏为主,在一定程度上可体现疾病发生后肝脏的受累[39]。现代研究亦认为,CIS后的主要系统性并发症之一是肝功能不全,其与死亡率和总体预后不良有关[40]。临床研究表明,急性脑血管病合并MODS患者中,肝功能异常者占15.5%以上。研究人员向脑缺血再灌注模型小鼠体内注射示踪剂,发现肝脏是有害物质聚集最高的器官之一,亦表明肝脏是脑缺血再灌注损伤后非常敏感的脏器之一[41-42]。徐欣萍等[43]发现CIS早期时大鼠肝细胞就出现了损伤,主要表现为水肿、变性,然后逐渐出现核破碎和细胞坏死,且随时间延长肝损伤有加重趋势。CIS所致肝损伤的机制可能为CIS后,体内循环的促炎细胞因子对肝脏造成损伤;氧化应激反应,如活性氧的过度产生诱导肝细胞DNA发生氧化性损伤将引起肝脏的损伤[40,44];肝脏作为人体最大的代谢器官,也是众多抗氧化物质的合成场所,CIS病程中抗氧化物质被大量消耗,将加重肝脏的合成压力,引起肝损伤[45];在实验性脑缺血过程中,病理状态下Ca2+浓度的异常增高可激活钙蛋白酶,被激活的钙蛋白酶可直接或间接对肝细胞及组织造成损伤[46]。目前针对中药干预CIS所致肝损伤主要为实验研究,见表2,临床相关研究较少。

表1 中药治疗CIS致心损伤的应用
MCAO-大脑中动脉闭塞cTnI-心肌肌钙蛋白I BNP-脑钠肽 ET-内皮素 CAT-过氧化氢酶
MCAO-middle cerebral artery occlusion cTnI-cardiac troponin I BNP-brain Natriuretic Peptide ET-endothelin CAT-catalase
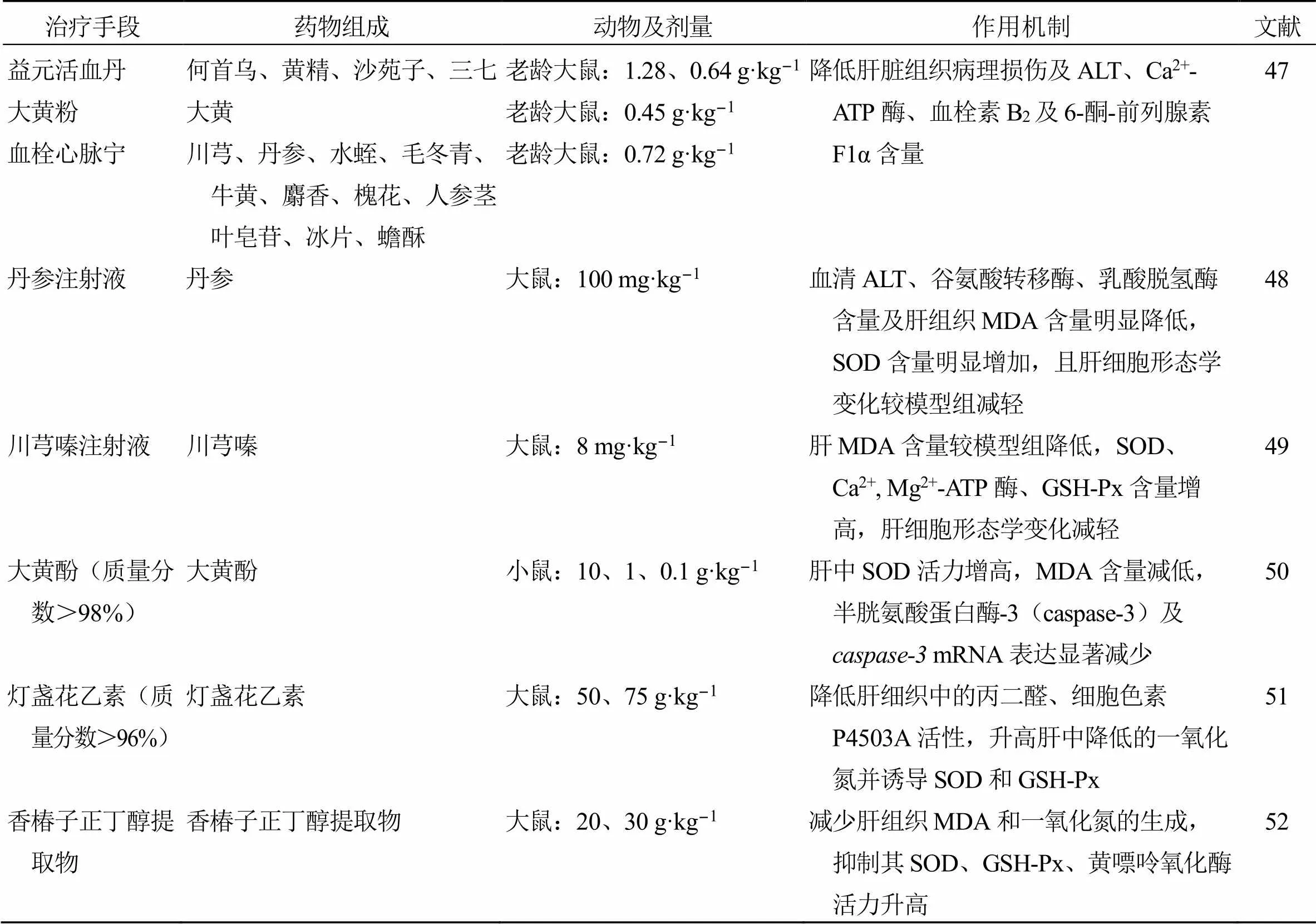
表2 中药治疗CIS所致肝损伤的应用
ALT-丙氨酸氨基转移酶 MDA-丙二醛 SOD-超氧化物歧化酶 GSH-Px-谷胱甘肽过氧化物酶
ALT-alanine aminotransferase MDA-malondialdehyde SOD-superoxide dismutase GSH-Px-glutathione peroxidase
2.3 脾脏损伤
现代医学认为,脾与生命科学中许多基本问题密切相关,不仅指中医学的整个消化系统,而且与神经、内分泌、血液、循环、免疫、运动等系统生理功能密切相关[53]。传统医学与现代医学中关于脾的定义略有不同,但皆认为CIS类疾病与各自理论下脾脏有着重要的联系。中医理论认为脑与脾不仅存在着生理上的联系,病理上也互相影响。若脾胃受损,升降气机失常,津液不循常道而诸邪内生,如湿浊内生酿痰、经络郁滞、血行不畅,上蒙脑窍,可导致中风发生[54-55]。同时,中风后脑受损,其病理状态下亦影响着脾的活动。研究发现,急性CIS患者易厌食纳少、体倦乏力、脉细,可体现病发后脾脏的受累[39],可能与脾脑之间有着共同的物质基础脑肠肽有关。脑肠肽峰值变化具有调节情志、改善记忆能力、调节胃肠功能等作用。CIS后脑肠肽的水平变化,可影响胃肠道的变化,而出现厌食、纳呆等症[56-57]。现代医学则认为CIS所导致的脾状态的改变主要体现在免疫功能上,CIS后导致脾脏中有大量炎症介质浸润,细胞大量凋亡。CIS诱导的免疫病理改变是双向的,首先表现为免疫反应被激活,随后出现脾和胸腺的抑制。淋巴器官的激活使免疫细胞移位到脑内,加剧CIS损伤,同时导致脾脏和胸腺免疫细胞的破坏,继之出现免疫抑制[58]。CIRI可致小鼠的脾脏体积下降[59],这种减少可能反映了免疫细胞从脾脏流出到血液中的增加,以及脾脏内细胞死亡的增加[60],且脾脏缩小也与交感神经系统的激活有关[61]。
目前关于CIS所致脾损伤的研究相对较少,部分研究亦证实中药及其成分的确对CIS所致脾脏改变具有干预作用,可抑制CIS后脾脏萎缩,如给予小鼠ig 0.4、0.8 g/kg蒲参益智胶囊18、24 d,可提高MCAO模型小鼠的脾脏指数[62];人参皂苷Rb1能够抑制MCAO/R损伤模型小鼠脾脏的萎缩[63]。
2.4 肺脏损伤
中医藏象理论认为,肺位于胸腔,左右各一,且各有分叶,左二右三,共五叶,覆盖于心之上。中医理论中肺主气、司呼吸的作用与现代医学基本一致[64]。脑与肺有着密切关系,这体现在2种不同的理论体系中。中医理论认为肺功能正常,可保证脑的正常运行,若肺之功能异常,轻则呼吸不爽,可影响脑部,出现头痛、头昏等症,重则出现耳不能闻、目不能视、神昏谵语等危重症候。而脑病常累及肺部,由此形成恶性循环。现代医学认为肺的呼吸功能正常,脑的正常功能活动及精神活动得以维持,若二氧化碳潴留,将造成脑水肿,严重者将对脑神经造成不可逆损伤[65]。同时脑作为最高中枢神经系统,发生病变后可使肺功能紊乱。肺作为CIS中最易受累的器官之一,常在脑血管疾病后产生病理损伤,研究显示,CIS住院患者院内并发症位列首位的是肺炎/肺部感染[1]。近年来,CIS发病率不断上升,部分CIS患者其直接死因非CIS本身,而是其肺损伤引起的并发症[66],其临床表现常为不同程度的呼吸窘迫,严重者可致呼吸衰竭甚至死亡。CIS后肺损伤具体机制可能为炎症反应、能量代谢异常[67]、氧化应激损伤[68-69]、离子转运障碍、组织缺氧等综合作用。具体表现为CIRI后,肺内巨噬细胞的活化及中性粒细胞的凋亡延迟,使得其分泌炎性介质及氧自由基增多,对肺组织造成损伤;CIS后出现钙稳态失调,细胞内钙超载,可进一步导致肺血管通透性增加,导致肺部水肿及感染;活性多肽物质ET含量增加起到缩血管效应,造成肺组织缺氧。
中医药治疗CIS所致肺损伤具有整体观念,辨证论治的鲜明特点。针对特定CIS急性期患者给予化痰通腑方治疗能够显著改善患者的预后情况,达到中医“治未病”“肺与大肠相表里”的理论要求[70]。而现代研究发现,中药被证实可通过多条途径抑制炎症反应,减少氧化应激,改善能量代谢异常等作用缓解肺组织损伤,见表3。
2.5 肾脏损伤
中医理论所述肾与现代解剖学基本一致,而传统中医理论中关于肾的功能与现代医学理论中则有出入,然则中西医各自理论体系中肾与脑皆有着重要的联系。传统中医理论认为肾的功能赖于脑髓充足,以脑髓充足为前提,脑髓充足又源自于肾精充足,二者息息相关。两者的关系可概括为“肾脑互济”,强调二者在功能上的升降相因和相互作用。中风发生后,人体阴阳失衡,必会影响肾脏功能的正常运行。现代医学认为,肾精与全能干细胞有相似之处,是脑形成的物质基础[81],二者关系相互依赖。病理状态下,CIS和肾功能异常之间有着联系,CIS患者常并发急性肾损伤,可能因素有:神经内分泌功能紊乱造成肾小管缺血损伤[82];下丘脑和脑干的自主神经调节中枢兴奋,分泌多种活性物质,循环至肾脏使其受损[83];大剂量脱水性药物的使用,进一步造成肾脏损伤[84];溶栓治疗后低肾小球滤过率水平和高尿酸水平导致急性肾损伤[85];内皮素、一氧化氮等活性物质使肾小球处在高滤过状态引起肾损害;炎症反应;既往有高血压病史的卒中患者,其血管弹性降低,肾脏血管易形成微小血栓,造成肾损伤。
研究发现,中药治疗CIS所致肾脏损伤,可通过抗氧化应激、抗炎、调节神经内分泌等药理作用进行干预,且干预途径多样,常规途径如口服,静注等,临床上也有通过通腑泻浊法采用中药灌肠手段防治病程中甘露醇所致肾损伤,所用中药包括大黄、玄明粉、槐花、蒲公英、煅牡蛎、丹参和芒硝等[86]。除单用中药外,亦有中化学药联合应用的临床研究,如在治疗CIS后肾功能不全时除常规治疗外,加用前列地尔和大黄水煎液,发现可明显改善患者肾功能[87]。见表4。
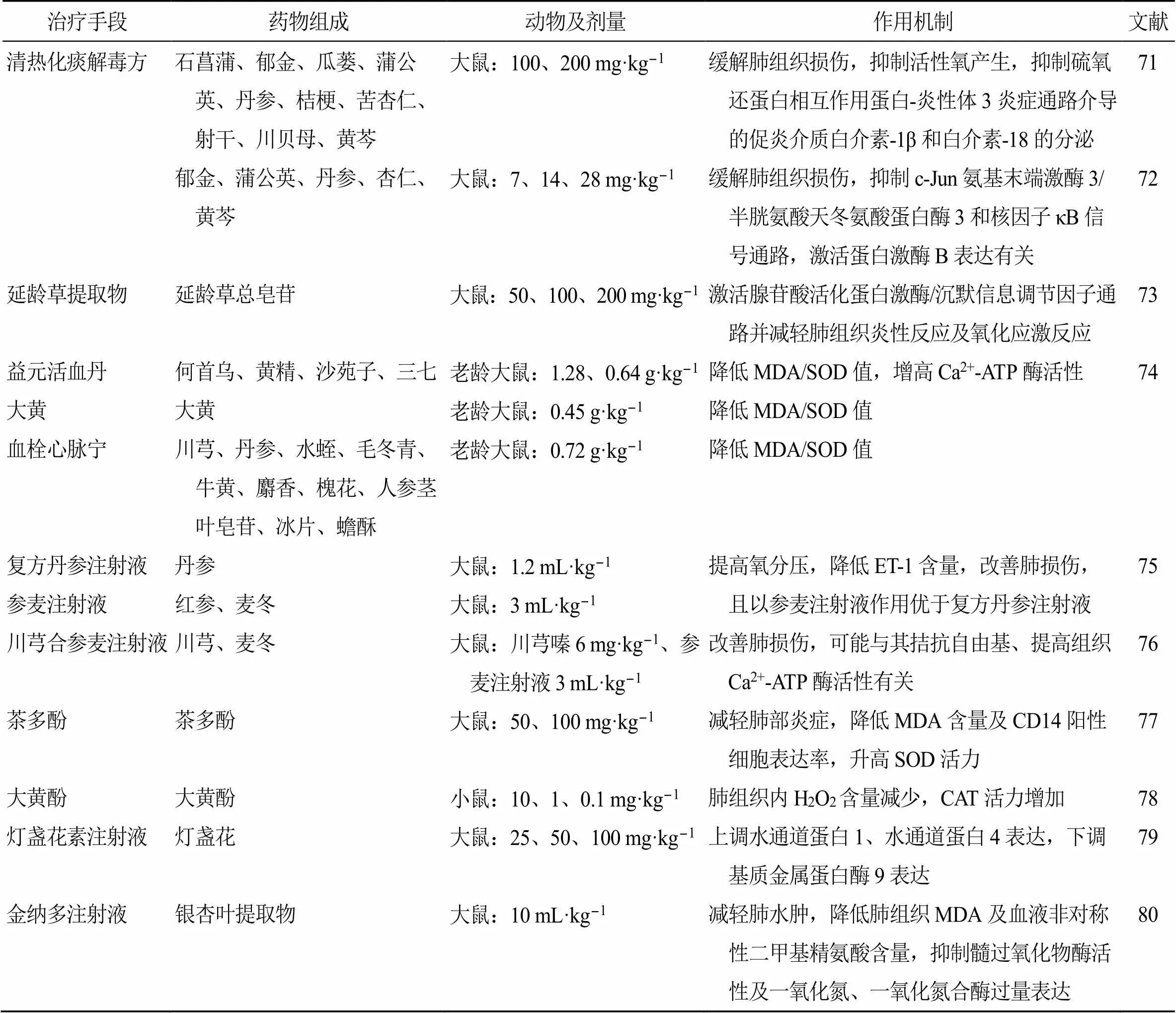
表3 中药治疗CIS所致肺损伤的应用
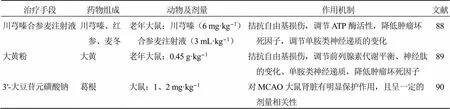
表4 中医药治疗CIS所致肾损伤的应用
3 结语与展望
缺血性脑血管类疾病发生后可引发包括炎症反应、氧化应激、能量代谢障碍等在内的一系列级联反应,可对心、肝、脾、肺、肾等器官造成损伤,严重威胁着人类健康,故研究CIS致多器官损伤机制及治疗方法具有重要的社会意义。中医理论认为,部分脏器的异常亦可诱导中风的发生。同时人体受脑所统,若脑部发生病变,可导致五脏六腑功能异常,由此形成恶性循环。基于心脑相通、肝脑相维、脑脾相关、脑肺相系和脑肾相济的关系,治疗脑病可从五脏入手。中药成分丰富,且常以组方形式出现,有效物质可作用于多个靶点,或可干预1个乃至多个脏腑,使得中药在治疗中风的同时对五脏亦有保护作用,体现了中医药整体观念的特点。现代研究发现CIS所致多器官损伤病理机制复杂,单一化学药治疗恐效果不佳,而中药及其有效成分常可干预病程中的多个阶段,达到整体治疗的效果。相对于化学药,中药环保安全,不良反应较小,目前临床上已有其成功干预CIS所致多器官损伤的案例。故研究中药干预CIS所致多器官损伤可为该类疾病的临床治疗提供重要的参考,为后续药物的开发提供依据。且临床上部分疾病病程较长,常常伴有多种并发症,极大程度地损害了患者的健康。亦可基于中药不良反应小,治疗靶点较多的特点,结合针刺、化学药等手段综合治疗,以期更大程度地服务于临床。
但目前针对中医药干预CIS所致多MODS的研究仍存在着一些问题需进一步的思考和解决。如临床研究中样本较少,且研究时阐述药物干预的具体分子机制较为模糊,后期研究时应对其具体机制进行详细探讨。部分中药存在单个药物或成分的研究,但并未用于其他药物的联合研究,将来可进行配伍使用,以期更大发挥中医药的治疗作用。部分中药其有效成分具有较好的治疗效果,但其自身的特性,如溶解度低、生物半衰期短、化学性质不稳定等限制了临床的应用,可结合其特点,选择适宜的剂型,将其制备为现代药物剂型,如脂质体和微囊等,改善其性质。研究发现在临床上使用现代医学对中医药干预加以辅助具有较好的治疗效果,因此该种方法具有极佳的推广意义。
利益冲突 所有作者均声明不存在利益冲突
[1] Wang Y J, Li Z X, Gu H Q,. China stroke statistics 2019: A report from the national center for healthcare quality management in neurological diseases, China national clinical research center for neurological diseases, the Chinese stroke association, national center for chronic and non-communicable disease control and prevention, Chinese center for disease control and prevention and institute for global neuroscience and stroke collaborations [J]., 2020, 5(3): 211-239.
[2] 何婷婷, 陈维铭, 钱涯邻. 论缺血性中风血脑屏障病变玄府病机 [J]. 江苏中医药, 2015, 47(1): 8-9.
[3] Han J Y, Li Q, Ma Z Z,. Effects and mechanisms of compound Chinese medicine and major ingredients on microcirculatory dysfunction and organ injury induced by ischemia/reperfusion [J]., 2017, 177: 146-173.
[4] 马晓媛, 肖雅, 田李星,等. 创伤后多器官功能障碍综合征预警指标的研究进展 [J]. 中华创伤杂志, 2016, 32(1): 89-92.
[5] Akpınar O, Nazıroğlu M, Akpınar H. Different doses of dexmedetomidine reduce plasma cytokine production, brain oxidative injury, PARP and caspase expression levels but increase liver oxidative toxicity in cerebral ischemia-induced rats [J]., 2017, 130: 1-9.
[6] Long Y, Yang Q, Xiang Y,. Nose to brain drug delivery - A promising strategy for active components from herbal medicine for treating cerebral ischemia reperfusion [J]., 2020, 159: 104795.
[7] 张慧, 李宣东, 郭洪志, 等. 急性脑梗死诱发全身炎症反应综合征致多器官功能障碍综合征的机制探讨 [J]. 神经疾病与精神卫生, 2007, 7(6): 449-452.
[8] Palasik W, Fiszer U, Lechowicz W,. Assessment of relations between clinical outcome of ischemic stroke and activity of inflammatory processes in the acute phase based on examination of selected parameters [J]., 2005, 53(4): 188-193.
[9] 林棋. 中医心理论与现代医学的联系 [J]. 中华中医药学刊, 2011, 29(12): 2610-2615.
[10] 刘文通, 赵轩竹, 陈宝贵. 脑心综合征的中西医研究进展 [J]. 中医药导报, 2020, 26(10): 151-153.
[11] 张迪, 曾芳, 杨洁, 等. 心脑相关理论的现代研究进展 [J]. 四川中医, 2014, 32(5): 179-181.
[12] 符少萍. 内皮素-1在大鼠脑缺血继发心肌损伤中的变化及再灌注对其的影响 [D]. 广州: 中山大学, 2004.
[13] Scheitz J F, Nolte C H, Doehner W,. Stroke-heart syndrome: Clinical presentation and underlying mechanisms [J]., 2018, 17(12): 1109-1120.
[14] 楼小亮, 李晓萍. 急性脑血管病患者血清酶学及心电图检测分析 [J]. 中国实用内科杂志, 2004, 24(2): 98-99.
[15] 胡奇华, 胡富增, 胡兆霆. 脑心综合征患者血浆炎性标志物的变化及临床意义 [J]. 中西医结合心脑血管病杂志, 2014, 12(9): 1159-1160.
[16] 张中福, 周厚援, 罗志强. 解毒通腑法对卒中后神经肽Y及心肌酶谱影响的临床观察 [J]. 中国现代医生, 2017, 55(35): 139-141.
[17] 陆珊珊. 从中风病探讨心和脑的关系 [D]. 南京: 南京中医药大学, 2010.
[18] 李建生, 赵君玫, 郭盛典, 等. 川芎嗪和参麦注射液对脑缺血再灌注损伤老龄大鼠心肌组织ATP酶和自由基代谢的影响 [J]. 中国中西医结合急救杂志, 2001, 8(6): 347-350.
[19] 李建生, 闫新慧, 赵君玫, 等. 川芎嗪和参麦注射液对老龄大鼠脑缺血再灌注心肌损伤的保护作用 [J]. 中国急救医学, 2001, 21(3): 134-136.
[20] 贾维宁. 小鼠脑缺血再灌注后蛇床子素对心肺组织氧化应激反应的影响 [D]. 石家庄: 河北医科大学, 2017.
[21] 王允琴. 气虚血瘀证急性脑梗死并发脑心综合征的临床特征及脑络欣通干预研究 [D]. 合肥: 安徽中医药大学, 2015.
[22] 徐小良, 吴德军, 崔益明. 脑心通胶囊联合西药治疗脑心综合征心律失常临床研究 [J]. 新中医, 2020, 52(6): 31-34.
[23] 黄帅金. 心安颗粒对局灶性脑缺血大鼠心肌细胞动作电位的影响研究 [D]. 泸州: 泸州医学院, 2014.
[24] 董婷, 杨文明, 汪美霞, 等. 补阳还五汤治疗急性脑梗死并发脑心综合征(气虚血瘀证)90例临床观察 [J]. 中国中医急症, 2011, 20(1): 5-7.
[25] 李仕妹. 桃红四物汤合半夏白术天麻汤治疗急性脑梗死并发脑心综合征60例 [J]. 西部中医药, 2017, 30(8): 77-79.
[26] 唐文成, 王树青. 步长脑心通脑心同治治疗急性后循环脑梗死致脑心综合征疗效观察 [J]. 新中医, 2014, 46(9): 30-31.
[27] 任艳丽, 郭根明. 冠心舒通胶囊治疗急性脑梗塞致脑心综合征疗效观察 [J]. 亚太传统医药, 2014, 10(13): 116-118.
[28] 关海林, 张利兰. 麝香保心丸治疗急性脑卒中致脑心综合征的临床观察 [J]. 中西医结合心脑血管病杂志, 2015, 13(12): 1452-1453.
[29] 孙乐羽, 姜炎, 贺刚锐. 参附注射液治疗急性脑梗死后脑心综合征临床观察 [J]. 中国实用神经疾病杂志, 2015, 18(14): 118-119.
[30] 王宏. 参芎葡萄糖注射液治疗急性脑梗死后脑心综合征的疗效 [J]. 中国实用神经疾病杂志, 2013, 16(13): 78-80.
[31] 何丽萍, 马学琴. 参芎注射液治疗脑心综合征56例临床分析 [J]. 基层医学论坛, 2015, 19(26): 3644-3645.
[32] 刘雪梅, 陶冶, 王凤丽, 等. 从“脑心同治”探讨苦碟子注射液对急性脑缺血后心肌血管活性物质的影响 [J]. 北京中医药, 2016, 35(7): 619-624.
[33] 王四海, 郭桢, 张秀敏, 等. 大黄酚对脑缺血再灌注小鼠心脏组织过氧化氢及过氧化氢酶的影响 [J]. 河北中医, 2014, 36(11): 1710-1711.
[34] 马云枝, 朱世瑞, 沈晓明, 等. 大株红景天注射液治疗急性脑卒中并发脑心综合征临床观察 [J]. 中西医结合心血管病电子杂志, 2014, 2(9): 43-44.
[35] 王允琴. 川芎注射液并舒血宁注射液治疗脑心综合征临床观察 [J]. 中医药临床杂志, 2014, 26(10): 1013-1014.
[36] 袁博博, 舒庆, 王晓叶. 丹参酮ΙΙA磺酸钠注射液联合前列地尔治疗急性脑梗死并发脑心综合征的临床效果 [J]. 中华心脏与心律电子杂志, 2019, 7(3): 141-143.
[37] 於永婷, 李玉堂, 张志超, 等. 谷红注射液联合前列地尔治疗急性大面积脑梗死并发脑心综合征疗效及对血浆ET-1、NO及8-iso-PGF2α的影响 [J]. 现代中西医结合杂志, 2017, 26(22): 2440-2443.
[38] 林棋. 中医肝理论与现代医学理论的联系[J]. 中华中医药学刊, 2015, 33(12): 2997-3005.
[39] 臧运华, 张连运, 郑志轩, 等. 急性缺血性中风与慢性脑供血不足的藏象对比研究 [J]. 山东中医药大学学报, 2013, 37(2): 122-124.
[40] 宫伟红. 高脂血症合并急性脑缺血再灌注诱导大鼠肝损伤机制的研究 [D]. 武汉: 武汉科技大学, 2012.
[41] 牛文民, 刘智斌, 杨晓航, 等. 针刺保肝护脑对脑缺血再灌注肝损伤大鼠γ-谷氨酰半胱氨酸合成酶表达的影响 [J]. 广州中医药大学学报, 2012, 29(5): 537-540.
[42] Cortes-Wanstreet M M, Giedzinski E, Limoli C L,. Overexpression of glutamate-cysteine ligase protects human COV434 granulosa tumour cells against oxidative and gamma-radiation-induced cell death [J]., 2009, 24(3): 211-224.
[43] 徐欣萍, 朱玉群, 啜佳然. 缺血性脑卒中大鼠肝脏和肠黏膜损伤的实验研究 [J]. 医学临床研究, 2012, 29(6): 1024-1026.
[44] Gong W H, Zheng W X, Wang J,. Coexistence of hyperlipidemia and acute cerebral ischemia/reperfusion induces severe liver damage in a rat model [J]., 2012, 18(35): 4934-4943.
[45] 刘智斌, 牛文民, 杨晓航, 等. 保肝护脑针法对脑缺血再灌注大鼠谷胱甘肽抗氧化系统的影响 [J]. 陕西中医, 2012, 33(3): 371-373.
[46] 于英男, 李燕. 钙蛋白酶与肝损伤 [J]. 中国药理学通报, 2008, 24(6): 708-711.
[47] 李建生, 李建国, 高爱社, 等. 补肾活血、泻下及开窍活血方药对老龄大鼠脑缺血再灌注肝脏损伤的保护作用 [J]. 河南中医, 2001, 21(4): 14-17.
[48] 熊伟, 涂献坤. 丹参注射液对大鼠脑缺血再灌注肝损伤影响的实验研究 [J]. 福建医药杂志, 2015, 37(1): 53-55.
[49] 朱晓琴, 雷水生. 川芎嗪对大鼠脑缺血/再灌注肝损伤的影响 [J]. 数理医药学杂志, 2007, 20(4): 463-465.
[50] 赵薇, 李方江, 王树. 大黄酚对小鼠脑缺血再灌注引起肝损伤的保护作用 [J]. 神经药理学报, 2014, 4(4): 1-9.
[51] Yang X F, He W, Lu W H,. Effects of scutellarin on liver function after brain ischemia/reperfusion in rats [J]., 2003, 24(11): 1118-1124.
[52] 胡敏, 陈超, 周聪, 等. 香椿子正丁醇提取物对脑缺血后肝肺损伤的保护作用研究 [J]. 时珍国医国药, 2014, 25(7): 1560-1562.
[53] 朱慧渊, 王江, 苗琦. 基于“脾主运化”理论仙鹤草调控线粒体能量代谢抗脑缺血损伤的探讨 [J]. 中华中医药学刊, 2015, 33(12): 2929-2931.
[54] 韩文刚. 脑中风从脾胃论治浅谈 [J]. 中国中医药现代远程教育, 2011, 9(10): 136.
[55] 徐银琴, 雷衍东, 吕明庄, 等. 从脾胃论治中风病研究进展 [J]. 新中医, 2019, 51(2): 36-39.
[56] 窦志芳, 张俊龙, 赵琼. 脑脾相关理论研究 [J]. 山西中医学院学报, 2015, 16(4): 6-7.
[57] 李珍. 缺血性卒中急性期血浆脑源性神经营养因子及脑肠肽水平变化与中医证候相关性的研究 [D]. 北京: 北京中医药大学, 2018.
[58] 张兵. 雌激素改善脑卒中后的免疫抑制状态 [D]. 南京: 南京大学, 2009.
[59] 韦思宇, 和静, 张娜, 等. NAC对MT Ι/ΙΙ敲除小鼠脑缺血再灌注后脾细胞损伤的保护作用 [J]. 山东医药, 2013, 53(18): 13-15.
[60] Offner H, Subramanian S, Parker S M,. Splenic atrophy in experimental stroke is accompanied by increased regulatory T cells and circulating macrophages [J]., 2006, 176(11): 6523-6531.
[61] 崔兴华, 王晶, 孙超, 等. 急性脑梗死后脾脏体积的变化及其与免疫炎性反应和血小板反应性的关系 [J]. 中华神经科杂志, 2018, 51(7): 526-532.
[62] 王长海, 李铎, 杨兰文. 蒲参益智胶囊治疗脑卒中后遗症的临床及机理研究 [J]. 浙江中医学院学报, 2002, 26(6): 21-22.
[63] 吕梦捷. 人参皂苷Rb1对小鼠免疫细胞行为影响和脑缺血再灌注损伤小鼠的免疫调节作用 [D]. 广州: 暨南大学, 2011.
[64] 吕玉宝, 段晓虹, 董竞成. 中医肺的现代研究进展 [J]. 中国中西医结合杂志, 2013, 33(11): 1579-1583.
[65] 刘耀东, 王敬华, 孙丽萍. 浅谈肺与脑中风的关系 [J]. 浙江中医药大学学报, 2010, 34(4): 473-474.
[66] 杨钧哲. 急性缺血性脑卒中并发肺损伤相关危险因素分析 [J]. 饮食保健, 2018, 5(15): 40.
[67] Yeşil H, Tuğlu I. The relation of oxidative stress and apoptosis to histopathologic alterations in the lungs as a result of global cerebral ischemia [J]., 2019, 94(8): 555-568.
[68] Fan J H, Lv H, Li J,. Roles of Nrf2/HO-1 and HIF-1α/VEGF in lung tissue injury and repair following cerebral ischemia/reperfusion injury [J]., 2019, 234(6): 7695-7707.
[69] 赵薇, 王树, 李方江. 脑缺血再灌注引起多器官损伤的研究进展 [J]. 神经药理学报, 2014, 4(2): 55-63.
[70] 江颖, 王凯华, 方兴, 等. 清肺化痰通腑方预防痰蒙清窍证脑卒中急性期肺部感染临床研究 [J]. 中医临床研究, 2017, 9(2): 21-23.
[71] 王涛, 刘宏祥, 王颖, 等. 清热化痰解毒方对脑缺血再灌注大鼠肺组织TXNIP/NLRP3炎性通路的影响 [J]. 中国实验方剂学杂志, 2018, 24(12): 114-122.
[72] 王涛, 刘宏祥, 王颖, 等. 清热化痰解毒方对卒中相关性肺炎大鼠 Akt/JNK3/Caspase-3和NF-κB信号通路的影响 [J]. 中国比较医学杂志, 2018, 28(10): 42-48.
[73] 黄桔秀, 符巧瑜, 陶楚楚, 等. 基于AMPK/Sirt1通路延龄草总皂苷对脑缺血再灌注继发肺损伤大鼠的保护作用 [J]. 中国药师, 2019, 22(11): 1986-1991.
[74] 李建生, 赵晶, 高爱社, 等. 补肾活血和泻下及开窍活血方药对脑缺血再灌注肺损伤老龄大鼠ATP酶和自由基代谢的影响 [J]. 中国中医急症, 2001, 10(6): 345-347.
[75] 韩宁, 张永. 参麦注射液对脑缺血再灌注后肺损伤大鼠血浆ET-1的影响 [J]. 中华中医药学刊, 2009, 27(2): 314-316.
[76] 李建生, 赵君玫, 郭盛典, 等. 川芎嗪和参麦注射液对脑缺血-再灌注肺损伤老龄大鼠心肌组织ATP酶和自由基代谢的影响 [J]. 中国中西医结合急救杂志, 2001, 8(6): 347-350.
[77] 宋晓丽. 茶多酚对于全脑缺血再灌注后继发肺损伤保护作用及机制的研究 [D]. 大连: 大连医科大学, 2007.
[78] 王四海, 郭桢, 张秀敏, 等. 大黄酚对脑缺血再灌注小鼠肺组织过氧化氢和过氧化氢酶的影响 [J]. 河北中医, 2014, 36(10): 1546-1547.
[79] 王丽英, 欧阳亮, 周瑞, 等. 灯盏花素注射液对卒中相关性肺炎大鼠肺损伤及AQP1、AQP4、MMP-9表达的影响 [J]. 临床和实验医学杂志, 2019, 18(18): 1909-1913.
[80] 王树青. 银杏叶对大鼠脑缺血再灌注后急性肺损伤的保护作用及机制探讨 [D]. 南宁: 广西中医药大学, 2011.
[81] 孟胜喜, 霍清萍. 从肾论治脑小血管病 [J]. 中西医结合心脑血管病杂志, 2016, 14(11): 1242-1246.
[82] 李红艳, 秦历杰, 王龙安. 急性脑梗死合并肾损伤患者血压与肾功能的关系 [J]. 中国实用医刊, 2019, 46(20): 17-20.
[83] 何文贞, 欧利民, 郑俊忠, 等. 巴曲酶治疗急性脑梗死后肾功能不全的疗效 [J]. 中国新药杂志, 2002, 11(10): 789-791.
[84] 郭勇, 杨茜, 柳晓锋, 等. 甘露醇导致脑梗死患者急性肾损害的早期诊断 [J]. 河北医科大学学报, 2017, 38(2): 214-216.
[85] 明莹莹, 郭艳霞. 急性缺血性脑卒中溶栓后发生急性肾损伤的危险因素分析及护理对策 [J]. 护理研究, 2019, 33(15): 2692-2695.
[86] 潘东, 陈可为, 白慧梅. 通腑泻浊法灌肠防治急性脑梗塞后甘露醇肾损害临床疗效研究 [J]. 时珍国医国药, 2012, 23(12): 3072-3074.
[87] 黄芳. 前列地尔联合大黄治疗脑梗死后肾功能不全 [J]. 河北医药, 2012, 34(10): 1547.
[88] 李建生, 赵君玫, 郭胜典, 等. 川芎嗪和参麦注射液对老龄大鼠脑缺血再灌注肾脏损伤的作用 [J]. 河南中医学院学报, 2003, 18(3): 9-11.
[89] 李建生, 赵君玫, 郭盛典, 等. 大黄对老龄大鼠脑缺血再灌注肾脏损伤保护作用的研究 [J]. 河南中医, 2002, 22(6): 15-17.
[90] 陈江林, 曾靖, 黄志华, 等. 3′-大豆苷元磺酸钠对大鼠脑缺血再灌注肾脏损伤保护作用的研究 [J]. 时珍国医国药, 2009, 20(4): 773-774.
Research progress on traditional Chinese medicine in treatment of multiple organs injury caused by cerebral ischemic stroke
LONG Yu1, ZHANG Yu-lu1, WAN Jin-yan1, LIU Song-yu1, NI Li1, LI Nan1, YANG Ming2
1. College of Pharmacy, Chengdu University of Traditional Chinese Medicine, Chengdu 611137, China 2. College of Pharmacy, Jiangxi University of Traditional Chinese Medicine, Nanchang 330004, China
Cerebral ischemic stroke (CIS) can cause multiple organ injuries, which includes the heart, liver, spleen, lung, and kidney injuries. These diseases are composed of multiple pathological links, which have complex pathogenesis, high incidence rate, high disability rate, and high mortality rate. Severe cases can develop the multiple organ dysfunction syndromes (MODS). At present, any treatment aiming at single link and single target is not adequate to cure the disease. While it has been found that traditional Chinese medicine can intervene in many aspects of the diseases through multiple targets. Traditional Chinese medicine has obvious protective effect on MODS caused by CIS through antioxidant effect, inhibition of inflammatory reaction and regulation of energy metabolism. However, there are few related reviews. Therefore, the effects of traditional Chinese medicine and its active ingredients on multiple organ injuries after CIS are reviewed in this paper, so as to give full play to the therapeutic effect and treatment scope of traditional Chinese medicine, to provide scientific basis and reference for clinical intervention of traditional Chinese medicine in cerebrovascular diseases with multiple organ injuries.
traditional Chinese medicine; multiple targets; cerebral ischemic stroke; multiple organs injury; multiple organ dysfunction syndromes
R282.710.5
A
0253 - 2670(2021)07 - 2106 - 11
10.7501/j.issn.0253-2670.2021.07.028
2020-08-17
国家自然科学基金资助项目(81673615);国家大学生创新创业训练计划项目(S201910633028);全国中药特色技术传承人才培训项目(T20194828003);四川省人力资源和社会保障局资助项目(00809503);四川省中医药管理局项目(2018QN009);成都中医药大学杏林学者(QNXZ2018018);成都中医药大学新冠病毒应急专项(XGZX2010);江西中医药大学现代中药制剂教育部重点实验室开放基金资助项目(TCM-201908)
龙 宇,女,硕士研究生,从事药剂学研究。Tel: 18482123308 E-mail: 1548650993@qq.com
李 楠,女,硕士生导师,教授,从事中药新剂型、新技术、新工艺研究。Tel: 13880703849 E-mail: 55743198@qq.com
杨 明,男,博士生导师,教授,从事中药新剂型、新技术、新工艺研究。Tel: (0791)87118108 E-mail: yangming16@126.com
[责任编辑 崔艳丽]

