水系锌离子电池用钒基正极材料的研究进展
衡永丽,谷振一,郭晋芝,吴兴隆,,*
1东北师范大学化学学院,长春 130024
2东北师范大学,紫外光发射材料与技术教育部重点实验室,长春 130024

1 引言
随着化石燃料的不断消耗和温室效应的逐步加剧,能源匮乏和环境污染已经成为人类社会可持续性发展所面临的两大难题1,2。开发利用风能、太阳能等可再生能源来代替煤、石油等不可再生能源已刻不容缓,然而这些新能源对外界的自然条件有很大的依赖性。因此,高效的能量存储和转化装置必不可少3。近年来,锂离子电池具有高能量密度、长使用寿命以及成熟的制备工艺等特点,已逐步占据了商用可充电电池的市场。但是,锂资源有限、成本高、有机电解液使用造成的安全性和环境等问题,严重阻碍了锂离子电池的进一步发展和大规模化应用4–7。相比于有机电解液的易燃、易挥发等安全隐患,水系电解液则具有更高的安全性,以及价格低、离子传导率高、易于制造等工艺优点,被广泛地研究,有望用于开发下一代的绿色环保可充电电池8,9。在众多水系可充电电池中,水系锌离子电池(aqueous zinc-ion batteries,AZIBs)以锌为负极而表现出的独特优势而备受关注,主要体现在高理论容量(820 mAh·g-1和5855 mAh·cm-3)、低氧化还原电位(相对于标准氢电极,电压为-0.76 V)、在水中具有高稳定性,以及储量丰富和便宜廉价等10–14。因此,AZIBs具有安全性高、成本低、资源丰富和环境友好等优点,被认为是可应用于大规模储能的先进二次电池体系。
19世纪60年代,碱性Zn/MnO2电池发展成为一次电池的主要领导者。但早期的Zn/MnO2电池系统技术相对落后、成本较高、资源浪费较为严重,为节省资源和提高利用效率,研究人员开发了可充电碱性Zn/MnO2电池。然而,可充电碱性Zn/MnO2电池在充放电过程中MnO2正极和Zn负极发生不可逆副反应,导致电池容量损失,库仑效率降低。直到2012年,Xu等15用温和的硫酸锌作电解质,α-MnO2作正极材料,Zn作负极材料,成功地研制出可充电的AZIBs。随着可充电AZIBs的发展,一系列正极材料被研究:主要包括多态MnO2(包括α、β、γ和δ型)16–21和普鲁士蓝的类似物(例如Zn3[Fe(CN)6]2)22–24。MnO2晶体结构不稳定,在充放电过程中表现出较差的循环性能;而普鲁士蓝类似物虽然晶体结构稳定,但储Zn性能较差(容量小于100 mAh·g-1)。因此,开发具有稳定结构和高容量的锌离子可脱嵌正极材料已成为AZIBs的研究关键之一。2016年,研究者们将层状的Zn0.25V2O5·nH2O作为储存Zn2+的正极材料,其放电比容量可达300 mAh·g-1,循环寿命超过1000周期25。随着钒基材料展现出令人惊喜的储Zn性能,钒基化合物,如层状或隧道型钒氧化物和钒酸盐、钒基钠离子超导体(NASICON,通式为A1B2(PO4)3,其中A为一价阳离子,B为多价态过渡金属离子),受到了广泛的关注和研究。与MnO2和普鲁士蓝类似物相比,钒基化合物用作储Zn正极材料时具有可逆容量高和结构丰富可变等优点。然而,钒基化合物仍存在一些问题,例如:较为复杂和具有争议性的储Zn机理,低的平均工作电压和不能令人满意的性能表现。
在本综述中,我们将系统地阐述各类钒基正极的储能机制和结构特征,并探讨钒基材料在AZIBs的应用和发展近况,以及它们的性能优化策略,包括结构设计(如预先插入金属离子和水分子)、形貌调控(如碳包覆)、电解质优化(如调节组成和浓度)等。在最后一节中,我们展望了新型钒基AZIBs正极未来的发展方向。
2 钒基材料概述
钒元素性质活泼、价态多变,并且在我国资源丰富。钒的常见化合价为+2、+3、+4、+5,因此可以发生多电子转移的氧化还原反应,表现出较高的容量性质。而且,钒基化合物通常具有不同的晶体结构和电化学特性。常见的钒基化合物主要有钒基氧化物、钒基硫化物和钒基磷酸盐,它们具有多种开放式结构,有利于离子的嵌入/脱出。因此,钒基化合物被广泛应用到电池电极材料之中。尤其近年来,钒基材料被广泛地用于水系锌离子电池体系中,展现出较高的储锌性能。在水系锌离子电池中,V2O5、VO2、VS2、Na3V2(PO4)3、Na3V2(PO4)2F3是钒基化合物中研究较为广泛的正极材料,这主要归因于它们独特的晶体结构而具有优异的储锌能力。V2O5、VO2、VS2材料具有层状结构和较大的层间距,并且通过对其层间距调节可以获得高储锌性能的正极材料。而Na3V2(PO4)3、Na3V2(PO4)2F3是钠快离子导体(NASICON)具有代表性的材料,晶体结构是由[VO6]八面体和[PO4]四面体通过共O/F相桥接,堆积成独特的三维隧道结构,具有较强诱导效应的和F-提升了晶体结构稳定性和工作电压,更有利于Zn2+的传输与储存。关于钒基材料在水系锌离子电池中的具体应用,将在下文进行详尽的描述,在此不做过多的赘述。
3 AZIBs用钒基正极材料的研究现状
3.1 V2O5基正极材料
3.1.1 V2O5
V2O5是一种典型的层状钒基化合物,其中V原子和O原子构成[VO5]四方棱锥,进而通过共顶点或者共边的方式形成层状结构;相邻层间通过范德华力连接,层间距约为0.58 nm,远大于Zn2+的半径(0.075 nm)11,26,利于Zn2+在V2O5层间扩散。在充放电过程中,V2O5发生两电子氧化还原反应(V5++ 2e-⇌ V3+),可以提供高的理论储锌容量(589 mAh·g-1)27。通常,V2O5材料在储锌过程中存在两个明显的充放电平台。放电时,Zn2+嵌入到V2O5层间,V5+被还原为V4+,对应于0.8 V左右的电压平台,随着Zn2+的继续嵌入,部分V4+被还原为V3+,呈现出约0.4 V的电压平台;反之,充电时,发生Zn2+的脱出反应,V3+被氧化为V4+和V5+。但是,多价Zn2+与V2O5晶体结构间存在强静电相互作用,导致Zn2+嵌入/脱出过程的可逆性和动力学性能受限。此外,纯相V2O5导电性差,结构稳定性低,易溶解在低浓度的水系电解液中,用作AZIBs的正极材料,通常呈现出较低的电压平台(约0.8 V)和不能令人满意的循环性能(< 1000圈)28,29。因此,近年来,许多研究人员已经采用不同的方法来克服上述缺点,从而改善AZIBs的电化学性能。
对于水系可充电金属离子电池体系普遍存在的电压问题,早期的研究已证明优化电解质是一种简单有效的策略,可以显著地拓宽水系电解液的电化学稳定窗口,从而有效提升电池的能量密度以及循环稳定性8,30,31。在传统的电解液(即“水包盐”电解液)中,自由水分子可以与金属Zn负极反应生成H2,Zn2+可被溶剂化,形成或者惰性的Zn(OH)2、ZnO副产物32,降低AZIBs的库伦效率和电化学性能。因此,研究人员考虑将高浓度的电解液(即“盐包水”电解液)引入AZIBs。Mai课题组33设计出新型的Zn/V2O5电池体系,如图1a所示,采用21 mol·L-1双三氟甲基磺酰亚胺锂(LiTFSI)-1 mol·L-1三氟甲烷磺酸锌为电解质。图1b–f为合成的V2O5正极材料的一系列表征,可以看出V2O5具有较大的内层间距。电化学测试结果表明V2O5正极具有良好的倍率性能和循环性能:在50 mA·g-1的电流密度下,V2O5正极具有238 mAh·g-1的放电比容量,在1000 mA·g-1时仍有156 mAh·g-1的容量贡献;而且在2000 mA·g-1的大电流密度下循环2000圈之后,容量保持率可达80%。此外,相比于Zn(CF3SO3)2电解液(图2),“盐包水”电解液能够有效抑制H2O分子在高电压区分解而释放出H2和O2的反应,从而显著地提高了AZIBs的电压平台(从0.6 V增加至1.0 V),可同时实现长循环和高能量密度。电解液组成的改变,使得Zn/V2O5电池的工作机制也随之发生变化。由于电解液中存在大量的Li+,在电化学测试过程中Li+可能在V2O5晶体中进行脱嵌。作者通过原位X射线衍射(XRD)测试证明了高度可逆的Li+嵌入/脱出过程;同时,根据非原位X射线光电子能谱(XPS)测试结果,当完全放电至0.2 V时,在1046和1023 eV处可以观察到两个明显的谱峰,分别对应于Zn 2p1/2和Zn 2p3/2,证明Zn2+也嵌入V2O5正极材料中,因此说明Zn2+和Li+均参与到该Zn/V2O5电池的电化学过程中。

图1 (a) Zn/V2O5电池体系的示意图,(b–f) V2O5正极的一系列表征33Fig.1 (a) Schematic illustration of Zn/V2O5 battery system, (b–f) a series of characterization techniques for V2O5 cathode 33.

图2 Zn/V2O5在Zn(CF3SO3)2-LiTFSI和Zn(CF3SO3)2中的电化学性能对比33Fig.2 Electrochemical performance of Zn/V2O5 in Zn(CF3SO3)2-LiTFSI electrolyte and Zn(CF3SO3)2 electrolyte 33.
上述的研究表明V2O5在不同电解液中的性能和反应机理有所差异。同时,也有可能发生相转变。例如,Chen等34将合成的多孔V2O5纳米纤维正极在3 mol·L-1Zn(CF3SO3)2电解液中进行充放电。研究发现在首圈放电时,随着Zn2+嵌入,会产生一个新相焦钒酸锌Zn3+x(OH)2V2O7·2H2O。充电时,部分Zn2+从焦钒酸锌中脱出。在后续的充放电过程中,仅在焦钒酸锌中发生Zn2+的脱嵌过程。并且,在循环过程中,形貌也会逐渐发生变化,转变为纳米片状,利于电子的传输和Zn2+的扩散,因此表现出优异的循环性能。相比之下,在3 mol·L-1Zn(SO4)2中进行充放电时,则表现出较差的电化学性能。这可能是由于阴离子的体积较大,可降低溶剂化作用,提高离子电导率,实现快速的动力学过程。一系列研究证实了电解液(组成、浓度、pH等)对于一个电池体系的重要作用,以及对于电池的电化学原理和电化学性能的影响35–38。
此外,还可以通过微观形貌调控的方式改进V2O5正极材料。商用的V2O5通常为较大块状,离子和电子传输速率慢,并且在Zn2+的嵌入/脱出过程中结构易坍塌,从而影响电池的倍率性能和循环性能。而纳米结构材料具有较大的比表面积和较多的活性位点,可以改善电池的动力学性能。到目前为止,研究已发现的具有不同类型纳米结构的V2O5正极材料(图3),主要包括零维的纳米球39、一维的纳米管28、二维的纳米片40–42以及三维的多孔结构43,44等。最近Sun小组41采用简易的水热法合成出V2O5@AB纳米片(图4a–e),与传统的V2O5纳米片相比,该材料的独特之处在于:添加乙炔黑(AB)作为相邻两片的间隔物,不仅可以有效解决纳米片的堆叠问题,充分发挥出纳米片结构的优势,为嵌入的Zn2+提供大量活性位点,缩短离子扩散路径,提高离子扩散速率;而且AB作为常用的一种导电添加剂,能够提高V2O5的导电性。因此,该正极材料在0.1 A·g-1的电流密度下具有高达452 mAh·g-1的放电比容量,甚至在30 A·g-1的高电流密度下仍有268 mAh·g-1的比容量,表现出优异的倍率性能(图4f);同时,在10 A·g-1的电流密度下,经过5000个循环后,容量保持率高达92%,表现出好的循环性(图4g)。这项有趣的研究为进一步地改进其他正极材料的纳米结构提供了新的思路。

图3 不同类型纳米结构的V2O5正极材料Fig.3 V2O5 cathode materials with different types of nanostructures.

图4 (a)添加AB作为间隔物的V2O5和没有添加AB的V2O5的合成过程;(b,c)扫描电子显微镜(SEM)图;(d) XRD图;(e)拉曼图;(f,g) AZIBs的电化学性能:(f)倍率性能和(g)循环性能41Fig.4 (a) Strategies of adding AB spacer to prepare spaced V2O5 and without adding AB to prepare stacked V2O5;SEM images of (b) spaced and (c) stacked V2O5; (d) XRD patterns of spaced and stacked V2O5; (e) Raman spectra of spaced and stacked V2O5; electrochemical performance of AZIBs: (f) rate performance and (g) cycling performance 41.
3.1.2 V2O5·nH2O
不同于上述具有典型层状结构的V2O5材料,V2O5·nH2O由两个[VO6]八面体层构成,呈现特殊的双层结构。水分子通常处于两层中间,可作为支柱,提供更大的内层间距(>1.0 nm)45,46;同时,水分子也可以减小Zn2+的有效电荷,使得Zn2+的脱嵌过程更加容易进行,因此表现出更好的电化学性能。Yan等46采用液相法设计合成了具有双层结构的V2O5·nH2O/石墨烯(VOG)作为AZIBs正极材料,Zn片作负极,3 mol·L-1Zn(CF3SO3)2作电解质,组成电池,以探究H2O分子在Zn2+嵌入/脱出过程中的作用。他们通过透射电子显微镜(TEM)、能谱仪(EDS)元素分析等分析技术对制备的VOG材料的微观形貌进行表征(图5a,b),可以看出V2O5·nH2O纳米线骨架通过还原氧化石墨烯支撑形成板状结构。热重分析可以探究出结构水分子的含量(n=1.29)。随后,该材料在350 ℃下退火可得到不含结构水的VOG (即VOG-350)。从这两种正极材料的电化学测试结果中可以明显看到VOG比VOG-350具有更优异的倍率性能和循环稳定性,如图5c,d所示,当电流密度从0.3 A·g-1增加至15 A·g-1,前者的比容量仅降低了14%,并且在6 A·g-1的电流密度下循环900圈后仍有71%的容量保持率。此外,对充放电过程中不同状态的正极材料进行XRD测试可以证明Zn2+嵌入/脱出过程的可逆性。同时,他们发现在放电过程中,随着Zn2+的嵌入,VOG的层间距从1.04 nm增加至1.35 nm (图5e)。这种现象可能是由于H2O分子的溶剂化作用使得Zn2+的有效电荷数降低,从而与V2O5结构中O2-的静电相互作用减弱,因此层间距离增加,表现出更快的动力学性能和更优异的倍率性能。以上的研究结果证实在V2O5层间插入H2O分子是一个可行的方法去改善AZIBs的电化学性能。但是,插入H2O分子(半径约0.2 nm)的数量对于V2O5结构和性能的影响有待进一步探索。
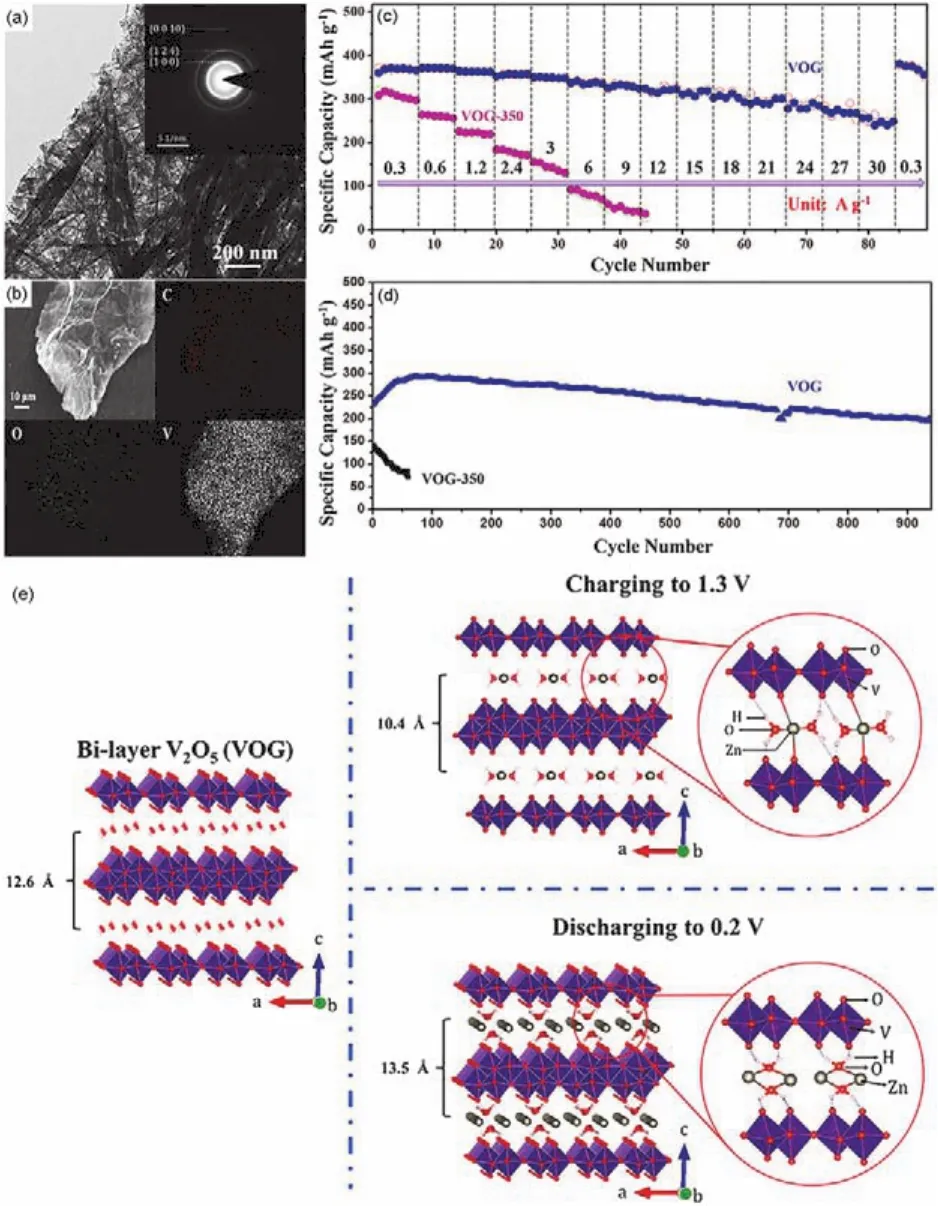
图5 VOG的(a) TEM图和电子衍射图以及(b) EDS元素图谱;(c) VOG和VOG-350的倍率性能;(d) VOG和VOG-350在6 A·g-1时的循环性能;(e) 原始的VOG、充电至1.3 V、放电至0.2 V的晶体结构46Fig.5 (a) TEM image and electron diffraction pattern and(b) EDS elemental mappings of VOG; (c) rate performance of VOG and VOG-350; (d) cycling performance of VOG and VOG-350 at 6 A·g-1; (e) the crystal structures of pristine VOG, VOG after charging to 1.3 V, and discharging to 0.2 V 46.
3.1.3 MxV2O5·nH2O
自从2016年,Nazar团队25首次合成出层状的Zn0.25V2O5·nH2O并将其作为AZIBs的正极材料,表现出较高的容量(约300 mAh·g-1)和良好的循环性能(>1000圈),在V2O5层间预先插入金属离子已经成为一种常用的提高其结构性能和电化学性能的有效策略,受到广泛的关注和研究。到目前为止,研究人员已设计将许多不同种类的金属离子(包括碱金属离子Li+、Na+、K+,碱土金属离子Ca2+、Mg2+,过渡金属离子Ag+、Zn2+等)插入到V2O5层间,合成出一大批结构独特、性能优异的钒酸盐类衍生物(例如,LixV2O547、Na0.33V2O548、Ca0.25V2O549、Ag0.33V2O550)。这一系列研究发现预先嵌入的金属离子可以作为支柱,提高结构稳定性,实现充放电过程中Zn2+快速可逆的嵌入/脱出反应51。然而,这些预先嵌入的金属离子可能导致V2O5的初始结构发生变化,并且大量金属离子的插入可能降低V2O5基材料的比容量。因此预嵌入的金属离子的种类和数量是一个值得深入研究的问题。最近,Zhou课题组52以过渡金属离子为例,探究其种类和数量对V2O5基正极材料的结构和电化学性能的影响。他们采用水热法将一系列过渡金属离子预先插入V2O5层间,得到TxV2O5·nH2O (TVO,T为过渡金属Fe、Co、Ni、Mn、Zn、Cu);进而在300 ℃下退火,可得到TxV2O5·nH2O-300 (TVO-300)。作者以CuVO为例,根据不同Cu含量的材料退火所得复合物的XRD测试结果(图6a–c),分析发现Cu的含量会影响(001)平面的晶格间距。从图6d中可以看出在退火时Cu0.05VO中(001)平面的晶格间距会缩小,而Cu0.1VO和Cu0.2VO则基本保持恒定,这意味着通过添加0.1摩尔比的Cu即可提升其结构稳定性和提高其结晶度。电化学测试结果表明该正极材料(CuVO-300)具有优异的长循环稳定性,在10 A·g-1的电流密度下循环10000圈后仍有180 mAh·g-1的比容量,容量保持率为88%,远远优于相同条件下未插入金属离子的V2O5(VO-300),如图6e所示。研究发现预先插入其他过渡金属离子也表现出相近的电化学性能(图6f,g),然而当预先插入半径较大的Ag+时,则表现出较差的电化学性能。根据XRD和XPS测试结果可以分析出该电池体系的工作机理,在首圈放电过程中,Zn2+嵌入正极CuVO-300中,形成两个不同的可逆相ZnxCu0.1V2O5·0.08H2O、Zn0.25V2O5·H2O以及一个稳定的不可逆相Zn3(OH)2V2O7·2H2O;后续的循环过程中,大部分Zn2+脱出形成ZnyCu0.1V2O5·0.08H2O,同时Zn0.25V2O5·H2O消失,然而由于OH-的存在,Zn3(OH)2V2O7·2H2O中的Zn2+无法脱出。此外,CuVO-300在极端环境中(0、50 ℃)仍表现出优异的电化学性能,在高温环境下,离子扩散能力提高,容量增加;低温下,ZnSO4溶解度降低,离子扩散能力降低,容量降低。因此,这类正极材料在AZIBs中有广阔的发展空间和良好的应用前景53,而且这种插入金属离子的方法也同样适用于其他电极材料,可以有效解决离子扩散能力低、导电性差和结构不稳定的问题。更有趣的是,这些研究为开发新型的钒基AZIBs正极材料提供了新的方向,例如,设计合成具有混合价态的钒的正极54,以及考虑插入其他更优的粒子以期获得高性能电极材料55。
3.2 VO2基正极材料
VO2具有d1电子体系,存在多种不同的晶型,主要包括热力学稳定的金红石型VO2(R),单斜晶VO2(M)和亚稳的四方晶VO2(A)56,单斜晶VO2(B)、VO2(C)、VO2(D)57,58。尽管化学式相同,但他们的晶体结构和电子结构却完全不同且比较复杂。其中,金红石型VO2(R)和单斜晶VO2(M)的金属-绝缘体转变温度接近室温(约68 ℃)57,因此在电子和光学方面的应用非常广泛。而亚稳的单斜晶VO2(B)通常表现出开放的骨架59,60,研究人员考虑将其用作AZIBs的正极材料。表1总结了近年来报道的钒基AZIBs正极材料的电化学性能。

表1 近年来报道的几种钒基AZIBs正极材料Table 1 Several vanadium-based cathode materials for AZIBs reported in recent years.

continued Table 1
3.2.1 VO2(B)
近年来,VO2(B)作为AZIBs的正极材料已经取得了一系列较好的研究成果。2018年,Park等60最早提出用VO2(B)作为AZIBs的正极材料并且采用第一性原理计算证实其可行性。该小组采用低温溶剂热法成功合成出VO2(B),之后与还原氧化石墨烯(rGO)复合形成VO2(B)/rGO以克服自身导电能力弱的缺点。复合前后,VO2(B)的晶体结构不会改变,仍是由上下相对的2个[VO6]八面体共用顶点形成[VO6]双层,然后与其他的[VO6]八面体通过共边的方式,沿(011)方向堆叠,产生宽0.3725 nm、高0.4083 nm的隧道,为Zn2+提供了传输路径,利于Zn2+的扩散。为了确定具有最低自由能的Zn2+的稳定位点和扩散路径,他们根据价键和(BVS)能量图预测了Zn2+嵌入的四个位点,分别称为ZnC、ZnA1、ZnA2、ZnC’(图7a–c)。在此基础上,又依据第一性原理计算分析了VO2(B)的相变反应和理论氧化还原电势。图7d–f所示的结果表明ZnxVO2(B)(0 ≤x≤ 0.5)在Zn2+的嵌入/脱出过程中经历了一个x≈ 0.12的中间相,预测的氧化还原电势约为0.61 V,与实验所得结果相近。研究发现当Zn2+嵌入VO2(B)结构时,ZnA2被认为是最优的储锌位点,Zn2+在其中扩散所需的活化能约为586 meV,这意味着Zn2+能够容易地迁移到VO2(B)晶体结构中。不幸的是,在循环过程中会生成惰性的副产物Zn4SO4(OH)6·0.5H2O,影响活性正极材料的电子传导,加速容量衰减。用其他锌盐(如Zn(CF3SO3)2)替代Zn(SO4)2作为电解质70,71或者调节电解液的pH可以解决这一问题。此外,与V2O5相似的是,结构水分子的存在也可以扩展VO2(B)的内部空间63,加速Zn2+的传输速率,提高AZIBs的电化学性能。

图7 VO2(B)在(a) a–b,(b) a–c,(c) b–c平面上的BVS能量图展示了VO2(B)晶体结构中所有可能的Zn2+位点;(d) ZnxVO2(B) (0 ≤ x ≤ 0.5)的生成能;(e)计算所得ZnxVO2(B)的平均氧化还原电势和实验测得充放电曲线;(f)预测Zn2+嵌入VO2(B)的机理60Fig.7 Bond-valence sum energy map of VO2(B) for the (a) a–b, (b) a–c, (c) b–c planes show all possible zinc sites in the VO2(B) crystal structure; (d) formation energy of ZnxVO2(B) (0 ≤ x ≤ 0.5); (e) calculated average redox potential and experimentally measured charge/discharge curve of ZnxVO2(B); (f) predicted mechanism of Zn2+ intercalation into VO2(B) 60.
3.2.2 VO2(D)
研究人员也合成了其他亚稳态的VO2用作AZIBs的正极材料。例如,Yang小组62采用简易的无模板水热法制备了VO2(D)空心纳米球,通过场发射扫描电子显微镜(FESEM) (图8a)和TEM (图8b)测试显示球体直径约为400 nm,外壳厚度约为50 nm,所有球体表面粗糙,由众多纳米棒堆积而成。薄的外壳和大的内部空腔利于Zn2+快速扩散到电极材料的中空内部,从而提高了VO2(D)电极材料的利用率。该正极材料在0.1 A·g-1的电流密度下具有408 mAh·g-1的放电比容量,甚至在20 A·g-1的高电流密度下仍有200 mAh·g-1的容量,表现出良好的倍率性能(图8c);令人惊讶的是,该电极材料在3 mol·L-1Zn(SO4)2电解液中实现了高达30000圈的超长循环使用寿命,远远超过已报道的其他钒基材料。XRD和XPS测试可以进一步研究Zn2+的嵌入/脱出反应对VO2(D)结构的影响,经分析发现在充放电过程中VO2(D)转变为V2O5·xH2O,同时在电极表面会发生可逆的Zn4SO4(OH)6·xH2O沉淀/溶解反应,这可能与电解液的pH变化有关,由此推断出Zn2+和H2O会一同在电极材料中进行可逆的嵌入/脱出过程,可以实现良好的动力学。

图8 VO2(D)的(a) FESEM和(b) TEM图,(c)不同电流密度下的充放电曲线62;VO2(M)/CNT的(d) TEM和(e) HR-TEM图,(f)不同电流密度下的充放电曲线63Fig.8 (a) FESEM and (b) TEM images and (c) charge/discharge curves at different current densities of VO2(D) 62;(d) TEM and (e) HR-TEM images and (f) charge/discharge curves at different current densities of VO2(M)/CNT 63.
3.2.3 VO2(M)
VO2(M)由扭曲的[VO6]八面体构成,其中[VO6]八面体交错排列并且通过共用O原子连接成网状,形成约0.318 nm长的隧道。与VO2(B)相比,VO2(M)具有更致密的隧道和更高的空间利用率,便于离子迁移;而且研究发现VO2(M)具有更好的热稳定性。近期,Miao课题组63开发了一种简便的方法成功制备出与碳纳米管(CNT)复合的VO2(M)/CNT薄膜正极(图8d,e),并且探究了不同的温度条件和碳含量对该电极材料结构和电化学性能的影响。他们将含有90 mg CNT的样品分别在400、600、800 ℃温度条件下退火,可以得到3种不同的钒氧化物,分别为V2O5、VO2(M)、V2O3;对于不同碳含量的样品的研究揭示了高碳含量的重要作用:CNT不仅可以促进离子的扩散,而且能够增强VO2(M)晶体结构的应变能力。此外,借助多种分析技术,对VO2(M)正极中H+的脱嵌过程进行了研究。与传统的Zn2+脱嵌过程相比,H+脱嵌机制的特点主要表现在:(1)反应过程中,正极VO2(M)的体积效应较小,V原子的价态变化也不明显;(2)电解液的pH反复变化,导致羟基硫酸锌水合物存在沉淀溶解平衡;(3) H+的扩散速率比Zn2+的更快,表现出更好的倍率性能(图8f)。这项研究为设计高性能的钒基AZIBs正极提供了新思路。许多钒基AZIBs正极材料在低电流密度下具有较高的容量,但是在高电流密度下的容量则普遍较低,这可能是由于高电流密度下离子扩散速率无法达到要求,限制了他们的实际应用。因此,开发具有稳定结构的新型钒基正极材料,或者对现有材料进行修饰(例如,与导电物质复合),引入H+的脱嵌反应,有望实现超高倍率性能。
尽管目前的研究已经证明将VO2用于新型AZIBs正极可以表现出优异的电化学性能,但是它仍然面临一些难题。例如,作为传统的多晶型物,制备纯相的VO2仍是一个巨大的挑战,而且,VO2的不同相之间容易发生转换,对于不同相VO2的合成条件需要严格控制。
3.3 磷酸钒盐类正极材料
在NASICON型磷酸钒盐(基本形式为M3V2(PO4)3,M = Li、Na)的晶体结构中,每2个[VO6]八面体和3个[PO4]四面体通过共用顶点O原子的方式连接,形成一个[V2(PO4)3]结构基元,然后再通过[PO4]与其他的[V2(PO4)3]连接起来,构成开放的三维骨架,可以提供稳定的位点和离子迁移通道。M3V2(PO4)3晶体结构存在2种不同化学环境的金属离子位点:六配位环境的6b (M1)位点和八配位环境的18e (M2)位点72。在Na3V2(PO4)3晶体结构中,1个Na+占据M1位点,2个Na+占据M2位点;充放电过程中M2位的2个Na+进行可逆的嵌入/脱出反应,发生2个电子的转移,表现出高达117.6 mAh·g-1的比容量73–75,在钠离子电池中具有广泛的应用。Zn2+的离子半径(0.075 nm)比Na+(0.102 nm)的更小,所以将Na3V2(PO4)3用于锌离子电池在理论上是有可能的。近年来,相关的研究已经开展,以获得一种新型的高性能AZIBs正极材料64,65,67。
3.3.1 Na3V2(PO4)3
2016年,Huang课题组64采用传统的水热法合成出碳包覆的Na3V2(PO4)3纳米颗粒(Na3V2(PO4)3/C),如图9a–c所示,并且尝试将其用作AZIBs的正极材料,Zn片作为负极,弱酸性的0.5 mol·L-1Zn(CH3COO)2作为水系电解液。图9d是该电池前两圈的恒流充放电曲线,从中可以看出首次充电曲线的电压平台与后续过程的存在明显的不同。首次充电时,两个Na+从Na3V2(PO4)3中脱出,形成脱钠相NaV2(PO4)3,产生1.40 V左右的电压平台;随后在放电时,Zn2+嵌入到脱钠相中,产生另一新相ZnxNaV2(PO4)3,呈现出一个较低的电压平台(约1.25 V);后续的充放电过程,可以观察到两个接近的电压平台(1.05/1.28 V),仅发生Zn2+的可逆嵌入/脱出反应。图9f为充放电过程中Na3V2(PO4)3正极的相变示意图。该电池体系表现出良好的电化学性能,如图9e所示,在0.5C的电流密度下,首圈放电容量达到97 mAh·g-1,其中前10圈的容量衰减较快,这可能是由于Zn2+嵌入导致晶格畸变,活性位点损失;在之后的循环中容量衰减会变慢,100圈之后,减至72 mAh·g-1(容量保持率为74%)。此后,通过XRD、TEM和元素分布分析技术对ZnxNaV2(PO4)3的结构进一步分析发现Zn2+的嵌入可能导致NASICON结构中离子的占据位点发生变化。在最近的研究中,Cui课题组76将脱钠相NaV2(PO4)3直接用作AZIBs的正极,通过多种分析技术证实了Zn2+的嵌入可以激活NASCION结构的M1位点,Zn2+和Na+在ZnxNaV2(PO4)3晶格中混合占据、协同迁移,可以稳定晶体结构,并且提高材料的力学性能和导电性能,从而表现出优异的电化学性能。

图9 合成的Na3V2(PO4)3/C的(a, b) SEM和 (c) TEM图;Zn/0.5 mol·L-1 Zn(CH3COO)2/Na3V2(PO4)3电池的电化学性能:(d)前两圈的充放电曲线;(e) 0.5 C时的循环性能;(f) Na3V2(PO4)3正极的相变过程64Fig.9 (a, b) SEM and (c) TEM images of Na3V2(PO4)3/C sample; (d) charge/discharge curves for the first two cycles; (e) cycling performance at 0.5 C for Zn/0.5 mol·L-1 Zn(CH3COO)2/Na3V2(PO4)3 battery;(f) phase transition of Na3V2(PO4)3 cathode 64.
上述研究证实了NASICON型材料作为AZIBs正极,提供了多价锌离子脱嵌的可行性,虽然其电化学性能不及钠离子电池,但该研究为开发高性能的AZIBs正极材料提供了一个新的发展方向。同时,针对NASCION型材料自身导电性差的缺点以及多价离子在嵌入过程对晶体结构的影响,研究人员可采用表面碳包覆、元素掺杂等方法对Na3V2(PO4)3进行优化,进一步提高其电化学性能。
3.3.2 Na3V2(PO4)2F3
目前已报道的Na3V2(PO4)3正极通常具有较高的容量(相比于118 mAh·g-1的理论容量,基于2个电子的氧化还原反应),但是AZIBs的能量密度与钠离子电池仍有一定的差距,难以实际应用。Li等66首次报道了碳包覆的Na3V2(PO4)2F3(即N3VPF@C)作为AZIBs的正极材料(图10a),采用碳膜功能化的Zn(即CFF-Zn)作为负极,以及2 mol·L-1Zn(CF3SO3)2水溶液,组成电池。该电池表现出更高的电压(1.62 V,图10b,c)以及显著的循环稳定性(在1 A·g-1的电流密度下,循环4000圈后,容量保持率高达95%)。这可能是N3VPF@C正极与CFF-Zn负极共同作用的结果:一方面,Na3V2(PO4)2F3框架中[VO4F2]八面体、[PO4]四面体的有序排列和堆叠为Zn2+提供了大量的扩散通道(图10d),并且强电负性的F元素的引入使得结构更加稳定。此外,在首次充电时,电解质Zn(CF3SO3)2在高电压区(约1.8 V)发生氧化分解为ZnF2、ZnCO3等不溶产物,覆盖于正极表面,形成正极电解质界面(CEI膜)。在之后的充放电过程中,正极表面的CEI膜可以有效抑制正极的溶解和减少水的分解,利于长循环。另一方面,包覆碳膜的Zn负极可以有效抑制循环过程中的枝晶生长,为整个电池的循环使用提供了有利条件。研究还发现该正极可用于柔性锌离子电池,表现出良好的机械性能和电化学性能,因此该电池有望用于可穿戴型电子器件。

图10 (a) N3VPF@C的XRD和SEM图;(b) CFF-Zn/2 mol·L-1 Zn(CF3SO3)2/N3VPF@C电池在0.8–1.9 V之间,在0.2 mV·s-1下的CV;(c)在0.08 A·g-1下,前三圈的充放电曲线;(d)电池构造和储能机制66Fig.10 (a) XRD pattern and SEM image of N3VPF@C; (b) CV curves in the potential range of 0.8–1.9 V at a scan rate of 0.2 mV·s-1 and (c) initial three charge/discharge profiles at 0.08 A·g-1 for CFF-Zn/2 mol·L-1 Zn(CF3SO3)2/N3VPF@C battery; (d) battery structure and Zn storage mechanism illustrations 66.
3.4 其他钒基正极材料
前面所述的V2O5、VO2、磷酸钒盐等钒基正极均为含氧的钒基化合物,除此之外,已报道的钒基化合物中还包括VS2、VS4等不含氧的钒硫化合物。VS2具有层状结构,层间距约为0.576 nm,有利于Zn2+的嵌入/脱出反应。2017年,Mai课题组68首次报道了层状的VS2作为AZIBs的正极材料,锌金属作负极,弱酸性的ZnSO4作电解质,在0.05 A·g-1的电流密度下具有190.3 mAh·g-1的容量,而且也表现出良好的倍率性能和循环稳定性。这可能是由于VS2结构中不含氧,Zn2+在脱嵌过程中所受到的静电相互作用较钒基氧化物的小,则扩散速率会加快;同时,较大的内层间距可以减弱Zn2+的嵌入对于正极晶体结构的影响。作为一种新型的钒基正极材料,尽管目前对VS2的研究刚起步,但它表现出很好的发展前景。2018年,Qin等69采用水热法制备出VS4@rGO复合物用作AZIBs的正极材料,在1 A·g-1的电流密度下具有180 mAh·g-1的容量。并且,VS4具有独特的链式结构和rGO具有高导电性,因此也表现出良好的倍率性能。然而,基团的存在,使得将其用作电极材料时通常表现出复杂的反应机理。该研究小组通过电化学测试和XRD等分析技术深入探究了VS4@rGO正极在充放电过程中的储锌机理。根据循环伏安测试,可以看出首次充放电时,仅存在一个氧化峰(1.53 V),可能是VS4@rGO正极的电化学活化过程;而在后续充放电过程中,存在两对明显的氧化还原峰(0.54/0.67 V,0.89/1.01 V),对应于Zn2+的脱嵌反应,并且1.53 V处的氧化峰逐渐增至1.62 V,对应于复杂的转化反应。进一步通过分析正极在第三圈时不同充放电状态下的XRD测试证明了脱嵌反应和转化反应组成的协同反应机理。在完全放电状态(0.35 V)下,12.3°、30.1°处的两峰表明生成新相Zn3(OH)2V2O7·2H2O,其中V为+5价,这可能是由于电子从V4+转移至。并且从1.8 V放电至0.8 V时可以观察到S的出现,继续放电,出现28.8°、48.1°、57.2°处衍射峰表明ZnxVS4的产生。在0.35到0.8 V充电时,Zn2+脱出,ZnxVS4变为VS4,从1.4至1.8 V,Zn3(OH)2V2O7·2H2O和S对应的衍射峰强度增加,而VS4的衍射峰强度减弱,发生转化反应。
上述典型的无氧钒基材料,包括VS2、VS4等,具有高的导电率以及与金属离子间低的静电相互作用等优点,在下一代金属离子电池高性能电极中有巨大的潜力。但是,这些化合物的合成面临挑战,因此它们在能量存储方面的研究仍处于起步阶段,需要设计高效的合成策略并进一步研究这些材料的电荷存储机理和电化学特性。
4 总结与展望
AZIBs具有安全性高、制备工艺简单、生产成本低、环境友好等优点被广泛研究,有望成为下一代绿色环保的可充电电池。作为一类重要的AZIBs正极材料,钒基化合物具有高的天然储量、低的开发成本、理论储锌容量高、丰富的价态变化等优点,因此表现出广阔的发展空间和良好的应用前景。我们总结了几种常见的钒基AZIBs正极材料如V2O5、VO2、磷酸钒盐等近期的研究进展,重点介绍了他们的结构特征和储能机制,并且提出了以下几个优化策略,以获得高性能的钒基AZIBs正极材料:(1)采用碳材料进行表面包覆,可以有效地改善钒基材料的导电能力;(2)在层状结构中预先插入适量的金属离子或者水分子,能够提高钒基正极的结构稳定性,加快离子的扩散速率;(3)形貌调控,通过合成出不同类型纳米结构的钒基材料,也可以提高离子的扩散速率;(4)电解液优化,高浓度电解液可以显著提高AZIBs的电压平台,同时抑制正极材料的溶解等副反应。
近年来,钒基化合物已经被广泛地研究用于AZIBs的正极材料并且表现出优异的电化学性能,但是目前这些研究仍处于起步阶段,他们的实际应用面临着一些挑战:储锌机制比较复杂,工作电压通常较低,导致电池的实际能量密度受限;而且钒基化合物通常易溶解于水系电解液中,导致电池的倍率性能和循环稳定性变差。在此基础上,我们总结了钒基材料未来的几个发展方向:(1)依据更多样的原位分析测试技术和理论计算,深入分析钒基正极材料的储能机制和相变过程;(2)探讨多价离子嵌入/脱出反应对钒基材料晶体结构的影响,分析其结构坍塌的详细机理;(3)为钒基材料设计更完善的合成方法,以便于大规模生产;(4)开发具有稳定结构和高容量的新型钒基材料,引入新的氧化还原反应机理;(5)进一步拓宽水系电解液的电压窗口,提高AZIBs的能量密度,促进AZIBs的实际应用;(6)设计开发钒基柔性材料用于AZIBs以满足未来柔性器件发展的需求。

