基于臭氧氧化对煤化工废水中苯系污染物去除的研究
彭思伟,何绪文,刘海洋,白玉勇,谷小兵,李叶红
1.大唐环境产业集团股份有限公司,北京 100097;2.中国矿业大学(北京)化学与环境工程学院,北京 100083
臭氧通常作为水处理的氧化剂和消毒剂。臭氧作为氧化剂,可攻击富电子官能团,如双键、胺类、芳香环等物质[1]。由于臭氧在实际废水处理中会生成自由基,因此臭氧氧化通常被认为是高级氧化过程[2]。在臭氧反应的初始阶段,反应速率较为缓慢,伴随反应进行,自由基作为臭氧和有机物反应时的副产物参与反应,从而达到对废水中有机物降解的效果[3-5]。
苯系物(苯、甲苯、乙苯、二甲苯,简称BTEX)是典型的致畸、致癌、致突变的有毒有害有机物,它主要存在于人类工业生产过程,如工业溶剂、塑料合成、农药医药等[6]。煤化工行业是BTEX的主要来源,除伴随生产废水排放外,在化工产品制造过程、勘探开采、运输加工的各个环节都不可避免会有渗漏,导致BTEX以多种方式进入自然水体,造成环境污染[7-8]。
在前人的研究中,郑瑾等发现与微生物技术相结合的联合修复技术,如物理-生物技术、化学-生物技术对BTEX的去除颇具优势[9];李翔君利用高级氧化技术对BTEX模拟废水处理时发现BTEX的降解产物为低分子简单有机物,如醇、醛、酸类等[6];张方等制备了含铜复合催化剂,并以甲苯为探针测试其催化性能,结果表明在最优条件下甲苯的转化率达25.6%,其他苯系物的氧化反应也取得了较好的氧化效果[10]。本研究采用臭氧氧化法对水中BTEX进行降解,探讨臭氧去除水体中BTEX时的最佳反应条件,并在此基础上探究臭氧氧化降解BTEX的反应机理,为废水的实际处理提供可靠的理论基础。
1 材料与方法
1.1 模拟废水配制
本实验配制了含有苯、甲苯、乙苯、二甲苯分别为100 mg/L的目标有机污染物混合溶液。样品溶液的初始总有机碳(TOC)为460 mg/L。
1.2 仪器及数据测定方法
使用重铬酸钾法测定化学需氧量(COD)浓度;使用日本岛津公司的TOC-L CPH CN200型总有机碳分析仪进行测定总有机碳(TOC);使用PHS-3C精密pH仪器(LeiCi,上海)测量pH值;使用水温计测定反应体系温度;使用气相色谱质谱联用仪(GC-MS)测定苯、甲苯、乙苯、二甲苯的浓度,在测试前需使用二氯甲烷进行萃取[11]。
臭氧发生器为北京同林高科科技有限公司生产的3S-A10气源两用型臭氧发生装置,最大臭氧产量为10 g/h;蠕动泵为保定申辰泵业生产的LABV1型智能型蠕动泵。
1.3 反应装置及反应条件
本研究的反应装置如图1所示。实验发现,目标有机物在反应体系中经过处理,当反应时间达到120 min时,目标有机物的含量没有发生明显变化,因此本研究选取反应时间为120 min。
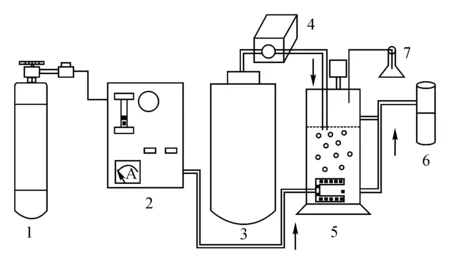
1—氧气罐;2—臭氧发生器;3—废水存储装置;4—蠕动泵;5—臭氧氧化反应装置;6—取样点;7—KI尾气回收装置图1 臭氧氧化反应系统Fig.1 Ozonation reaction system
2 结果与讨论
本研究主要探究不同因素对臭氧氧化降解BTEX的处理效果影响。比较了pH值、温度、臭氧投加量、臭氧投加模式等因素对降解效率的影响。通过比对不同反应条件下BTEX的处理效能,筛选出臭氧氧化去除BTEX的最佳参数[12]。
2.1 pH值对臭氧氧化降解BTEX的影响
图2为不同pH值对臭氧氧化降解BTEX效率的影响。从图2可以看出,苯、甲苯、乙苯、二甲苯的降解效率随pH值变化的趋势基本相同。当水体环境为酸性时(pH值为3~6),臭氧氧化对目标有机物的降解效率较低。有报道显示,当水环境的pH值较低时,臭氧降解有机物的过程主要由臭氧分子为主导,而臭氧分子对有机物的去除具有选择性,因此有机物在降解中受到了限制[13]。
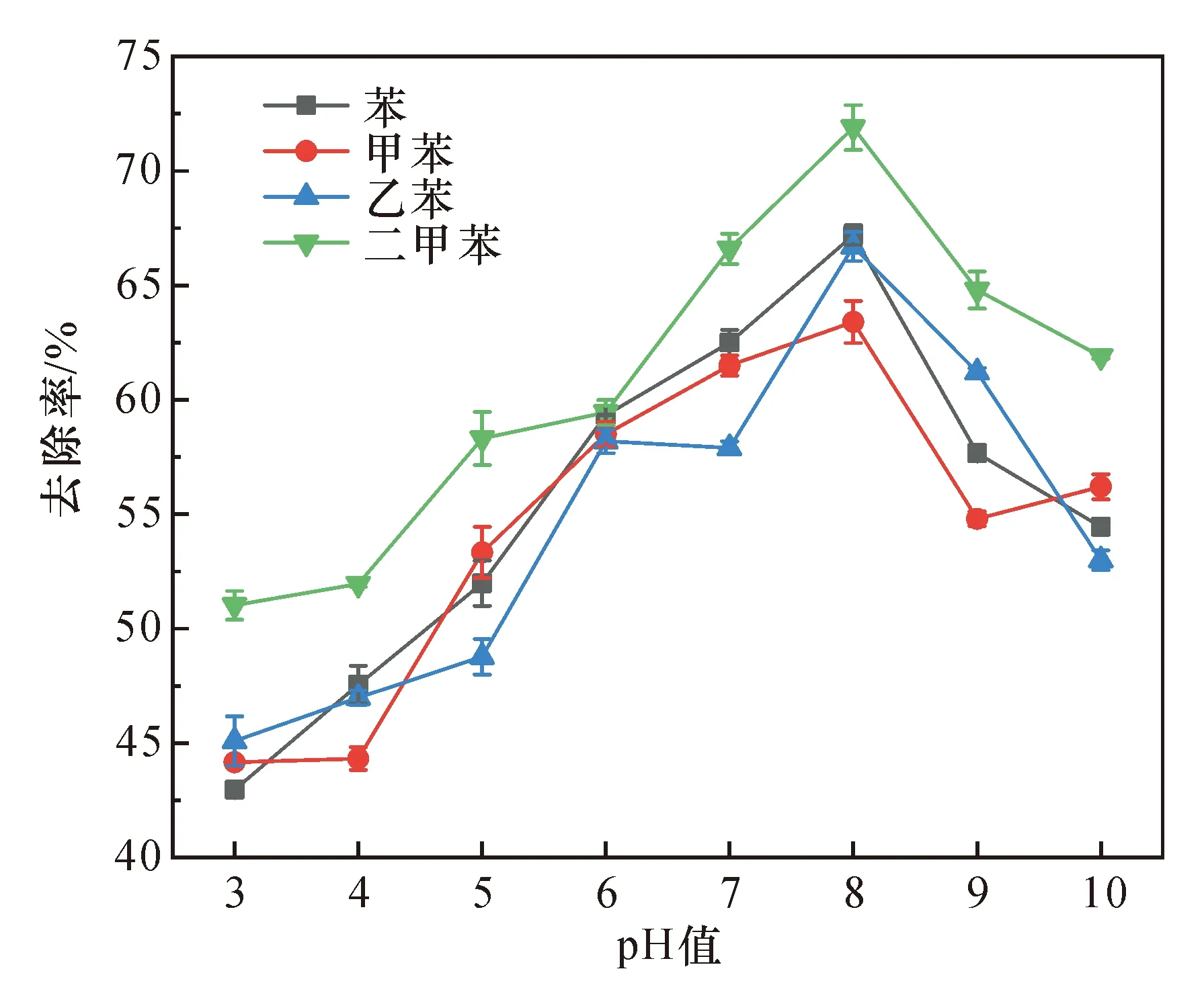
图2 pH值对臭氧氧化去除BTEX的影响Fig.2 Effect of pH value on removal of BTEX by ozonation
当溶液pH值为6~8时,目标有机物的降解效率明显提高。当pH值为8时,4种目标有机物的降解效率均达到最高点,苯、甲苯、乙苯、二甲苯的去除效率分别为67.2%、63.4%、66.7%和71.9%。其中,二甲苯的去除效率最高,而甲苯的去除效率最低,这说明二甲苯较其他有机物更容易被臭氧氧化,而甲苯在有机物共存体系中稳定性相对较强。出现这一现象的原因是,当溶液为碱性时水体中OH-含量增加,有助于加速臭氧分子分解,生成了氧化电位更高的自由基。除此之外,碱性条件有利于有机物的解离,有机物为解离状态时的降解效率较分子状态时更高[14]。
当溶液pH值升至8~10时,目标有机物的去除率下降。这是因为高碱度的水体中容易存在自由基捕获剂,这些捕获剂消耗了自由基致使其浓度下降,从而降低了自由基对有机物的降解效率。不仅如此,有报道称当碱度达到一定程度时,由于臭氧分子加速分解导致自由基浓度过高,高浓度的自由基发生相互碰撞会产生自由基的淬灭效应,阻碍自由基的链式反应,这可能是当溶液pH值为8~10时,目标有机物去除率下降的原因之一。
综上所述,本研究选取pH值为8作为臭氧氧化目标有机物的最佳pH值[15-16]。
2.2 温度对臭氧氧化降解BTEX的影响
本实验的主要目标是寻找臭氧降解BTEX的最佳反应温度。实验设定5个温度变量,分别为10 ℃、20 ℃、30 ℃、40 ℃、50 ℃。实验中目标有机物的去除效率以TOC的浓度变化来评定。温度对臭氧氧化去除BTEX的影响如图3所示。
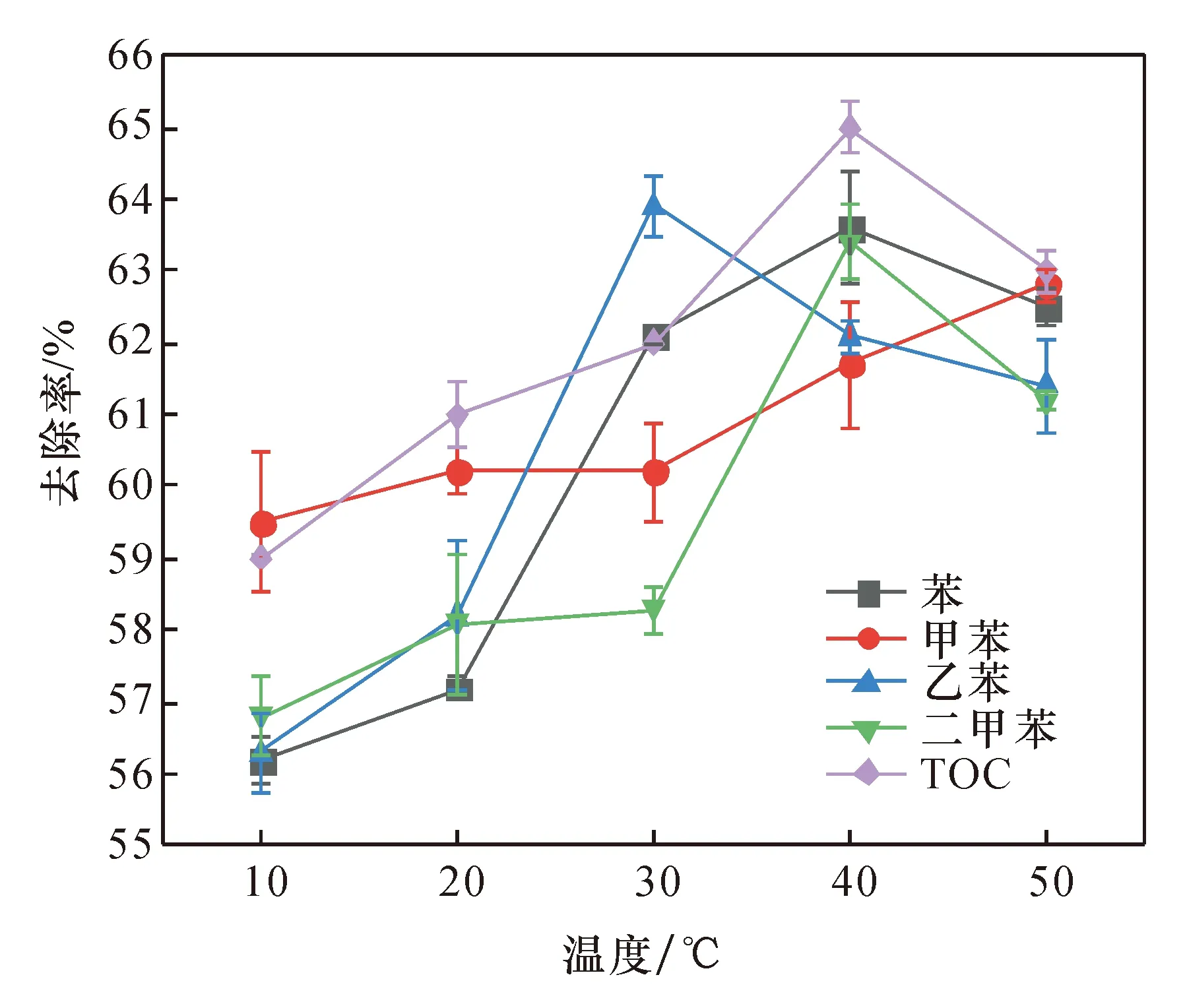
图3 温度对臭氧氧化去除BTEX的影响Fig.3 Effect of Temperature on removal of BTEX by ozonation
从图3可以看出,当温度从10 ℃升至40 ℃的过程中,有机物的去除率逐渐增加。其中,10 ℃时去除率为59.2%,20 ℃时去除率为61.1%,30 ℃时去除率为62.5%,40 ℃时去除效果达到最佳,为65.3%;当温度升至50 ℃时,相比较40 ℃时的去除率有所下降,为63.3%。
有研究发现,反应体系中温度越高其反应的活化能就越低,从而增加反应速率常数,促进臭氧反应有效进行,因此在反应体系温度从10 ℃至40 ℃的过程中,目标有机物的降解效率逐渐升高。但随着反应温度的逐渐增加,臭氧在反应体系中的溶解度会降低且臭氧的自分解效果增强,从而造成传质推动力降低的现象。根据亨利定律可知,温度升高时挥发性溶质的挥发能力变强,亨利系数就会增大。换而言之,同样分压下反应环境的温度越高,气体的溶解度就越小。因此,可以推断反应体系温度过高时,臭氧从气相进入液相的传质推动力减小,从而引起BTEX降解效率和臭氧自身利用率的降低。此外,还有报道称当温度过高时,有机污染物的相互富集和吸附被抑制,这一现象会降低反应速率,从而降低目标有机物的去除效果。除上述分析外,目标有机物的挥发性会随温度升高而增加。因此,在臭氧对有机物氧化的过程中不可盲目地增加反应温度。结合实际处理过程中温度的影响,本研究采用30 ℃作为最佳反应温度。
2.3 臭氧投加量对臭氧氧化降解BTEX的影响
臭氧的通气量直接影响目标有机污染物的降解效果和实际处理过程中的工艺成本。根据前人的研究成果可知,臭氧浓度越高则有机物去除率越大。但在实际处理过程中,考虑运行成本等因素,不能一味增加臭氧投加量来提高反应效率。因此,本研究主要探索臭氧投加量对BTEX去除的影响(图4)。
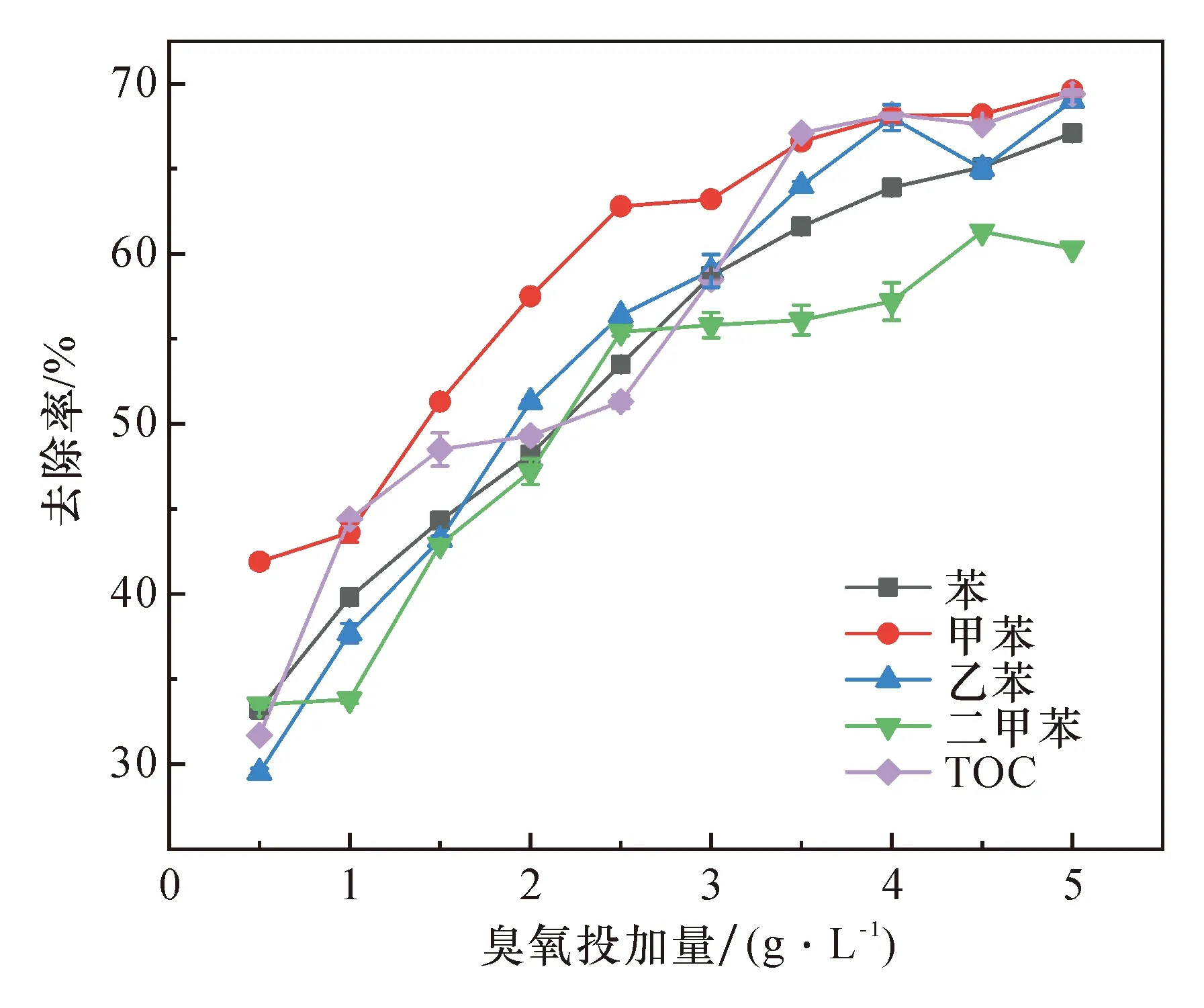
图4 臭氧投加量对臭氧氧化去除BTEX的影响Fig.4 Effect of O3 dosage on removal of BTEX by ozonation
从图4可以看出,当臭氧投加量为0.5~3.5 g/L时,溶液中有机污染物去除率逐渐升高,在0.5 g/L、1.0 g/L、1.5 g/L、2.0 g/L、2.5 g/L、3.0 g/L和 3.5 g/L的臭氧投加量时,目标有机物的去除率分别为31.7%、44.4%、48.5%、49.3%、51.3%、58.5%和67.1%;当臭氧投加量为4~5 g/L时,有机污染物的去除率虽然增加,但增加趋势降低。当臭氧投加量为4.0 g/L、4.5.0 g/L和5.0 g/L时,有机污染物的去除率分别为68.2%、67.9%和69.2%。这是因为当臭氧投加量较低时,反应体系中自由基浓度逐渐升高,自由基氧化有机污染物致使有机物矿化程度提升,从而被有效降解;但当臭氧浓度较高时,臭氧产生的自由基浓度较高,自由基在与目标有机物反应的同时自身也会相互作用,形成自由基的淬灭效应。此外,较高浓度的臭氧还会导致臭氧的传质作用下降,降低臭氧的使用效率。
综合上述分析,本研究认为使用臭氧氧化去除BTEX时臭氧的最佳投加量应为3.5 g/L。
2.4 臭氧投加模式对臭氧氧化降解BTEX的影响
根据上述结果,本实验在pH值为8、温度30 ℃、臭氧投加量3.5 g/L的条件下,对反应体系进行臭氧投加模式的影响实验。实验中臭氧的投加模式分逆流投加和顺流投加。对比目标有机物的去除效果,分析逆流投加和顺流投加对BTEX去除的影响(图5)。
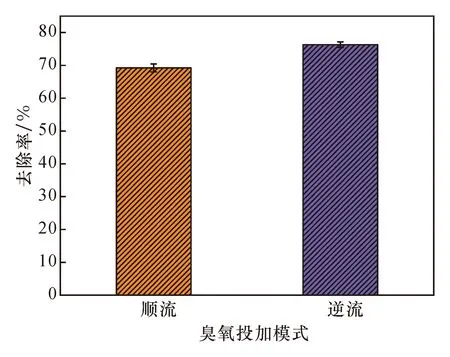
图5 臭氧投加模式对臭氧氧化去除BTEX的影响Fig.5 Effect of different ozone dosing methods on removal of BTEX by ozonation
从图5可以看出,当臭氧的投加模式为顺流时,BTEX的去除效率为69.2%;当臭氧的投加模式为逆流时,其降解效率为76.3%,增加了7.1%。逆流投加模式的去除效果明显优于顺流投加模式。这很可能是因为逆流投加时,反应体系中臭氧及臭氧分解所释放的自由基与废水中的有机物增加了接触机会,增强氧化剂的使用效能。自由基的有效利用可以高效去除目标有机物,从而达到更理想的处理效果。
3 臭氧氧化降解BTEX的机理分析
为了确定臭氧氧化的反应机理,判断臭氧氧化降解BTEX时起作用的是臭氧分子还是自由基的强氧化性,本研究中使用叔丁醇(TBA)作为羟基自由基抑制剂,使用自由基歧化酶(SOD)作为超氧自由基抑制剂。实验分为无抑制剂添加、含有 50 mmol/L的TBA和含有50 mmol/L的SOD三个反应体系,即O3、 O3-TBA、O3-SOD进行对比,考察目标有机物的降解情况。图6为不同反应体系下目标有机物的去除效果。

图6 不同反应体系中BTEX的去除效果Fig.6 Removal effect of BTEX in different reaction systems
臭氧分子直接氧化机理和自由基激发原理如下:


(1)


(2)
(3)
(4)
(5)
(6)
(7)
(8)
(9)

(10)
(11)
(12)

(13)
从图6可以看出,臭氧单独氧化时,苯、甲苯、乙苯、二甲苯降解效率分别为71.3%、76.7%、78.2%和77.6%。
当反应体系中加入TBA后,苯、甲苯、乙苯、二甲苯的降解效率分别降低至44.6%、49.3%、52.1%和54.6%,比臭氧单独氧化时分别降低了26.7%、27.4%、26.1%、23.0%,说明TBA的投加明显降低了臭氧氧化降解BTEX的效率。这是因为TBA作为羟基自由基抑制剂参与反应体系中,抑制了自由基与有机物反应,降低了羟基自由基的氧化效果。
当反应体系中加入超氧自由基抑制剂SOD时,目标有机物的降解效率骤减,其中二甲苯的降解效率几乎为零,这是因为SOD的加入高效抑制了超氧自由基的产生,超氧自由基的抑制直接影响了羟基自由基的生成,从而导致水体中强氧化性物质的消失。
通过本研究我们认为,强氧化物质超氧自由基和羟基自由基的存在是臭氧氧化有效去除BTEX的根本因素,因此在反应体系中合理有效地增加自由基的浓度是高效去除目标有机物的必要手段[17-20]。逆流投加模式更有利于提高有机物去除效果的实验结果,与此研究结果一致。
4 结 论
本研究使用臭氧氧化降解水中BTEX,为实际生产过程中BTEX的去除提供了理论基础。研究主要得出以下结论:
(1) 在使用臭氧氧化技术降解水中BTEX时,当pH值为8、反应温度为30 ℃、臭氧投加量为3.5 g/L、臭氧逆流投加时,BTEX的降解效果最佳,BTEX的去除率可达76.3%。
(2) 强氧化性物质超氧自由基和羟基自由基的存在是臭氧去除水中BTEX的根本因素,在反应体系中合理有效地增加自由基的浓度是高效去除BTEX的必要手段。

