血浆P-选择素在初次全髋置换术后深静脉血栓形成的预测价值
杨松运,李刚池,徐少华,莫松全,王飞凤,何兴川
(1.三台县人民医院,四川 三台 621100;2.遵义医科大学附属医院,贵州 遵义 563000)
深静脉血栓(DVT)形成是骨科大手术,特别是髋关节置换术后常见并发症,形成率为42%~57%[1],DVT脱落可导致肺栓塞,其中以致死性肺栓塞为其最严重后果[2],致死性肺栓塞形成率为2%~7%,抢救成功率低。但目前对于DVT形成的预测指标价值不高,临床上需要寻找一种快速且准确性高的预测指标。本研究通过选取来我院行初次单侧全髋关节置换术的患者122例,通过术前术后检测血浆中P-选择素的含量来探讨其预测DVT形成的价值。
1 资料与方法
1.1研究对象
1.1.1纳入标准:①患者术前诊断:单侧股骨头缺血坏死(FicatⅢ~Ⅳ期),按照Ficat分期(Ⅲ期80例、Ⅳ期42例);②对照组为自愿者、体检结果健康;③本研究获得研究对象的知情同意;④本次研究经过我院医学伦理委员会同意。
1.1.2排除标准:糖尿病足微血管疾病、血友病等血液疾病,静脉血栓病史,慢性肾脏疾病史,心房纤颤、心室纤颤、不稳定型心绞痛等心脏疾病,心脏瓣膜缺失或瓣膜手术后病史,妇科恶性肿瘤手术病史,术前3个月内有骨折及卧床病史。
选择2016年1月~2018年3月在我院行初次单侧全髋关节置换术的住院患者122例,男67例,女55例,平均年龄(62.0±16.8)岁,手术均为同一术者,手术入路均采用髋关节后外侧切口,手术患者均无相关血栓病史。患者术前12 h及术后10 d均使用低分子肝素钠进行抗凝治疗,所有患者均于术前及术后3 d、6 d、10 d行患肢彩色多普勒超声检查,但如果健侧肢体或双上肢出现肿胀则同时行该部位的彩色多普勒超声检查;另外根据患者随访情况(出院后随访3个月),如随访中发现患肢肿胀未消退或加重行彩色多普勒超声检查。根据术后彩色多普勒超声检查结果将患者分为深静脉血栓(DVT)组(浅静脉或肌间静脉血栓未纳入此组)和非DVT组(浅静脉或肌间静脉血栓未纳入此组),与正常对照组比较;正常对照组为来我院做健康检查者70例,既往均无相关血栓病史,其中男45例,女25例,平均年龄(55±13.8)岁。
1.2标本收集、处理及保存方法
1.2.1收集标本:使用不含热原和内毒素的试管,试管内使用柠檬酸盐抗凝,操作过程中避免任何细胞刺激;分别于术前及术后2 d收集患者清晨空腹静脉血液后,3 000 r/min离心10 min取上清液备用。
1.2.2保存:标本收集后冻存于-20℃医用冰箱待测。
1.3操作步骤:使用仅用于科研的人(Human)P-选择素(P-Selectin/CD62P/GMP140)ELISA 检测试剂盒。①从室温平衡20 min后的铝箔袋中取出所需板条,剩余板条用自封袋密封放回4℃;②设置标准品孔和样本孔,标准品孔各加不同浓度的标准品50 μl;③样本孔先加待测样本 10 μl,再加样本稀释液40 μl;空白孔不加;④除空白孔外,标准品孔和样本孔中每孔加入辣根过氧化物酶(HRP)标记的检测抗体 100 μl,用封板膜封住反应孔,37℃水浴锅或恒温箱温育 60 min;⑤弃去液体,吸水纸上拍干,每孔加满洗涤液,静置1 min,甩去;⑥每孔加入底物 A、B 各50 μl,37℃避光孵育15 min;⑦每孔加入终止液50μl,15 min内,用酶标仪在450 nm 波长处测定各孔的OD值。
1.4绘制标准曲线:在Excel工作表中,以标准品浓度作横坐标,对应OD值作纵坐标,绘制出标准品线性回归曲线,按曲线方程计算各样本浓度值。试剂盒由上海羽朵生物有限公司提供。酶标仪为上海科美KHBST-360酶标仪。

2 结 果
2.1随访情况:出院后3个月内到门诊随访共103例,门诊随访率84.43%。其中因DVT脱落致肺栓塞死亡1例(通过尸检明确),本组病例中DVT脱落至肺栓塞死亡率为8.3%。随访中发现肢体肿胀行彩色多普勒超声检查共31例。术后患者下肢静脉血栓形成有30例,其中浅静脉及肌间静脉血栓形成者共18例,未纳入数据分析;DVT形成者12例。
2.2髋关节置换手术前、后血浆P-选择素含量比较:DVT组、非DVT组术前P-选择素与正常对照组血浆P-选择素含量差异无统计学意义(P>0.05);DVT组、非DVT组术前D-二聚体与正常对照组血浆D-二聚体含量差异无统计学意义(P>0.05)。DVT组、非DVT组术后P-选择素含量差异有统计学差异(P<0.05)。见表1。
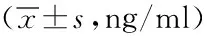
表1 髋关节置换手术前、后血浆P-选择素含量比较
2.3髋关节置换手术前、后血浆D-二聚体含量比较:DVT组、非DVT组术后血浆D-二聚体含量差异无统计学意义(P>0.05)。见表2。

表2 髋关节置换手术前、后血浆D-二聚体含量比较
2.4术后深静脉血栓患者P-选择素及D-二聚体相关统计学列表及图示:术后DVT患者不同P-选择素临界值时的敏感度、特异性、阳性似然比。见表3。

表3 DVT患者不同P-选择素临界值时的敏感度和特异性
术后DVT患者不同D-二聚体临界值时的敏感度、特异性、阳性似然比。见表4。术后DVT患者P-选择素ROC曲线图,见图1。术后DVT患者D-二聚体ROC曲线图,见图2。两种方法的ROC曲线图比较,P-选择素ROC曲线下面积(0.726)>D-二聚体ROC曲线下面积(0.512),见图3。当 P-选择素诊断临界值为8 ng/ml 时,AUC(曲线下面积)最大为0.687。见图1。
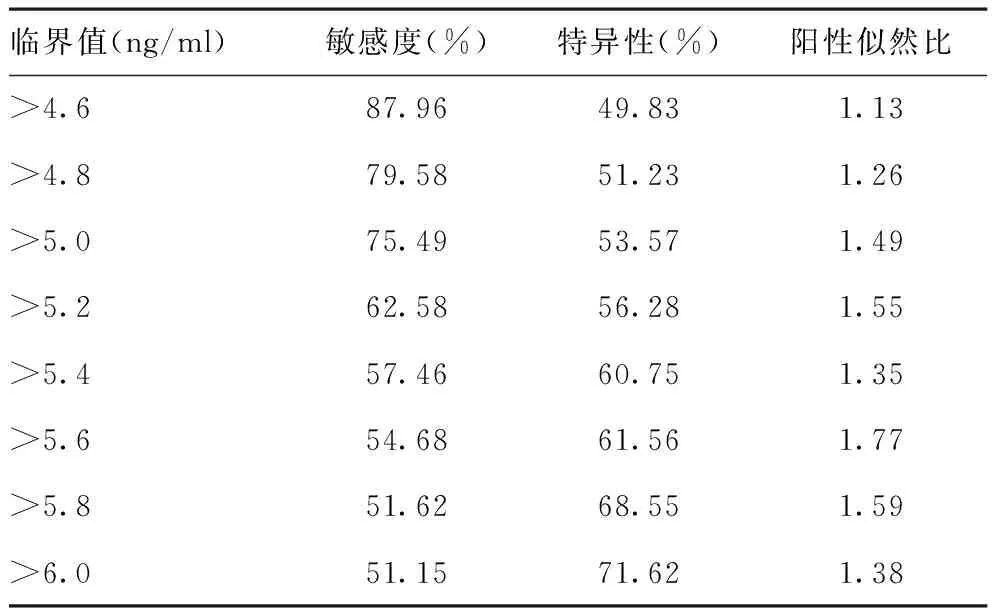
表4 DVT患者不同D-二聚体临界值时的敏感度和特异性
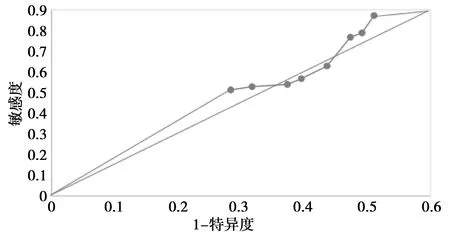
图1 术后DVT患者P-选择素ROC曲线
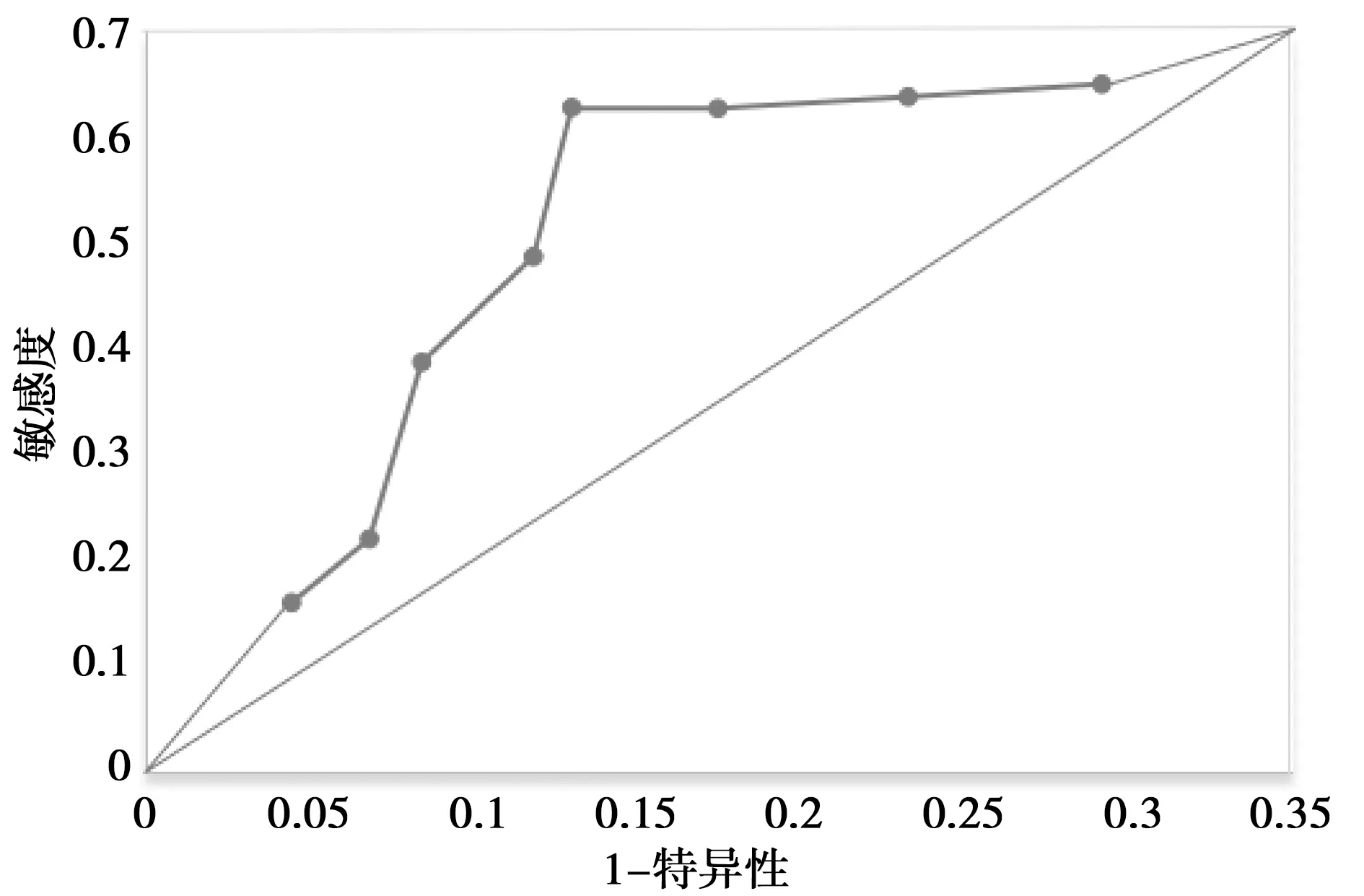
图2 术后深静脉血栓患者D-二聚体ROC曲线

图3 两种方法的ROC曲线比较
3 讨论
DVT是指血液非正常地在深静脉内凝结,属于下肢静脉回流障碍性疾病。血栓形成大都发生于制动状态(尤其是骨科大手术)。致病因素有血流缓慢、静脉壁损伤和高凝状态三大因素。血栓形成后,除少数能自行消融或局限于发生部位外,大部分会扩散至整个肢体的深静脉主干。下肢DVT形成约占周围血管性疾病的60%,如果在急性期阶段不能及时诊断并给予有效的治疗,可引起静脉血栓后遗症以及致命性肺栓塞[3]。
DVT在髋关节置换术后发生率较大,根据美国骨科医师学会发布的择期髋膝关节置换患者静脉血栓栓塞性疾病预防临床实践[4],美国每年开展大约250 000例髋关节置换,如果不采取抗凝预防措施,大约37%的患者置换后会出现影像学或者超声手段可以检测出的DVT。
目前预测DVT形成的方法主要是检测血浆D-二聚体含量。各国学者也进行了大量研究,Watanabe等研究发现,行多排计算机断层CT扫描的无症状DVT患者中,DVT组的D-二聚体水平在置换后第4天比无DVT组显著增高,敏感性和特异性分别为75%和63%,作者得出结论血浆D-二聚体正常可排外DVT诊断,但不能作为预测DVT形成的特异性指标[5]。2014年欧洲心脏病学会发布的急性肺栓塞诊断和管理指南指出,D-二聚体的特异性随着年龄的增长下降[6]。本研究发现:术后患者血浆中D-二聚体含量普遍增高,超过500 μg/L,术后DVT组与非DVT组D-二聚体含量差异无统计学意义(P>0.05)。表明D-二聚体不能作为髋关节置换术后预测DVT形成的特异性指标。
目前诊断血栓形成的方法主要是下肢血管彩色多普勒超声及血管造影技术,血管彩色多普勒超声对下肢DVT形成的诊断较高,静脉造影虽然是诊断血栓的金标准,但它是一种有创性检查,且上述两种方法只针对已形成血栓的检查,并不能早期预测DVT的形成。
P-选择素是近年来发现的血栓起始形成的重要启动参与者,是血栓早期的一个分子标志物。正常情况下血小板处于静息状态,当受到病理性的刺激时,血小板活化,在血栓形成过程中,血小板的活化具有重要意义,是血栓前状态的重要指标[7],在血小板活化过程中随着活化血小板的脱颗粒,静息血小板胞质内α颗粒膜上的糖蛋白P-选择素(CD62P)和溶酶体膜上的CD63与血小板膜融合进行标记[8],P-选择素主要存在于静息状态下血小板的α颗粒膜上,是反映血小板活化的重要标志物,当血小板出现活化反应时,通过开放的管道系统,血小板内的α颗粒与质膜融合,从而使血小板质膜上的P-选择素分子表达量增加[9]。Trzeciak等也发现P-选择素是衡量血小板释放功能的重要指标[10]。国内研究发现P-选择素在静止血小板的α颗粒及活化的血小板质膜上的膜糖蛋白颗粒均有表达,是评估血小板活化的“金标准”[11]。国内有学者研究发现,在一定程度上P-选择素作为下肢DVT形成的早期诊断和早期预测指标具有重要意义[12]。赵红丽等研究也发现监测外周血P-选择素水平有益于识别存在高凝状态及血栓形成倾向的患者,及时干预,预防栓塞发生[13]。
本研究122例患者中有30例发生下肢静脉血栓,发生几率为24.59%,其中12例形成下肢DVT,发生几率为9.8%,其中7例DVT形成是发生在术后2周~3个月左右,这7例中有1例患者(肥胖且平时活动量少)术后15 d因DVT致肺栓塞死于家中,该患者因怕疼痛拒绝下地功能锻炼,其余6例调查发现患者患肢稍肿胀,运动功能良好,彩色多普勒超声检查血栓形成但血流信号通畅,追问患者并未按时服用抗凝药物预防血栓形成,这与美国骨科医师学会发布的报告相符合[4]:如果不采取抗凝预防措施,大约37%的患者置换后会出现影像学或者彩色多普勒超声手段可以检测出的DVT。本研究发现,术后DVT组、非DVT组P-选择素含量差异有统计学意义(P<0.05),且P-选择素ROC曲线下面积>D-二聚体ROC曲线下面积,表明P-选择素对初次全髋关节置换术后DVT的形成其预测价值更加合理,应该优先选择,可以作为初次全髋关节置换围手术期预测下肢DVT形成的特异性指标。
需要说明的是本研究选择的患者是股骨头缺血坏死行髋关节置换手术,对于股骨颈骨折未纳入此次研究,另外研究检测使用的是上海科美KHBST-360酶标仪,试剂盒是由上海羽朵生物有限公司提供。不同试剂盒的测量原理及试剂成分可能不同,因而测量得到的相关数据不一定适合于其他品牌的仪器和试剂。

