全腹腔镜与腹腔镜远端胃癌根治术治疗胃癌的临床比较
白亚珍 张倩 王淑娟
(郑州大学第一附属医院 河南郑州 450052)
胃癌是临床常见的恶性肿瘤,严重危害患者生命安全。目前,临床多采用手术、放化疗等方式治疗胃癌,其中外科手术仍是主要治疗手段,随着微创理念的深入,腹腔镜胃癌根治术较开腹手术更具有微创性,可减轻患者手术损伤,利于患者术后康复[1]。腹腔镜根治术包含全腹腔镜远端胃癌根治术(Totally Laparoscopic Distal Gastrectomy, TLDG)、腹腔镜辅助远端胃癌根治术(Laparoscopy-assisted Distal Gastrectomy, LADG)。TLDG、LADG 的癌组织切除与淋巴结清扫均可在腹腔镜下进行[2~3],但两种术式治疗的安全性及术后恢复情况仍未有统一定论。鉴于此,本研究将探讨全腹腔镜与腹腔镜远端胃癌根治术治疗胃癌的临床疗效。现报道如下:
1 资料与方法
1.1 一般资料 收集 2018 年 9 月 ~2020 年 10 月于我院行TLDG 的47 例胃癌患者临床资料,纳入A 组;收集同期我院行LADG 的47 例患者临床资料,纳入 B 组。A 组男 28 例,女 19 例;年龄 46~73岁,平均(57.43±4.50)岁;临床分期:Ⅰ期 25 例,Ⅱ期 22 例;体质量指数(Body Mass Index, BMI)19.3~26.4 kg/m2,平均(23.02±2.16)kg/m2。B 组男32 例,女 15 例;年龄 43~75 岁,平均(57.69±4.28)岁;临床分期:Ⅰ期 22 例,Ⅱ期 25 例;BMI 18.2~26.5 kg/m2,平均(22.91±2.20)kg/m2。两组一般资料对比无显著差异(P>0.05),有可对比性。纳入标准:符合《内科学》[4]中胃癌诊断标准,经内镜活检病理确诊;凝血功能正常;临床资料完整。排除标准:术前行放化疗治疗者;有手术禁忌证者;既往有上腹部重大创伤及手术史者;合并肝肾等重要器官功能障碍者;患有精神疾病者;合并其他恶性肿瘤者;合并全身性感染者。
1.2 手术方法 两组患者取平卧位,术前留置导尿管、胃管,采用全身麻醉,常规消毒铺巾。经脐下穿刺,建立气腹,CO2压力为13 mm Hg,置入戳卡,作为观察孔,选择左侧腋前线肋缘下2 cm 左右作为主操作孔,右侧腋前线肋缘下2 cm,左、右锁骨中线平脐上2 cm 作为辅助操作孔。在腹腔镜下,观察癌组织部位、分期等情况。根据患者不同肿瘤位置,确认胃切除与淋巴结清扫的范围,同时排除肿瘤远处转移的可能。两组术后均给予常规抗感染药物,以预防感染。
1.2.1 A 组 采用TLDG 治疗,BillrothⅠ式三角吻合:在病变下缘3 cm 左右,十二指肠预定吻合部位,使用直线切割闭合器(美国强生公司,型号:Echelon)离断十二指肠;选择病变上缘5 cm 左右,保留胃体胃部,以直线切割闭合器离断胃壁。在上腹正中作一3 cm 开口,取出标本后,包含肿瘤切缘充分,重建气腹行消化道重建。对胃近端与十二指肠近端行三角吻合。病灶靠近胃上部位时,行Roux-en-Y 吻合:在距离幽门下3 cm 处使用直线切割闭合器离断十二指肠,在病灶上缘5 cm 左右离断胃,将标本置于标本袋后,经上腹部切口取出,切缘充分后,重建气腹,行胃空肠Roux-en-Y 吻合,在十二指肠悬韧带20 cm 提起空肠,应用超声刀贴近肠管,并向远端游离。上提远端空肠结肠至左上腹,在胃断端大弯侧、空肠系膜对侧戳孔,置于直线切割闭合器行吻合,在近端空肠、远端空肠系膜对侧戳孔行空肠侧侧吻合,再对切割闭合器闭合的共同开口处,离断近端空肠。
1.2.2 B 组 采用LADG 治疗,操作如下:取上腹正中6 cm 左右切口,将胃、空肠牵拉至腹腔外部,行吻合;BillrothⅠ吻合:距幽门3 cm 处切断十二指肠,移出标本,将十二指肠残端放入吻合器钉座,后使用直线切割缝合器,距病变部位3.5 cm 左右切断胃体,并将残胃放置吻合器长头,经残胃大弯穿出,与十二指肠吻合,后关闭残胃裂口。Billroth Ⅱ吻合与布朗吻合:在距屈氏悬韧带20 cm 空肠处,对胃断端、系膜边缘做一切口(约0.5 cm),经腹腔镜切割闭合器行胃大弯、空肠近端侧侧吻合;后使用切割闭合器行近端空肠与远端空肠侧侧吻合。
1.3 评价指标 (1)记录两组手术时间、手术切口长度、术中出血量、术后首次排气时间。(2)记录两组术后胃瘫、感染、吻合口瘘等并发症发生情况。
1.4 统计学方法 采用SPSS23.0 统计学软件分析数据,以%表示计数资料,用χ2检验;计量资料均经Shapiro-Wilk 正态性检验,符合正态分布的计量资料采用()表示,用独立样本t检验组间数据,用配对样本t检验组内数据。以P<0.05 为差异有统计学意义。
2 结果
2.1 两组围术期指标对比 与B 组比较,A 组手术时间长,手术切口长度短,术中出血量少,术后首次排气时间短,差异有统计学意义(P<0.05)。见表1。
表1 两组围术期指标对比()
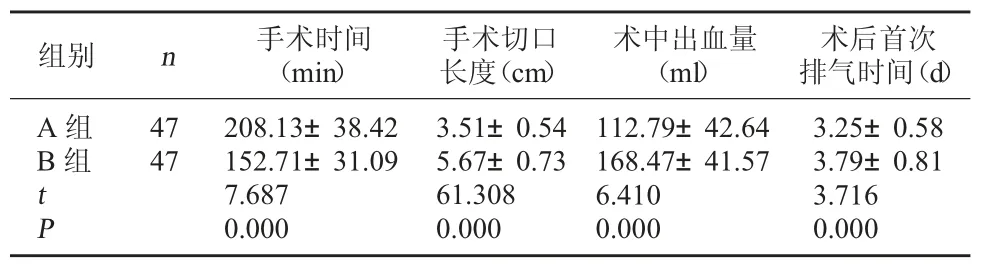
表1 两组围术期指标对比()
术后首次排气时间(d)A 组B 组组别 n 手术时间(min)手术切口长度(cm)术中出血量(ml)47 47 tP 208.13±38.42 152.71±31.09 7.687 0.000 3.51±0.54 5.67±0.73 61.308 0.000 112.79±42.64 168.47±41.57 6.410 0.000 3.25±0.58 3.79±0.81 3.716 0.000
2.2 两组术后并发症发生情况对比 两组术后并发症发生率对比,差异无统计学意义(P>0.05)。见表2。

表2 两组术后并发症发生情况对比[例(%)]
3 讨论
胃癌主要治疗方式是手术切除,因此,如何保证手术安全进行,促进患者术后快速康复尤为重要。腹腔镜技术因具有高清镜头及放大效果,在手术中可清晰识别血管、神经、淋巴结组织,减轻术中造成的医源性损伤,发挥微创、出血量少等优势,在胃癌的治疗中的应用较为广泛[5]。
LADG 是在腹腔镜下完成游离与淋巴结清扫,辅助小切口切除标本与完成消化道重建,达到减少创伤。但辅助切口仍未达成极致微创理念,术中需通过上腹部切口进行消化道重建,可能会增加切口组织过度牵拉风险,影响手术治疗效果。对于部分肥胖或腹壁较厚的患者可能影响手术视野与操作空间,增加手术难度。若是病灶较大或瘤体位于胃体中部的患者,术中需切除更多胃体,导致残胃与空肠难以通过上腹小切口进行吻合,需扩大切口,导致切口长度与术中出血量增加,影响患者术后早期康复[6~7]。因此,临床需寻找其他更加微创、安全的术式。
TLDG 是指胃切除、淋巴结清扫、消化道重建等手术步骤均在腹腔镜下完成,腹腔镜手术的腔外吻合技术改进为腔内操作的治疗方式。本研究中,与B组比较,A 组手术时间长,手术切口长度短,术中出血量少,术后首次排气时间短,可见TLDG 治疗胃癌虽然延长手术时间,但可缩短手术切口,减少术中出血量,利于患者术后康复。究其原因在于,TLDG术中省去了辅助小切口,在腹腔镜下腔内完成消化道重建,虽然在一定程度上增加了手术难度,需要手术医师具备更加熟练的手术技巧与操作经验,延长了手术时间,但术中利用直线切割吻合器,可完成残胃与十二指肠断端的吻合,不用扩大切口,具有创伤小的优点,可减少术中出血量,且切口较小,具有较好美容效果,患者接受度较高[8]。术中通过行三角吻合,可利于重建消化道,促进术后胃肠道功能的恢复,缩短患者术后首次排气时间,利于胃肠道内营养的吸收与消化,改善机体营养状况,促进术后康复进程。此外,TLDG 在腹腔镜下完成消化道重建,吻合时具有较好手术视野,可减少对吻合口的牵拉,且使用的切割闭合器行胃肠侧侧吻合,患者的血供良好,可降低吻合口瘘发生风险[9~10]。此外,本研究发现两种术式并发症发生率比较无显著差异,可见LADG、TLDG 治疗胃癌均具有较高安全性。
综上所述,LADG、TLDG 治疗胃癌的安全性均较高,TLDG 虽然手术时间较长,但可缩短手术切口长度,减少术中出血量,更利于术后早期恢复,值得临床推广。

