1例头孢他啶/阿维巴坦个体化给药案例报道
陈昆 王玥媛 刘梦颖 方洁
摘 要 目的:探讨肾功能不全的重症患者头孢他啶/阿维巴坦个体化给药治疗策略,为优化头孢他啶/阿维巴坦给药方案積累经验。方法:临床药师参与1例由碳青霉烯类耐药肺炎克雷伯菌所致重症感染的急性肾功能不全患者的治疗,运用治疗药物监测(TDM)协助临床医师优化抗感染治疗方案,对患者初始给药方案选择、后续方案调整、疗效观察和不良反应监测等方面提出建议或进行药学监护。结果:TDM结果表明头孢他啶/阿维巴坦达到了理想的PK/PD靶值。患者感染得到了迅速有效的控制,且未出现不良反应。结论:临床药师可运用药学知识特长,协助临床制定合理的治疗方案,评估药物疗效,监测不良反应,保证药物治疗安全、有效、经济。
关键词 头孢他啶/阿维巴坦 急性肾功能不全 治疗药物监测 个体化用药
中图分类号:R978.11; R692.5 文献标志码:C 文章编号:1006-1533(2021)01-0074-04
A case report of ceftazidime-avibactam individualized administration
CHEN Kun1,2*, WANG Yueyuan3, LIU Mengying4, FANG Jie2**
(1. Department of Pharmacy, the Hospital affiliated to Southwest Medical University, Sichuan Luzhou 646000, China; 2. Department of Pharmacy, Ruijin Hospital affiliated to School of Medicine, Shanghai Jiao Tong University, Shanghai 200025, China; 3. Department of Pharmacy, Sichuan Provincial Key Laboratory for Personalized Drug Therapy, Sichuan Academy of Medical Sciences, Sichuan Provincial Peoples Hospital, the Hospital affiliated to University of Electronic Science and Technology of China, Chengdu 610072, China; 4. Department of Pharmacy, Nanjing Drum Tower Hospital affiliated to Medical College of Nanjing University, Nanjing 210008, China)
ABSTRACT Objective:To explore the treatment strategy of individualized administration of ceftazidime-avibactam in critically ill patients with renal impairment so as to accumulate clinical experience for the optimization of the ceftazidimeavibactam dosage regimen. Methods: The clinical pharmacists participated in the treatment of infections caused by carbapenemresistant Klebsiella pneumoniae in a patient with acute renal insufficiency and assisted clinicians in optimizing anti-infective treatment plans using therapeutic drug monitoring (TDM) and perform pharmaceutical care in the selection of patients initial dosing plan, subsequent plan adjustments, efficacy observations and adverse reaction monitoring. Results: TDM showed that the PK/PD target rate of ceftazidime-avibactam was 100% and the patient experienced rapid clearance of his carbapenem-resistant Klebsiella pneumoniae without adverse reactions. Conclusion: The clinical pharmacists can use their expertise in pharmaceutical knowledge to assist clinicians in formulating reasonable treatment plans, assess drug efficacy, monitor adverse reactions and ensure the safety, economy, effectiveness and rationality of drug treatment.
KEy WORDS ceftazidime-avibactam; acute renal insufficiency; therapeutic drug monitoring; individualized medication
近年来由碳青霉烯类耐药肠杆菌科细菌(carbapenem-resistant Enterobacteriaceae,CRE)引起的感染發生率不断升高。我国肺炎克雷伯菌对碳青霉烯类耐药率已达到26.3%,ICU病房中甚至达到了48.1%,大大限制了抗感染方案的选择[1-2]。头孢他啶/阿维巴坦(4∶1)是由头孢他啶和新型的b-内酰胺酶抑制剂阿维巴坦组成的复合制剂,它对头孢他啶不敏感的肠杆菌科细菌和铜绿假单胞菌均具有出色的体外抗菌活性。但目前头孢他啶/阿维巴坦在我国临床应用并不多,尤其对于肾功能不全患者的给药方案制定、疗效评估、耐药情况和不良反应等尚缺乏经验。本文介绍临床药师参与的1例急性肾功能不全患者头孢他啶/阿维巴坦个体化给药方案的案例及其分析。
1 病史摘要
患者,男性,86岁,身高168 cm,体重67 kg,BMI 23.74 kg/m2。1月前因“咳嗽、咳痰伴活动后气促”于2020年1月20就诊于我院呼吸科,入院诊断:①肺部感染;②慢性阻塞性肺疾病急性加重,予以静脉滴注头孢他啶+莫西沙星抗感染。其间患者出现双下肢红肿热痛,分泌物培养结果示溶血葡萄球菌(+),予以调整抗感染方案为静脉滴注头孢他啶+口服利奈唑胺片。2月3日患者无咳嗽、咳痰等症状,双下肢肿胀较前好转,遂转至我院卢湾分院,继续予以美罗培南、万古霉素、氟康唑等抗感染治疗,2月17日出现无尿,予以留置导尿,效果不佳,遂于2月19日停用万古霉素。2月20日Cr 514 mmol/L、脑钠肽2 255 pg/ml,2月23日开始予以连续性肾脏替代治疗(CRRT),透析期间患者肌酐进行性下降。3月10日患者为进一步治疗收入我院RICU。
1)既往史 患者有青霉素过敏史,有前列腺增生病史、肺栓塞史,长期药物治疗;有膀胱肿瘤切除术(示低级别膀胱上皮乳头状癌)、白内障手术史。
2)体格检查 体温37.1 ℃,脉搏57次/min,呼吸14次/min,血压100/54 mmHg ,双下肢红肿,左侧腋下红色瘀斑,两肺呼吸音低,两肺少量湿啰音,未闻及干性啰音。
3)入院辅助检查 ①血常规:白细胞计数(WBC)14.43×109/L,中性粒细胞比例(N%) 77.9%,血红蛋白(Hb)69 g/L,血小板计数151×109/L;②C反应蛋白34 mg/L;③降钙素原(PCT)1.06 ng/ml;④肾功能:血肌酐(Cr)331 mmol/L,尿素 20.8 mmol/L;⑤肝功能:白蛋白33 g/L,丙氨酸氨基转移酶 4 IU/L,天门冬氨酸氨基转移酶 21 IU/L,碱性磷酸酶 75I U/L,g-谷氨酰基转移酶 16 IU/L;⑥血电解质:钠 133 mmol/L、钾4.56 mmol/L、氯 101 mmol/L、钙 2.11 mmol/L、磷 1.11 mmol/L;⑦动脉血气分析(鼻导管吸氧,流量3 L,浓度不详):pH 7.28、PaO2 23.83 kPa、PaCO2 7.02 kPa、氧饱和度 99.3%;⑧尿常规:白细胞 (+++)、蛋白质 (+)、潜血 (++);⑨心电图:窦性心律不齐 、室性早搏、一度房室传导阻滞;⑩胸部X-RAY:双下肺渗出,双侧胸腔少量积液。
入院诊断:①慢性支气管炎急性发作;②肺部感染;③急性肾功能不全;④丹毒;⑤前列腺增生;⑥膀胱恶性肿瘤个人史。
2 治疗经过
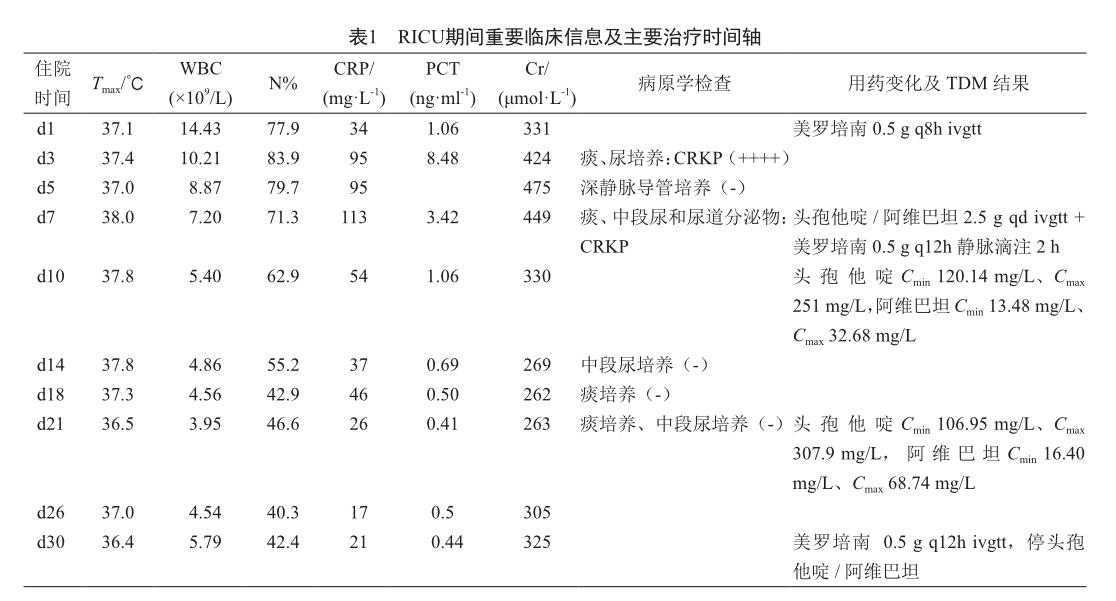
入院后暂停透析治疗,予以美罗培南0.5 g q8h 静脉滴注抗感染。入院第7天,患者痰、中段尿和尿道分泌物均培养出碳青霉烯类耐药肺炎克雷伯菌(carbapenemresistant Klebsiella pneumoniae,CRKP)(++++),药敏试验示:头孢他啶最低抑制浓度(MIC)64 mg/L、亚胺培南 MIC 16 mg/L、美罗培南抑菌圈直径 6 mm(纸片法),咽拭查KPC酶阳性,调整抗感染方案为头孢他啶/阿维巴坦2.5 g qd +美罗培南0.5 g q12h 静脉滴注2 h。入院第10天监测头孢他啶/阿维巴坦血药浓度。入院第21天,患者痰培养、中段尿培养均为阴性,复测头孢他啶/阿维巴坦血药浓度。入院第30天,患者各项感染指标明显好转,痰培养、中段尿培养连续两次阴性,停用头孢他啶/阿维巴坦,继续美罗培南0.5 g q12h 静脉滴注,转至呼吸科普通病房继续治疗。
住院期间重要信息及治疗经过详见表1。
3 分析讨论
3.1 治疗方案的确定及调整
阿维巴坦对A类、C类和部分D类b-内酰酶(ESBLs,KPC,AmpC和OXA-48)均具有抑制作用,尤其是对KPC酶的抑制活性显著优于传统酶抑制剂[3-4]。研究发现头孢他啶/阿维巴坦与美罗培南联合应用对于治疗产KPC酶的CRKP具有协同抗菌作用[5-7]。该患者入院后痰培养、中段尿培养均检出CRKP(++++),KPC阳性。因此结合患者肾功能和药敏试验结果,抗感染方案确定为头孢他啶/阿维巴坦2.5 g qd +美罗培南0.5 g q12h 静脉滴注2 h。
3.2 个体化给药
3.2.1 重症患者头孢他啶/阿维巴坦的药代动力学/药效动力学变化及初始剂量的确定
头孢他啶和阿维巴坦具有相似的药代动力学,两者之间不会相互影响,且均主要通过肾脏消除[8]。大量的研究表明[9-11],重症患者头孢他啶和阿维巴坦的表观分布容积(apparent volume of distribution, Vd)会明显的增大,使血药浓度过低导致治疗失败。Stein等[12]研究发现头孢他啶MIC<16 mg/L时,重症患者按照说明书推荐剂量给药时,可达到PK/PD最佳靶值。但当头孢他啶MIC>64 mg/L时PK/PD靶值达标率降到0。Veillette等[13]研究中收治的两例肾功能不全的CRKP感染患者,均接受了高于说明书推荐剂量的头孢他啶/阿维巴坦,抗感染疗效显著且未出现毒性反应。
肾功能不全时,头孢他啶和阿维巴坦的药物清除率(CL)降低,半衰期(t1/2)也随之延长,可能导致药物在患者体内大量蓄积引起中毒反应[14-15]。因此对于重症感染伴肾功能不全的患者,需要平衡重症感染和肾功能不全两者之间的影响,并定期进行TDM。
头孢他啶/阿维巴坦说明书[16]推荐成人常规用量为2.5 g q8h静脉输注2 h以上,中重度肾功能损伤应根据肌酐清除率(CCr)调整用量。该患者考虑急性肾损伤(acute kidney injury,AKI),用药前CCr为9.35 ml/min,按照说明书推荐剂量为0.94 g qd。该患者感染严重,痰、中段尿以及尿道口分泌物培养均为CRKP,且出现深静脉导管相关性感染风险高,若不能有效控制感染,可能进一步加重AKI危及患者生命。结合药物在感染部位组织分布情况的不同,临床药师建议头孢他啶/阿维巴坦初始剂量为2.5 g qd 静脉输注2 h以上,以期迅速有效控制感染。定期测定头孢他啶/阿维巴坦血药浓度,根据监测结果再评估是否调整给药剂量。
3.2.2 药物浓度监测
头孢他啶/阿维巴坦理想的PK/PD靶值为头孢他啶50% fT>MIC,即血浆中游离头孢他啶浓度大于MIC的时间占给药间期的比例大于50%;阿维巴坦50% fT>1 mg/L,即血浆中游离阿维巴坦浓度大于阈浓度(CT)1 mg/L的时间占给药间期的比例大于50%[12]。对于多重耐药菌感染或重症感染,时间依赖性抗菌药物% fT>MIC越高,达到100%,甚至% fT>4~5×MIC疗效越好[17]。
该患者分别于D10(用药后第4天)和D21(用药后第15天)进行头孢他啶和阿维巴坦的血药谷浓度(Cmin)和峰浓度(Cmax)测定(表1)。同时,药敏结果显示头孢他啶MIC=64 mg/L,对于KPC阳性菌株联合阿维巴坦后敏感性增强,MIC会显著降低。两次血药浓度监测结果头孢他啶和阿维巴坦的谷浓度均高于目标浓度,PK/ PD靶值达标率为100%。
3.3 不良反应监护
Sternbach等[18]荟萃分析结果示头孢他啶/阿维巴坦最常见的不良反应為胃肠道反应,主要表现为腹泻、恶心、呕吐、腹痛等,其他常见不良反应有神经系统不良反应(如头痛、眩晕)、艰难梭菌相关性腹泻、肝功能异常、外周水肿、超敏反应等。患者肾功能不全,使用高于说明书推荐剂量的头孢他啶/阿维巴坦,用药过程中应警惕药品不良反应的发生。TDM结果表明在达到理想的PK/ PD靶值同时,患者可很好地耐受这个剂量,没有出现不良反应。
4 小结
本文患者为高龄伴急性肾功能不全的CRKP感染患者。临床药师根据患者肾功能和感染情况,协助临床医师选用高于说明书推荐剂量的头孢他啶/阿维巴坦。TDM结果表明头孢他啶/阿维巴坦PK/ PD靶值达标率为100%,患者感染得到了有效的控制,且没有出现不良反应。临床药师可运用其药学知识的特长,为临床制定合理的治疗方案提供帮助,通过TDM评估药物疗效,监测不良反应,保证药物治疗安全、经济、有效、合理。
参考文献
[1] Hu F, Guo Y, Yang Y, et al. Resistance reported from China antimicrobial surveillance network (CHINET) in 2018[J]. Eur J Clin Microbiol Infect Dis, 2019, 38(12): 2275-2281.
[2] Li Y, Shen H, Zhu C, et al. Carbapenem-resistant Klebsiella pneumoniae infections among ICU admission patients in central China: prevalence and prediction model[J/OL]. Biomed Res Int, 2019, 2019: 9767313. doi: 10.1155/2019/9767313.
[3] Shirley M. Ceftazidime-avibactam: a review in the treatment of serious gram-negative bacterial infections[J]. Drugs, 2018, 78(2): 675-692.
[4] Kazmierczak KM, Biedenbach DJ, Hackel M, et al. Global dissemination of blaKPC into bacterial species beyond Klebsiella pneumoniae and in vitro susceptibility to ceftazidime-avibactam and aztreonam-avibactam[J]. Antimicrob Agents Chemother, 2016, 60(8): 4490-500.
[5] Gaudereto JJ, Perdig?o Neto LV, Leite GC, et al. Synergistic effect of ceftazidime-avibactam with meropenem against panresistant, carbapenemase-harboring Acinetobacter baumannii and Serratia marcescens investigated using time-kill and disk approximation assays[J/OL]. Antimicrob Agents Chemother, 2019, 63(5): e02367-18. doi: 10.1128/ AAC.02367-18.
[6] Gaibani P, Lewis RE, Volpe SL, et al. In vitro interaction of ceftazidime-avibactam in combination with different antimicrobials against KPC-producing Klebsiella pneumoniae clinical isolates[J]. Int J Infect Dis, 2017, 65: 1-3.
[7] Camargo JF, Simkins J, Beduschi T, et al. Successful treatment of carbapenemase-producing pandrug-resistant Klebsiella pneumoniae bacteremia[J]. Antimicrob Agents Chemother, 2015, 59(10): 5903-5908.
[8] Merdjan H, Rangaraju M, Tarral A. Safety and pharmacokinetics of single and multiple ascending doses of avibactam alone and in combination with ceftazidime in healthy male volunteers: results of two randomized, placebocontrolled studies[J]. Clin Drug Investig, 2015, 35(5): 307-317.
[9] Abdul-Aziz MH, Alffenaar JWC, Bassetti M, et al. Antimicrobial therapeutic drug monitoring in critically ill adult patients: a Position Paper[J]. Intensive Care Med, 2020, 46(6): 1127-1153.
[10] Owen EJ, Gibson GA, Buckman SA. Pharmacokinetics and pharmacodynamics of antimicrobials in critically ill patients[J]. Surg Infect (Larchmt), 2018, 19(2): 155-162.
[11] Vincent JL, Bassetti M, Francois B, et al. Advances in antibiotic therapy in the critically ill[J/OL]. Critical Care, 2016, 20(1): 133. doi: 10.1186/s13054-016-1285-6.
[12] Stein GE, Smith CL, Scharmen A, et al. Pharmacokinetic and pharmacodynamic analysis of ceftazidime/avibactam in critically ill patients[J]. Surg Infect (Larchmt), 2019, 20(1): 55-61.
[13] Veillette JJ, Truong J, Forland SC. Pharmacokinetics of ceftazidime-avibactam in two patients with KPC-producing Klebsiella pneumoniae bacteremia and renal impairment[J]. Pharmacotherapy, 2016, 36(11): e172-e177.
[14] Merdjan H, Tarral A, Das S, et al. Phase Ⅰ study assessing the pharmacokinetic profile and safety of avibactam in patients with renal impairment[J]. J Clin Pharmacol, 2017, 57(2): 211-218.
[15] Walstad RA, Dahl K, Hellum KB, et al. The pharmacokinetics of ceftazidime in patients with impaired renal function and concurrent frusemide therapy[J]. Eur J Clin Pharmacol, 1988, 35(3): 273-279.
[16] 趙锦锦, 张菁. 头孢他啶-阿维巴坦药品说明书[J]. 国外医药(抗生素分册), 2019, 40(2): 115-127.
[17] 张菁, 吕媛, 于凯江, 等. 抗菌药物药代动力学/药效学理论临床应用专家共识[J]. 中华结核和呼吸杂志, 2018, 41(6): 409-446.
[18] Sternbach N, Leibovici Weissman Y, Avni T, et al. Efficacy and safety of ceftazidime/avibactam: a systematic review and meta-analysis[J]. J Antimicrob Chemother, 2018, 73(8): 2021-2029.

