高效液相色谱法测定头孢拉定胶囊有关物质及方法学验证
杜玮炜(1. 广州白云山医药集团股份有限公司白云山制药总厂,广州 510515;2. 广东省化学药原料与制剂关键技术研究企业重点实验室,广州 510515)
头孢拉定(cefradine,Velosef)是由百时美施贵宝公司于1972年研究成功的第一代半合成头孢类抗菌药物。其适应证为用于敏感菌导致的各种呼吸道、泌尿生殖道及皮肤软组织感染等。除注射剂外,头孢拉定可制成多种口服制剂,包括头孢拉定干混悬剂、头孢拉定片、头孢拉定胶囊和头孢拉定颗粒。
头孢拉定原料有关物质HPLC 检查方法收载于《中国药典》2020年版[1],其有关物质检验方法的色谱条件与含量测定方法(同时测定头孢氨苄含量)相同,以水-甲醇-3.86%醋酸钠溶液-4%醋酸溶液(1564∶400∶30∶6)为流动相等度洗脱各杂质。2020年版《中国药典》中头孢拉定的各种制剂产品要么没有设置有关物质检查项(头孢拉定干混悬剂和头孢拉定颗粒),要么采用和原料相同的色谱条件进行杂质检验(头孢拉定胶囊、头孢拉定片和注射用头孢拉定)。然而《中国药典》方法具有一定的局限性:对弱保留的杂质分离效果较差[2-3]。起始原料7-ADCA 峰和二氢苯甘氨酸(杂质B)峰与溶剂峰保留时间相近(见图1 和图2);其他主要降解杂质杂质C、D、E 均在3 ~5 min 内出峰(见图3)。并且按照《中国药典》方法,除头孢氨苄峰和头孢拉定主峰外,起始原料7-ADCA 作为已知杂质按照外标法定量,而最大的另一个工艺杂质——4',5'-二氢头孢拉定峰被认为是其他单杂,在头孢拉定胶囊中按照2.5%的限度控制,其他重要的能够体现制剂产品质量的降解产物(杂质C、D、E)反而不能得到有效的控制。
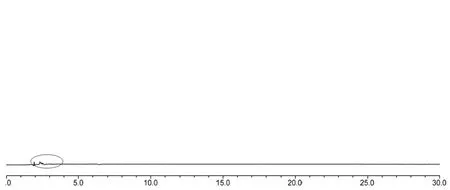
图1 《中国药典》有关物质测定方法溶剂色谱图Fig 1 Chromatogram of solvent by ChP method
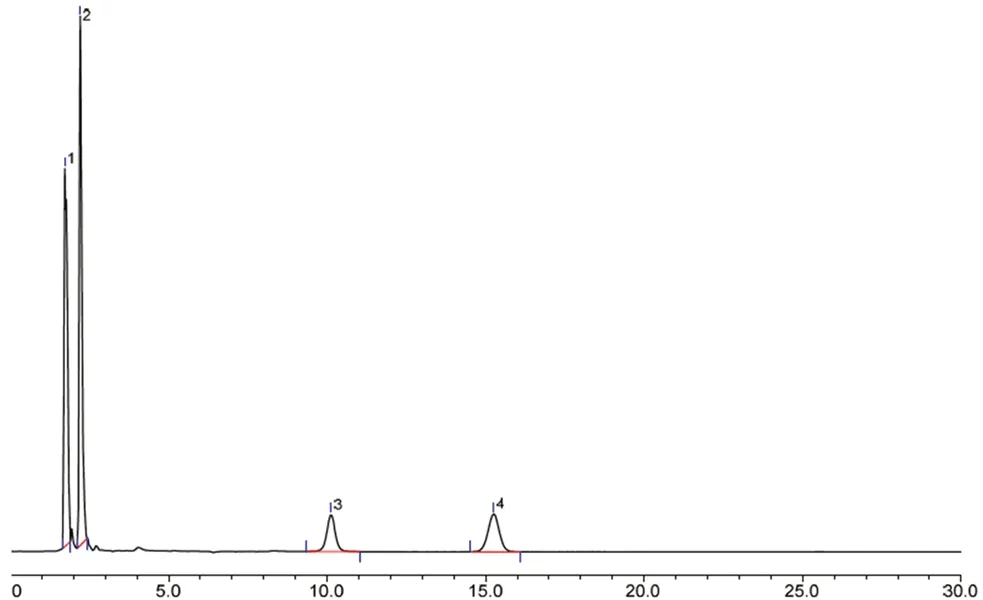
图2 《中国药典》方法杂质混合对照品溶液色谱图Fig 2 Chromatogram of mixed impurity standards by ChP method
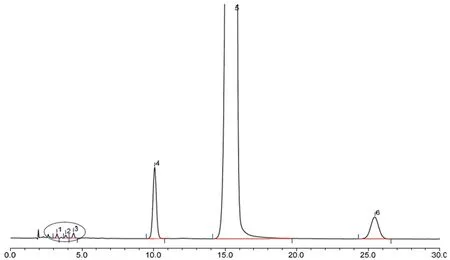
图3 《中国药典》方法供试品溶液色谱图Fig 3 Chromatogram of sample by ChP method
为解决上述问题,本研究参考英国药典[4]对方法进行了研究和改进,建立了方便、准确、专属性强及灵敏度高的头孢拉定胶囊有关物质HPLC 测定法并对其进行了方法学验证。
1 仪器与试药
安捷伦1260 高效液相色谱仪(DAD 检测器,Agilent 公司),戴安U-3000 高效液相色谱仪(DAD 检测器,Thermo Fisher 公司),CPA225D十万分之一电子天平(Sartorius 公司)。头孢拉定胶囊(施贵宝、英国KENT),头孢拉定(批号:130427-201107,纯度:88.3%)、杂质A(7-ADCA,批号:130416-201006,纯度:98.5%)(对照品,中国食品药品检定研究院),杂质B(二氢苯甘氨酸,EP,批号:3.0,纯度:100%);杂质C(批号:PILD0701-C01,纯度:96.84%)、杂质D(批号:PILD0607-D01,纯度:96.84%)、4',5'-二氢头孢拉定(批号:PILD1226-EQ01,纯度:98.75%)(对照品,广州牌牌生物科技有限公司);杂质E(深圳卓越生物科技有限公司,批号:PILD0419-E08,纯度:98.24%);杂质F(批号:1534-079A3,纯度:100%)、杂质G(批号:2144-023A2,纯度:99.8%)(美国TLC),甲醇(色谱纯,美国Merck公司),其他试剂均为分析纯,水为超纯水。
2 方法及结果
2.1 色谱条件
色谱柱:费罗门Luna 5u C18(2)100A(150 mm×4.6 mm,5 μm);检测波长:220 nm;柱温:30 ℃;进样量:25 μL;流动相:以2.72 g·L-1磷酸二氢钾溶液(用稀磷酸调pH 至3.0)为流动相A,以甲醇为流动相B,按表1 进行线性梯度洗脱;流速:1.0 mL·min-1。
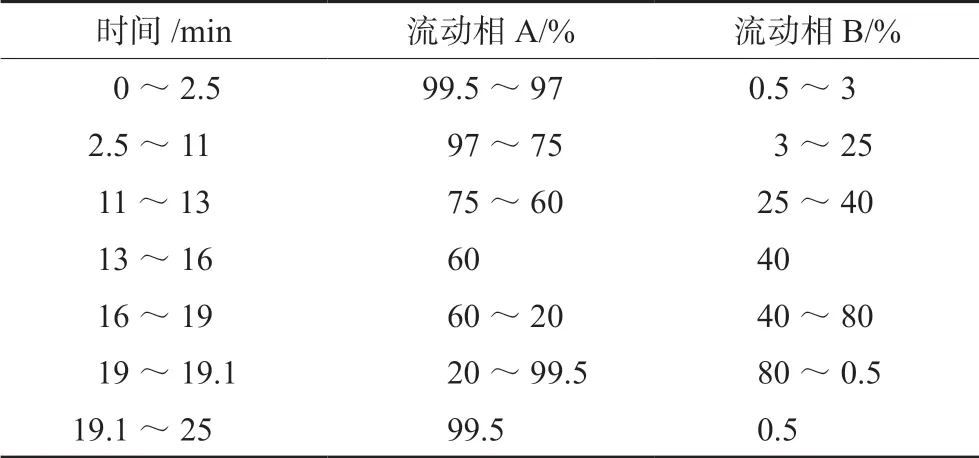
表1 流动相梯度洗脱程序Tab 1 Gradient elution program of mobile phase
2.2 系统适用性
取头孢拉定对照品和头孢氨苄对照品适量,用流动相A 溶解并稀释制成每1 mL 中约各含0.12 mg 的溶液,取25 μL 注入液相色谱仪,记录色谱图,头孢氨苄峰与头孢拉定峰间的分离度为6.7(不得低于4.0),符合系统适用性要求,见图4。
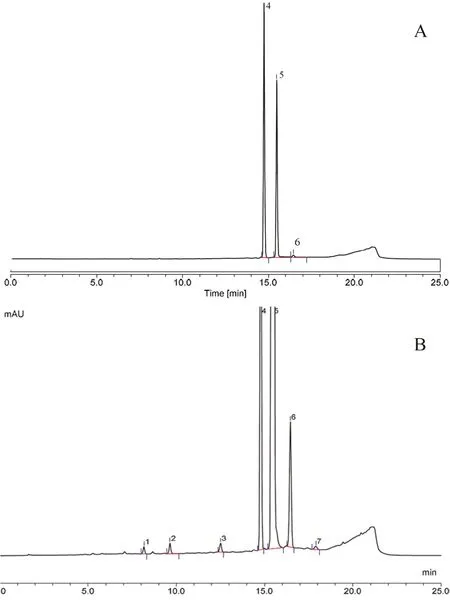
图4 系统适用性色谱图(220 nm)Fig 4 Chromatogram of system suitability(220 nm)
2.3 供试品溶液的配制
取头孢拉定胶囊内容物,精密称取适量,加流动相A 溶解并定量稀释制成每1 mL 中含6 mg的溶液,滤过,取续滤液作为供试品溶液。
2.4 对照溶液的配制
精密量取供试品溶液1.0 mL,置100 mL 量瓶中,用流动相A 稀释至刻度,摇匀,作为对照溶液(1%自身对照)。
2.5 测定法
分别精密量取供试品溶液和对照品溶液各25 μL,注入液相色谱仪,记录色谱图。相对保留时间(以下简称RRT)为0.52 的峰为杂质C;RRT为0.62 的峰为杂质D;RRT 为0.80 的峰为杂质E;RRT 为1.06 的峰为4',5'-二氢头孢拉定。杂质C、D、E 及4',5'-二氢头孢拉定按自身对照法计算含量。
3 方法学验证
3.1 专属性
3.1.1 强制破坏试验 空白溶剂及各辅料对有关物质测定不会造成干扰。样品在酸、碱、氧化、光照、高温等条件下破坏得到的杂质峰均与头孢拉定峰的分离度符合要求(不低于1.5),降解产物峰之间也具有良好的分离度,各破坏条件下主峰纯度因子均大于990。通过比较试验前后总峰面积的变化,物料平衡(A破坏后总峰面积/A破坏前总峰面积×100%)在90%~110%,方法专属性符合要求,结果详见表2。
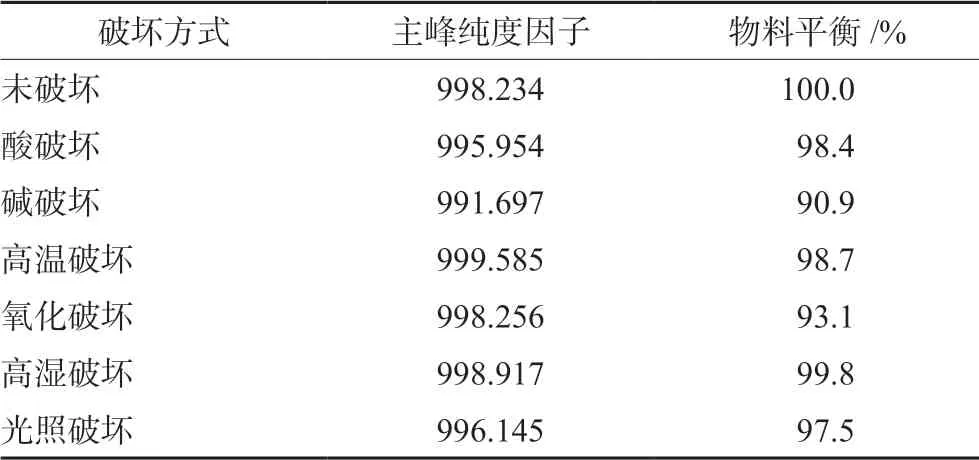
表2 强制破坏性试验测定结果Tab 2 Determination of forced degradation test
3.1.2 杂质对照品外加法 取杂质A、B、C、D、E、4',5'-二氢头孢拉定、杂质F 及杂质G 适量,分别溶解于流动相A 后加至供试品溶液中,精密量取25 μL,注入液相色谱仪,已知杂质无干扰(见图5)。
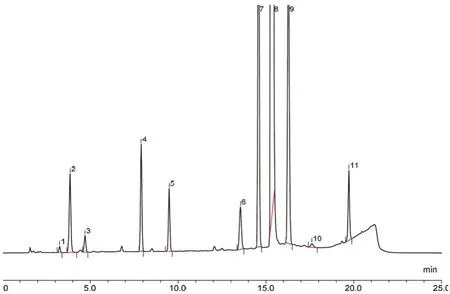
图5 杂质混合对照品外加溶液色谱图(220 nm 波长)Fig 5 Chromatogram of mixed impurity standards added in sample solution(220 nm)
3.2 线性关系及检测限和定量限
通过配制6 份系列浓度梯度的标准溶液对本方法的线性和范围进行验证。以各杂质浓度为横坐标,峰面积为纵坐标,进行线性回归。将杂质对照品溶液稀释至相应的浓度,根据信噪比10∶1,计算得各杂质的定量限;信噪比3∶1,计算得各杂质的检测限。结果表明杂质A ~G、4',5'-二氢头孢拉定及头孢拉定在相应范围内线性符合要求,方法灵敏度符合要求。
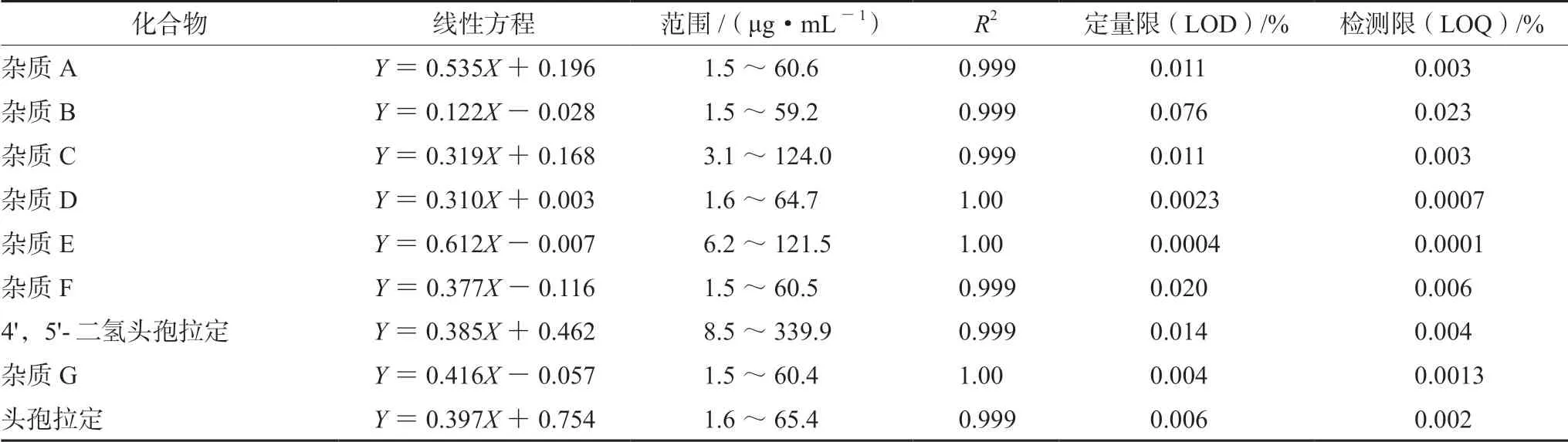
表3 杂质线性方程、检测限和定量限结果Tab 3 Regression equation,LOD and LOQ of impurities
3.3 准确度、精密度及耐用性试验
通过杂质对照品加样回收试验计算方法准确度;结合重复性和中间精密度判断方法精密度;改变柱温、流速、检测波长、流动相pH 对方法耐用性进行验证,结果见表4 ~5,表明该方法适用于头孢拉定胶囊有关物质检测。
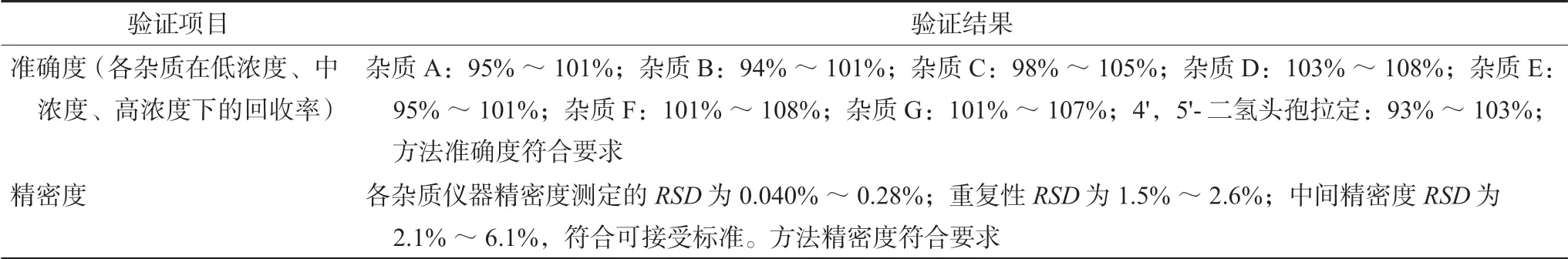
表4 验证项目测定结果Tab 4 Determination of validation

表5 耐用性试验结果Tab 5 Durability test
3.4 样品测定
取国内外上市头孢拉定胶囊样品5 批,按“2.3”项下方法制备供试品溶液,采用“2.1”项下色谱条件测定有关物质,结果见表6。在5 批头孢拉定胶囊制剂中均未检出杂质A、杂质B、杂质F 和杂质G,除去工艺杂质4',5'-二氢头孢拉定外,最大单杂均为杂质E。国内地产化原研产品(施贵宝)的有关物质略好于国外上市(英国KENT)的同品种制剂。
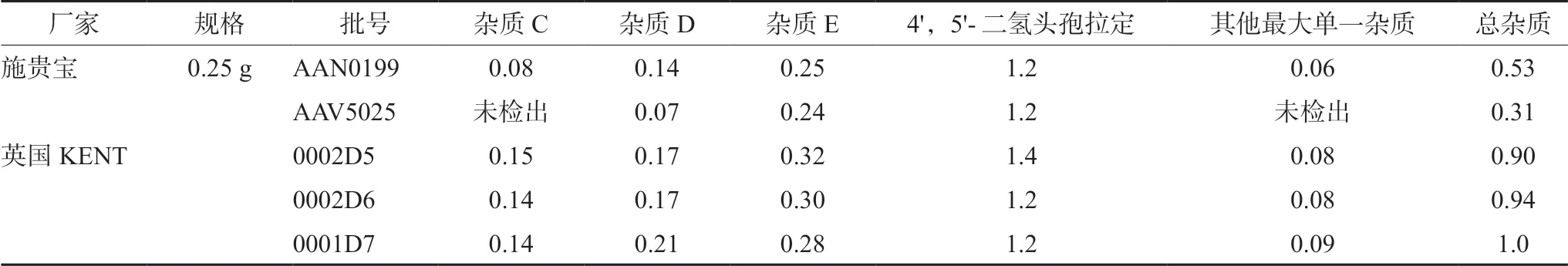
表6 头孢拉定胶囊有关物质测定结果(%)Tab 6 Determination of related substances in samples (%)
4 讨论
《中国药典》采用外标法控制杂质A(7-ADCA)不得过1.0%,而杂质A(7-ADCA)在国内上市的390 批次头孢拉定胶囊[2]和国内外上市制剂(施贵宝、英国KENT)以及强制破坏样品中均未检出。较为复杂的外标法操作显得必要性不强,并且药典对杂质A(7-ADCA)规定标准过高,需要进行适当的降低。
4',5'-二氢头孢拉定是头孢拉定合成的工艺产物(还原产物),其含量稳定,不会随着稳定性留样过程而增加。英国药典中4',5'-二氢头孢拉定用含量测定方法测定(检测波长254 nm),限度定为2.0%(外加校正因子1.6),并将4',5'-二氢头孢拉定、头孢氨苄和头孢拉定一起作为活性成分计入含量。虽然《中国药典》的色谱条件和英国药典不同,但有关物质的检测波长也是254 nm,从理论上判断,两种方法中4',5'-二氢头孢拉定的校正因子应相当,《中国药典》中有关物质单个杂质2.5%的限度算上校正因子其实为4.0%,显著高于英国药典的这一限度。在全国范围内选择9 个代表性头孢拉定制剂生产地区,从中随机抽取20 批头孢拉定胶囊(每个地区1 ~4批),有关物质最大单杂为1.2%~1.7%[5],显著小于《中国药典》中有关物质单个杂质2.5%的限度要求,进一步说明药典规定标准过高。而本研究提供的方法,用220 nm 检测4',5'-二氢头孢拉定,校正因子经计算在0.9 ~1.1(1.03),适合用自身对照法定量。
除头孢菌素外(头孢拉定、头孢氨苄、4',5'-二氢头孢拉定),杂质C、杂质D 和杂质E 的含量较大(其降解见图6 ~7),且随稳定性放样时间的延长及稳定性放样温度的升高而增长,其含量可反映头孢拉定降解水平,有必要对其进行限量规定。

图6 杂质C、D 降解机制图Fig 6 Degradation mechanisms of impurity C and impurity D
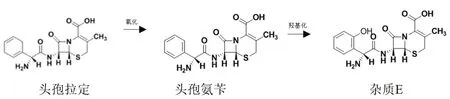
图7 杂质E 降解机制图Fig 7 Degradation mechanisms of impurity E
综上所述,《中国药典》标准中头孢拉定有关物质方法杂质分离效果不佳,单杂限度过高,且对反映头孢拉定胶囊降解水平的杂质C、杂质D和杂质E 无法控制。本研究建立的头孢拉定胶囊有关物质分析方法,能更有效的分离出各杂质,且简单、灵敏,专属性高,适用于头孢拉定胶囊有关物质的测定。

