基于多指标-响应曲面法优选“建昌帮”姜天麻提取工艺
周莉莉,张霞,彭巧珍,谢宇璐,叶喜德*,金镭*(. 中国人民解放军联勤保障部队第九〇一医院药剂科,合肥 00;. 江西中医药大学药学院,南昌 0004;. 南昌航空大学信息工程学院,南昌 006)
天麻为兰科无绿叶并寄生草本植物天麻Gastrodia elataBl.的干燥块茎[1]。性甘、味平,入肝经。具熄风止痉、祛风之痛之效,为治偏头痛之要药。始载于《神农本草经》并列之为上品[2]。天麻主含酚类、多糖、有机酸类、甾醇类、氨基酸及多种微量元素等成分[3]。
天麻炮制方法较多,如煨法、酒炙、蜜麸炒等,但未见炮制机制的研究。天麻姜制始载于《幼幼集成》[4],后为江西“建昌帮”列为其特色饮片之一[5]。目前江西、广东、福建等各地方炮制规范均收录了姜天麻[6-8],但均未见其炮制机制的研究。“建昌帮”认为姜制天麻可增强其祛痰熄风,定眩止痛之功。研究表明,天麻经姜制后,其化学成分发生了变化,而且动物行为学试验表明该炮制利于天麻对大鼠脑组织的保护[9-10],且姜天麻对硝酸甘油诱导的大鼠偏头痛抑制作用强于《中国药典》收录的天麻炮制品[11-12]。显然,天麻经姜制后药效增强,与其发生的有效成分变化有关。但如何使这些成分充分溶出,仍缺乏最佳提取工艺。基于前期炮制品制备探讨的姜天麻炮制工艺[13],本研究采用UPLC 定量分析,以天麻素,天麻苷元,对羟基苯甲酸,巴利森苷A、B、C、E 等多指标为质量评价方法,并结合响应曲面法[14]对料液比、提取温度及提取溶剂之间的交互作用进行考察,优选出姜天麻最佳提取工艺参数,提高该炮制品中有效成分得率,为后续研究提供数据支撑。
1 材料
1.1 仪器
Waters Acquity(e2695)超高效液相色谱仪(新加坡Waters 公司);TGL-16B 高速离心机(上海安亭科学仪器厂);AR240 十万分之一电子天平(Mettler Toledo 公司);KQ-500E 超声清洗仪(昆山市超声仪器有限公司)。
1.2 试药
天麻素(批号:CHB190212)、 天麻苷原(CHB190214)、 对羟基苯甲醇(批号:CHB180226)、巴利森苷A(批号:CHB180222)、巴利森苷B(批号:CHB180223)、巴利森苷C(批号:CHB180224)、 巴利森苷E(批号:CHB180225)(对照品,质量分数≥98%,成都克洛玛生物科技有限公司);水为超纯水,乙腈、甲醇为色谱纯,磷酸为分析纯。
天麻、生姜于(代富安虫草参茸行,批号:20200173),经江西中医药大学龚千锋教授鉴定分别为兰科天麻(Gastrodia elataBlume.)干燥块茎、植物姜(Zingiber officinaleRose.)的新鲜根茎。
2 方法与结果
2.1 色谱条件
色谱柱为Acquity UPLC BEH C18(100 mm×2.1 mm,1.7 μm),体积流量0.2 mL·min-1,柱温35℃。流动相为乙腈(A)-0.05%磷酸水溶液(B),梯度洗脱:0 ~14 min,3%~29%A;检测波长为220 nm。理论塔板数按天麻素峰计算不低于5000。
2.2 对照品制备
精密称取天麻素0.002 58 g、天麻苷元0.004 96 g、对羟基苯甲酸0.002 48 g、巴利森苷A0.002 54 g、巴利森苷B 0.004 97 g、巴利森苷C 0.002 37 g、巴利森苷E 0.002 22 g,用水溶液(乙腈-水=3∶97)定容于5 mL 量瓶中。
2.3 供试品制备
2.3.1 姜天麻制备[13]按“建昌帮”炮制规范炮制,打粉过3 号筛,备用。
2.3.2 供试品制备 精密称取姜天麻粉末1.00 g,置50 mL 锥形瓶中,加入20 mL 70%乙醇溶液,摇匀,静置30 min,称定重量,30℃超声30 min,放冷,再称定重量,用70%乙醇溶液补足减失量,过滤,取续滤液10 mL,挥去溶液,用水溶液(乙腈-水=3∶97)溶解,定容置25 mL 量瓶。取溶液适量,离心(15 000 r·min-1、10 min),0.22 μm滤膜过滤,即得供试品溶液。
2.3.3 混合对照品的制备 吸取“2.2”项下各对照品天麻素200 μL、天麻苷元10 μL、对羟基苯甲酸20 μL、巴利森苷A 200 μL、巴利森苷B 200 μL、巴利森苷C 150 μL、巴利森苷E 250 μL 加入2 mL EP 管,高速离心后,过0.22 μm 滤膜,即得混合对照品。
2.4 方法学考察
分别精密吸取混合对照品、供试品溶液各2 μL,注入液相色谱仪测定。天麻素,天麻苷元,对羟基苯甲酸,巴利森苷A、B、C、E 的保留时间分别为2.91、4.74、6.81、7.07、11.46、9.39、10.03 min。混合对照品与供试品各成分分离度良好,见图1。
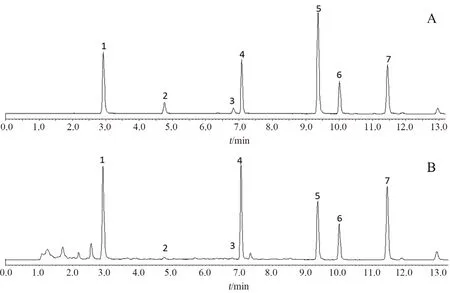
图1 天麻对照品(A)和供试品溶液(B)Fig 1 Gastrodia elata reference substance(A)and test solution(B)
2.4.1 线性关系考察 吸取“2.3.3”项下混合对照品溶液,逐级稀释并进样测定,结果见表1。
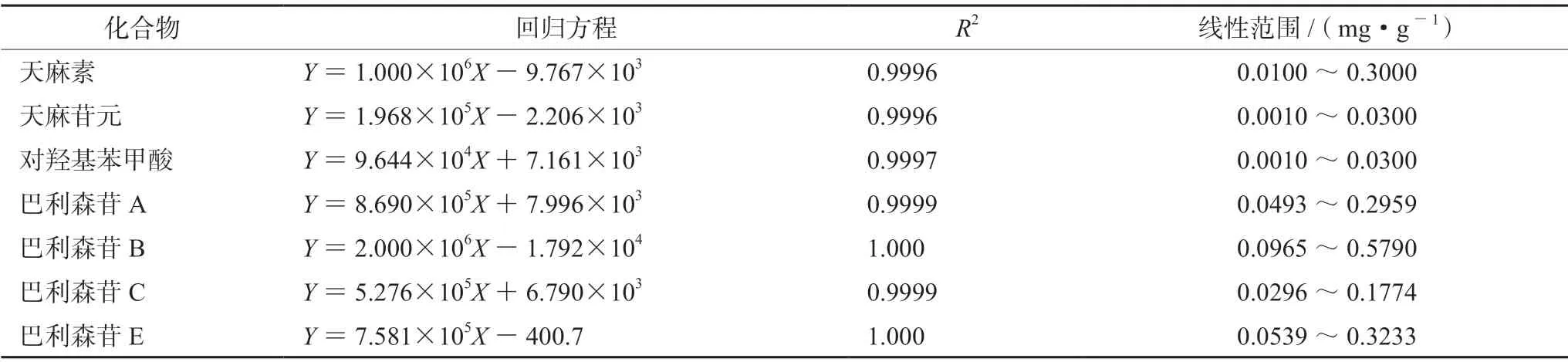
表1 各成分线性关系考察结果Tab 1 Linearity of each component
2.4.2 精密度考察 取混合对照品重复进样6 次,进行精密度试验。天麻素、天麻苷元和对羟基苯甲酸的峰面积RSD分别为0.68%、1.1%、1.3%;巴利森苷A、B、C、E 的峰面积RSD分别为0.19%、0.22%、0.46%、0.37%。
2.4.3 稳定性考察 于1、4、8、12、16、24 h测定同一份供试品溶液(7 号样品)的稳定性,得天麻素、天麻苷元和对羟基苯甲酸的峰面积RSD分别为0.27%、2.82%、3.0%;巴利森苷A、B、C、E 的峰面积RSD分别为1.3%、0.57%、2.1%、0.37%。
2.4.4 重复性考察 精密称取同一炮制方法下姜天麻粉末1.00 g,依“2.3.2”项下方法(7 号样品)制备,分别平行制备6 份。分别进样2 μL,测定峰面积,得天麻素、天麻苷元和对羟基苯甲酸的峰面积RSD分别为2.8%、2.0%、2.8%;巴利森苷A、B、C、E 的峰面积RSD分别为2.4%、2.8%、1.4%、1.5%。
2.4.5 加样回收考察 精密量取已测定的供试品溶液 3 份,每份1 mL,分别按供试品的80%、100%、120%加入混合对照品溶液(天麻素0.100 mg·mL-1,天麻苷元0.010 mg·mL-1,对羟基苯甲酸0.010 mg·mL,巴利森苷A、B、C、E分别为0.099、0.193、0.059、0.108 mg·mL-1)每个平行3 份,进样测定各指标含量,测得天麻素、天麻苷元和对羟基苯甲酸平均回收率(RSD)分别为103.12%(1.8%)、98.67%(2.8%)、100.34%(1.8%)。巴利森苷A、B、C、E 平均回收率(RSD)分别为101.56%(3.0%)、104.65%(1.8%)、99.13%(2.4%)、102.43%(2.5%)。
2.5 提取工艺单因素考察
由于天麻中巴利森苷类成分具有热不稳定性[15]。因此,选择适宜的提取溶媒、提取时间和提取温度是提高该类成分得率的主要因素。本研究选择提取溶媒、提取时间、超声温度、提取时间、料液比、粒径条件进行考察。
称取姜天麻粉末1.0000 g 5 份,固定其他条件不变,分别考察不同提取溶剂(水和不同浓度乙醇)、超声温度(20、30、40、50、60 ℃)、提取时间(20、30、40、50、60 min)、料液比(1∶15、1∶20、1∶25、1∶30、1∶35)、 粒径(过10、24、50、60、80 目筛)对提取效率的影响,结果如图2 所示。
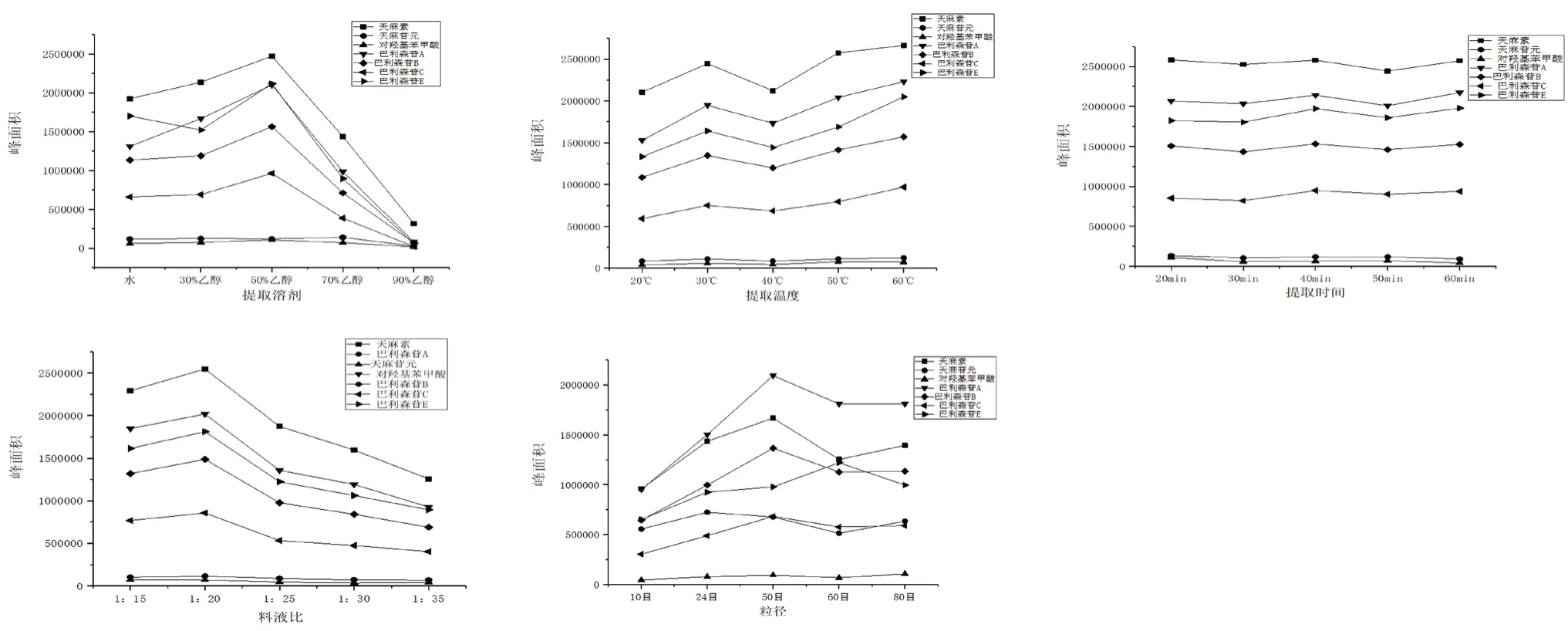
图2 不同提取条件对提取效率的影响Fig 2 Effect of different extraction conditions on extraction efficiency
2.6 响应曲面试验
2.6.1 试验设计 根据“2.5”项下单因素试验考察结果,设计因素水平见表2。

表2 响应面因素及水平Tab 2 Factor and level of response surface
2.6.2 试验结果 通过天麻目前研究进展及药理作用权重分配,确定综合评分(Z)=天麻素×30% +天麻苷元×20% +对羟基苯甲酸×10%+巴利森苷A×10%+巴利森苷B×10%+巴利森苷C×10%+巴利森苷E×10%。设计3 因素3 水平试验设计方案,应用Design-Expert V8.0.6 软件,中心组合设计Box-Behnken 分析处理,得到3 因素3 水平共17 组试验。试验方案分析及结果见表3。
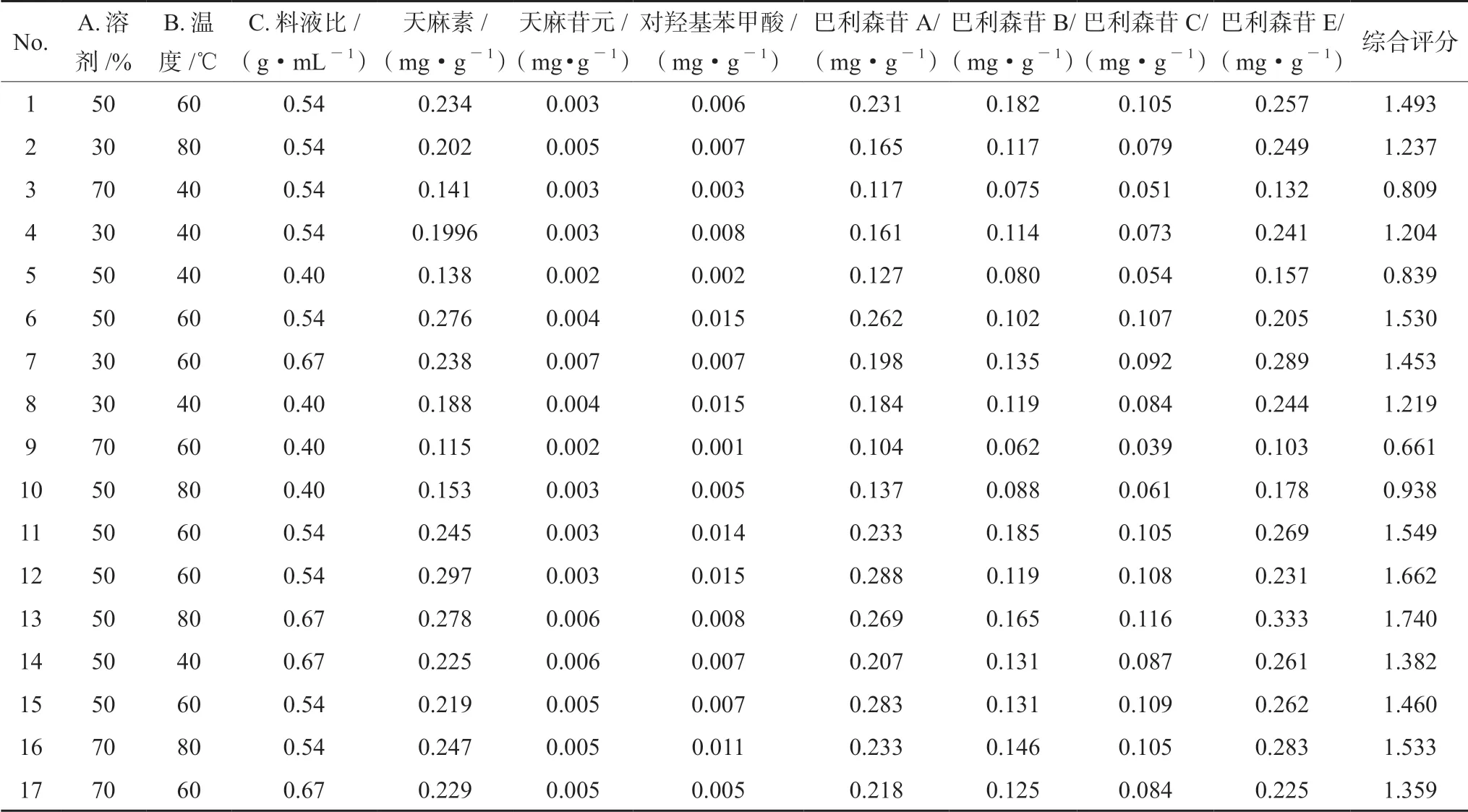
表3 响应面设计方案及试验结果Tab 3 Response surface design
2.6.3 响应面分析 响应曲面3D 图(见图3)分析可得,倾斜度越高说明两因素交互作用越明显,并且颜色越深变化加剧[16]。由3D 响应图可知溶剂与温度、料液比交互作用显著,响应面存在极值,由等高图可得提取温度对综合得分的影响大于提取溶剂与料液比。
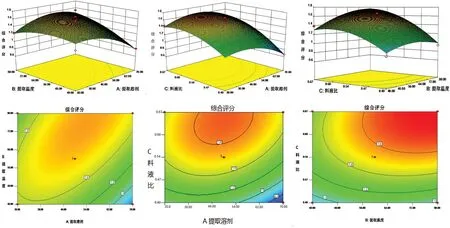
图3 提取溶剂(A)、提取温度(B)、料液比(C)交互作用Fig 3 Interaction of extraction solvent(A),extraction temperature(B)and solid-liquid ratio(C)
最后得到姜制天麻最佳工艺条件为70%乙醇提取溶剂,提取温度78.49℃,料液比1∶15,天麻素,天麻苷元,对羟基苯甲酸及巴利森苷A、B、C、E 和综合得分预测值分别为0.2641、0.0066、0.0107、0.2759、0.11676、0.1170、0.3294、1.7599 mg·g-1。基于此,结合单因素和实际生产考虑,姜制天麻工艺条件可为清蒸切片润制,70%乙醇、80 ℃、1∶15 超声提取40 min。
2.6.4 验证试验 精密称取1.0000 g 姜天麻3 份,按照优选最佳工艺进行提取,结果平均综合评分为1.8083 与模型预测值(1.7599)相近,相对误差小于5%。
3 讨论
课题组前期相继开展了姜天麻炮制前后主成分差异、药效等方面研究[17-19],证实了天麻经姜制后可使其药效增强,并与炮制后的变化成分密切相关,但未就姜天麻有效成分提取工艺开展研究。而响应曲面法依据试验中的随机误差,可连续对试验中各个水平进行分析,能用相对较少的试验次数,对试验因素水平中的交互作用做较全面的分析[20-22]。因此,本试验采用响应曲面设计法对姜天麻提取工艺进行优选。
对天麻化学成分研究,常选择天麻素和天麻苷元为主,其工艺优化也多局限于单个成分。但随着研究的深入,天麻中酚类成分更多地被证实为其入血效应成分。如巴利森苷A、B 分别具有改善学习记忆力、抗哮喘等作用[23-25]。为此,本试验在考察提取时间、提取温度、料液比、提取溶剂、提取粒径等单因素试验的基础上,选取提取溶剂、料液比和提取温度的交互作用进行响应曲面试验,以天麻素,天麻苷元,对羟基苯甲酸,巴利森苷A、B、C、E 为指标进行综合评价,建立了天麻7 种主要成分UPLC 含量测定方法,确定“建昌帮”姜天麻最佳提取工艺,且综合评价优化工艺稳定可行,响应模型拟合度良好,达到工艺优化目的。
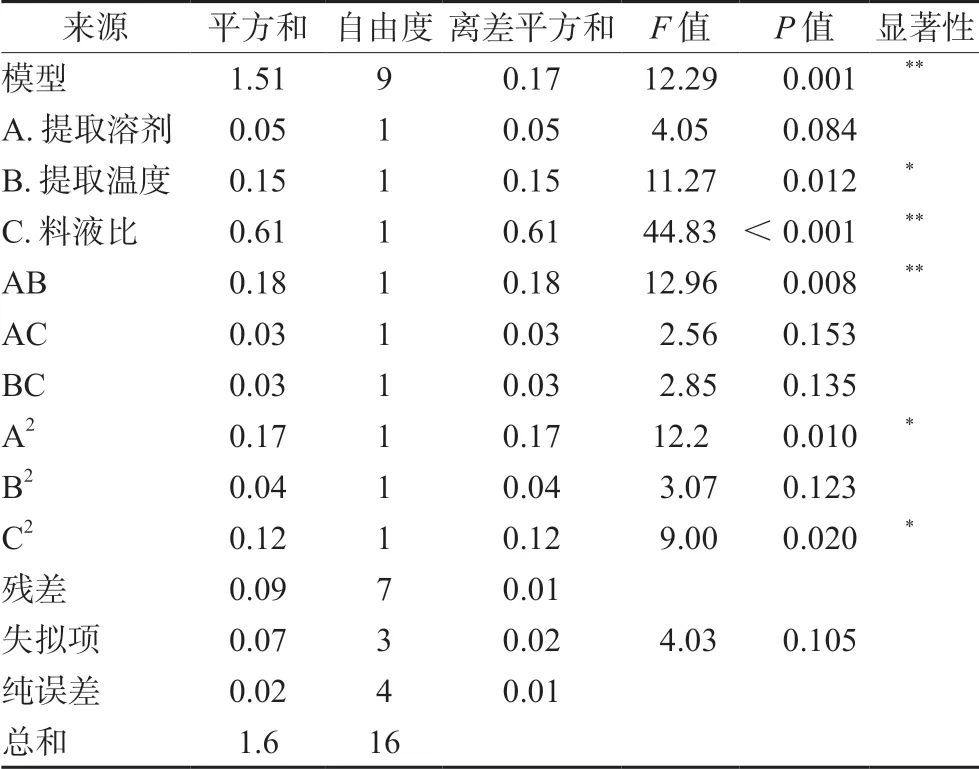
表4 差分析Tab 4 Variance analysis

