胆汁淤积症的生物机制研究进展
卢颖,秦琳,谭道鹏,鲁艳柳,何芋岐,杨艳,张倩茹*,周旭美*(. 遵义医科大学药学院 国家级药学实验教学示范中心 基础药理教育部重点实验室,贵州 遵义 563000;. 遵义医科大学附属医院药剂科,贵州 遵义 563000)
胆汁淤积是由于胆汁分泌及排泄障碍引起的肝脏以及体循环内胆汁酸、胆固醇及胆红素等胆汁成分过度堆积的一种病理生理过程。在具有原发性硬化性胆管炎、原发性胆汁性肝硬化(PBC)、非酒精性脂肪性肝病等慢性肝病史的住院患者中,胆汁淤积发病率高达10.26%[1]。胆汁淤积的临床表现以发热、疲劳、瘙痒、黄疸等非特异性症状为主[2],起病隐匿且妊娠、药物、手术、环境等多种因素均可导致其恶化,若不能及时改善则可能发展为肝硬化乃至肝衰竭,对患者的生命健康造成巨大危害,而目前对于胆汁淤积的发生机制及病程变化尚不十分明确。因此,本文对近10年来胆汁淤积的相关研究进展进行回顾,对胆汁淤积症的发病机制、形成因素及相关疾病进行总结与呈现,以期为胆汁淤积症的临床治疗与药物研发提供相关线索。
1 胆汁淤积症的类型
按照发病部位的差异,胆汁淤积症可分为肝内胆汁淤积与肝外胆汁淤积两种类型[3]。肝内胆汁淤积主要由于肝脏内部胆汁酸代谢和转运障碍,导致胆汁成分入血;肝外胆汁淤积则是由胆结石、寄生虫、肿瘤等因素导致胆总管部分或完全阻塞、肝外疝和嵌顿,引起肝外胆管系统异常梗阻。按照发病机制的不同,胆汁淤积症可分为遗传性胆汁淤积(又称原发性胆汁淤积)与获得性胆汁淤积(又称继发性胆汁淤积)两种[4]。遗传性胆汁淤积是致病基因突变引起的胆汁淤积,且具有一定的家族遗传性;获得性胆汁淤积通常是由后天因素(包括妊娠、药物、手术、环境等)引起的胆汁淤积。
2 胆汁淤积的发病机制
胆汁淤积症普遍认为是肝细胞和胆管上皮细胞结构与功能发生异常,转运蛋白功能受损,胆汁酸通路中酶活性降低或细胞骨架发生改变,导致胆汁流量的减少和胆汁淤积形成[5]。例如,进行性家族性肝内胆汁淤积症(PFIC)是一种常发生在婴儿时期的遗传性胆汁淤积性肝病,其发病机制与调控肝细胞运输系统的ATP8B1、ABCB11、ABCB4、TJP2、NR1H4等基因发生突变,胆酸盐外排泵(BSEP)、多药耐药3 蛋白(MDR3)等肝细胞转运蛋白表达减少甚至缺失有关。目前发现的PFIC 有1 ~6 型,肝组织病理通常可见肝细胞及毛细胆管胆汁淤积,其中PFIC-1 型肝组织病理特征为电镜下的粗颗粒状胆汁,部分肝细胞可形成腺泡样假玫瑰花结[6],免疫组化可发现γ-谷氨酰转肽酶表达缺失;PFIC-2 型肝组织病理特征为肝巨细胞的形成,肝细胞排列紊乱,免疫组化可发现BSEP 表达缺失;PFIC-3 型肝组织的病理特征为胆管增生和纤维化,免疫组化显示MDR3蛋白表达减少;PFIC-4 型电镜可见紧密连接异常,免疫组化显示紧密连接蛋白2 的表达缺失[7]。
随着人们对胆汁淤积的研究不断深入,其发病机制还被认为有:① 胆汁成分改变或胆管发生损伤,胆囊结石、肿瘤栓塞、药物、寄生虫等因素引起肝内外胆管阻塞导致胆汁淤积,发生胆道梗阻的大鼠肝脏可观察到肝细胞肿胀、炎症细胞浸润、小胆管增生、胆管壁增厚、肝细胞点状坏死、纤维组织增生等病理改变[8];② 机体发生炎症反应诱导肝细胞内信号通路或刺激炎症细胞因子[9],导致胆汁流动受阻引起胆汁淤积。在环境、病毒等刺激下机体产生自身免疫反应被认为是PBC 最为可能的发病机制,PBC 依据其病理学特征可分为胆管炎期、胆管增生期、瘢痕和纤维化期和肝硬化期,病理表现包括肝内胆管结构破坏、炎症扩张或碎屑样坏死、纤维化间隔和再生结节等[10]。
近年来,胆管上皮细胞的碳酸氢根分泌功能受损被认为是胆汁淤积的发病机制之一,有假说提出,碳酸氢根分泌减少并在胆管上皮细胞内累积,使胆汁酸进入胆管上皮细胞致细胞损伤凋亡,胆道屏障破坏,机体发生免疫损伤或氧化应激反应从而引起胆汁淤积[11]。
3 胆汁淤积的形成因素
3.1 遗传性因素
SLC25A13、ATP8B1、ABCB11等基因缺陷可能引起PFIC、良性复发性肝内胆汁淤积症等遗传性胆汁淤积性疾病[12]。
3.2 获得性因素
3.2.1 年龄 新生儿胆汁淤积性黄疸分为先天性胆道闭锁性黄疸和非胆道闭锁性胆汁淤积性黄疸,造成新生儿胆汁淤积的因素包括胆汁酸合成异常、胆管闭锁、结石等[13]。而老年人因肝脏功能减退,对药物的代谢能力降低,更容易发生药物性肝损伤,造成胆汁淤积性黄疸[14]。由此可见,新生儿与老年人由于肝脏等器官发育不成熟或出现衰退等原因均可能造成胆汁淤积。
3.2.2 妊娠 在妊娠期间,孕妇体内雌激素水平异常可损害BSEP、MDR3、多药耐药相关蛋白2(MRP2)等转运蛋白的表达与功能,抑制卵母细胞胆汁酸外排,造成妊娠期肝内胆汁淤积(ICP),危及胎儿生命健康[15]。ICP 的危险因素除常见的激素紊乱与病毒、尿道感染外,还包括孕妇的年龄、孕前体重、受教育程度、多胎妊娠、口服避孕药史等[16]。
3.2.3 手术 特发性术后胆汁淤积通常发生在心脏外科手术或腹部大手术后1 ~2 周,可能是由于术中使用麻醉剂、体外循环血量降低、失血过多等原因引起肝脏缺氧缺血,导致肝细胞功能障碍甚至肝细胞死亡。此外,长期的肠外营养与肠道功能衰竭均可导致肝内胆汁淤积[17],这种胆汁淤积被称为肠外营养相关胆汁淤积,与新生儿喂养不当、肠道菌群失衡、禁食时长、感染等有关[18]。手术造成的胆汁淤积通常与患者营养与能量得不到充分供给导致肝脏、胃肠道正常生理功能无法有效维持相关。
3.3 药物
非甾体抗炎药、抗高血压药、抗糖尿病药、抗惊厥药、降脂药和精神药物等多种临床药物可引起胆汁淤积、药物性胆管病和消失性胆管综合征,其中阿莫西林等抗菌药物比其他种类的药物更容易造成急性或慢性的胆汁淤积[19]。药物造成的胆汁淤积通常是由于药物自身毒性、自身免疫反应等原因造成胆道生理结构被破坏[20]。
3.4 疾病
胆汁淤积是败血症、肝外细菌感染和酒精性肝炎的常见并发症。当机体发生炎症反应或致病菌侵入血液循环并在体内生长繁殖产生毒素引起全身性感染,可继发肝脓肿、胆结石以及胆管炎等疾病,造成胆汁淤积,胆汁酸激活炎症巨噬细胞中的NLRP3 炎症小体被认为是胆汁淤积相关脓毒症的发病机制[21]。
3.5 生活习惯
胆石症是指胆道系统形成结石,大部分的结石为胆固醇结石,胆固醇结石中胆固醇含量约占90%。胆固醇摄入过多引发高胆固醇血症,进而导致胆固醇结石的形成。胆固醇积聚于胆道中造成胆汁淤积,而胆石症的发生与膳食结构、日常用水水质等均有着密切联系[22]。
3.6 其他
胆汁淤积的形成还可能与地理位置、季节交替等环境变化有关,例如妊娠期肝内胆汁淤积症的发病率差异在不同地理位置之间为0.05%~20%。在芬兰等低硒地区ICP 发病率较高[23],有假说提出,血清硒水平的降低可能是ICP 的病因之一,原因是谷胱甘肽过氧化物酶是一种依赖于硒的强抗氧化剂,硒水平的降低可能引起氧化应激反应[24]。此外,研究人员发现ICP 发病率具有季节性变化,在冬季达到峰值,而在夏季有下降的趋势[23]。与此同时,有研究显示ICP患者在夏季的血清硒水平明显高于冬季[25],进一步表明地理位置与季节变化共同影响着ICP 的发病率。此外,环境改变可使处于PBC 潜伏期的患者病情恶化为临床症状明显期,在长期吸烟、接触某些特殊化学物品及有毒垃圾的人群中PBC 发病率较高,这可能与环境改变造成机体免疫功能低下引起肝内胆汁淤积有关[26]。
4 胆汁淤积的生物机制
4.1 胆汁酸合成
胆汁酸作为胆固醇的代谢产物,可分为初级胆汁酸和次级胆汁酸。在胆汁酸合成过程中发生多级酶促反应,涉及到多种酶[27],例如胆固醇7α-羟化酶(CYP7A1)、3β-羟基-C27-类固醇脱氢酶(HSD3B7)等[28]。若这些酶的功能与活性发生改变甚至失活时均可能会导致胆汁酸合成速度异常,正常的胆汁酸结构与生理功能受到破坏,胆汁酸亲水性降低,有毒的胆汁酸中间产物形成,造成胆汁淤积。
CYP7A1、HSD3B7 是初级胆汁酸合成的关键酶。CYP7A1 属于细胞色素P450 氧化还原酶系,受法尼醇X 受体(FXR)的调控进而影响胆汁酸合成速度[29],当CYP7A1 表达过低时抑制胆固醇分解,导致胆固醇在体内蓄积形成高胆固醇血症。HSD3B7 是初级胆汁酸合成通路中唯一的异构酶,可维持胆汁酸正常生理功能、促进胆固醇吸收[30]。HSD3B7 缺乏或失活通常表现为儿童时期的肝脏受损,可引发胆汁淤积性肝病、新生儿黄疸、先天性胆汁酸合成缺陷症等多种疾病[31]。
Δ4-3-氧代类固醇5β-还原酶(AKR1D1)、胆汁酸-辅酶A 氨基酸-N-酰基转移酶(BAAT)等是次级胆汁酸合成的关键酶。AKR1D1 是一种具有还原能力的酶,对固醇核环结构具有修饰作用并参与类固醇激素代谢,当AKR1D1 发生缺陷时,具有肝毒性的胆汁酸在肝内积累,造成新生儿进行性胆汁淤积症、新生儿肝衰竭、先天性胆汁酸合成缺陷症等疾病[32]。BAAT 参与胆汁酸酰化,催化胆酸、鹅去氧胆酸等游离型胆汁酸与甘氨酸或牛磺酸结合,形成结合型胆汁酸[33]。BAAT 发生缺陷引起胆汁酸与氨基酸错误结合,导致肝内胆汁淤积、家族性高胆烷血症等疾病,临床上可表现为瘙痒、黄疸、生长迟缓、凝血时间延长、脂溶性维生素吸收不良等症状[34]。胆汁酸合成途径见图1。
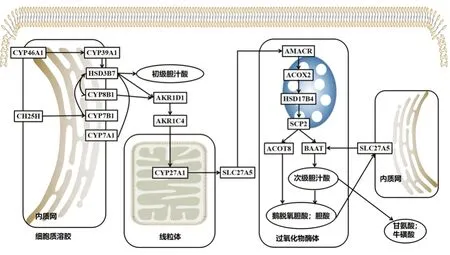
图1 胆汁酸合成途径(KEGG:ko00120)Fig 1 Synthesis pathway of bile acid(KEGG:ko00120)
4.2 胆汁酸转运
胆汁酸在肠道通过顶端Na+依赖性胆汁酸转运体(ASBT)、有机溶质转运蛋白α/β被重吸收进入门静脉,并通过肝细胞基底膜上的Na+依赖性牛磺胆汁酸盐协同转运多肽(NTCP)、非Na+依赖型有机阴离子转运多肽(OATPs)返回肝脏。重吸收回肝脏的胆汁酸再与新合成的结合型胆汁酸一起由肝细胞胆管侧膜BSEP 分泌入胆道系统,而未被重吸收的胆汁酸由MRP2 分泌入胆道系统,完成胆汁酸由胆囊至小肠的转运。胆汁酸转运促进胆汁流动,也促进了内源性化合物如胆红素、激素以及包括药物在内的外源性物质的消除。而当胆汁酸转运体受到抑制或发生缺陷时,胆汁酸的转运与排泄受损,肝脏和血液中胆汁酸水平升高,引起炎症反应或胆管堵塞,造成胆汁淤积。胆汁酸转运蛋白主要分为ABC 转运蛋白家族、溶质载体蛋白家族两类。胆汁酸转运与重吸收见图2。
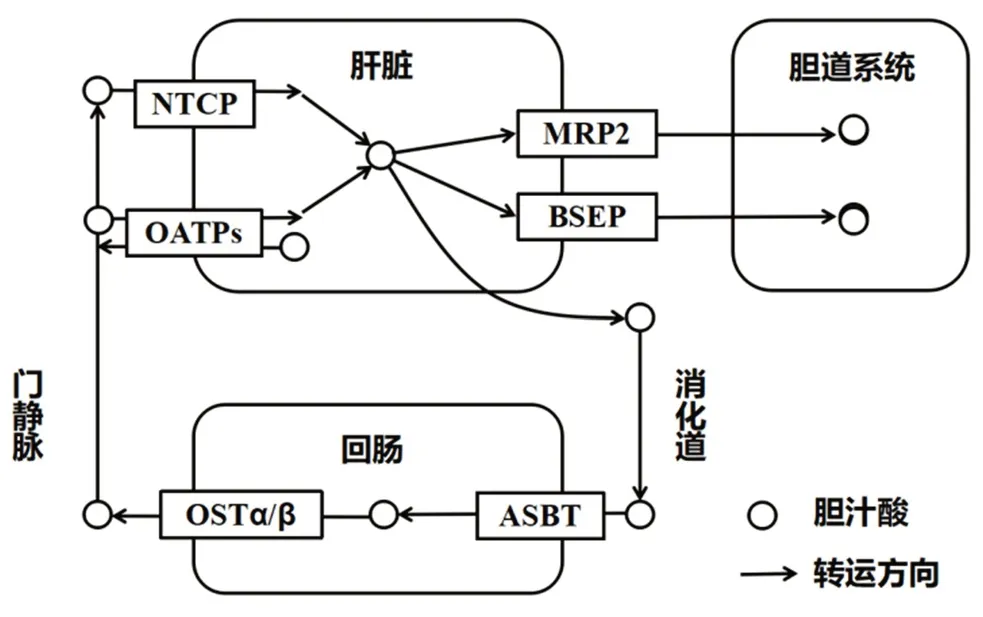
图2 胆汁酸转运与重吸收Fig 2 Transport and reabsorption of bile acid
4.2.1 溶质载体蛋白家族 溶质载体蛋白家族为跨膜转运蛋白,包括NTCP、ASBT 等转运蛋白。NTCP 可将大约90%的结合型胆汁酸摄入肝细胞[35],剩余约10%的结合型胆汁酸由OATPs摄入肝细胞内,当NTCP 转运胆汁酸功能被抑制时,OATPs 表达上调对胆汁酸转运起代偿作用[36]。NTCP 使肝细胞对胆汁酸敏感,胆汁酸在肝细胞中不断积累刺激炎症细胞因子的表达,使机体产生炎症反应造成胆汁淤积性肝损伤[37]。
ASBT 又称回肠胆汁酸转运蛋白,肠道内95%以上的胆汁酸经ASBT 转运。ASBT 与胆汁淤积症的发病和治疗有关。ASBT 的表达显著上调、FXR 表达下调时可引发PFIC[38]。A4250、volixibat、maralixibat 等ASBT 抑制剂减少了胆汁重吸收,使得胆汁的消除速率大于胆汁生成速率,用于多种类型胆汁淤积性肝病的治疗。
Citrin 蛋白属于线粒体内溶质载体蛋白家族载体蛋白,其编码基因为SLC25A13,主要参与氨基酸在线粒体内外的转运,与尿素循环密切相关。SLC25A13基因突变是婴儿发生胆汁淤积的常见诱因,可导致新生儿肝内胆汁淤积症。
4.2.2 ABC 转运蛋白家族 ABC 转运家族有7个亚族,BSEP 属于ABC 转运蛋白家族B 亚族,其编码基因为ABCB11,是胆酸盐分泌的限速转运体,可将胆酸盐从肝细胞内排出至胆管,并贮存于胆囊内。BSEP 蛋白缺陷导致PFIC2、良性复发性肝内胆汁淤积症、ICP 等多种疾病[39]。
MRP2 属于ABC 转运蛋白家族C 亚族,编码基因为ABCC2。MRP2 可将胆红素转运并随胆汁进入胆管,减轻胆酸盐细胞毒性作用。当毛细胆管排泌胆酸的正常通道受阻引起胆汁淤积时MRP2 表达下调,而位于肝细胞基底外侧膜的胆酸转运蛋白(MRP3)表达上调,MRP3 与MRP4可介导胆汁酸、胆红素、药物等底物外排入血液,在MRP2 功能受损时形成代偿机制[40]。
MDR3 属于ABC 转运蛋白家族B 亚族,MDR3 缺陷可导致胆固醇从胆汁中析出结晶形成结石阻塞胆道,影响胆道磷脂分泌,造成PFIC3、ICP、PBC、低磷脂相关胆石症等[41]。
4.3 胆汁酸代谢调控
胆汁酸作为代谢调控因子可以激活核受体和膜受体,对胆汁酸代谢进行负反馈调节。多条通路与胆汁酸负反馈调节有关,其中较为重要的通路是FXR-SHP 通路,在此通路中,FXR 由于胆汁酸的不断累积而被激活,诱导下游的小异二聚体伴侣表达,抑制CYP7A1 活性,负反馈调节胆汁酸的合成[42]。另一方面,胆汁酸-FXR-FGF15/19 信号通路是胆汁酸代谢调控的重要肠道途径,在此通路中,肠道FXR 被过度蓄积的胆汁酸激活,诱导回肠细胞上的成纤维细胞生长因子15/19 表达,成纤维细胞生长因子与肝细胞表面成纤维细胞生长因子受体发生特异性结合,从而抑制胆汁酸合成,避免胆汁酸过度累积[43]。胆汁酸代谢调控见图3。
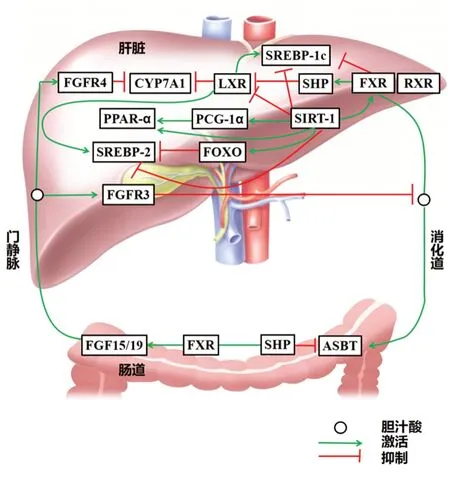
图3 胆汁酸代谢调控Fig 3 Regulation of bile acid metabolism
4.3.1 核受体 核受体是调控胆汁酸代谢的一类关键信号传导蛋白。FXR 等核受体位于细胞核内,可与进入细胞内的配体发生特异性结合,并通过信息传导调控多种蛋白的表达。FXR 又称胆汁酸受体,可上调BSEP、MDR2/3、MRP2、ASBT、OSTα/OSTβ表达,促进胆汁酸肠道重吸收。同时,FXR 可下调NTCP、OATPs 表达,避免胆汁酸在肝脏过度累积[44]。FXR 编码基因为NR1H4,有研究显示,PFIC5 是由NR1H4基因突变引起的胆汁淤积症[45]。类视黄醇X 受体为维生素A 类似物,可以和FXR 等多种核受体形成二聚体从而发挥生理功能,参与胆汁酸代谢[46]。
维生素D 受体为甾体激素受体,与维生素D3结合诱导CYP3A4 表达上调,促进石胆酸代谢[47]。在妊娠期间母体免疫系统中,维生素D 还可以通过维生素D 受体作用于辅助性T 细胞,使Th1 型细胞向Th2 型细胞方向转换,防止ICP 发生[48]。
4.3.2 膜受体 G 蛋白胆汁酸偶联受体5 作为膜受体,可被胆汁酸特异性识别。研究表明,具有G 蛋白胆汁酸偶联受体5 缺陷的小鼠易发生胆汁淤积性肝损伤[49]。
5 展望
胆汁淤积是一种由胆汁分泌或排泄障碍引起的病理生理过程,胆汁淤积未得到及时有效的治疗将会造成肝脏进一步的损伤,甚至引发肝纤维化、肝硬化等较为严重的肝脏相关疾病。本文通过将胆汁淤积的生物机制同胆汁酸合成、转运、代谢调控等生物过程及相关靶点进行联系,进一步阐述了FXR、NTCP、ASBT 等蛋白可能具有作为胆汁淤积临床治疗潜在靶点的可能性,对胆汁淤积的形成与发展进行了总结,对后续研究具有一定的启发性。

