基于美国FAERS数据库的新型降脂药前蛋白转化酶枯草溶菌素9抑制剂药物不良信号的数据挖掘与分析
张莎,祝德秋(同济大学附属同济医院,上海 200065)
药品不良事件(adverse drug events,ADE)监测是上市后再评价的重要途径,可以反映药品在实际使用中的安全性。其主要方法是基于对自发呈报数据库(spontaneous reporting system,SRS)的数据挖掘,从而获取药物与ADE 之间可能存在的因果关联,尽早发现潜在的ADE 信号,可及时进行药品上市后安全性再评价[1]。美国食品药品管理局(FDA)不良事件报告系统(adverse events reporting system,FAERS) 数据库是自发报告系统(spontaneous reporting system,SRS)最主要的数据库之一,可有效用于药物警戒,反映药物上市后在真实世界的安全性[2-4]。
随着生物技术及免疫学技术的快速发展,新型降脂药——前蛋白转化酶枯草溶菌素9(proprotein convertase subtilisin/kexin type 9,PCSK9)进入研究者的视野,通过选择性抑制PCSK9 靶点降低低密度脂蛋白胆固醇(LDL-C),进而减少心血管不良事件的发生[5]。因此,对PCSK9 抑制剂的研究成为降脂治疗的一个里程碑,具有十分重要的意义[6]。目前上市的PCSK9抑制剂主要有alirocumab 与evolocumab 两种药物,于2015年获美国FDA 正式批准上市,并先后于2018年/2019年获国家药品监督管理局批准在中国上市。由于其上市时间短,目前关于其安全性研究大多源于临床试验数据[6-7],缺乏大数据的系统性分析研究,药物上市后在真实世界的安全性有待更多的研究论证。因此,本研究通过对FAERS 数据库进行挖掘和筛选,利用报告比值比法(reporting odd ratio,ROR)对PCSK9 抑制剂ADE 信号进行分析,以期为临床安全用药提供参考。
1 资料与方法
1.1 数据来源
本研究数据来源于美国FAERS 数据库,该数据库相比其他数据库的数据要更加真实准确、规范与完善,并且在ADE 的发现、报告、评价与控制过程中得到了广泛的认同[8]。FAERS 数据库于2004年1月起开始对公众开放,每三个月会将最新的数据汇总发布[9]。收集alirocumab 和evolocumab 上市后至2020年第2 季度在FAERS数据库中能检索到的所有ADE 报告进行分析。本研究以alirocumab 与evolocumab 通用名为检索词,下载相对应的报告进行后续分析,每份报告内包含报告编号、报告日期、报告来源、患者的基本信息、给药途径、ADE 及结局等相关信息。
1.2 数据筛选
根据FAERS 的使用方法,去除重复的报告,从中选出用药名称为alirocumab 与evolocumab 为目标药物及首要怀疑药物的报告。
1.3 数据标准化
由于FAERS 数据库是SRS 数据库,其上报的数据存在上报名称不规范、存在冗余报告等问题[10],为减少因语言描述不同造成的偏倚,需要对所得到的数据进行标化。采用《ICH 国际医学用语词典》(MedDRA)将其标化成首选语(preferred terms,PT),并映射到对应的系统器官分类(system organ class,SOC),完成ADE 国际术语统一化。
1.4 数据分析
比例失衡法中的ROR 是目前在ADE 分析统计方法中灵敏度较高的方法。该方法基于四格表(见表1),通过比较目标药品的ADE 报告数与其他所有药品的报告数,以检测其潜在的ADE 信号。报告数≥3 且ROR 的95%CI下限>1,则提示生成一个信号,即药品与事件之间存在潜在关联[9]。统计分析采用SPSS 22.0 软件和Microsoft Excel 软件。

表1 比例失衡法四格表Tab 1 Fourfold table of measures of disproportionality
1.5 不良事件分类
通过MedDRA 筛选出对应PT,再通过系统器官分类(SOC)进行分类。
2 结果
2.1 alirocumab 和evolocumab 的不良事件报告基本情况
自alirocumab 和evolocumab 上市至2020年第2 季度以来,FAERS 数据库共收到alirocumab药物相关ADE 报告共34 491 例,evolocumab 药物相关ADE 报告共101 939 例。其中以alirocumab 和evolocumab 为首要怀疑药物的ADE 报告分别为12 341 例和69 462 例。均以女性患者居多,分别为55.76%和53.99%,ADE 报告国家以欧美为主,其中美国报告数最多,占总ADE 数的97%以上,详见表2。
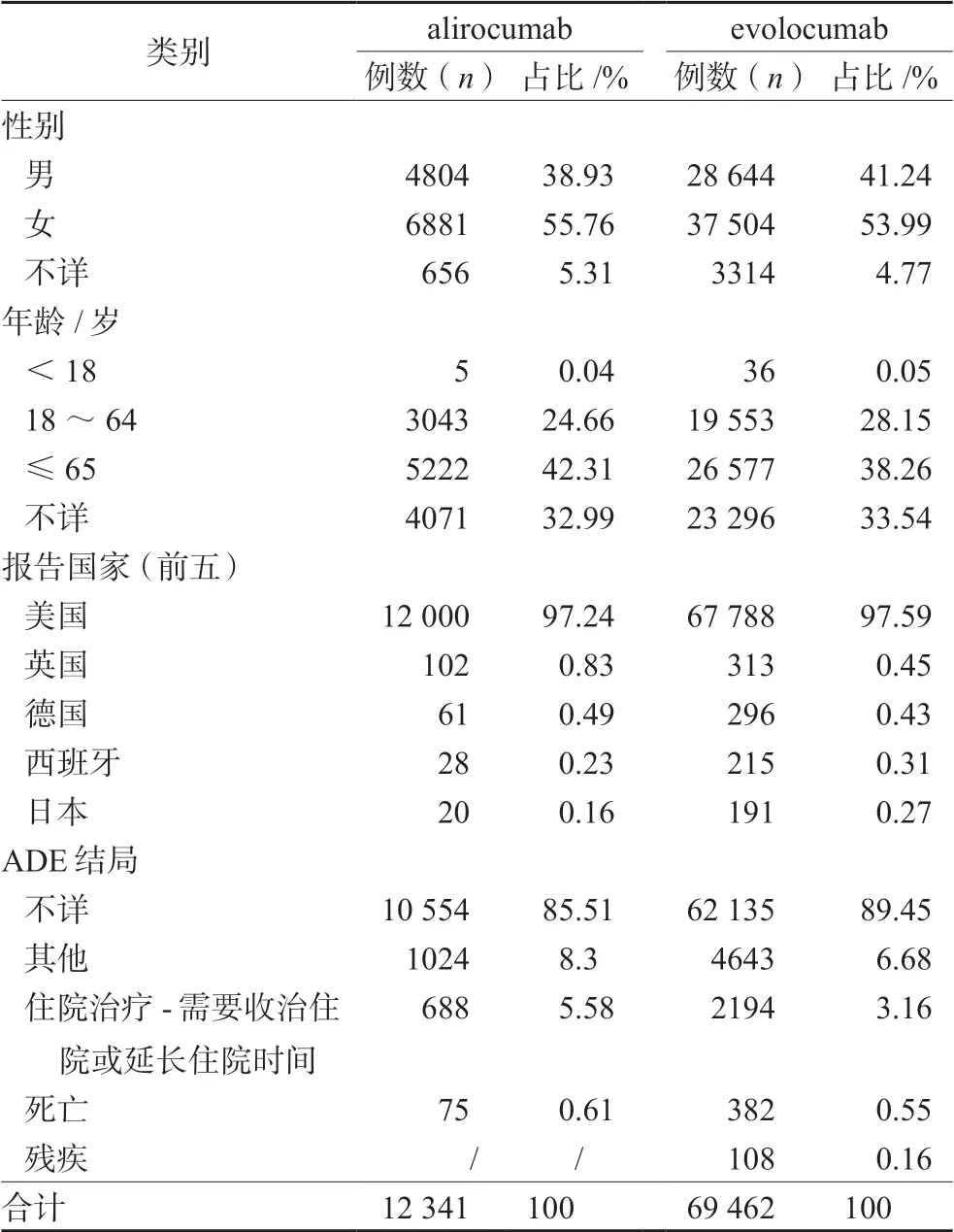
表2 FAERS 中alirocumab 和evolocumab 相关不良事件报告基本信息Tab 2 Primary information of alirocumab and evolocumab related adverse events reports in FAERS
2.2 alirocumab 和evolocumab 信号强度和报告数排名前20 位的ADE 信号
对分别以alirocumab 和evolocumab 为首要怀疑药物的ADE 进行信号分析,以PT 信号强度与出现频次对前20 个信号进行排序。详见表3 和表4。
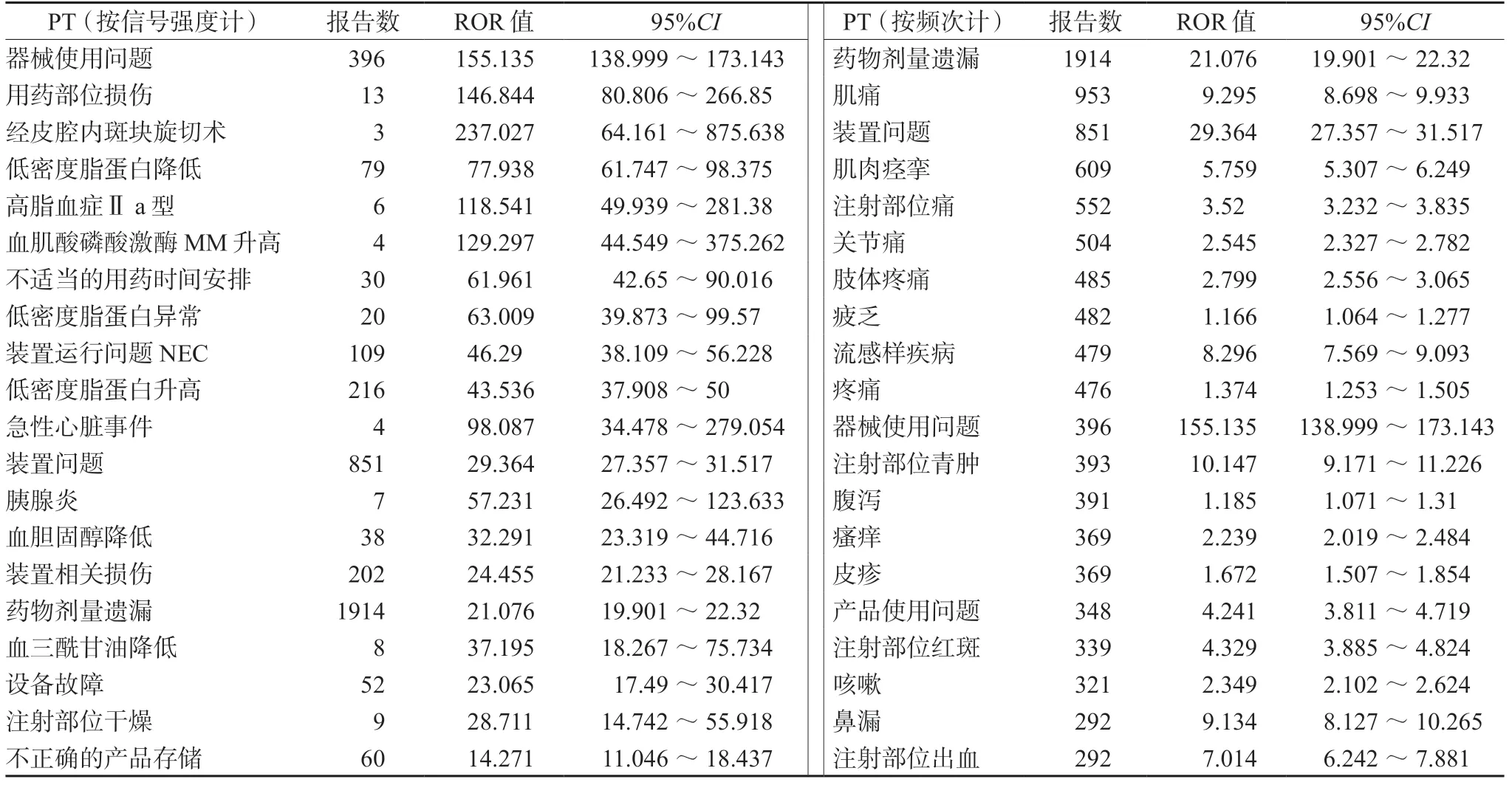
表3 alirocumab 信号强度和报告数排名前20 位的ADE 信号Tab 3 Top 20 ADE signals of alirocumab of strength and number of reports
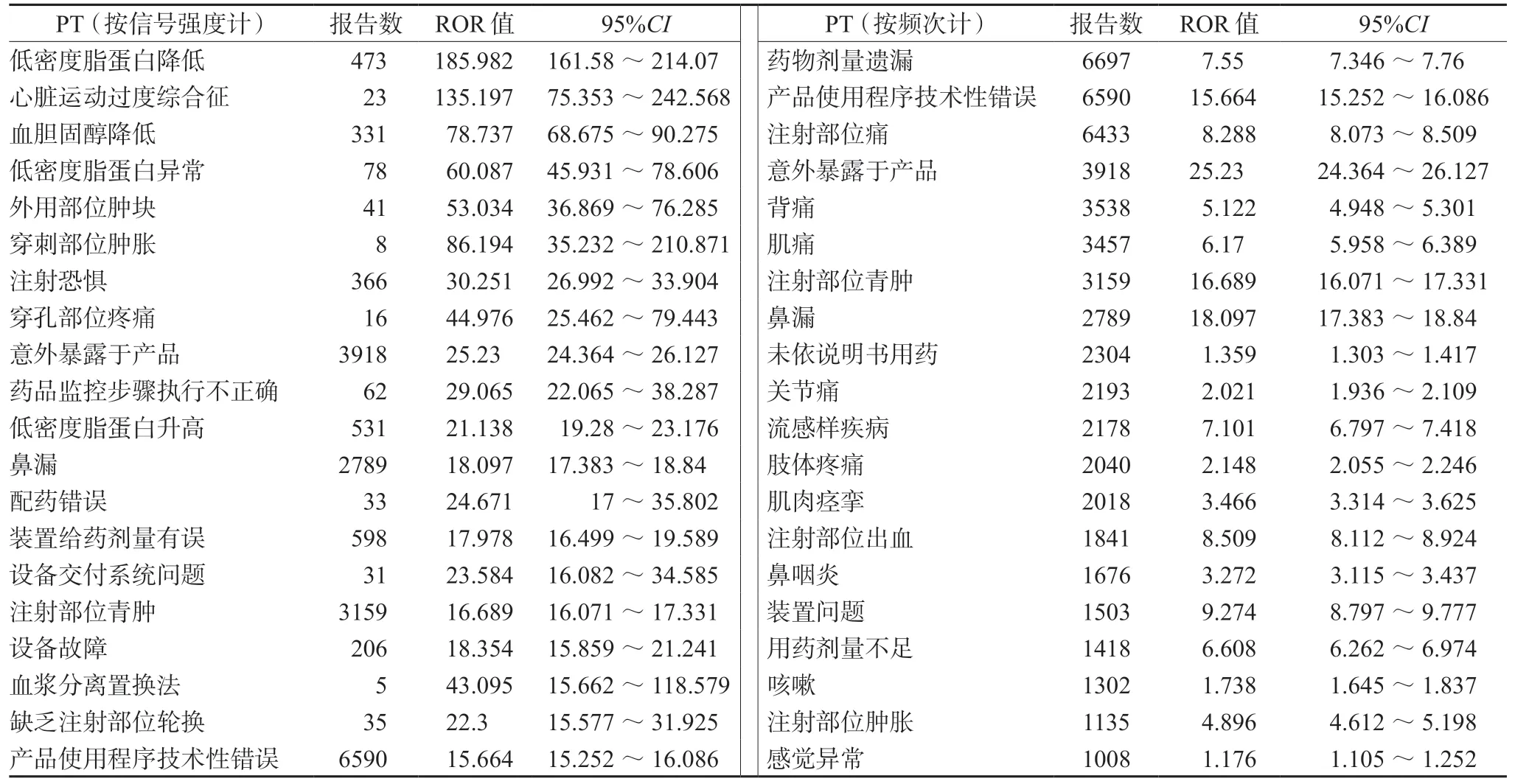
表4 evolocumab 信号强度和报告数排名前20 位的ADE 信号Tab 4 Top 20 ADE signals of evolocumab of signal strength and reports
2.3 alirocumab 和evolocumab 新的可疑ADR 信号
挖掘出信号强且分别与alirocumab 和evolocumab 相关且未在说明书上标注的新的可疑ADR 信号。alirocumab 最终获得37 个信号,其中包括已被药品说明书收录的ADE 17 个(45.95%),未收录的20 个(54.05%);evolocumab 最终获得36 个信号,其中包括已被药品说明书收录的ADE 18 个(50%),未收录的18 个(50%)。将上述二次筛选后有信号的PT 按照 SOC 进行分类,alirocumab 信号数最多的SOC 为全身性疾病及给药部位各种反应(n=7,18.92%),其次主要涉及各类损伤、中毒及手术并发症、各类检查、各种肌肉骨骼及结缔组织疾病等;evolocumab 信号数最多的 SOC 为全身性疾病及给药部位各种反应(n=9,25%)和各类损伤、中毒及手术并发症(n=9,25%),详见表5。排除非ADR 后,alirocumab 和evolocumab 相关的未在药品说明书中提及的新的疑似的ADR 信号主要涉及各类检查,呼吸系统、胸及纵隔疾病,心脏器官疾病等SOC,包括有低密度脂蛋白升高、血肌酸磷酸激酶MM 升高、鼻漏、急性心脏事件、注射部位干燥、胰腺炎等,详见表6。

表5 alirocumab 和evolocumab 不良事件信号与累及的系统和器官Tab 5 alirocumab and evolocumab related ADE signals and systems and organs involved

表6 新的疑似不良反应信号与累及的系统和器官Tab 6 New signs of suspected ADRs of alirocumab and evolocumab and systems and organs involved
3 讨论
本研究通过对FEARs 数据库进行ADE 信号挖掘发现,alirocumab 和evolocumab 相关ADE报告主要分布在年龄>18 岁的患者,这可能与血脂异常患病人群多为中老年人有关。ADE 上报人员国家主要集中在欧美,中国较少,这可能与该药在中国上市不久,其使用率不高以及FARES为美国数据库在国内使用不多等因素有关。
3.1 非ADR 且信号强烈的 ADE
FAERS 数据库包括了一切与药品使用有关的环节所出现的不利的和非预期的结果(如检查结果的异常)、体征或疾病均应上报,包括偶然或故意的药物使用过程问题、药物剂量问题、药物滥用等导致的ADE,以及由于患者自身的背景疾病等因素导致的ADE 等[11],即ADE 包括了药物直接导致的药物不良反应(ADR)以及其他的不良事件。因此本研究将挖掘到的ADE 信号分为非ADR 的ADE、说明书已收录的ADR 和新的疑似ADR 三类逐一进行分析。
本研究首先对非ADR 且信号强烈的ADE 进行数据挖掘分析发现,alirocumab 的相关信号中发生例次和信号强度排名均在前20 位的PT 均为非ADR 的ADE,包括器械使用问题、装置问题以及药物剂量遗漏;evolocumab 的相关信号中发生例次和信号强度排名均在前20 位的PT 包括意外暴露于产品、鼻漏、注射部位青肿以及产品使用程序技术性错误,4 个PT 中有2 个均为非ADR 的ADE。Alirocumab 和evolocumab 的相关信号中发生例次和信号强度排名均在前20 位的PT 主要都是非ADR 且信号强烈的ADE,这可能与该类药品的剂型以及使用方法有关,因PCSK9 抑制剂为注射剂,且需要通过皮下注射给药,给药方法较为复杂。这提示使用该药品前,医务人员应对患者如何正确使用提供适当训练,并将此作为患者用药教育的重点,以提高患者用药安全性。
3.2 说明书已收录的ADR
本研究对信号强度和信号频次排名前20 位的ADE 报告进行分析发现,alirocumab 和evolocumab所得的ADR 信号与药品说明书和文献研究基本一致[6-7]。排除非ADR 后,两药药品说明书中提及且信号强烈的ADR 信号种类数最多的SOC 均为“全身性疾病及给药部位各种反应”,主要表现为注射部位反应,包括注射部位疼痛、青肿、出血、肿胀、感觉异常以及流感样疾病等。这与PCSK9 抑制剂类药物说明书记载的一致,这可能与该药为针剂,需要定期皮下注射给药有关,从而导致注射部位反应明显。因此如何减轻患者注射部位症状,改善患者用药感受值得深思;其次,两药主要涉及的SOC 均为“组织疾病”,包括背痛、肌痛、关节痛、肢体疼痛等骨骼肌肉相关ADR,这与目前PCSK9 抑制剂临床试验的结果一致。有临床研究显示alirocumab 组肌痛发生率高于安慰剂组(5.4%vs2.9%,P<0.01)[12];目前尚无文献报道 PCSK9抑制剂会引发严重肌肉组织损伤横纹肌溶解症。在之后的研究中,仍应关注PCSK9 抑制剂的骨骼肌相关ADR,并重视有无横纹肌溶解症的发生。此外,本研究发现相较于evolocumab、alirocumab 在皮肤及皮下组织类疾病,各类损伤、中毒及手术并发症和胃肠系统疾病等发生了更多的ADR,在之后的临床使用中需要更加注意。
3.3 新的疑似 ADR 信号
本研究对信号强度和信号频次排名前20位的ADE 报告进行分析发现,alirocumab 和evolocumab 相关信号中分别发现了20 个和18 个新的ADE 信号,排除非ADR 后,药品说明书中未提及且信号强烈的ADR 信号共有15 个,主要涉及的SOC 为各类检查、心脏器官疾病、胃肠系统疾病、呼吸系统、胸及纵隔疾病。
横纹肌溶解症为他汀类药物引起的严重肌肉组织损伤的ADR,严重者可致死。FDA 报道称每100 万名患者中将会有0.3 ~13.5 例发生横纹肌溶解症[13]。虽然目前尚无文献报道 alirocumab会引发横纹肌溶解症,但是本研究发现药品说明书中未提及且信号强烈的ADR 血肌酸磷酸激酶MM 升高,虽然该信号频次低但是信号强度高(ROR =44.549)。因此,考虑到横纹肌溶解症的危害性,在临床应用PCSK9 抑制剂类药物时,一旦发生可疑血肌酸磷酸激酶MM 升高,建议立即停药观察。
Alirocumab 和evolocumab 发现心脏器官疾病的新的可疑高风险信号,包括急性心脏事件和心脏运动过度综合征等不良反应,虽然发生频次低但信号强度高,ROR 分别为34.478 和75.353。理论上,ROR 值越高,ADR 与用药之间的关系就越密切。然而在alirocumab 和evolocumab 说明书中均未记载对心血管患病率和死亡率的影响,这可能与药品上市前研究的局限性有关。考虑到此类ADR 的风险性与信号强度较高,在之后临床应用过程中应注意监测,提高警惕。此外,alirocumab 和evolocumab 均发现“鼻漏”这一新的疑似ADR 信号,且发生频次均排名在前20位,以evolocumab 发生信号强度更高(ROR =17.383)。这一信号与药品说明书中记载的鼻咽炎、咳嗽等呼吸系统ADR 尚有联系,可进一步提示该风险信号可能是PCSK9 抑制剂新的警戒信号,建议临床关注。
本研究还挖掘到evolocumab 未出现,但alirocumab 出现的胰腺炎、高脂血症Ⅱa 型、注射部位干燥、疲乏等新的疑似ADR 信号,但是发生例数均较少,后续需要更多的研究去探究这些疑似ADR 信号与该药的关联性。
3.4 研究局限性
由于FAERS 数据库为自发呈报数据库,对报告者身份没有限制,因此报告数据可能质量不一:① 上报名称不规范;② 存在冗余报告与重复数据;③ 数据信息不全;④ 药物与ADR 报告信息不对应等。
另外通过ROR 法挖掘目标药物与目标ADR的统计学关联性时,当ADR 报告数量很少时,ROR 法用于信号挖掘的准确性可能降低[14]。当信号检测出现比例失衡时,仅代表信号的产生,但对于结果的临床意义仍需进一步验证。
4 结论
临床使用 PCSK9 抑制剂时,除应密切关注注射部位反应、骨骼肌肉组织疾病、呼吸系统疾病等安全问题外,还应警惕心脏器官疾病以及相关检查指标等潜在的高风险 ADR 信号。本研究通过对FAERS 数据库的ADE 报告进行数据挖掘与分析,探索alirocumab 和evolocumab 上市后在真实世界临床应用中的可疑ADR 信号,获得了相对更加真实完整的药品安全信息,为临床用药提供参考,以保障患者用药安全。

