miR-3122靶向CMTM5调控口腔鳞癌细胞GNM凋亡的分子机制
刘一鹏 乔永明 朱保玉 王海业 耿玉东 张月兰
口腔鳞状细胞癌(OSCC)是全球常见的高度致死性癌症,这归因于其复发和转移[1]。尽管已观察到OSCC的治疗持续改善,但患者的存活率并未显著提高[2]。为了提高口腔癌患者的生存率,重要的是了解口腔肿瘤发生的分子机制。Manikandan M等[3]通过高通量测序描绘了OSCC的miRNA表达谱,发现了许多表达异常的miRNA,包括miR-29b,miR-142-3p,miR-144,miR-3122。然而,miR-3122在OSCC中的生物学功能尚不明确。基于此,本研究以口腔鳞癌细胞GNM为研究对象,旨在探讨miR-3122靶向CMTM5调控口腔鳞癌细胞GNM凋亡的分子机制。
1 材料与方法
1.1 材料
口腔鳞癌细胞GNM购自广州一科生物科技有限公司(货号:CL-0086)。GCSAM,PSMC4,SKP1,LIAS,SMAD2,ZNF704,CMTM5,STK17A,YWHAQ的siRNA、CMTM5过表达质粒、miR-3122 mimics和miR-3122 inhibitor均由天津擎科合成。CMTM5抗体购自上海群己生物科技有限公司(货号:H00116173-B01)。GAPDH抗体购自武汉市武昌区科迈实验用品经营部(货号:KF703)。Annexin V-PE凋亡检测试剂盒购自广州威佳科技有限公司(货号:C1065L)。TRIzol试剂购自生工生物工程(上海)股份有限公司(货号:B610409-0100)。pEZX-MT01质粒购自BioVector质粒载体菌种细胞基因保藏中心(货号:pEZX-MT01)。荧光素酶标记试剂盒购自广州一科生物科技有限公司(货号:A1001-8)。BCA蛋白定量试剂盒购自北京迈瑞达科技有限公司(货号:M052460-500T)。Lipofectamine®2000购自广州泰勒生物科技有限公司(货号:11668-019)。青链霉素混合液(100×)购自上海亿言生物科技有限公司(货号:SL6040-100ml)。第一链cDNA合成试剂盒购自北京兰博利德商贸有限公司(货号:C1802)。
1.2 方法
1.2.1 细胞培养与转染 口腔鳞癌细胞GNM在DMEM培养基中培养,添加10%胎牛血清,青霉素100 U/ml,链霉素0.1 mg/ml,37 ℃,100%空气。GNM细胞以2×105/孔的密度接种于6孔板,用于转染。使用Lipofectamine®2000进行GCSAM,PSMC4,SKP1,LIAS,SMAD2,ZNF704,CMTM5,STK17A,YWHAQ的siRNA、CMTM5过表达质粒、miR-3122 mimics和miR-3122 inhibitor的转染。转染后48 h进行下游实验。
1.2.2 RNA抽取与实时荧光定量PCR 纳入2018年6月至2020年6月我院收治的口腔鳞癌患者60例,收集此60例患者的口腔鳞癌组织和癌旁组织。采用qRT-PCR检测基因表达。使用TRIzol试剂提取组织或细胞的总RNA,并使用第一链cDNA合成试剂盒根据生产协议进行逆转录。在ABI 7500系统上进行qRT-PCR,条件为:95 ℃ 30 s;95 ℃ 5 s(40次循环);60 ℃ 30 s,72 ℃ 15 s。以GAPDH为内参对照,计算基因的相对表达量。每个样本检测3次。
1.2.3 免疫印迹 收集细胞裂解液后,用BCA蛋白检测试剂盒检测蛋白浓度。等数量的蛋白用10% sds-聚丙烯酰胺凝胶分离电泳,然后转移到聚偏二氟乙烯(PVDF)膜上。用5%脱脂牛奶封闭后,以抗GINS2抗体为一抗,抗GAPDH抗体为内参,4 ℃孵育过夜。随后,膜与适当的二抗孵育在室温下1 h。用化学发光基质试剂盒对信号进行成像,用凝胶成像系统检测。Western blotting实验进行了3个重复。
1.2.4 荧光素酶报告实验 荧光素酶报告质粒pEZX-MT01包含CMTM5的野生型或突变型3'UTR。使用荧光素酶报告基因系统分析荧光素酶活性前,将miR-3122 mimic或阴性对照(NC)和荧光素酶报告基因共转染至口腔鳞癌细胞GNM。
1.2.5 细胞凋亡水平的检测 根据制造商的说明,使用Annexin V-PE凋亡检测试剂盒对不同处理的细胞进行凋亡分析。简而言之,经过不同处理后,收集在6孔板上生长的漂浮口腔鳞癌细胞GNM和胰蛋白酶分离的细胞,并用冷的1×PBS洗涤。然后将细胞沉淀物用结合缓冲液重悬,并根据试剂盒方案用Annexin-V染色。荧光显微镜观察。将实验组中凋亡细胞的百分比与对照转染组进行比较。所有样品一式三份测量。
1.3 统计学分析

2 结果
2.1 miR-3122在口腔鳞癌组织和癌旁组织中的表达
收集60例口腔鳞癌组织和癌旁组织后,通过RNA抽取和实时荧光定量PCR发现,miR-3122在癌旁组织中的表达水平高于口腔鳞癌组织(P<0.05),见图1。

图1 miR-3122在口腔鳞癌组织和癌旁组织中的表达
2.2 miR-3122促进口腔鳞癌细胞GNM的凋亡
使用miR-3122 mimics过表达miR-3122后,口腔鳞癌细胞GNM的凋亡水平上升(P<0.05),而使用miR-3122 inhibitor敲低miR-3122后,口腔鳞癌细胞GNM的凋亡水平下降(P<0.05),见图2。

图2 miR-3122对口腔鳞癌细胞GNM凋亡的影响
2.3 miR-3122靶向CMTM5的3端非编码区
TargetScan、miRcode、miRDB在线分析发现miR-3122分别潜在靶向69、82、184个基因,通过取三者交集发现miR-3122共同潜在靶向22个基因,见图3A。使用miR-3122 mimics过表达miR-3122后,口腔鳞癌细胞GNM中GCSAM,PSMC4,SKP1,LIAS,SMAD2,ZNF704,CMTM5,STK17A,YWHAQ的表达水平下降(P<0.05),见图3B。使用siRNA敲低口腔鳞癌细胞GNM中上述基因后,发现敲低CMTM5后口腔鳞癌细胞GNM的凋亡水平上升(P<0.05),见图3C。通过荧光素酶报告实验发现miR-3122靶向CMTM5的3端非编码区(P<0.05),见图4A。同时,过表达miR-3122后,CMTM5的mRNA水平和蛋白水平均下降(P<0.05),而敲低miR-3122后,CMTM5的mRNA水平和蛋白水平均上升(P<0.05),见图4B,图4C和图4D。
2.4 miR-3122靶向CMTM5调控口腔鳞癌细胞GNM凋亡
同时敲低miR-3122和CMTM5时,口腔鳞癌细胞GNM凋亡水平无显著变化(P<0.05),见图5A;同时过表达miR-3122和CMTM5时,口腔鳞癌细胞GNM凋亡水平无显著变化(P<0.05),见图5B。
3 讨论
口腔癌的肿瘤分布广泛,包括嘴唇、硬腭、上、下牙槽嵴、舌前三分之二、舌下、颊黏膜、臼齿后三角区和口底[4]。2012年,OSCC在全世界造成14.5万人死亡[5]。OSCC的发展阻碍了多模式治疗的成功,导致预后不良和5年生存率低[6]。因此,研究OSCC的发生发展的分子机制对治疗OSCC是必不可少的。
在本研究中,miR-3122在癌旁组织中的表达水平高于口腔鳞癌组织(P<0.05)。过表达miR-3122后,口腔鳞癌细胞GNM的凋亡水平上升(P<0.05),而敲低miR-3122后,口腔鳞癌细胞GNM的凋亡水平下降(P<0.05)。提示miR-3122是一个潜在的抑制肿瘤发生发展的分子。
MicroRNAs(miRNAs)是一种短(19-25nt)单链非编码RNA,通常与目标mRNA的3端非编码区中的互补序列结合,并通过随后招募RNA诱导的沉默复合物来抑制其翻译[7]。由于大于30%的人类基因被预测受到miRNAs的调控,这些miRNA控制着所有的细胞的生理和发育过程[8]。TargetScan,miRcode,miRDB在线分析发现miR-3122分别潜在靶向69,82,184个基因,三者交集为22个基因。过表达miR-3122后,口腔鳞癌细胞GNM中GCSAM,PSMC4,SKP1,LIAS,SMAD2,ZNF704,CMTM5,STK17A,YWHAQ的表达水平下降(P<0.05)。敲低上述基因后,敲低CMTM5后口腔鳞癌细胞GNM的凋亡水平上升(P<0.05)。尽管敲低除CMTM5外的其他基因并不能引起口腔鳞癌细胞GNM凋亡水平的改变,但是这些基因在OSCC发生发展中的生物学功能值得进一步探索。此外,miR-3122靶向CMTM5的3端非编码区(P<0.05)。过表达miR-3122后,CMTM5的mRNA水平和蛋白水平均下降(P<0.05),而敲低miR-3122后,CMTM5的mRNA水平和蛋白水平均上升(P<0.05)。因此miR-3122通过靶向CMTM5的3端非编码区来抑制其翻译。

注:*P<0.05。

注:*P<0.05。
先前的研究表明,CMTM5通过启动子甲基化作用在许多肿瘤中发挥抑癌功能,并频繁发生表观遗传失活[9]。CMTM5位于14q11.2,这是一个包含与多种癌相关的多个基因的基因座[10]。研究表明,染色体14q11.2上的基因异常会导致各种癌症的产生或生长,例如鼻咽癌,白血病,胶质母细胞瘤,脑膜瘤和口腔鳞癌[11-12]。这些结果表明CMTM5在致癌作用中具有重要作用。本研究同时敲低miR-3122和CMTM5时,口腔鳞癌细胞GNM凋亡水平无显著变化(P<0.05);同时过表达miR-3122和CMTM5时,口腔鳞癌细胞GNM凋亡水平无显著变化(P<0.05)。因此,可以通过体外合成miR-3122 mimics,再通过合适的呈递方式将miR-3122 mimics运送到口腔鳞癌组织中可能起到缓解或治疗OSCC的效果。
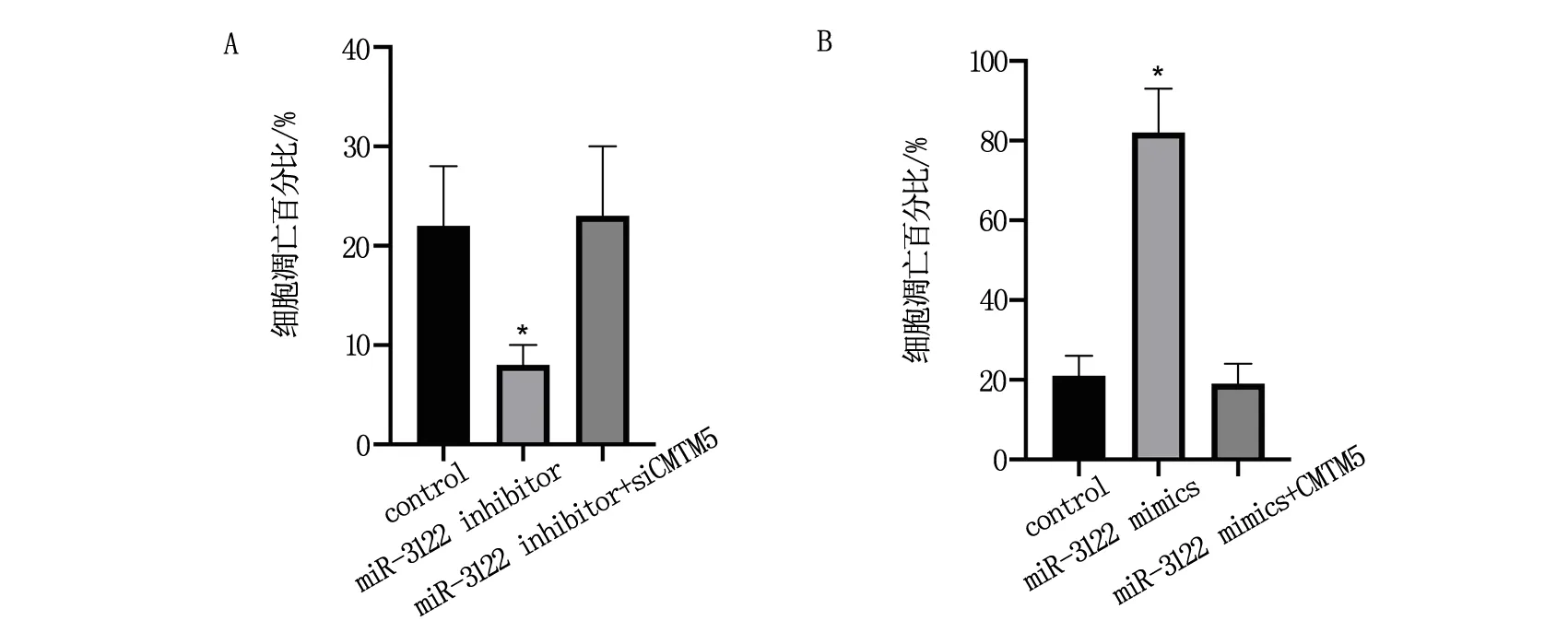
注:*P<0.05。
综上所述,miR-3122通过靶向CMTM5 mRNA的3端非编码区后,降解了CMTM5的mRNA并降低了CMTM5的蛋白水平,随后促进了口腔鳞癌细胞GNM的凋亡。

