氯氮平联合阿立哌唑对精神分裂症患者代谢综合征的应用价值研究Δ
彭冬红,张亚平,钟宝亮
(华中科技大学附属精神卫生中心/武汉市精神卫生中心精神科,湖北 武汉 430000)
氯氮平是具有5-羟色胺(5-HT)受体/多巴胺受体拮抗作用的高效抗精神病药,其功效优于许多第1代和第2代抗精神病药[1-2]。氯氮平被广泛用于精神分裂症的治疗,但其功效和安全性仍不令人满意。许多精神分裂症患者的氯氮平治疗效果较差,其中多数患有与氯氮平相关的心脏代谢异常,例如体重增加、血脂异常等[3-4],这可能导致其无法持续使用氯氮平。氯氮平与阿立哌唑联合应用是精神分裂症的一线治疗方案。阿立哌唑与其他药物的不同之处在于,在治疗精神分裂症患者症状的基础上,对体重和糖脂代谢影响较小[5]。随着肥胖症被公认为一种严重危害健康的疾病,抗精神病药使用导致的体重增加引起了人们的重视[6]。精神分裂症患者中超重和肥胖症的患病率很高。尽管躁动、焦虑、头痛和失眠是阿立哌唑的常见不良反应,但其不太可能引起体重增加或血脂异常[7]。单用阿立哌唑的效果往往不能让人满意,但联合其他药物又有代谢综合征(metabolic syndrome,MS)的隐患。阿立哌唑联合氯氮平的临床试验结果表明,该方案可减轻精神病症状和在一定程度上减少体重增加[8]。因此,本研究探讨了氯氮平联合阿立哌唑在精神分裂症患者MS中的应用价值,现报告如下。
1 资料与方法
1.1 资料来源
选取2017年7月1日至2018年6月30日于华中科技大学附属精神卫生中心就诊的120例精神分裂症患者作为研究对象,进行回顾性分析。纳入标准:(1)病历资料完整;(2)符合精神分裂症诊断标准;(3)入院前至少2周未服用过抗精神病相关药物。排除标准:(1)病历资料不完整者;(2)合并其他精神疾病者;(3)有阿立哌唑或氯氮平不良反应史者。将患者随机分为氯氮平组、阿立哌唑组和联合治疗组。氯氮平组40例,其中男性21例,女性19例;年龄19~47岁,平均(24.3±6.5)岁。阿立哌唑组40例,其中男性18例,女性22例;年龄21~49岁,平均(23.6±7.2)岁。联合治疗组40例,其中男性20例,女性20例;年龄18~48岁,平均(24.2±5.6)岁。三组患者一般资料的均衡性较高,具有可比性。
1.2 方法
氯氮平组患者给予氯氮平片(规格:25 mg)口服治疗,首次剂量为1次25 mg,1日3次,治疗2周后逐渐增加剂量至1次100~150 mg,1日3次。阿立哌唑组患者给予阿立哌唑片(规格:5 mg)治疗,初始剂量为1次5~10 mg,1日1次,治疗2周后逐渐增加剂量至1次30 mg,1日1次。联合治疗组患者给予氯氮平联合阿立哌唑治疗,氯氮平的用药方法同氯氮平组,阿立哌唑的用药方法同阿立哌唑组。三组患者的疗程均为16周。有睡眠障碍者给予苯二氮或安坦类药物,限制给药剂量,有其他不良反应者对症处理。
1.3 观察指标
(1)比较两组患者治疗前和治疗4、8、16周后的阳性和阴性症状量表(positive and negative syndrome scale,PANSS)评分。(2)于治疗前和治疗16周后观察三组患者代谢相关指标(空腹血糖、甘油三酯、高密度脂蛋白及体重指数)水平的变化。(3)比较三种治疗方案对患者MS发生率的影响。MS的诊断标准依据中华医学会糖尿病学分会(2004年)的标准[9]。(4)比较两组患者治疗4、8、16周后的副反应量表(treatment emergent symptom scale,TESS)评分。
1.4 统计学方法
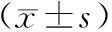
2 结果
2.1 三组患者治疗前后PANSS评分比较
治疗前,三组患者的PANSS评分、阳性症状和阴性症状评分的差异均无统计学意义(P>0.05)。治疗4周后,三组患者的PANSS评分、阴性症状评分明显低于治疗前;治疗8、16周后,三组患者的PANSS评分、阴性症状以及阳性症状评分明显低于治疗前;治疗4周后,联合治疗组的PANSS评分和阴性症状评分明显低于氯氮平组,差异均有统计学意义(P<0.05);治疗8、16周后,联合治疗组患者的PANSS评分、阴性症状评分以及阳性症状评分明显低于氯氮平组,差异均有统计学意义(P<0.05);治疗4周后,联合治疗组与阿立哌唑组PANSS评分、阴性症状评分的差异无统计学意义(P>0.05);治疗8、16周后,联合治疗组患者的PANSS评分、阳性症状评分以及阴性症状评分明显低于阿立哌唑组,差异均有统计学意义(P<0.05),见表1。
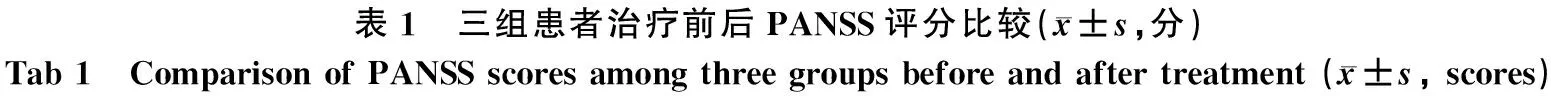
2.2 三组患者治疗前后代谢相关指标水平比较
治疗前,三组患者空腹血糖、血脂及体重指数等代谢相关指标水平的差异均无统计学意义(P>0.05)。治疗16周后,联合治疗组患者的空腹血糖、甘油三酯及体重指数水平明显低于氯氮平组,高密度脂蛋白水平明显高于氯氮平组,差异均有统计学意义(P<0.05),而与阿立哌唑组比较的差异均无统计学意义(P>0.05);阿立哌唑组患者空腹血糖、甘油三酯及体重指数水平明显低于氯氮平组,高密度脂蛋白水平明显高于氯氮平组,差异均有统计学意义(P<0.05),见表2。
2.3 三组患者治疗后MS发生情况比较
治疗4周后,三组均有患者出现MS。联合治疗组、氯氮平组和阿立哌唑组的MS发生率分别为7.5%(3/40)、32.5%(13/40)和5%(2/40)。联合治疗组的MS发生率明显低于氯氮平组,差异有统计学意义(χ2=7.813,P=0.005);但是与阿立哌唑组比较的差异无统计学意义(χ2=0.213,P=0.644)。
2.4 三组患者治疗后TESS评分比较
三组患者治疗4、8及16周后TESS评分组间比较,差异均无统计学意义(P>0.05),见表3。

表3 三组患者治疗后TESS评分比较分)Tab 3 Comparison of TESS scores among three groups before and after treatment scores)
3 讨论
在过去的十年中,随着第2代抗精神病药的应用增加,人们越来越担心某些药物与代谢紊乱有关,如体重增加、糖尿病和血脂异常等[10]。这些代谢紊乱与心血管疾病之间具有密切的关联。
体重增加是长期的健康隐患,特别是当表现为腹内肥胖时,因为其与胰岛素抵抗以及随之而来的代谢反应(如甘油三酯升高,引发糖尿病和高血压)有关,增加了心血管疾病的发生风险[11-12]。同时,可影响精神分裂症患者的整体生活质量,对患者的自尊心造成影响[13]。因此,在规划治疗方案时,必须认真考虑精神分裂症患者体重增加的程度和影响。体重指数是国际常用的衡量人体胖瘦程度以及是否健康的标准。因此,本研究将体重指数作为衡量患者有无代谢紊乱的指标之一。阿立哌唑可激动多巴胺D1、D2、D3受体,同时拥有拮抗突触后多巴胺D2受体和激动突触前多巴胺D2受体的作用,可部分拮抗或激动5-HT1A受体,对5-HT2A呈完全拮抗作用,是一种新型的喹啉酮衍生物。有研究报道,患者使用阿立哌唑对体重、脂质、血糖等代谢指标无明显影响[14]。这可能与阿立哌唑有持续抑制多巴胺D2受体的作用有关[15]。本研究结果发现,治疗16周后,联合治疗组患者的空腹血糖、甘油三酯及体重指数等代谢相关指标水平明显低于氯氮平组,高密度脂蛋白水平明显高于氯氮平组,差异均有统计学意义(P<0.05),而与阿立哌唑组比较的差异均无统计学意义(P>0.05)。代谢失调最初表现为体重增加,可迅速导致肥胖,并发血脂异常和糖耐量降低,可能发展为2型糖尿病。其进一步的后果可能是心血管疾病,可能导致合并糖尿病的精神疾病患者的预期寿命缩短和因心血管疾病致死的发生风险增加[16-17]。因此,抗精神病药引起的代谢紊乱为临床关注的重点之一,多通过MS的存在来评估。本研究结果显示,联合治疗组、阿立哌唑组患者的MS发生率明显低于氯氮平组,表明联合治疗方案在控制代谢失调上明显优于奥氮平单药治疗,且与阿立哌唑单药治疗的效果相当。
PANSS评分是一种有效评估精神分裂症患者阴性、阳性以及一般症状严重程度的评分。本研究结果表明,治疗8周后联合治疗组患者的PANSS评分、阳性症状和阴性症状评分较单一药物治疗组明显降低,差异有统计学意义,提示相比单一药物治疗,氯氮平联合阿立哌唑治疗可以显著改善精神分裂症患者的阳性症状、阴性症状和一般症状。同时,三组患者TESS评分的差异无统计学意义,说明氯氮平联合阿立哌唑治疗与单一药物治疗相比,未增加药物的副作用,相对安全。这也与本研究的假设相符合,单独使用阿立哌唑或许可以控制MS发生率和不良反应发生率,但精神分裂症患者病情复杂,临床上使用单一药物治疗可能出现耐药性、不能达到预期效果等情况。
综上所述,氯氮平与阿立哌唑联合治疗精神分裂症的效果优于氯氮平、阿立哌唑单药治疗,患者的MS发生率低于氯氮平单药治疗。

