渗透性髓鞘溶解综合征MRI 表现
赵海峰,吕秀花,周永怀,焦飞涵,张天敏
(1.甘肃医学院附属医院磁共振室,甘肃平凉 744000;2.空军军医大学第一附属医院放射科,西安 710032)
0 引言
渗透性髓鞘溶解征(osmotic demyelination syndrome,ODS)是由于脑的渗透压波动引起的一类较少见的具有潜在致命风险的脱髓鞘疾病[1],包括脑桥中央髓鞘溶解症(central pontine myelinosis,CPM)、脑桥外髓鞘溶解症(extra pontine myelinolysis,EPM),两者可以单独发生,也可合并发生。MRI 是ODS 最为有效的影像学检查方法。尽管有文献报道[2]MRI 的异常表现与ODS 预后并不存在明确的相关性,但是早期发现病变并做出正确的诊断,仍有助于临床及时开展有效治疗、降低死亡率。本研究回顾性分析14 例ODS 患者的病历资料及其在MRI 各序列上的表现,旨在提高对ODS 的认识,以达到尽早诊断的目的。
1 资料与方法
1.1 一般资料
回顾性分析2014—2019 年经临床及影像确诊的14 例ODS 患者的病历资料,其中男9 例、女5 例,年龄 3~62 岁,中位年龄 46.5 岁。纳入标准:(1)伴有可导致低钠血症(血钠水平低于136 mmol/L)的基础疾病,或者有酗酒、厌食等不良生活习惯;(2)临床上有以下运动障碍,如下肢瘫、四肢瘫或帕金森综合征为主的精神神经系统症状[3]。排除标准:(1)有中毒病史者;(2)有缺血、缺氧病史者;(3)临床和(或)实验室检查结果支持肝豆状核变性或有相关疾病家族史者;(4)合并自身免疫性疾病者;(5)病毒性脑炎或其他可能导致腰穿脑脊液检查结果异常者。本研究经过医院医学研究伦理委员会审核并批准,且患者均签署知情同意书。
1.2 检查方法
采用PHILIPS Achieva 1.5T MR 扫描仪,使用8通道相控阵头颅线圈。14 例患者行MRI 平扫,其中8 例行 DWI 序列扫描。MRI 平扫序列及参数:(1)横轴位 FSET2WI 序列:重复时间(repetition time,TR)3 600 ms,回波时间(echo time,TE)100 ms;(2)SE T1WI 序列:TR 480 ms,TE 15 ms;(3)T2-FLAIR 序列:TR 6 000 ms,TE 120 ms,反转时间(invert time,TI)2 000 ms。以上序列相同参数:视野(field of view,FOV)23 cm×23 cm,矩阵 256×256,层厚 6.0 mm,层间距0.6 mm。DWI 序列参数:TR 2600 ms,TE 90 ms,b 值1 000 s/mm2,FOV 220 cm×100 cm,矩阵 112×128,层厚6.0 mm,层间距0.6 mm。
1.3 图像分析及评价
所有图像均由2 名长期从事中枢神经系统诊断的放射科医师独立分析并达成一致意见,有分歧时由高年资医师结合患者影像及临床资料重新判读核准。
1.4 观察指标
观察并记录各病例在MRI 平扫(T2WI、FLAIR、T1WI)时异常信号发生的部位并总结其信号特点,如是否对称分布以及是否具有特征性形态(三叉戟征、猪鼻征等);观察并记录各病例DWI 的信号特点。
2 结果
2.1 病灶特点
本组 14 例患者中CPM 5 例,CPM 合并EPM 9例,其中合并基底节区(尾状核和壳核)受累6 例,合并丘脑受累3 例。CPM 表现为脑桥类圆形、类三角形病灶,以脑桥中央为中心向外扩展,均未累及全脑桥;EPM 表现为尾状核和壳核(或丘脑)同时出现病灶,双侧对称分布。
2.2 MRI 表现
所有病灶均表现为T1WI 低信号、T2WI 高信号、FLAIR 高信号,边界清晰,病灶内信号均匀,不合并占位效应。CPM 中3 例病灶形态表现为“三叉戟征”,1 例表现为“猪鼻征”,如图 1 所示;EPM 中 6例呈双侧基底节区对称性、沿尾状核及壳核分布,3 例表现为双侧丘脑对称分布的点状病灶,如图2 所示,本组病例中EPM 均合并CPM。

图 1 CPM 的 MRI 图像
DWI 序列:8 例患者行 DWI 序列扫描,5 例弥散受限,表现为均匀稍高信号,如图3 所示;1 例表现为中央低、边缘高信号;2 例呈阴性。
3 讨论

图 2 EPM 的 MRI 图像
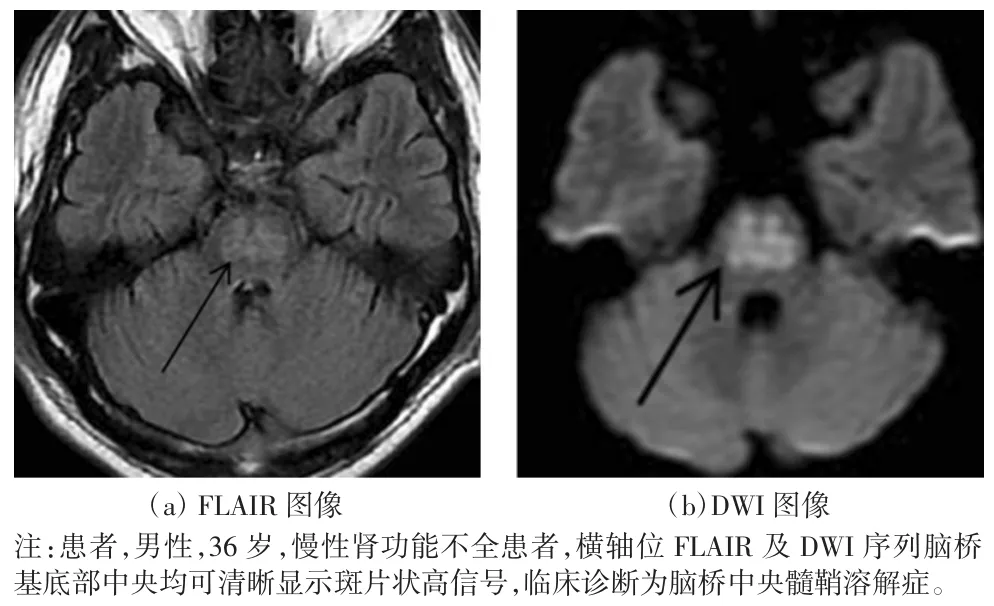
图 3 CPM 的 MRI(FLAIR、DWI)图像
ODS 于1959 年首次报道[4],被认为是一种与慢性酒精中毒和营养不良相关的非炎症性脑桥中央脱髓鞘病变(CPM),后逐渐将发病部位扩展至脑桥外的不同部位(EPM)。近年来相继有学者认为[2,5]该病与慢性低钠血症过度纠正有关:血钠水平改变过快导致脑组织内环境紊乱,胞外渗透压升高使细胞脱水,进而导致对渗透压变化最敏感的少突胶质细胞发生损伤,造成髓鞘破坏,因此最易受损的区域往往是富少突胶质细胞和髓鞘的灰质[6]。除此之外,其他能引起血浆渗透压改变如低磷血症、低钾血症、血糖的急剧变化等,或导致电解质紊乱的因素如肝、肾功能衰竭及激素分泌异常等,嗜酒酒精中毒者与厌食者等也可导致ODS 的发生[7],另外叶酸缺乏、血磷酸盐减少以及某些药物也可诱发ODS[8]。CPM 在临床上表现为四肢瘫以及不同程度的脑干功能障碍,如假性延髓麻痹、延髓麻痹,而闭锁综合征或缄默症少见;EPM 主要表现为运动障碍 [可仅表现为帕金森综合征和(或)肌张力障碍],少有合并脑干和(或)锥体束损害者,仅有小脑体征者罕见。若有迅速低血钠症纠正史,症状多于低钠血症纠正后2~10 d 内发生[3]。
虽然该病发生率较低,文献多为个案报道,但其具有潜在致命性。以往对于ODS 的诊断主要通过尸检,但随着MRI 检查的普及,很多临床上疑诊的患者,早期通过其MRI 表现[桥脑和(或)纹状体对称性损害]即可得以证实。
CPM 通常对称性累及脑桥基底部、桥小脑纤维,相对保留了腹外侧桥和皮质脊髓束,在MRI 上表现为脑桥基底部呈对称性分布的T1WI 低信号、T2WI 高信号;发病早期在横轴位上呈类圆形,随着病程发展,病变可逐渐演变为蝴蝶形或“三叉戟样”,冠状位上较具特征者可呈“蝙蝠翼状”;边界较清,仅累及脑桥中央区、边缘部分不受累,严重的前方及侧方可仅存线状正常脑组织,而后方能达到脑桥背盖腹侧,部分患者随着病程进展能观察到典型的“猪鼻征”[9-10]。EPM 分布的范围较广,主要分布在基底核团、外侧膝状体、脑白质、外周皮质、海马、小脑甚至颈髓[11-12],但常呈对称性分布。本组病例中CPM 均表现为脑桥类圆形、类三角形病灶,其中3 例病灶形态表现为“三叉戟征”,1 例表现为“猪鼻征”;EPM 表现为累及尾状核和壳核(或丘脑)的对称性T1WI 低信号、T2WI高信号,双侧基底节区受累6 例,沿尾状核及壳核分布,3 例为双侧丘脑对称分布的点状病灶;本组14例患者中以 CPM 合并 EPM 多见(9 例),与文献[13]相符。另有文献报道[14],应用FLAIR 序列能提高病灶的检出及定量诊断能力,这是由于FLAIR 序列抑制了液体信号,对于血管源性水肿具有信号增强、突出显示的作用[15]。观察本组病例FLAIR 序列,在抑制了液体信号后,水肿信号表现得更清晰、边界更明显,与上述文献描述一致。MRI 平扫对于诊断ODS 有局限性,临床发病后需要一定的时间窗才能发现典型的影像表现,有文献报道该时间窗为1~2 周[16],所以如果临床怀疑为ODS,一次影像学检查正常并不能排除该病,需要1~2 周后再复查。
本研究中8 例患者行DWI 序列扫描,6 例有异常信号改变,其中均匀稍高信号5 例,中央低、边缘高信号1 例。文献报道[17]ODS 在DWI 序列上的信号改变与病程变化有关。DWI 序列通过探测组织中水分子弥散运动的程度来反映受检组织的功能有无异常,对水分子横向弥散高度敏感,且随b 值越大敏感性越高,对于早期发现水分子弥散运动异常有着不可替代的作用[18]。而ODS 的病理改变是渗透压失衡导致的髓鞘脱失,疾病早期细胞外间质内自由水分子减少,细胞内结合水增多,所以相较于T2WI 和FLAIR序列,DWI 序列对于ODS 的早期诊断更重要、更敏感[19]。穆学涛等[20]根据ODS 患者在长期随访中DWI信号的变化,认为急性期ODS 存在细胞毒性水肿。Garg 等[9]发现,EPM 在 MRI 上出现异常早于 CPM,并且最初都表现为较小的不具特征性的弥散受限信号,随病程进展,病变逐渐扩大而出现典型特征,表现为病灶中央高信号周围出现信号相对较低的高信号,提示病变区的水肿逐渐由细胞内水肿演变为血管源性水肿,此后病灶在DWI 序列上的信号逐渐降低、在ADC 上逐渐升高,与本组8 例DWI 序列有阳性表现者相似。Juergenson 等[21]发现DWI 序列上的高信号一般只能持续3 周左右,本组中有2 例DWI序列为阴性表现,即与发病时间过长有关。
对于有可引起血浆渗透压改变或电解质紊乱基础疾病的患者,若近期出现以运动障碍为主的精神神经系统症状,结合影像上脑桥中央和(或)基底节区、丘脑对称性病变,尤其是DWI 序列和FLAIR 序列上出现典型表现,则要考虑ODS 的可能。ODS 需要与以下疾病相鉴别:(1)丘脑静脉性梗死:临床表现为头痛、意识障碍等,一般以双侧丘脑对称或不对称水肿为主,可累及丘脑邻近结构如基底节区和中脑,可合并出血[22]。(2)病毒性脑炎:起病急,进展迅速,有发热、头痛等感染症状,表现为单个或多个分布的水肿病灶,少数也可累及深部白质、丘脑、脑干及小脑[23]。(3)肝豆状核变性:慢性起病,多见于青少年,MRI 上可见双侧基底核团对称性T2WI 高信号,随病程进展可出现局限性或弥漫性脑萎缩[24],实验室检查血清游离铜升高,角膜缘有特异性角膜色素环。(4)急性播散性脑脊髓炎、多发性硬化:病灶分布范围广,可见于大脑、脑干、小脑和脊髓,常表现为双侧分布的多灶性、对称或非对称性的病灶,呈空间上的多变性,以皮质下白质较为多见。急性播散性脑脊髓炎多见于儿童和青少年,通常呈单相病程,而多发性硬化在病程中有复发—缓解—再复发的多相型表现,典型者可见垂直脱髓鞘表现[25-26]。
综上所述,MRI 是ODS 诊断和后续随访的首选成像方法,对于临床高度怀疑ODS 的患者,MRI 能更早、更准确地明确诊断,对于临床早期干预和治疗具有较大的指导价值。但由于该病相对罕见,没有绝对的金标准作为参考,且本研究选取的样本量较小,所选样本的疾病时间窗较难把握,MRI 特点总结仍然存在一定的局限性,有待于后续进一步扩大样本研究。

