3-甲基-2-丁烯醛液相加氢反应
邓寒霜,李筱玲
(商洛学院 生物医药与食品工程学院,陕西 商洛 726000)
3-甲基-2-丁烯醇又名异戊烯醇、3-甲基巴豆醇或3,3-二甲基丙烯醇,是农药、医药的重要中间体或原料,主要用于生产柠檬醛、维生素E的中间体异植物醇、二氯菊酯甲酯、合成维生素A、类胡萝卜素中间体、橡胶单体等[1]。3-甲基-2-丁烯醇的合成方法有异丁烯法、异戊二烯羧酸酯化法、3-甲基-2-丁烯醇异构化法和3-甲基-2-丁烯醛加氢法[2-5]。异丁烯法包含普林斯缩合和异构化两个步骤,异戊二烯羧酸酯化法包含酯化、双键加氢和水解步骤,两种方法均存在原料利用率低、污染严重的缺点。3-甲基-3-丁烯醇异构化法转化率较低,副产物较多。3-甲基-2-丁烯醛加氢法副产物少、收率高、污染低,属于绿色化学反应,有较好的原子经济性,逐渐成为研究热点。
Serp等[6-7]以RuH2(PPh3)4或RuCl3·3H2O为均相催化剂、异丙醇和水为溶剂,在35~50 ℃、2~3 MPa条件下进行反应,3-甲基-2-丁烯醇收率达90.6%以上,但因为是均相反应,催化剂回收困难且污染环境。Bakera等[8]以非贵金属Co为活性组分,研究了Co/Al2O3催化剂催化3-甲基-2-丁烯醛选择性加氢反应的性能,当3-甲基-2-丁烯醛转化率为39.7%时,不饱和醇选择性为61%、目标产物选择性较低。Xing[9]以Al2O3和SiO2载体负载的Pt为催化剂,该催化剂对不饱和醇有较高的选择性,但转化率较低。宋绍飞[10]以多壁碳纳米管(MCNT)为载体,将Pt纳米颗粒负载到MCNT上,考察了反应条件的影响,转化率接近100%时,3-甲基-2-丁烯醇选择性可达90%以上,反应装置为高压磁力搅拌反应釜,催化剂与反应产物分离回收复杂。已有的3-甲基-2-丁烯醛催化加氢催化剂的活性和选择性有待提高。3-甲基-2-丁烯醛是具有C=O和C=C共轭体系的α,β-不饱和醛,C=C和C=O键都能被加氢生成相应的产物,其中C=C键键能约为615 kJ/mol,而C=O键键能约为715 kJ/mol,从热力学上很容易发生C=C键的选择加氢[10]。Delbecq等[11]等指出,不饱和醇的选择性与原料在催化剂表面表现出的空间位阻效应息息相关,只有当催化剂活性金属粒子达到一定尺寸时,才能在不影响催化活性的情况下首先发生C=O键加氢,提高不饱和醇选择性。因此开发一种活性金属粒径适中、对不饱和醇有较高低温活性和选择性的催化剂很有现实意义。
本工作以NaOH溶液处理后的活性炭(AC)为载体,采用饱和浸渍法制备了Pt/AC催化剂,并对催化剂进行了N2吸附-脱附、FTIR、TPT-MS、TEM和H2-TPR表征,测定了催化剂的金属分散度;将Pt/AC催化剂用于3-甲基-2-丁烯醛加氢反应,考察了NaOH溶液处理对催化剂性能的影响。
1 实验部分
1.1 催化剂制备
载体预处理:为改善AC表面特性,将AC用质量分数为0,2%,5%,8%,10%的NaOH溶液在70 ℃下浸泡12 h,水洗,在120 ℃下烘干至恒重,所得载体记为AC-0,AC-2,AC-5,AC-8,AC-10。
催化剂制备:采用饱和浸渍法制备催化剂。称取一定量氯铂酸溶液,按质量比1∶1加入纯水和乙二醇溶液配成的混合浸渍液,用20%(w)Na2CO3溶液调节浸渍液的pH>9;将载体在搅拌下快速加入到浸渍液中,在90 ℃下搅拌回流8 h,冷却后抽滤、洗涤,在70 ℃下真空干燥10 h,再在200 ℃下用氢气还原2 h,制得Pt/AC催化剂。
1.2 催化剂表征
采用美国麦克公司ASAP2010型自动吸附仪进行N2吸附-脱附表征。试样预先在300 ℃、真空条件下预处理4 h,通过BJH模型和吸附曲线计算孔径分布和孔体积。
采用德国Bruker公司TENSOR 27型傅里叶变换红外光谱仪分析试样表面官能团的变化。将试样与KBr混合均匀后压片,检测器为DTGS,光谱采集范围为400~4 000 cm-1,分辨率为4 cm-1。
采用美国麦克公司AutoChem Ⅱ化学吸脱附仪进行程序升温脱附实验,采用美国安捷伦公司7800 型等离子发射光谱-质谱仪在线检测脱附气体。试样在高纯氦气下200 ℃预处理1 h,然后在氦气中以10 ℃/min升温速率升温至800 ℃,脱附气经MS在线检测。
采用美国FEI公司Tecnai G2 F20 u-TWIN型场发射透射电子显微镜观察金属在载体表面的分散状态。将试样研磨成粉,取少量试样加入到乙醇溶液中超声分散10 min,用滴管少量多次取上层清液,滴加在铜网上,试样烘干后进行测试。
采用美国麦克公司AutoChem Ⅱ化学吸附仪测定催化剂的金属分散度。试样在高纯氦气中120℃下预处理30 min,10%(φ)H2-90%(φ)Ar混合气中200 ℃下还原1 h,切换高纯氦气吹扫30 min,吹扫至基线稳定,通过六通阀进行CO脉冲吸附,吸附至脉冲峰面积保持不变,由CO的吸附量计算金属的分散度。
采用德国Chember公司PULSAR型化学吸附仪进行试样的程序升温还原实验,未经还原的催化剂在200 ℃抽真空预处理3 h,除去催化剂中的水分及表面吸附的易分解物种,进行H2-TPR表征。
1.3 催化加氢反应
3-甲基-2-丁烯醛(南京恒旺生物医药有限公司,含量大于等于95%(w))催化加氢反应在200 mL高压反应釜中进行。将0.1 g催化剂、3.0 mL的3-甲基-2-丁烯醛、20 mL的无水乙醇和3 mL的水依次加入高压反应釜中,用氮气置换数次,再用氢气置换数次并充压至1.2 MPa,以300 r/min转速启动搅拌,程序升温至60 ℃保持恒定,连续反应30 min。反应结束后,降温,排空泄压,取样。采用日本岛津公司GC-2014型气相色谱分析仪分析产物组成,色谱柱为RTX-1毛细管柱,FID检测,进样口温度260 ℃,柱温150 ℃,检测器温度280℃,进样分流比50∶1。
3-甲基-2-丁烯醛的加氢反应路径如图1所示。3-甲基-2-丁烯醛中的C=C和C=O键都可发生双键加氢反应,C=O键选择加氢生成目标产物3-甲基-2-丁烯醇、C=C键加氢生成3-甲基丁醛;3-甲基-2-丁烯醇和3-甲基丁醛进一步加氢生成3-甲基丁醇。
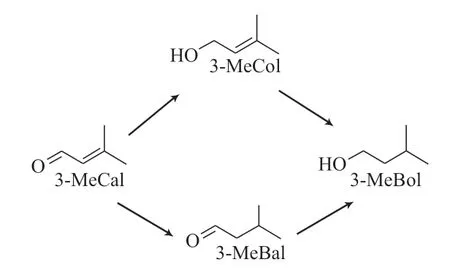
图1 3-甲基-2-丁烯醛的加氢反应路径Fig.1 The route of 3-MeCal hydrogenation.
2 结果与讨论
2.1 催化剂的表征结果
2.1.1 比表面积及孔结构
载体的N2吸附-脱附等温线见图2。

图2 AC载体的N2吸附-脱附等温线Fig.2 N2 adsorption-desorption isotherms of activated carbon(AC) support.
由图2可知,NaOH处理前后AC的N2吸附-脱附等温线有回滞环,存在介孔,且均为Ⅳ型等温线。相对压力小于0.1时,为单层微孔吸附;随着相对压力的升高,吸附量平缓增加,饱和后为多层介孔吸附;相对压力进一步升高,等温线快速上升,吸附质出现毛细管凝聚,内部孔结构存在较大孔隙。AC经NaOH处理后,回滞环在较宽的分压范围内接近水平平行,没有明显饱和吸附平台,为典型的H4型滞后环,说明载体具有微孔和介孔。
载体和催化剂的孔结构参数如表1所示。由表1可知,随着NaOH含量的增大,AC比表面积和孔体积降低,平均孔径略有增大。这主要是由于NaOH在液相高温条件下不断扩散进入AC孔道深处,甚至是微孔,由于NaOH的强腐蚀性,导致AC微孔烧蚀,微孔结构坍塌导致微孔数量减少,孔道扩大,AC的比表面积和孔体积下降、平均孔径呈增大趋势。负载Pt后,催化剂的比表面积及孔体积增加,推测Pt前体与载体的相互作用强,容易浸湿,利于Pt的扩散,Pt前体进入孔道产生了更小的微孔。

表1 载体和催化剂的孔结构参数Table 1 Pore structure parameters of supports and catalysts
2.1.2 FTIR表征结果
AC载体的FTIR谱图如图3所示。由图3可知,AC载体经NaOH处理后,表面官能团种类基本不发生改变,但官能团含量发生变化。其中,1 560,1 430,1 382 cm-1附近的吸收峰为羧酸盐离子C—C键对称振动或羧酸酯不对称振动特征吸收峰,1 170 cm-1和1 033 cm-1处的吸收峰为酯基C=O和C—O键伸缩振动吸收峰。NaOH处理后载体在1 170 cm-1和1 033 cm-1处的吸收峰强度变弱,而在1 560,1 430,1 382 cm-1处的吸收峰强度增强,表明羧酸含氧基团数量增加,有利于活性金属的分散与吸附。

图3 AC载体的FTIR谱图Fig.3 FTIR spectra of AC supports.
2.1.3 TPD-MS表征结果
AC载体的TPD-MS表征结果如表2所示。由表2可知,AC经NaOH处理后,羧基酸性基团数量显著增加,内酯峰有所降低,整体看催化剂表面含氧官能团数量增加。但随着NaOH含量的增加,酸性基团数量下降,推测NaOH含量较高时,在强腐蚀作用下,AC表面部分含氧官能团烧蚀脱落,官能团数量减少。AC表面酸性基团是活性金属纳米颗粒的吸附位点[12-13],能够增加表面金属纳米颗粒的分散度。
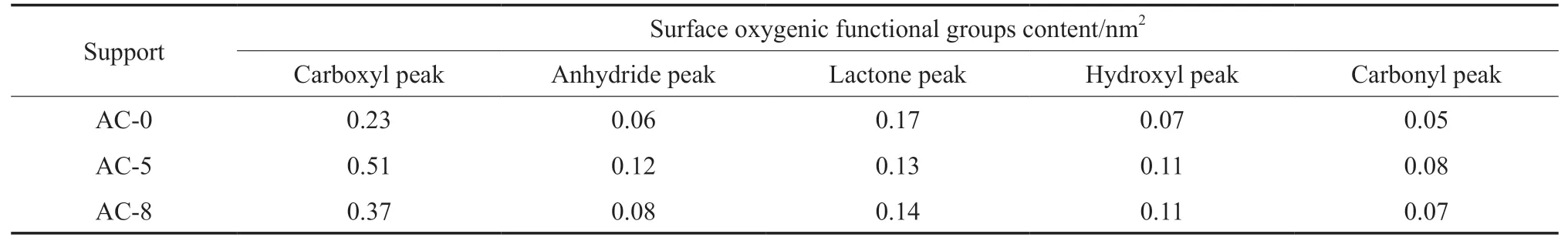
表2 AC载体的TPD-MS表征结果Table 2 TPD-MS characterization results of different AC supports
2.1.4 TEM表征结果
催化剂的TEM图片如图4所示。由图4可知,经NaOH处理的AC负载的Pt催化剂中Pt纳米粒子分散均匀,粒径较小,且随着NaOH含量的增加Pt纳米粒子尺寸先减小后增大。其中,Pt/AC-5催化剂的Pt纳米粒子高度分散在AC表面,粒子尺寸较小,粒径约为1.40~2.50 nm;NaOH含量增至8%(w)时,Pt纳米粒子增大,粒径约为2~5 nm。

图4 催化剂的TEM图片Fig.4 TEM images of different catalysts.
2.1.5 金属分散度
催化剂的金属分散度如表3所示。由表3可知,Pt/AC-0的金属分散度为17.34%,而Pt/AC-5,Pt/AC-8,Pt/AC-10的金属分散度均大于20%,结合表1和表2结果可知,活性金属分散度与载体丰富的孔结构及表面含氧官能团数量有关,高比表面积及丰富的孔结构有利于活性金属的分散,载体表面官能团数量越多,越有利于Pt前体的浸润扩散,可提高金属的分散度。Pt/AC-5,Pt/AC-8,Pt/AC-10催化剂的金属分散度分别为47.68%,23.38%,20.52%,有效粒子直径分别为2.31,4.61,5.14 nm,表明AC载体经一定含量NaOH处理后能显著提高活性金属的分散度,降低金属粒径;随NaOH含量的增加,Pt分散度反而降低,金属粒径变大,这一结果与TEM表征结果一致。
2.1.6 H2-TPR表征结果
催化剂的H2-TPR曲线如图5所示。由图5可知,所有催化剂在85 ℃附近出现一个微弱的小峰,归属于催化剂表面少部分Pt(Ⅳ)物种被还原为Pt(Ⅱ)。随着还原温度的升高,在100~250 ℃范围内均出现一个较为宽泛的还原峰,归属于催化剂表面及孔道内部Pt(Ⅳ)物种的还原,包括Pt(Ⅳ)直接还原为Pt(0)、Pt(Ⅳ)还原为Pt(Ⅱ)和Pt(Ⅱ)还原为Pt(0)。对比几种催化剂,Pt/AC-5,Pt/AC-2,Pt/AC-8,Pt/AC-0催化剂还原峰的顶点温度分别为156,162,167,182 ℃,其中,Pt/AC-5催化剂还原温度最低,还原峰面积最大,Pt/AC-0还原峰温度最高。结合TEM及金属分散度表征结果可知,Pt/AC-5催化剂活性金属分散性好,Pt纳米粒子粒径小,相对较易被还原。

表3 催化剂的金属分散度Table 3 Metal dispersion of different catalysts
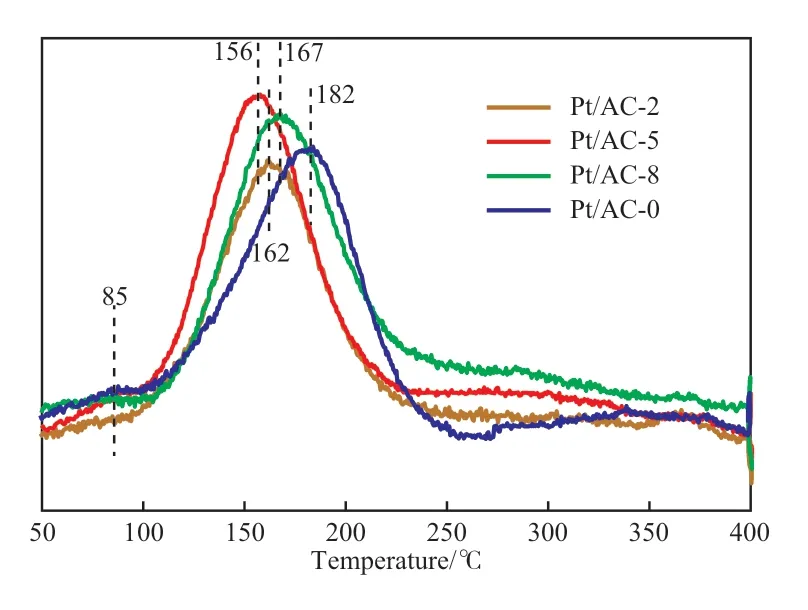
图5 催化剂的H2-TPR曲线Fig.5 H2-TPR curves of different catalysts.
2.2 3-甲基-2-丁烯醛催化加氢反应
在反应温度60 ℃、反应压力1.2 MPa、反应时间30 min条件下,对催化剂性能进行评价,实验结果如表4所示。由表4可知,在相同的反应条件下,Pt/C催化剂的活性随NaOH含量的增加先增大后降低,3-甲基-2-丁烯醛的转化率先增加后减小,而3-甲基-2-丁烯醇的选择性大小顺序为Pt/AC-10>Pt/AC-0>Pt/AC-8>Pt/AC-2>Pt/AC-5。由此可知,NaOH处理能够增加AC表面的含氧官能团数量,有利于提高反应活性,影响了3-甲基-2-丁烯醇的选择性。结合上述表征结果,Pt/AC-5催化剂金属粒子分散性好,Pt纳米粒子尺寸小于3 nm,3-甲基-2-丁烯醛转化率为100%,但3-甲基-2-丁烯醇选择性较低,只有87.54%;对于Pt/AC-0和Pt/AC-10催化剂,金属分散度小,Pt纳米粒子尺寸较大,反应活性低,但3-甲基-2-丁烯醇选择性稍高;Pt/AC-8催化剂的Pt纳米粒子尺寸为2~5 nm,转化率较高(99.54%),3-甲基-2-丁烯醇选择性大于96%。说明催化剂反应性能与催化剂表面活性金属Pt纳米颗粒的分散情况紧密相关[14-15],当Pt粒子较小,3-甲基-2-丁烯醛分子以平面形式接触催化剂活性中心,C=C和C=O键均可加氢,不饱和醇选择性降低。当Pt纳米粒子尺寸达到3~5 nm,催化剂活性较高,且由于原料中甲基的空间位阻效应,使C=O键优先于C=C键加氢,不饱和醇选择性增大。

表4 催化剂的催化性能Table 4 Catalytic performance of different catalysts
3 结论
1)AC载体具有大量中孔,经NaOH处理后,AC载体比表面积和孔体积降低,平均孔径略有增加,表面官能团种类未发生变化,但羧酸含氧基团数量增加。
2)与未处理载体制备的催化剂相比,NaOH处理的载体制备的催化剂的金属分散度增大,表面活性位增加,还原温度降低。随着NaOH含量的增加,Pt/AC催化剂表面金属分散度先增大后减小,Pt纳米粒子尺寸先减小后增大。Pt/AC-5和Pt/AC-8催化剂金属分散度分别为47.68%和23.38%,有效粒子直径分别为2.31 nm和4.61 nm。
3)催化剂的反应性能与催化剂表面Pt纳米颗粒分散性相关。当Pt纳米粒子较小,3-甲基-2-丁烯醛分子以平面形式接触催化剂活性中心,C=C和C=O键均可加氢,不饱和醇选择性低。当Pt纳米粒子尺寸达到3~5 nm,催化剂活性较高,且由于原料中甲基的空间位阻效应,使C=O键优先于C=C键加氢,不饱和醇选择性增加。Pt/AC-8催化剂Pt纳米粒子尺寸介于2~5 nm,3-甲基-2-丁烯醛转化率达99.54%,3-甲基-2-丁烯醇选择性为96.06%。

