新型酰胺类缓蚀剂的合成及缓蚀性能的研究
王恩东
(重庆工贸职业技术学院教务处,重庆 408000)
金属材料具有良好的物理性能、力学性能、化学性能和可加工性能等优点,广泛应用于交通、医疗、化工过程、建筑施工和基础设施建设等领域[1-4]。但在金属材质与环境腐蚀性介质间存在着强烈的物理化学作用,对金属材质造成严重的破坏,严重危害人们的生产、生活[5]。
在金属防护众多的方法中,缓蚀剂其施工简单、用量少、缓释性能优良等特点,被广泛应用于金属腐蚀与防护领域[6]。噻二唑缓蚀剂是一类性能优良的表面活性剂,其分子中含有稳定的五元环,能够和金属络合牢牢的吸附在金属表面,在金属表面形成一层保护膜,从而使金属免遭腐蚀,是现代学者研究的重点[7-8]。笔者选择以噻二唑为原料,通过化学反应在噻二唑杂环上引入极性官能团,增加其结合力,在分子中引入憎水基团增加疏水层的厚度来阻隔腐蚀介质与金属的接触来提高缓蚀的目的。
1 实验部分
1.1 试剂及材料
5-甲基-2-巯基-1,3,4-噻二唑,AR,湖北远成赛创生化科技有限公司;乙二醇胺,AR,上海辰建化工有限公司;丙烯酸,AR,天津市风船化学试剂科技有限公司;不锈钢,304,天津汇鑫通远金属材料有限公司。
Bruker AVANCE-400 MHz核磁共振波谱仪,Bruker公司,瑞士;上海辰华仪器有限公司生产的CHI600D电化学测试系统,电化学阻抗谱测试频率范围为0.01~100 Hz,正弦交流波信号的振幅为8 mV。扫描电镜测试条件:电子分辨率1.2 nm(5.0 kV)。电解池为三电极系统,试件为工作电极,金属铂片为辅助电极,参比电极为饱和甘汞电极(SCE)。极化曲线测试范围为-0.5~0.9 V,扫描速率为1 mV/s。从负向至正向扫描。
1.2 缓蚀剂的合成
所合成3种缓蚀剂的分子设计不同。C1的分子结构上R为原子氢,为空间位阻;C2的分子结构有供电子基团,能增强分子之间的结合力;C3的分子结构上有苯环,此基团参与成膜,能增加其结合力。

图1 合成路线
1.2.1 中间体的合成
在三口瓶中加入5-甲基-2-巯基噻二唑3.52 g,10 mL苯,在剧烈搅拌下滴加1.81 mL丙烯酸,1 h滴完。滴加完毕后搅拌过夜,有大量黄色固体沉出。过滤,用冷的乙醇洗涤(10 mL×3),乙醇重结晶,得到浅黄色片状晶体4.72 g。B1产率:78%。1H NMR(DMSO-d6, 500 MHz, 298 K):δ=2.35(s, 3H, CH3), 2.71~2.73, (m,J=8.9Hz, 2H, CH2), 11.27(1H, OH). B2产率:71%。1H NMR(DMSO-d6, 500 MHz, 298 K):δ=1.05(s, 3H, CH3), 2.71~2.73,(m,J=8.9Hz, 2H, CH2), 2.39(s, 3H, CH3), 3.40~3.42,(m,J=8.1 Hz, 1H, CH), 11.05 (1H, OH)。B3产率:64%。1H NMR(DMSO-d6, 500 MHz, 298 K):δ=2.35(s, 3H, CH3), 4.79~8.80(m,J=8.4 Hz, 1H, CH), 7.07~7.09(m,J=8.9 Hz, 3H), 7.23=7.25(m,J=4.6 Hz, 2H),11.87(1H, OH)。
1.2.2 产物的合成
在装有电动搅拌器、回流冷凝管、 温度计的50 mL反应器中加入0.01 mol的上述产物,再加入50 mL的二甲苯,充分溶解并加热,开动搅拌器,缓慢加入稍过量的二乙醇胺,控制温度在 115~120 ℃,反应3 h。将反应混合物降温,蒸馏除去二甲苯,得到无色黏稠状的液体。C1产率:87%。1H NMR(DMSO-d6, 500 MHz, 298 K):δ=2.35(s, 3H, CH3), 3.39~3.41(m,J=7.2 Hz, 2×2H, CH2), 3.79~3.82(m,J=4.5Hz, 2×2H, CH2),3.82(1H, OH),10.5(1H, OH). C2产率:90%。1H NMR(DMSO-d6, 500 MHz, 298 K):δ=0.96(s, 3H, CH3), 2.71~2.73(m,J=8.9 Hz, 2H, CH2), 2.35(s, 3H, CH3), 3.39-3.41(m,J=7.2 Hz, 2×2H, CH2), 3.79~3.82(m,J=4.5 Hz, 2×2H, CH2),3.82(1H, OH)。C3产率:83%。1H NMR(DMSO-d6, 500 MHz, 298 K):δ=2.35(s, 3H, CH3), 3.37-3.39(m,J=3.4 Hz, CH2), 4.79~8.80, (m,J=8.4 Hz, 1H, CH), 7.07~7.09(m,J=8.9 Hz, 3H), 7.23=7.25(m,J=4.6 Hz, 2H), 11.87(1H, OH)。
1.3不锈钢/缓蚀剂膜的制备
将不锈钢(304不锈钢,不锈钢)切割成10 mm×10 mm×1 mm的方片,去离子水冲洗,然后分别在无水乙醇和去离子水中超声振荡清洗12 min,以除去表面有机杂质。用高纯氮气吹干。然后浸入含不同浓度的缓蚀剂中,在90 ℃下恒温30 min。取出不锈钢片,用无水乙醇反复清洗,置于烘箱内90 ℃保温30 min。
2 结果与讨论
2.1 失重法测缓蚀效率
2.1.1 缓蚀剂浓度对钢片缓蚀效率的影响
用腐蚀失重法测定了在30 ℃下, 1 mol/L 硫酸腐蚀介质中(pH=0),所合成的3种缓蚀剂在不同浓度下对不锈钢的缓蚀效率,所得到结果如图2所示。由图2可以看出,所合成的3种缓蚀剂在酸性介质中对不锈钢的缓蚀效率都随浓度的增加而增加,当用量达到50 mg/L时,其缓蚀效果达到最佳,其中C3的缓蚀效果最大,达到98%,优于C2、C1,当继续增加缓蚀剂的用量,缓蚀效果没有发生很大变化。这大概的原因可能是:缓蚀剂在金属表面的吸附是由杂原子提供孤对电子与金属表面的金属离子形成配位键。烷基是斥电子基, 碳链的增长可提高斥电效应, 而共轭苯环可提供电子使杂原子上的电子云密度增大,形成的配位键更加稳定,有利于提高缓蚀效率。
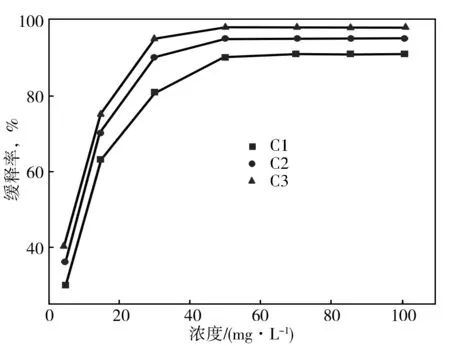
图2 不同浓度的缓蚀剂对不锈钢的缓蚀效率的影响
2.1.2 pH值对其缓蚀效率的影响
图3为不同pH值条件下3种缓蚀剂对不锈钢的缓蚀效果。由图3可以看出,当pH=0时,缓蚀效果最低,随pH值的增加,缓蚀效果逐渐增大,并且其中C3 的缓蚀效果最大,优于C2、C1。这主要由于不管是抑制阳极铜的溶解或者是抑制阴极O2的还原这两个过程都和缓蚀剂在不锈钢表面形成的聚合膜的致密程度有关。缓蚀剂分子在金属表面的吸附是由杂原子提供孤对电子与金属表面的金属离子形成配位键。烷基是斥电子基,碳链的增长可提高斥电效应,而共轭苯环可提供电子使杂原子上的电子云密度增大,形成的配位键更加稳定,所形成的聚合膜比较致密,所以提高了缓蚀效果。

图3 不同pH值对缓蚀效率的影响
2.2 电化学测试其缓释性能
2.2.1 极化曲线
测试了不锈钢和不锈钢/缓蚀剂的体系在25 ℃于1.0 mol/L硫酸溶液中的极化曲线,见图4。
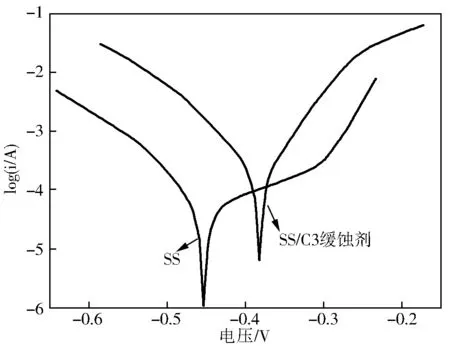
图4 不锈钢在含有缓蚀剂的1.0 mol/L硫酸中的极化曲线
由图4可以看出,没有加入所合成的缓蚀剂C3保护的不锈钢其腐蚀电位Ecorr值最低,腐蚀电流最大,表明此时不锈钢表面非常容易受到腐蚀介质的侵袭,使得不锈钢失去电子变成金属离子,从而发生腐蚀。而加入缓蚀剂C3以后,在不锈钢表面生成一层缓蚀剂保护膜,阻止不锈钢表面与硫酸等腐蚀性介质的接触,其不锈钢自腐蚀电位Ecorr值变正,并且腐蚀电流明显降低,从而保护了不锈钢免受腐蚀。其中随着缓蚀剂用量的增加,其缓释效果增强。这一结果与失重法测得的结果相一致。对图4的极化曲线数据根据极化公式进行拟合分析,得到表1所示的电化学参数。由表1可以看出,不锈钢在1.0 mol/L硫酸溶液中的腐蚀电位Ecorr值最低,大约为-0.490 V,自腐蚀电流最大,大约为3.26×103μA/cm2,向体系中加入缓蚀剂后,使不锈钢自腐蚀电位Ecorr值变正,腐蚀电流明显降低。当缓蚀剂的浓度为50×10-6mol/L时,其自腐蚀电位最高,其腐蚀电流密度最小,为1.5 μA/cm2。并且表明对不锈钢保护作用最好。

表1 不锈钢在含有不同浓度缓蚀剂的1.0 mol/L硫酸溶液中腐蚀的电化学参数
2.2.2 SEM
为了研究不锈钢表面物理形貌的变化以及成膜过程对不锈钢片表面的抗蚀性能的影响,采用SEM对标准不锈钢片、不加所合成缓蚀剂的情况和加有50×10-6mol/L C3缓蚀剂的1.0 mol/L硫酸介质中对不锈钢片进行了微观形貌分析,见图5。

图5 不锈钢表面SEM
由图5可知,未加50×10-6mol/L C3缓蚀剂的空白试样和标准的不锈钢片,不锈钢在硫酸介质中腐蚀较严重。而加有50×10-6mol/L C3缓蚀剂缓蚀剂的不锈钢片和标准不锈钢片相比较,可以看出加有50×10-6mol/L C3缓蚀剂的不锈钢片上形成了一层吸附保护膜,保护不锈钢免受腐蚀的原因。
2.2.3 EIS
为研究缓蚀剂分子对不锈钢在1 mol/L硫酸溶液中的保护作用,测量了不锈钢和不锈钢/缓蚀剂的电化学阻抗谱,如图6所示。由图6可以看出,所绘制的几种曲线的形状大体相似,未加缓蚀剂的试片其容抗弧半径最小,加入缓蚀剂以后,其容抗弧半径明显增加,加有C3缓蚀剂的不锈钢片其容抗弧半径最大,表明电化学电荷转移电阻最大,其对不锈钢保护作用最明显。这与失重法测得的结果相一致。

图6 双子表面活性剂的电化学阻抗谱
3 结 论
以5-甲基-2-巯基-1,3,4-噻二唑为原料,合成了3种新型酰胺类缓蚀剂。所合成的3种缓蚀剂在酸性介质中对不锈钢的缓蚀效率都随浓度的增加而增加。当用量达到50 mg/L时,其缓蚀效果达到最佳,其中C3的缓蚀效果最大,达到98%;当继续增加缓蚀剂的用量,缓蚀效果没有发生很大变化。加入缓蚀剂C3以后,极化曲线测试表明在不锈钢表面生成一层缓蚀剂保护膜,阻止不锈钢表面与硫酸等腐蚀性介质的接触,其不锈钢自腐蚀电位Ecorr值变正,并且腐蚀电流明显降低,从而保护了不锈钢免受腐蚀。当缓蚀剂的浓度为50×10-6mol/L时,其自腐蚀电位最高,其腐蚀电流密度最小,为1.5 μA/cm2。EIS结果表明所绘制的几种曲线的形状大体相似,未加缓蚀剂的试片其容抗弧半径最小,加入缓蚀剂以后,其容抗弧半径明显增加,加有C3缓蚀剂的不锈钢片其容抗弧半径最大,表明电化学电荷转移电阻最大,其对不锈钢保护作用最明显。

