恩替卡韦联合阿德福韦酯治疗乙型病毒性肝炎肝硬化的疗效与安全性评价
河南省驻马店市中心医院(463000)崔慧敏
乙型病毒性肝炎(乙肝)是由乙型肝炎病毒(HBV)引起的、以肝脏损害为主的慢性传染性疾病,是引起肝硬化的常见病因,因其高患病率、高死亡率的特点,被认为是威胁人类健康的世界性疾病之一[1]。我国是乙肝病毒感染的流行区,每年约有2%~6%的慢性乙肝患者进展为肝硬化[2]。有效的抗病毒治疗可延缓病情进展,改善临床结局。恩替卡韦(ETV)是环戊酰鸟苷类似物,耐药屏障高、副作用小、安全有效,是临床治疗慢性乙肝的首选药物[3]。阿德福韦酯(ADV)为腺嘌呤核苷类似物,可通过抑制DNA聚合酶的形成有效抑制病毒复制[4]。本研究ETV联合ADV治疗乙肝肝硬化的疗效及安全性,旨在为临床提供参考。现报告如下。
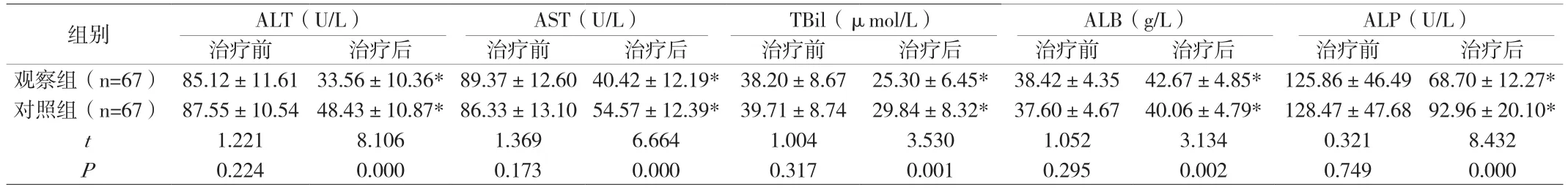
附表1 两组患者治疗前后肝功能指标比较(±s)
附表1 两组患者治疗前后肝功能指标比较(±s)
注:与同组治疗前相比,*P<0.05。
组别 ALT(U/L) AST(U/L) TBil(μmol/L) ALB(g/L) ALP(U/L)治疗前 治疗后 治疗前 治疗后 治疗前 治疗后 治疗前 治疗后 治疗前 治疗后观察组(n=67) 85.12±11.61 33.56±10.36*89.37±12.60 40.42±12.19* 38.20±8.67 25.30±6.45* 38.42±4.35 42.67±4.85* 125.86±46.49 68.70±12.27*对照组(n=67) 87.55±10.54 48.43±10.87*86.33±13.10 54.57±12.39* 39.71±8.74 29.84±8.32* 37.60±4.67 40.06±4.79* 128.47±47.68 92.96±20.10*t 1.221 8.106 1.369 6.664 1.004 3.530 1.052 3.134 0.321 8.432 P 0.224 0.000 0.173 0.000 0.317 0.001 0.295 0.002 0.749 0.000

附表2 两组患者治疗后不同时间段内的HBeAg及HBV-DNA转阴率比较[n(%)]
1 资料与方法
1.1 一般资料 选择我院2018年1月~2019年1月收治的134例乙肝肝硬化患者作为研究对象。纳入标准:①经实验室及影像学检查,符合《慢性乙型肝炎防治指南》[5]中乙肝肝硬化的标准;②年龄≥18岁,乙肝病毒表面抗原(HBsAg)阳性>6个月;③获得患者知情同意,经医院伦理委员会批准。排除标准:①曾使用过核苷(酸)类似药物;②合并其他病毒性肝炎;③严重精神疾病或认知障碍。按照随机数字表法将患者分为观察组67例和对照组67例。其中观察组:男50例,女17例,年龄18~68岁,平均(50.26±5.35)岁,病程6~48个月,平均(37.33±12.25)月,Child-Pugh肝功能分级:A级32例,B级24例,C级11例;对照组:男48例,女19例,年龄20~70岁,平均(48.65±5.68)岁,病程6~52个月,平均(38.60±12.50)月,Child-Pugh肝功能分级:A级30例,B级25例,C级12例。两组患者性别、年龄、病程、肝功能分级等一般资料比较,差异均无统计学意义,具有可比性(P>0.05)。
1.2 方法 两组患者给予相同的还原性谷胱甘肽、白蛋白、甘草酸苷类药物,预防和控制感染,防治电解质紊乱,加强对症支持治疗。对照组在此基础上使用ETV(博路定)治疗,0.5mg/次/d,口服。观察组在对照组的基础上使用ADV(明正)治疗,10mg/次/d,口服。
1.3 观察指标 ①肝功能指标:分别于治疗前后,取患者空腹静脉血,离心分离血清,使用日立7600全自动生化分析仪测定患者谷丙转氨酶(ALT)、谷草转氨酶(AST)、胆红素(TBil)、白蛋白(ALB)、碱性磷酸酶(ALP)水平。②血清HBV标志物及HBV-DNA定量变化:比较两组患者治疗后8周、16周、32周、48周时的HBeAg及HBV-DNA转阴率。血清HBV标志物采用酶联免疫分析法(ELISA)测定HBsAg浓度,严格按照试剂盒(由上海阿尔法生物技术有限公司提供)说明书进行操作,用酶标仪双波长读取吸光度(A)值,按说明书计算乙肝表面抗原正常值(S/CO),S/CO≥1为阳性;血清HBV-DNA浓度使用PCR酶联免疫吸附法(PCR-ELISA),严格按照试剂盒(由上海浩源生物科技有限公司提供)说明书进行操作,以HBV-DNA<1000cps/ml为阴性。③安全性评价:比较两组患者治疗过程中不良反应的发生情况。
1.4 统计学处理 用SPSS20.0软件进行数据分析。计数资料以[n(%)]表示,行χ2或连续性校正χ2检验;计量资料以均数 ± 标准差(±s)表示,行t检验。检验水准α=0.05。
2 结果
2.1 肝功能指标 治疗前,两组各项肝功能指标比较无明显差异(P>0.05);治疗后,两组血清ALT、AST、TBil及ALP水平明显降低,ALB水平明显升高,且观察组各指标升高或降低的幅度显著高于对照组(P<0.05)。见附表1。
2.2 血清HBV标志物及HBV-DNA定量变化 观察组治疗第8周、16周、32周的HBeAg转阴率、HBV-DNA转阴率与对照组相比,差异均无统计学意义(P>0.05);观察组治疗第48周的HBeAg转阴率及HBV-DNA转阴率均显著高于对照组(P<0.05)。见附表2。
2.3 安全性评价 观察组不良反应的发生率为10.45%(7/67),与对照组的4.48%(3/67)相比,差异无统计学意义(P>0.05)。
3 讨论
乙肝是由HBV持续感染引起的慢性肝脏疾病,以乏力、腹胀、肝区疼痛为主要临床表现,是导致肝硬化和肝癌的主要原因之一[6][7]。据不完全统计,我国每年因乙肝相关死亡约30万例,占传染病死亡的第一位[8]。因此,及时治疗、控制病情的进一步发展对改善乙肝肝硬化患者预后恢复及其生活质量均有重要意义。
抗病毒治疗是乙肝治疗的关键[9]。ETV和ADV是国内外公认有效的抗病毒药物。本研究结果显示,治疗后两组患者血清ALB、AST、TBil、ALP水平明显升高,ALT水平明显降低,且观察组各指标升高或降低的幅度显著高于对照组。由此表明ETV联合ADV较单一ETV治疗对乙肝肝硬化患者肝功能的改善效果更好,与谢靖婧等研究结果一致[10]。分析其原因是:ETV联合ADV可加速HBV病毒的清除和复制,减轻肝细胞炎症坏死及肝纤维化,降低肝脏损伤,从而促进肝功能的恢复。乙肝患者在病毒感染的不同时期随机体免疫功能的变化,血清中HBV抗原抗体也发生相应的变化[11]。本研究结果显示,两组患者治疗后第8周、16周、32周的HBeAg转阴率、HBV-DNA转阴率比较,差异无统计学意义,但观察组治疗后第48周的HBeAg转阴率、HBV-DNA转阴率均显著高于对照组。因此ETV联合ADV长期治疗可明显抑制乙肝病毒的复制,提升HBeAg及HBVDNA的转阴率。分析其原因是:ETV可通过降低HBV多聚酶活性抑制病毒复制,降低血液HBV水平[12];ADV则通过阻断T细胞中表达程序性死亡受体1(PD-1)的表达,减少T细胞数量和降低其功能,增强机体免疫应答,起到抗HBV复制的作用;但两种药物联合的短期抗病毒效果并不明显,长期治疗的效果更佳。此外,本研究结果发现,观察组不良反应的发生率为10.45%,与对照组的4.48%比较,差异无统计学意义。因此采用ETV联合ADV治疗乙肝肝硬化并不会增加患者不良反应的发生率,安全性较高。
综上所述,ETV联合ADV治疗乙肝肝硬化的疗效显著,可有效抑制HBV病毒的复制,减轻肝细胞损伤,改善患者肝功能,长期治疗可提升HBeAg及HBV-DNA转阴率,且不良反应少、安全性高,值得临床推广应用。

