利用心电散点图及其逆向技术快速识别起搏器不恰当开启MVP 功能1 例
顾红梅 曹洪浩 曾雁云 郑丽凤 王锐
患者男,89 岁,因“心率缓慢伴头晕、胸闷、黑矇”于2020 年2 月3 日入院,既往有冠状动脉粥样硬化性心脏病。 查体:神清,脉搏55 次/min,血压129/70 mmHg,双肺呼吸音清、未闻及明显干湿性啰音。 心率55 次/min,律齐,各瓣膜区未闻及病理性杂音。 入院心电图(图1)示:窦性心动过缓,心率52 次/min,一度房室传导阻滞。 动态心电图(图2)示:①窦性心律,24 h 总心搏74 815 次,平均53 次/min;②一度房室传导阻滞,一过性二度Ⅰ、Ⅱ型房室传导阻滞;③频发房性早搏,部分未下传;④>2.00 s 的长RR 间期2 907 次/24 h,最长3.01 s,为二度Ⅰ型房室传导阻滞,长间歇多数为房早未下传,个别为二度Ⅰ或Ⅱ型房室传导阻滞,长间歇多发生于夜间(24 h 时间散点图见图3,Lorenz 散点图见图4)。心脏彩超示:左房轻度增大,主动脉瓣及二、三尖瓣少量反流,左室射血分数39%。
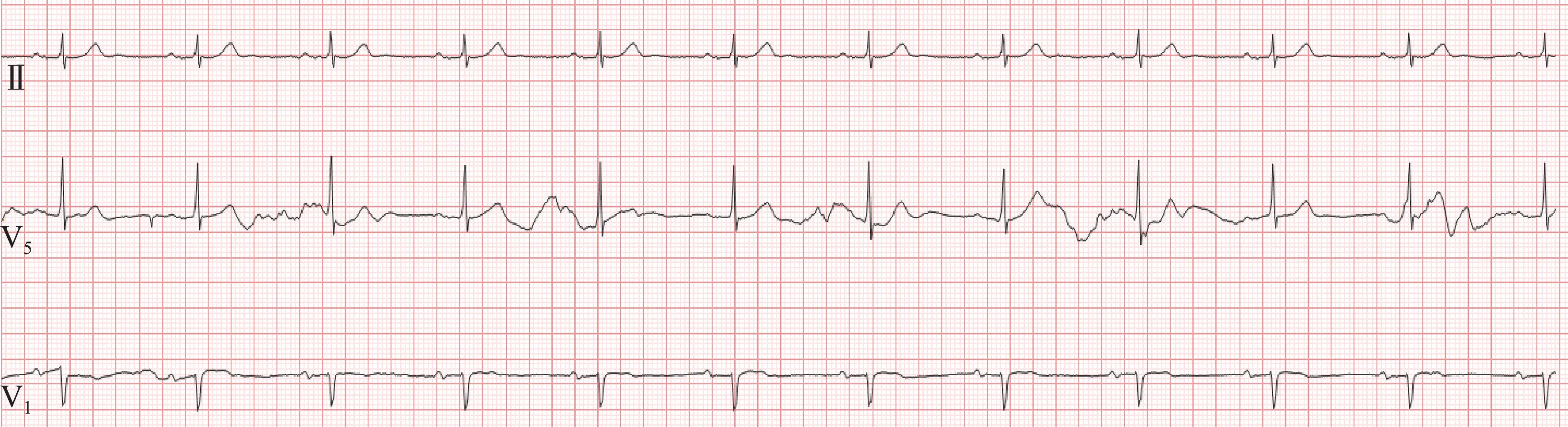
图1 12 导联心电图
入院诊断:①病态窦房结综合征? ②冠状动脉粥样硬化性心脏病;③心功能Ⅱ级。 动态心电图基础心律为窦性心动过缓,夜间出现频发房早未下传及二度Ⅰ、Ⅱ型房室传导阻滞所致长RR 间期。 除病理性因素外,不排除迷走神经兴奋性增高引起,但考虑到患者高龄,有头晕、黑矇等临床症状,药物治疗存在风险,且患者及家属对治疗期望值较高,故行双腔起搏器植入术。
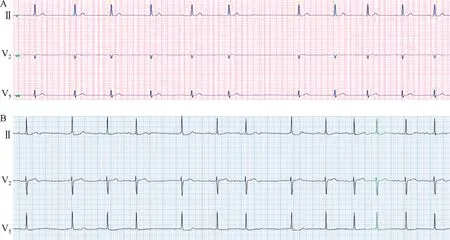
图2 术前24 h 动态心电图片段
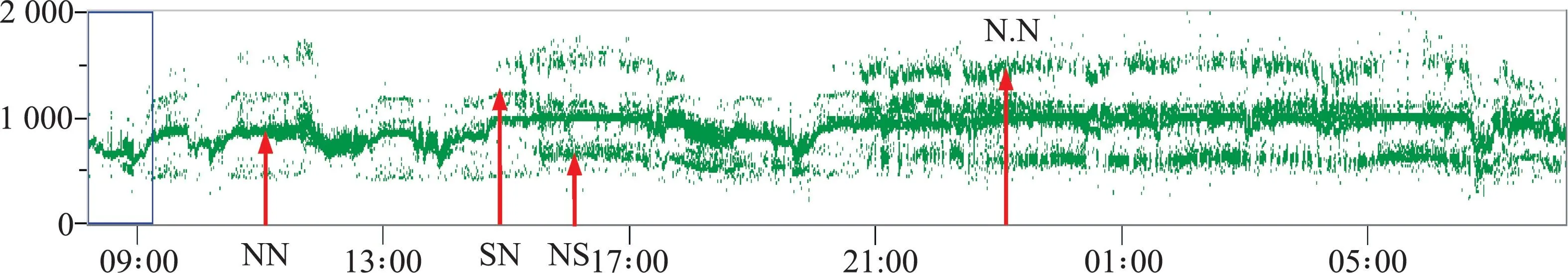
图3 24 h 时间散点图
植入起搏器型号为美敦力Adapta L ADDRL1,设置起搏模式AAIR⇔DDDR,低限频率60 次/min,上限跟踪频率130 次/min。 图4 是术前24 h Lorenz 散点图,以窦性心律为主,窦性心律点集基本在正常位置(0.6 ~1.5 s,40 ~100 次/min),频发房性早搏,在加速区与减速区的中部有短长、长短RR 间期交替时形成的阻滞前点和阻滞后点非稳态吸引子,逆向心电图片断为房早未下传或二度Ⅰ、 Ⅱ型房室传导阻滞。 术后1 周患者仍感胸闷不适,复查24 h动态心电图,其术后24 h Lorenz 散点图及术后1 h散点图如图5 所示。
起搏器植入后呈AAI 及DDD 工作模式,频率60 次/min,少数采用VAT 模式,可见少数室性早搏及频发房性早搏形成的散点集(图5A)。 散点图中更显著的特征在于,除了曲尺状内外边界形成的四方块散点图外,远离原点也有两簇形态对称且以起搏核为顶点、垂直分布于右上方的心搏点区,与起搏器植入前Lorenz 散点图类似。
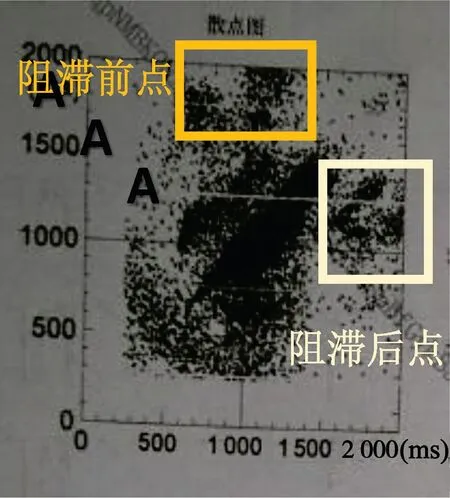
图4 术前24 h Lorenz 散点图
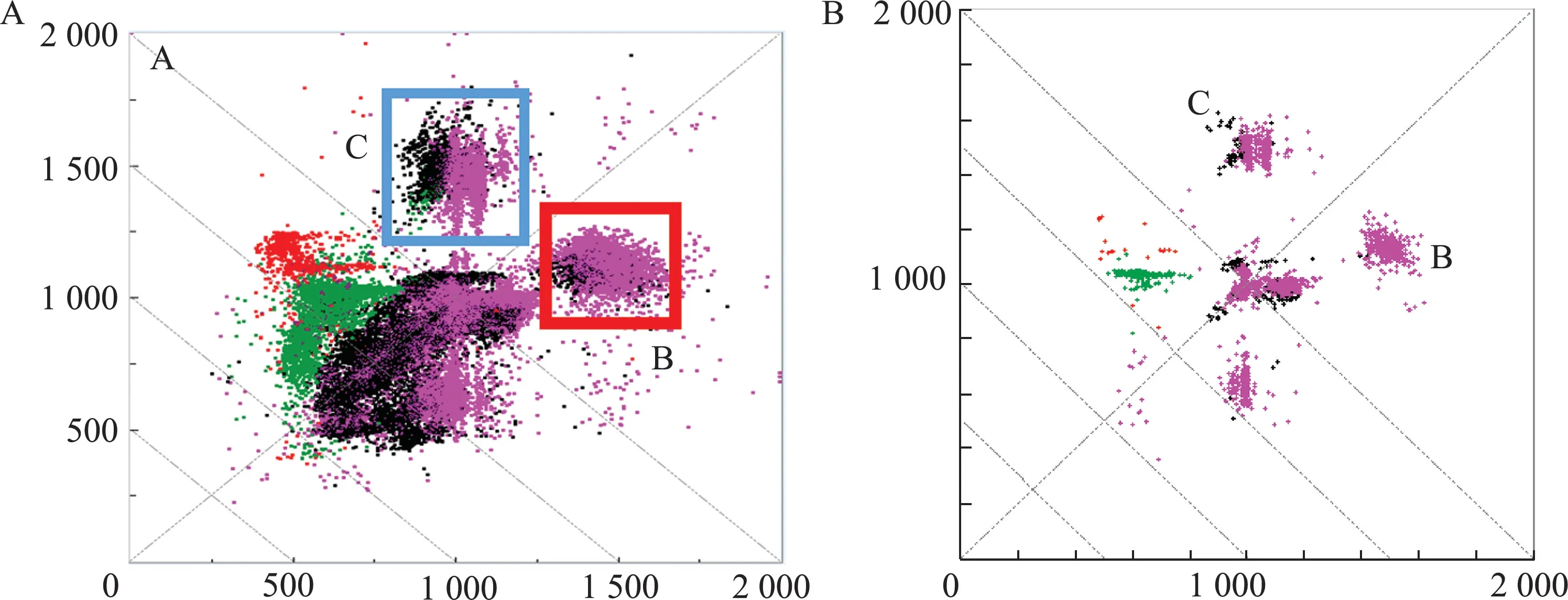
图5 术后24 h Lorenz 散点图(A)和1 h Lorenz 散点图(B)
图5B 中的散点酷似起搏前散点,术后1.3 ~2.0 s 长RR 间期计数有4 000 余次/24 h。 起搏器术后产生缓慢心搏的原因是起搏与感知功能障碍,还是某种特殊功能运作使然? 对图5 中C、B散点集进行逆向回放,相应的心电图片段如图6所示。
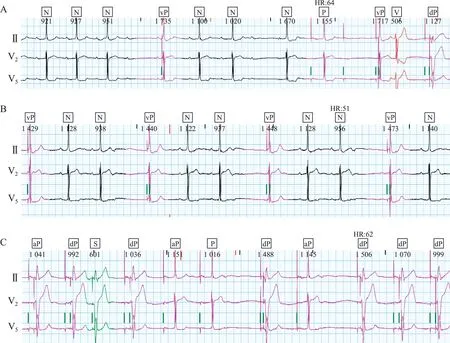
图6 术后24 h 散点逆向回放不同时程心电图片段
24 h 动态心电图中房室传导阻滞或房性P′波未下传而导致长RR 间期形成,随后心房起搏脉冲后80 ms 发放心室备用脉冲,此种现象称为心室起搏管理(managed ventricular pacing,MVP)功能[1]。它在心电图记录中频繁出现,具体运作模式如图7、图8 所示。
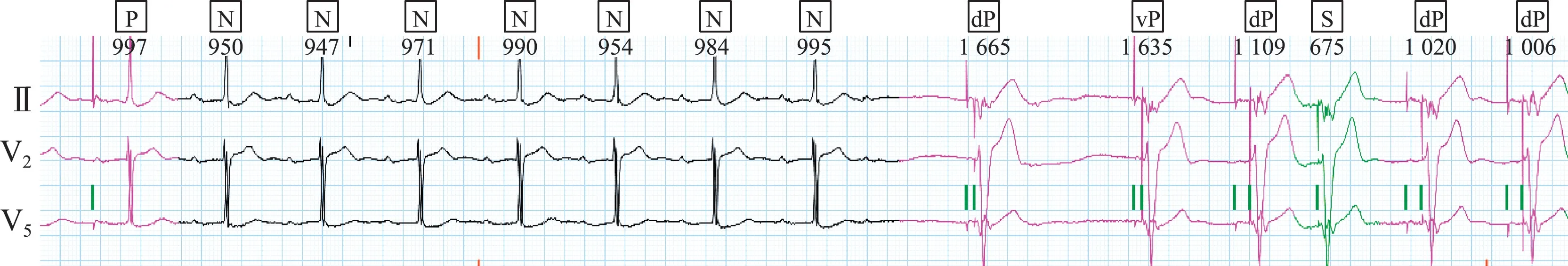
图7 AAI(R) +模式转换为DDD(R)模式实例
综上所述,动态心电图诊断:窦性心律+ 起搏器心律,起搏、感知功能正常,起搏器不恰当MVP 功能开启,频发房性早搏,少数室性早搏。
讨论该病例植入美敦力Adapta L ADDRL1起搏器后,理论上不应出现4 000 余次长达1.3 ~2.0 s 的长RR 间期。 假设起搏器基本功能发生障碍,综合图6,原因也只能是起搏器发生了过感知,即心室电极误感知心房电信号(窦性P 波、异位房性P′波、心房起搏P 波)。 根据双腔起搏器计时方式的特点,心房电信号后起搏AV 间期不会缩短,而此病例心房电信号起搏的AV 间期均固定性地缩短80 ms 且反复出现,认为应该是起搏器某种特殊功能的运作使然。
通过以上分析,该病例植入起搏器后的心电现象正符合美敦力MVP 功能的特点[2],与患者的起搏器程控报告单内容一致(起搏模式AAIR⇔DDDR),从而证实开启了MVP 功能。
MVP 功能是以心房为基础的双腔起搏模式,可实现在AAI(R)和DDD(R)模式之间自动转换。配备MVP 功能的目的是减少不必要的右心室起搏,通过保持心室感知和心室备用起搏支持下的AAI(R)起搏,既能使右心室起搏最小化,又能在出现房室传导阻滞时启动心室备用起搏,帮助患者实现生命安全与医疗获益之间的平衡。
应用MVP 模式时需注意以下几点,①MVP 模式允许长VV 间期,偶尔的心室停搏可导致出现近2 倍的起搏频率间期,选择该模式时需考虑对患者的影响。 ②对于完全性房室传导阻滞患者,起搏器每16 h 进行一次房室传导检查会导致一次长RR 间期,MVP 模式可能并不适合。 ③长PR 间期:开启MVP 模式后,只要在两次心房事件之间有自身心室感知,起搏器就会保持AAI(R)起搏模式;对于有症状的一度房室传导阻滞患者,永久的DDD(R)或DDD 模式可能更合适。
起搏器植入是治疗缓慢性心律失常的有效方法,但部分患者植入后仍存在缓慢性心律失常,因此,对它的准确识别和及时处理是起搏器患者术后随访和管理的重要内容[3]。 本例患者术前频繁出现胸闷、头晕、黑矇症状,心电图提示房早未下传、二度房室传导阻滞;植入起搏器后患者症状缓解不明显,复查动态Lorenz 散点图与植入起搏器前无明显变化,房性早搏未下传及房室传导阻滞形成的长周期未被“填补”。 利用Lorenz 散点图及其逆向技术[4],可快速甄别本病例是因频发房性早搏未下传而反复启动MVP 功能,导致反复出现RR 长间期,而房室传导阻滞可能并不是重点,与MVP 运作原理不相吻合。 另外,起搏器频繁发放心室备用脉冲,除了耗电以外,减少右心室起搏的效果也不明显(右心室起搏仍占总心搏的39.7%),最终未能使患者从起搏器治疗中获益。综合考虑,AAIR⇔DDDR 起搏模式并不适合该患者,报告临床后程控为DDDR 模式,且患者术前、术后合并有心律失常[5],在起搏器保驾护航的基础上,药物干预治疗的安全系数更高。
起搏器特殊功能开启应结合患者的自身情况,严格掌握开启的适应证,定期进行动态心电图随访[6]。 而利用Lorenz 散点图及其逆向技术,可快速确定起搏器的基本功能状态及某些特殊功能运作[7],开展起搏器程控随访,从而使起搏器植入患者获益最大化。

