原位合成ZIF-8/CS复合凝胶的结构与吸附性能
聂景怡, 梁建涛, 张美云*, 解宏滨, 宋顺喜
(1.陕西科技大学 轻工科学与工程学院, 陕西 西安 710021; 2.齐鲁工业大学(山东省科学院) 生物基材料与绿色造纸国家重点实验室, 山东 济南 250353)
0 引言
近几十年来,我国城市化和工业化快速发展,随之带来的环境治理压力也日益增大.对于水体污染而言,根据污染物种类主要可分为:有机染料污染(如亚甲基蓝、甲基橙、罗丹明),重金属污染(如铅、砷、汞、铜),农业污染(如化肥和农药),放射性污染及病原微生物污染等.其中工业废水的温度通常比较高,且pH等化学环境复杂,开发高效、稳定且可循环的吸附剂用于污水处理已成为研究人员关注的焦点.
类沸石咪唑酯支架材料(ZIFs)是一类多孔的金属-有机框架化合物(MOFs,Metal-Organic Frameworks),由金属中心离子(锌或钴)与有机配体咪唑或咪唑衍生物上的N原子通过配位所形成[1].其中ZIF-8是最具代表性的一种ZIFs,其具有高孔隙率和高比表面积[2],且具有良好的热稳定性及化学稳定性,在吸附分离[3,4]、光催化[5]和抗菌[6]等领域具有广阔的应用前景,有望用于环境治理[7].虽然ZIF-8性能优良,但其脆性大,且获得形式多为粉体,尺寸小,导致其加工性差,限制了实际应用.因此,需要寻找合适的基体来负载ZIF-8,以稳定地发挥其功能.
壳聚糖(Chitosan,CS)作为一种天然高分子,来源丰富、可再生,是一种绿色、可降解的基体材料,常制备成微球[8]、薄膜[9]、凝胶[10]等形态.CS基体/ZIF-8复合材料通常采用物理共混法[11]和静电纺丝法[12]制备,但缺点是ZIF-8的分布不均易团聚,导致功能发挥不充分.凝胶水热原位生长法[13]是近年来研究较热的一种复合材料制备方法,具体指的是将ZIF-8的金属离子加入到CS溶液中,再将ZIF-8的有机配体加入到NaOH凝固浴中,在CS凝胶化的同时,原位沉析ZIF-8,由此方法制备的ZIF-8分布均匀,且与CS基体结合紧密,可有效发挥ZIF-8的功能[14].另有研究表明,ZIF-8的形成会影响凝胶的结构,因此为了调控结构需要进一步探究其中的影响因素与机理.
用于处理污水的吸附分离材料主要有活性炭粉体、树脂或聚合物微球等[15],而这些形态的材料回收相对困难,因此可回收并可循环使用的块体吸附剂材料有待开发.本工作中,在CS凝胶中原位合成ZIF-8,研究制备过程中凝胶化作用与ZIF-8形成过程的相互影响.探究金属中心离子Zn2+与配体2-甲基咪唑的含量及金属离子-配体比例对ZIF-8/CS复合凝胶结构的影响,分析了形成机理,并研究了ZIF-8/CS块体复合材料对亚甲基蓝(Methylene Blue,MB)的吸附性能、光催化降解性能以及循环使用性能.
1 实验部分
1.1 实验原料
六水合硝酸锌(Zn(NO3)2·6H2O),天津大茂化学试剂厂;2-甲基咪唑(2-H-MeIM,C4H6N2),阿拉丁试剂(上海)有限公司;氢氧化钠(NaOH)、冰乙酸(CH3COOH)及壳聚糖(CS,粘均分子量Mη=1.20×106Da,脱乙酰度DD=89%),中国国药集团化学试剂有限公司;亚甲基蓝(MB),天津光夏精细化工研究所.上述化学试剂均为分析纯,使用时未经进一步纯化.
1.2 实验方法
1.2.1 ZIF-8晶体的制备
首先,将2.6 g 2-甲基咪唑于37.4 mL去离子水中搅拌溶解,配制咪唑溶液;将0.6 g Zn(NO3)2·6H2O于40 mL去离子水中搅拌溶解,配制锌离子溶液.然后,将锌离子溶液加入到咪唑溶液中,放入聚四氟乙烯高温高压反应釜(型号ZYF-DS04,安徽中研理工)中,于80 ℃反应12 h.反应结束后,离心分离沉淀,并用去离子水洗涤多次,以除去水溶性杂质.最后,使用冷冻干燥机(型号FD-2,上海比朗)将得到的样品在-56 ℃下干燥48 h,得到ZIF-8粉末.
1.2.2 CS水凝胶的制备
称取5 g CS粉末,在93 mL去离子水中充分分散,滴加2 mL冰乙酸,充分搅拌溶解CS,离心脱泡,得到5 wt.% CS溶液;将CS溶液注入方形单开口模具,而后整体转移至5 wt.% NaOH凝固浴中进行凝胶化;凝胶化结束后,将CS凝胶在去离子水中浸泡,洗去残余碱液;最终,冻干洗涤至中性的CS凝胶,得到CS干态材料.
1.2.3 ZIF-8/CS复合材料的制备
分别配制三份100 g 3.25 wt.%、6.5 wt.%和13 wt.% 2-甲基咪唑/5 wt.% NaOH混合凝固浴;再配制三份30 g锌离子/5 wt.%壳聚糖前体溶液,各含0.3 g、1.2 g和2.4 g Zn(NO3)2·6H2O.制备三种不同Zn2+与2-甲基咪唑比例的ZIF-8/CS复合凝胶:(1)将注入模具的含0.3 g 锌盐的锌离子-壳聚糖前体溶液置于13 wt.% 2-甲基咪唑/NaOH混合凝固浴;(2)将注入模具的含1.2 g 锌盐的锌离子-壳聚糖前体溶液置于6.5 wt.% 2-甲基咪唑/NaOH混合凝固浴;(3)将注入模具的含2.4 g 锌盐的锌离子-壳聚糖前体溶液放入3.25 wt.% 2-甲基咪唑/NaOH混合凝固浴.凝胶化完全后,放入反应釜于80 ℃反应12 h,得到ZIF-8/CS复合凝胶.冷冻干燥后,得到三种不同金属离子-配体比例的ZIF-8/CS干态复合材料.
1.2.4 凝胶结构影响因素探究
(1)金属锌离子
配制5 wt.% CS溶液,称取三份各30 g,向其中分别加入0.3 g、1.2 g和2.4 g Zn(NO3)2·6H2O,搅拌溶解,离心脱泡,得到锌离子-壳聚糖前体溶液;将前体溶液缓慢注入单开口模具中后,置于5 wt.% NaOH凝固浴中凝胶化,得到Zn2+/CS复合凝胶;洗涤至中性后冷冻干燥,得到不同Zn2+含量的Zn2+/CS干态复合材料.
(2)配体2-甲基咪唑
配制5 wt.% CS溶液;称取三份5 g NaOH溶于去离子水,再分别加入3.25 g、6.5 g和13 g 2-甲基咪唑,配制三份各100 g的2-甲基咪唑/NaOH混合凝固浴.将CS溶液缓慢注入三个方形模具中,然后分别置于上述三份混合凝固浴中.待CS溶液完全凝胶化后,得到2-甲基咪唑/CS复合凝胶;冷冻干燥后,得到不同咪唑含量的2-甲基咪唑/CS干态复合材料.
1.3 表征与测试
1.3.1 形貌表征
使用超景深显微镜(型号KH-8700,日本浩视)观察湿态CS凝胶、不同比例Zn2+/CS、2-甲基咪唑/CS和不同配比ZIF-8 /CS复合凝胶的微观结构.
通过扫描电子显微镜(SEM,型号S4800,日本日立)观察干态CS凝胶,Zn2+/CS、2-甲基咪唑/CS、ZIF-8/CS干态复合材料的微观结构.
1.3.2 结构表征
使用X射线衍射仪(型号D8 Advance,德国布鲁克)进行样品的X射线衍射(XRD)测试,采用D/max 2200PC Cu靶Kα辐射,2θ=5 °~45 °,扫描速率为2 °·min-1.
采用傅里叶变换红外光谱仪(型号Vectory-22,德国布鲁克)获得样品的红外(FT-IR)谱图,测试波长范围为4000~500 cm-1.
1.3.3 热重测试
采用同步热重分析仪(型号STA449F3,德国耐驰),在O2气氛下,温度范围35 ℃~800 ℃,升温速率10 ℃·min-1,测量样品的热重(TG)曲线,并通过公式(1)和(2)计算复合凝胶中各组分的含量:
ωZIF-8+ωCS=100%
(1)
ωZIF-8·RZIF-8+ωCS·RCS=Rgel
(2)
式(1)、(2)中:ωZIF-8表示ZIF-8在复合材料中的含量,ωCS表示CS在复合材料中的含量,RZIF-8表示ZIF-8的热重残余,RCS表示CS的热重残余,Rgel表示复合材料的热重残余.
1.3.4 吸附性能测试
(1)吸附量测试
配制100 mL 10 mg·L-1的MB溶液;称取0.5 g ZIF-8/CS干态复合材料,置于MB溶液中,在25 ℃恒温水浴中震荡;在不同的时间点吸取MB溶液上清液,采用紫外-可见分光光度计(型号Carry 500,美国安捷伦)检测在664 nm波长处的吸光度.结合MB标准曲线,利用公式(3)和(4)分别计算ZIF-8/CS复合材料对MB的吸附量和移除率[16]:
Q=(C0-Ci)×V/m
(3)
R=(C0-Ci))/C0
(4)
式(3)、(4)中:Q为MB的吸附量(mg·g_1),R为MB的移除率(%),C0为MB溶液的初始浓度(mg·L-1),Ci为吸附不同时间后MB溶液的浓度(mg·L-1),V为MB溶液的体积(L),m为ZIF-8/CS复合材料的质量(g).
(2)吸附动力学研究
采用准一级动力学模型和准二级动力学模型来反应ZIF-8/CS复合材料对MB的吸附动力学.准一级和准二级动力学速率方程如公式(5)和公式(6)所示:
ln(q1-qt)=lnq1-K1t
(5)
(6)
式(5)、(6)中:q1为拟合得到的MB最大吸附量,(mg·g-1),q2为拟合得到的平衡吸附量(mg·g-1),t为吸附时间(min),qt为不同时间的MB吸附量(mg·g-1),K1为一级动力学平衡常数,K2为二级动力学平衡常数.
(3)吸附热力学研究
分别配制10 mg·L-1、50 mg·L-1、100 mg·L-1、200 mg·L-1、300 mg·L-1和500 mg·L-1的MB溶液,向每份MB溶液中分别放入0.5 g的ZIF-8/CS复合材料,于25 ℃恒温水浴中震荡,取上层清液,检测其在664 nm波长处的吸光度.
Langmuir吸附等温式和Freundlish吸附等温式如公式(7)和公式(8)所示[17]:
(7)
(8)
式(7)、(8)中:qe为ZIF-8/CS在MB溶液中达到吸附平衡时的吸附量(mg·g-1),Ce为吸附平衡时MB溶液的浓度(mg·g-1),qm为理论吸附容量(mg·g-1),KL为 Langmuir等温吸附常数,KF为Freundlich等温吸附常数.
1.3.5 光催化降解测试
(1)不同pH下ZIF-8/CS复合材料的光催化降解效果
配制pH=3、7、10、12的20 mg·L-1的MB溶液各10 mL,分别放入0.5 g的ZIF-8/CS复合材料.将溶液置于光功率密度为100 mW·cm-2的光源之下,以模拟阳光照射.一定时间后取上层清液,检测其在664 nm波长处的吸光度,并利用公式(3)和公式(4)计算ZIF-8/CS复合材料对MB的吸附量和移除率.
(2)循环使用测试
将0.5 g的ZIF-8/CS干态复合材料放入10 mg·L-1的MB溶液中,置于光功率密度为100 mW·cm-2的光源下,取上层清液,检测其在664 nm波长处的吸光度.回收样品后,将其放入清水中进行解吸附,然后再次进行吸附试验,重复循环5次以检测材料的循环使用性能.
2 结果与讨论
2.1 复合材料的结构与形貌表征
CS凝胶、ZIF-8粉体以及ZIF-8/CS复合凝胶的XRD谱图如图1(a)所示.其中,ZIF-8的特征衍射峰位于2θ=7.3 °、10.4 °、12.7 °、16.4 °及18.0 °处,分别归属于(011)晶面、(002)晶面、(112)晶面、(013)晶面、(022)晶面[18].CS的特征峰位于2θ=9.2 °和19.8 °处,同归属于(100)晶面[19].XRD结果表明,ZIF-8成功在CS凝胶中合成,CS与ZIF-8同时存在于通过原位合成的ZIF-8/CS复合材料中.
CS凝胶、ZIF-8粉体以及ZIF-8/CS复合凝胶的FT-IR谱图如图1(b)所示.对于CS,3 427 cm-1处的吸收峰对应于酰胺基团的N-H伸缩振动;1 665 cm-1处的吸收峰对应于酰胺基团第I谱带的C=O伸缩振动;1 598 cm-1处的吸收峰对应于酰胺基团第II谱带的C-N键的伸缩振动和N-H键的弯曲振动;1 423 cm-1处的吸收峰对应于酰胺基团第III谱带的C-N键和N-H键的耦合振动吸收[20].对于ZIF-8,3138 cm-1处的吸收峰对应于配体2-甲基咪唑中甲基的C-H键伸缩振动吸收;2 993 cm-1处的吸收峰对应于咪唑环中的C-H键伸缩振动吸收;1 580 cm-1处的吸收峰对应于咪唑的C=N伸缩振动;1 145 cm-1和990 cm-1处的吸收峰对应于咪唑环的C-N伸缩振动[21,22],以上结果表明复合凝胶中存在ZIF-8晶体.综合XRD和FT-IR谱图可知,实验成功制得了ZIF-8/CS复合材料.
ZIF-8晶体和ZIF-8/CS复合材料的SEM图如图2所示.由图2(b)可以看出,ZIF-8/CS复合凝胶表现出各向异性结构,即沿凝胶化方向呈现孔道结构,而垂直于凝胶化方向呈现层状结构.由ZIF-8/CS复合凝胶的局部放大图2(c)可以看出,ZIF-8均匀地分散在CS凝胶内部,形貌为典型的菱形十二面体,尺寸约为1μm.以上结果表明通过原位合成法可在CS凝胶中制备ZIF-8晶体,并均匀地分布在复合材料中而不发生团聚.

(a)XRD谱图

(a)ZIF-8粉体
2.2 ZIF-8/CS复合材料的热稳定性及组分分析
CS、ZIF-8和ZIF-8/CS复合材料的TG曲线如图3所示.可以看出,ZIF-8/CS复合材料存在两个热失重阶段.第一阶段在130 ℃~370 ℃之间,主要是CS的热分解;第二阶段在400 ℃之后,且材料热损失速率加快,这主要是因为ZIF-8的配体2-甲基咪唑在高温下发生降解,造成ZIF-8有机骨架崩塌,同时和CS的键结合被破坏.另外在130 ℃之前材料有2.7%的质量损失,主要是材料中所存在的结合水受热脱除.由TG曲线还可以看出, CS的热重残余量接近于零,ZIF-8的热重残余量为42.1%,ZIF-8/CS复合材料的热重残余量为25.9%.利用公式(1)和(2)并结合以上数据,可以计算得到ZIF-8/CS复合材料中ZIF-8的含量为61.5%,且与直接水热合成相比,ZIF-8的产率为90.24%,表明CS的存在对ZIF-8的产率无显著影响.
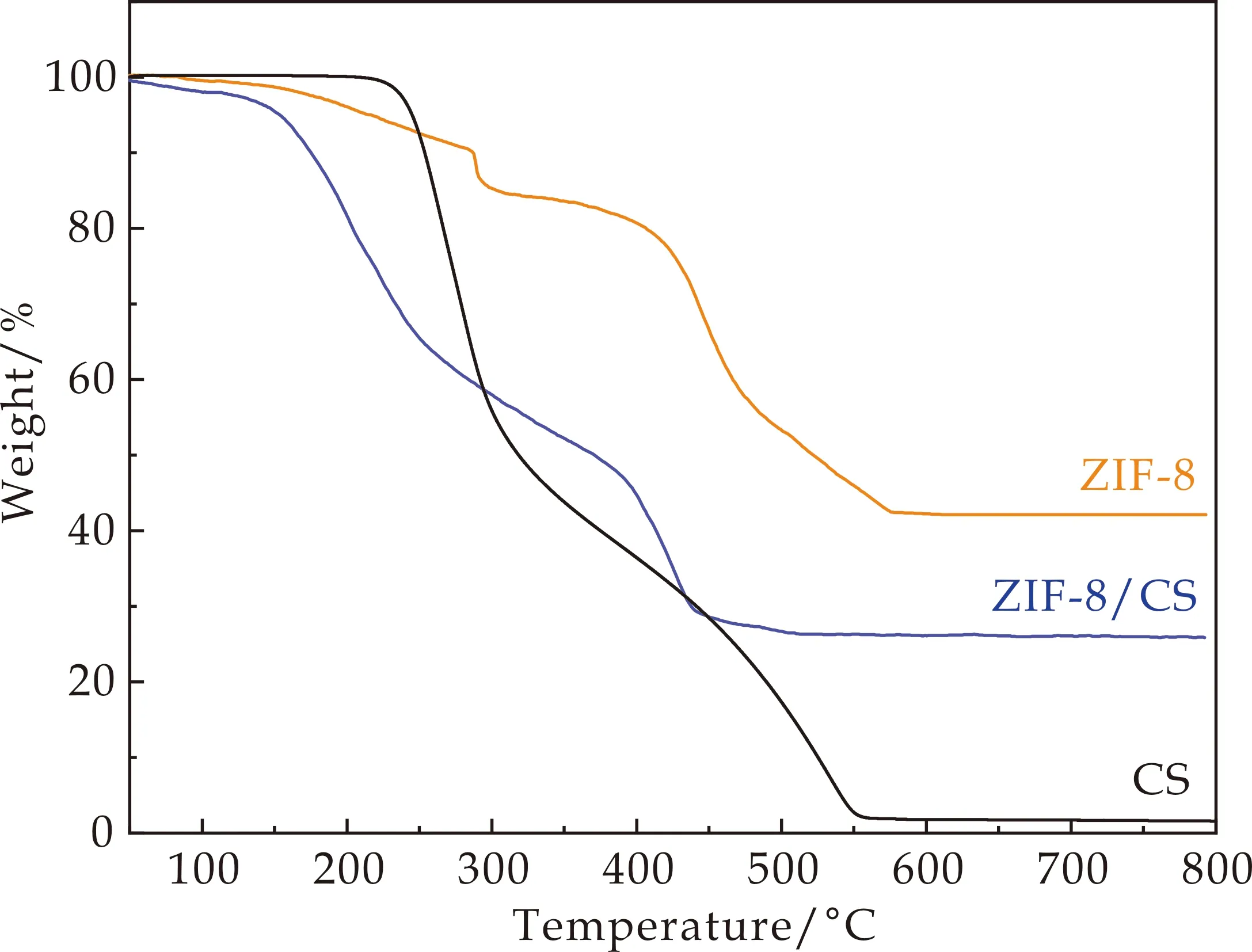
图3 CS、ZIF-8和ZIF-8/CS复合材料的TG曲线
2.3 原位合成ZIF-8对CS凝胶结构的影响
2.3.1 金属锌离子对凝胶结构的影响
图4为不同金属离子添加量的CS凝胶形貌.如图4所示,纯CS凝胶的内部为取向结构;而向CS溶液中加入0.3 g锌盐后,凝胶内部出现分层现象;加入0.6 g锌盐后,CS凝胶内部转化为孔道结构,并沿垂直于OH-扩散的方向发生收缩;加入1.2 g锌盐后,内部也出现孔洞结构,且整体凝胶收缩更加明显.以上结果表明,金属离子对CS凝胶结构有显著影响,能够使凝胶内部产生更多的孔洞,并且使凝胶发生收缩.

(a1)~(a4)湿态凝胶超景深照片 (b1)~(b4)SEM图像 (c1)~(c4)干态凝胶数码照片
2.3.2 配体2-甲基咪唑对凝胶结构的影响
图5为不同2-甲基咪唑添加量的CS凝胶形貌.如图5所示,在NaOH凝固浴中加入不同含量的2-甲基咪唑,凝胶化后CS凝胶的内部结构未发生明显变化,仍为取向结构,这表明有机配体对于CS凝胶的有序结构并不产生影响.

(a1)~(a4)湿态凝胶超景深照片 (b1)~(b4)SEM图像 (c1)~(c4)干态凝胶数码照片
2.3.3 金属离子-配体比例对凝胶结构的影响
图6为不同金属离了-配体比例的ZIF-8/CS凝胶形貌.如图6所示,当同时引入锌离子与2-甲基咪唑时,在CS凝胶内部将原位生成ZIF-8;当锌盐与咪唑的比例为0.3 g∶13 g时,复合凝胶内部出现分层现象,当锌盐与咪唑的比例为0.6 g∶6.5 g和1.2 g∶3.25 g时,复合凝胶内部呈现出孔洞结构,且发生一定的收缩.

(a1)~(a4)湿态凝胶超景深照片 (b1)~(b4)SEM图像 (c1)~(c4)干态凝胶数码照片
根据以上现象可以得出,纯CS凝胶内部为取向结构,配体2-甲基咪唑的加入不会对凝胶内部结构造成影响.而金属离子对凝胶内部孔洞结构的塑造起决定性作用,仅加入少量锌离子时会发生分层现象,当锌离子达到一定量时会出现孔洞结构,并且会引起凝胶收缩.同时引入一定比例的锌离子和2-甲基咪唑也会产生各项异性孔洞结构,这主要与金属离子的存在有关.研究表明,主族金属离子与CS存在一定的弱结合,而含有不饱和d、f轨道的过渡金属离子会与CS的-NH2和-OH配位,形成离子交联,从而影响凝胶的塑造[23].这为MOFs/CS复合凝胶的构造提供了一定的借鉴意义.
2.4 ZIF-8/CS复合材料的吸附性能
2.4.1 吸附时间对吸附性能的影响
ZIF-8/CS复合材料在不同时间对MB的移除效果如图7(a)所示.由图可知,当吸附时间为10 min时,ZIF-8/CS对MB的移除率达83.7%;随着吸附时间的延长,ZIF-8/CS复合材料对MB的吸附速率下降,吸附90 min时,对MB的吸附-脱附基本达到平衡,此时的移除率为98.3%.上述结果表明ZIF-8/CS复合材料可在短时间内对染料分子进行快速吸附,且最终的移除率高,是一种高效的染料吸附剂.
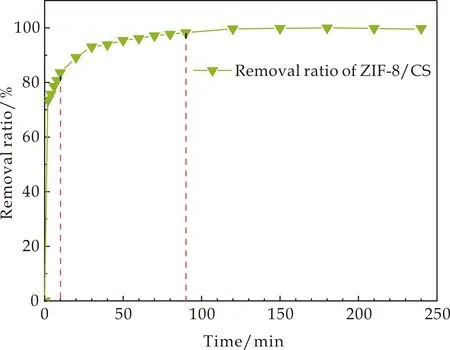
(a)吸附时间对吸附性能的影响
2.4.2 pH对吸附性能的影响
不同pH条件下ZIF-8/CS复合材料对MB的吸附效果如图7(b)所示.当MB溶液pH=3时,ZIF-8/CS复合材料对MB吸附20 min后,吸附量为1.57 mg·g-1,移除率为78%.而当pH=7、10、12时,吸附20 min后吸附量分别为1.85 mg·g-1、1.88 mg·g-1及1.87 mg·g-1,对MB的移除率分别为92%、94%和93%.可以看出,不同pH对材料的吸附性能有一定的影响,特别是在pH较低时,ZIF-8/CS复合材料的吸附性能较差,这主要是因为在酸性条件下,CS基体不稳定,并且氢离子会和阳离子MB发生竞争关系,导致吸附效果下降.而在pH较高时,CS基体稳定,其表面氨基显负电,对MB的吸附效果好,在较宽的pH值范围内ZIF-8/CS复合材料的吸附性能差别不大.
2.4.3 ZIF-8/CS复合材料的吸附动力学分析
ZIF-8/CS复合材料的准一级和准二级吸附动力学模型和参数如图8和表1所示.拟合出准二级动力学模型的相关系数为0.999,显著高于准一级动力学的0.871.除此之外,由准二级线性速率方程计算得到的平衡吸附量为2.02 mg·g-1,与准一级的平衡吸附量0.38 mg·g-1相比更接近实验测定值2 mg·g-1.因此,准二级线性速率方程能更好的反应ZIF-8/CS复合材料对MB的吸附过程,表明ZIF-8/CS复合材料对MB的吸附过程是一种化学吸附过程.
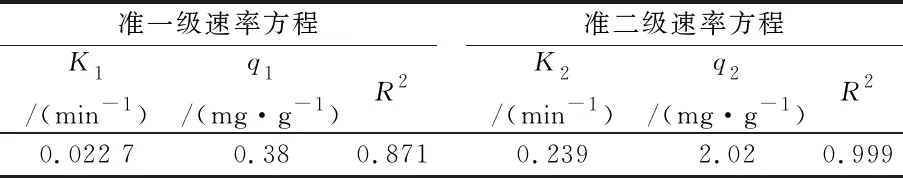
表1 动力学模型参数
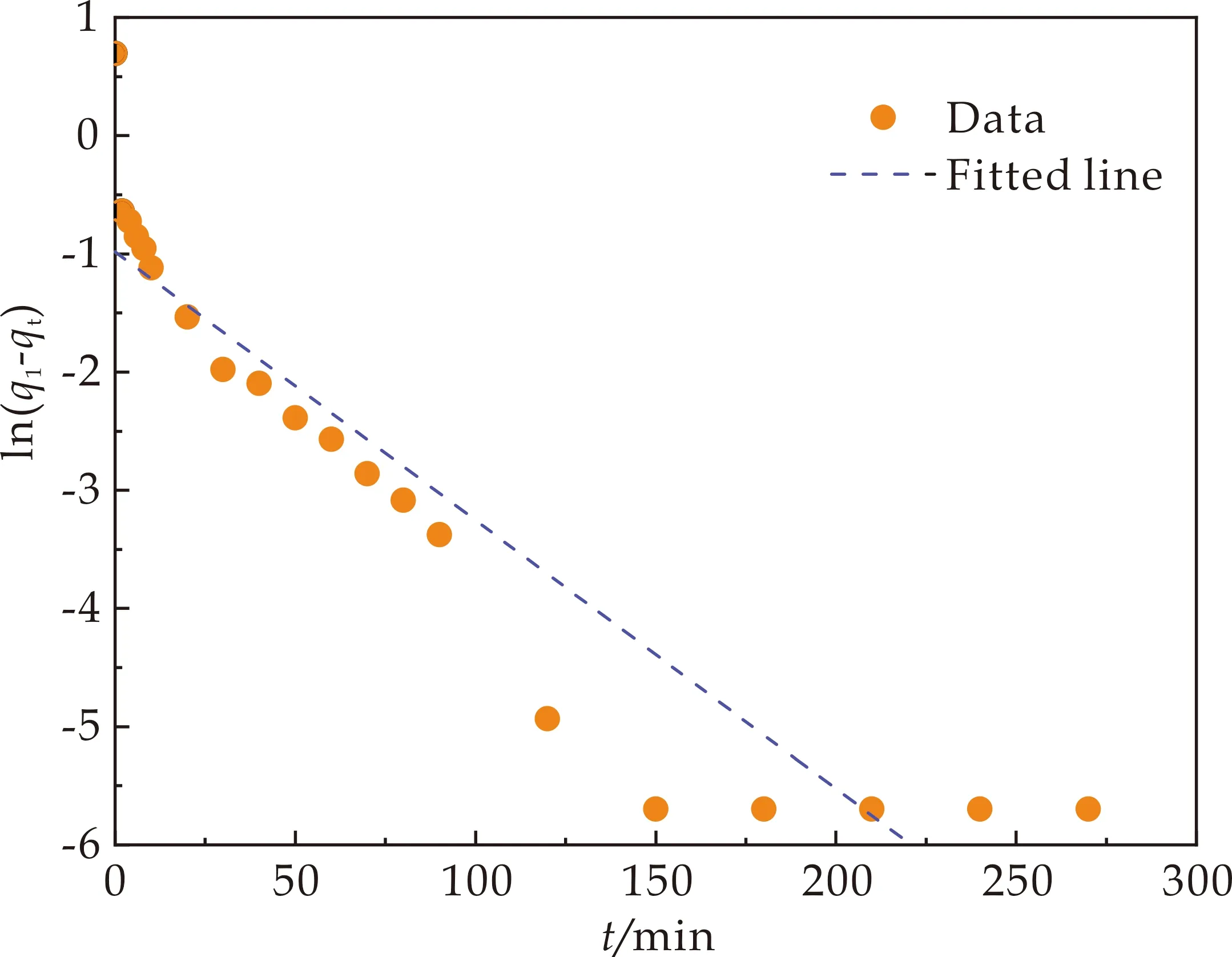
(a)准一级动力学模型
2.4.4 ZIF-8/CS复合材料的吸附热力学分析
ZIF-8/CS复合材料吸附MB的Langmuir、Freundlich吸附热力学模型和参数如图9和表2所示.ZIF-8/CS复合材料吸附MB的Langmuir模型拟合参数R2为0.991,明显高于Freundlich模型拟合参数R2=0.959,说明ZIF-8/CS复合材料对MB的吸附更符合Langmuir等温吸附过程,属于单层吸附.ZIF-8/CS复合材料对MB的最大吸附量qm为74.85 mg·g-1,表明ZIF-8/CS复合材料具有良好的吸附效果.

表2 Langmuir、Freundlich模型参数
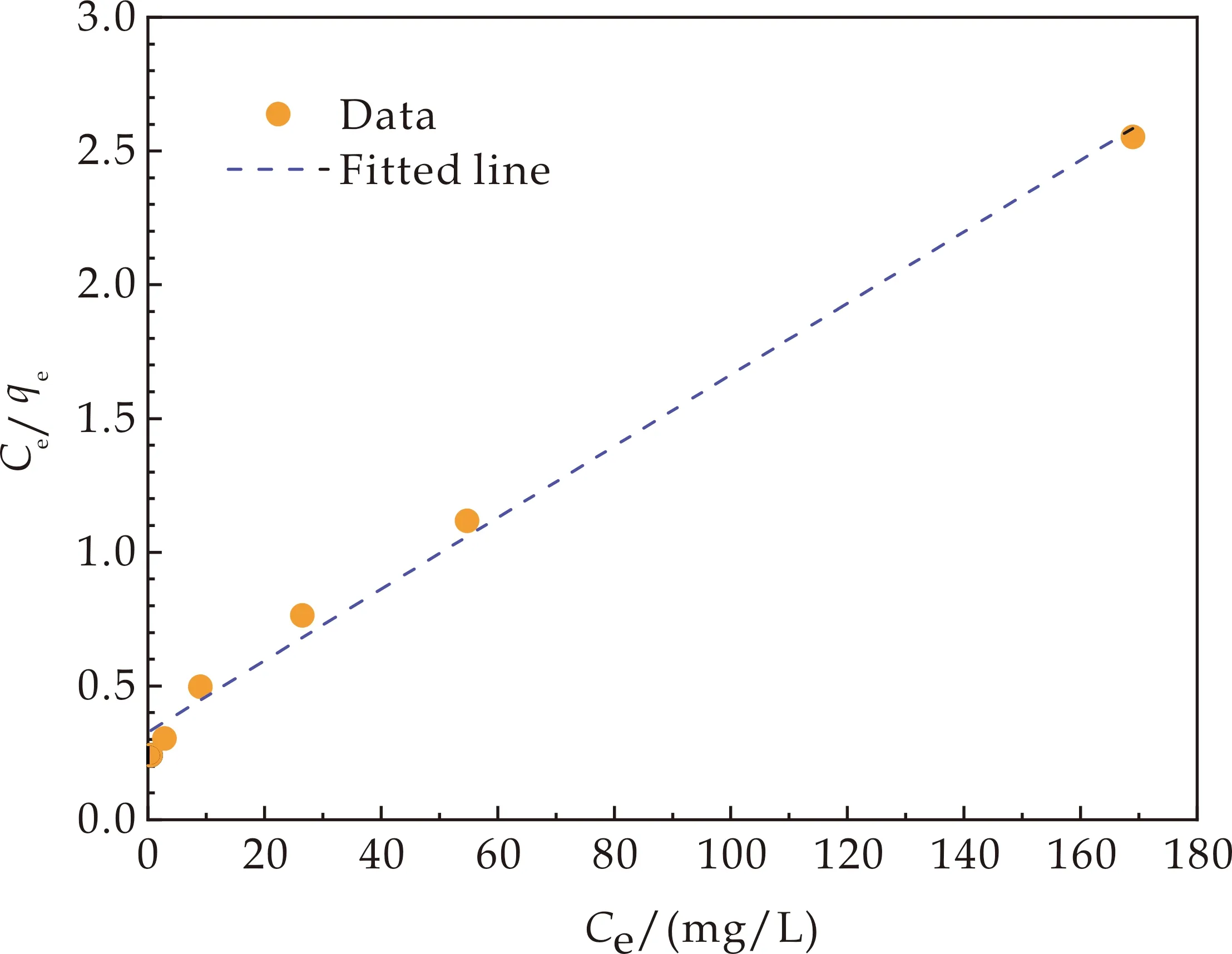
(a)Langmuir吸附等温线
2.5 ZIF-8/CS复合材料的光催化降解效果
进一步地,探究了ZIF-8/CS复合材料是否保留了ZIF-8对MB的光催化降解能力.研究发现,光照条件下,ZIF-8/CS复合材料在1 min内可使MB浓度降低95%以上;而无光照下,吸附10 min后MB浓度仅降低约80%.并且光照下移除MB测试后的ZIF-8/CS复合材料的颜色趋近于测试前的颜色,并未染成蓝色.因此,我们根据对MB的移除效率与测试后的样品状态,判断在光照条件下,ZIF-8/CS复合材料对MB的移除效果不仅是基于吸附原理,而主要是光催化降解作用.有研究表明,光照条件下,ZIF-8中的一个电子从最高占据分子轨道(HOMO)跃迁至最低未占据分子轨道(LUMO),HOMO缺失的电子从溶剂水分子中捕获,进而产生羟基自由基·OH,活性物质·OH进攻MB分子,使其发生降解完成光催化过程[24].
如表3所示,ZIF-8/CS复合材料在酸性和中性条件下不具备光催化降解MB的效果,而在碱性条件下对MB具有光催化降解作用.当MB溶液的pH值为10时,催化降解的速率最快.如图10所示,当循环使用ZIF-8/CS复合材料时,第一次光催化降解时间为30 s,使用结束后直接放入新配的MB溶液中进行第二次光催化降解,重复此操作,得到第二次、第三次、第四次和第五次的光催化降解时间依次为2 min、3 min、4 min和5 min.上述结果表明,在碱性条件下ZIF-8/CS复合材料对MB具有稳定的光催化降解作用,并可持续循环使用.

表3 光催化降解效果
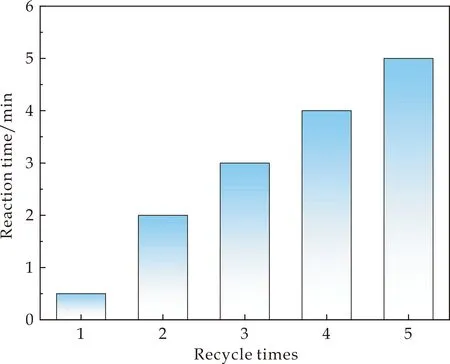
图10 ZIF-8/CS循环使用对MB的光催化降解效果
2.6 ZIF-8/CS复合材料的循环使用性能
ZIF-8/CS复合材料循环使用时对MB的移除效果如表4所示.首次使用时的移除率达99.8%,经过5次循环使用后,对MB的移除率仍然可达97.6%,由此表明,ZIF-8/CS复合材料具有一定的循环使用性能.

表4 ZIF-8/CS复合材料循环使用对MB的移除率
3 结论
本文通过CS凝胶化和ZIF-8原位合成过程同步进行,制备了ZIF-8/CS复合凝胶材料,研究发现,金属离子的加入会造成凝胶的分层或形成孔洞结构,并会引起凝胶收缩,而有机配体对凝胶结构无直接影响;原位合成的ZIF-8形态完整,在凝胶中分布均匀,产率达90.24%,含量为61.5%.此外,ZIF-8/CS复合材料具有良好的吸附性能,对MB的吸附过程更符合单分子层化学吸附;五次循环使用后对MB移除率仍可达97.4%,且在碱性条件下具有良好的光催化降解效果.本研究所制备的绿色、稳定、高效的ZIF-8/CS块体复合材料有望应用于污水治理.

