一步分光光度法检测肉制品中亚硝酸盐的含量
王盼雪, 孙 妍, 单锦瑞, 周甜甜
(陕西科技大学 食品与生物工程学院, 陕西 西安 710021)
0 引言
亚硝酸盐是肉制品加工中一种常用的发色剂,同时也具有一定的抑菌作用[1].亚硝酸盐可以分解产生亚硝基,与肌红蛋白反应,形成鲜红色的亚硝基肌红蛋白,使肉制品呈现良好的色泽.同时,亚硝酸盐可以抑制肉毒梭状芽孢杆菌及多种腐败菌的生长,产生一定的防腐效应[2].然而,人体摄入过量的亚硝酸盐会对健康产生危害[3].亚硝酸盐是一种强氧化剂,可以与血液中的血红蛋白结合,使氧合血红蛋白变为高铁血红蛋白,从而失去运输氧气的功能,引起组织缺氧.而且,亚硝酸盐容易与胺结合,生成具有致癌性亚硝胺.
目前,一些国家已经禁止在肉制品中添加亚硝酸盐,大部分国家制定了亚硝酸盐使用量的限量标准.我国国家标准(GB 2760-2014)规定,肉制品中亚硝酸盐的使用量不得超过0.15 g/kg,西式火腿类制品中最终的残留量不超过70 mg/kg,肉类罐头中不超过50 mg/kg,其他肉制品中不得超过30 mg/kg.然而,亚硝酸盐廉价易得,效果显著,不法商贩在利益的驱使下,违反国家标准法规,在肉制品加工过程中不规范使用亚硝酸盐,给消费者的身体健康造成了威胁.因此,建立一种灵敏的亚硝酸盐检测方法对保障食品安全和民众身体健康具有重要的意义.
目前开发的亚硝酸盐的检测方法包括分光光度法[4,5]、离子色谱法[6,7]、高效液相色谱法[8]、化学发光法[9,10]、毛细管电泳法[11]、催化荧光分析法[12]、电化学方法[13]等.其中,盐酸萘乙二胺法经济、方便,是亚硝酸盐检测中最常用的分析方法[14,15].该方法的原理是,在弱酸性条件下,亚硝酸根与对氨基苯磺酸进行重氮化反应,生成的重氮盐再与盐酸萘乙二胺偶合,生成紫红色的化合物,利用该化合物在538 nm处的吸光值分析亚硝酸盐的含量.该方法不需要使用大型的仪器设备,检测成本低.然而,该方法分多步进行,操作相对繁琐,且灵敏度低,无法满足实际检测的需求[16,17].
在酸性条件下,亚硝酸盐可以与硫醇化合物反应,生成S-亚硝基硫醇,S-亚硝基硫醇的水溶液在330~350 nm处有吸收峰[18,19].然而,烷基亚硝基硫醇的摩尔吸光系数小,吸光值低,检测灵敏度低.Zhang等人发现,含有共轭结构的化合物的摩尔吸光系数大,吸光值高[20].因此,本研究选用含有π-共轭结构的2-硫代巴比妥酸(TBA)为反应物,在酸性条件下与亚硝酸盐反应,生成吸光值高的S-亚硝基硫醇化合物(图1).利用分光光度法测定生成的S-亚硝基硫醇化合物的吸光值,实现亚硝酸盐的灵敏检测.并利用该方法检测市售猪肉火腿中亚硝酸钠的含量.研究结果可以为亚硝酸盐的检测提供一种更为灵敏、便捷、环保的分光光度检测方法,具有良好的应用前景.

图1 酸性条件下,2-硫代巴比妥酸与亚硝酸盐反应的化学反应方程式
1 材料与方法
1.1 试剂和仪器
1.1.1 主要试剂
亚硝酸钠(99%)、TBA、三水合亚铁氰化钾,上海阿拉丁生化科技有限公司;硝酸钠、磷酸钾、磷酸氢二钠、磷酸二氢钠,天津市大茂化学试剂厂;无水硫酸钠、无水碳酸钾、无水乙酸钠,天津市科密欧化学试剂有限公司;柠檬酸钠、碳酸氢钠、七水合硫酸锌,天津市天力化学试剂有限公司.以上试剂均为分析纯.
1.1.2 主要仪器
FC全波长酶标仪,赛默飞世尔科技有限公司;XW-80A旋涡混合器,上海驰唐电子有限公司;KH5200数控超声波清洗器,昆山禾创超声仪器有限公司.
1.2 反应条件优化
(1)最适检测波长的确定:10.0μg/mL NaNO2溶液与等体积的200μg/mL TBA溶液充分混合,测定反应液在300~500 nm间的吸收光谱,确定最适检测波长.
(2)TBA浓度的影响:10.0μg/mL NaNO2溶液与等体积的不同浓度的TBA溶液(50、80、100、160、200、300、400、500、1 000μg/mL)充分混合,在最适检测波长下测定TBA溶液和反应液吸光度,确定最佳的TBA浓度.
(3)最适反应pH的选择:10.0μg/mL NaNO2水溶液与等体积的pH 2.6、3.0、4.0、5.0、6.0、7.0、7.6的200μg/mL TBA溶液反应,在最适检测波长下测定反应液吸光值,确定反应的最适pH.
(4)最优反应时间的确定:10.0μg/mL NaNO2溶液与等体积的200μg/mL TBA溶液室温反应不同时间0、5 min、10 min、20 min、40 min、80 min、100 min,在最适检测波长下测定反应液吸光值,确定最佳反应时间.
1.3 共存离子干扰
测定反应体系中分别存在浓度为1 000倍亚硝酸根浓度的硝酸钠、无水硫酸钠、无水碳酸钠、无水乙酸钠、碳酸氢钠、柠檬酸钠、磷酸钠、磷酸二氢钠时,10.0μg/mL NaNO2溶液与等体积的200μg/mL TBA溶液室温反应20 min后,测定在最适检测波长处的吸光值.相同试验条件下,10.0μg/mL NaNO2溶液与等体积的200μg/mL TBA的反应液作为阳性对照组.同时单独测定100μg/mL干扰离子与200μg/mL TBA溶液在相同试验条件下的反应液的吸光值,验证反应的特异性.
1.4 标准曲线
浓度为0.1μg/mL、0.2μg/mL、0.4μg/mL、0.8μg/mL、1.0μg/mL、1.6μg/mL、2.0μg/mL、4.0μg/mL、8.0μg/mL、10.0μg/mL NaNO2的水溶液与等体积的200μg/mL的TBA的磷酸氢二钠-柠檬酸缓冲液(pH 4.0)溶液充分混合,室温反应20 min.测定反应液在最适检测波长下的吸光值,绘制标准曲线.按照公式(1)和(2)计算该方法的检出限(LOD)和定量限(LOQ).
LOD=3SD/k
(1)
LOQ=10SD/k
(2)
式(1)、(2)中:SD为空白组的标准偏差,k为标准曲线的斜率.
1.5 实际样品检测
从超市购买两种不同品牌的火腿,分别称取3×3份1.0 g样品切碎,加入0,20μg、30μg亚硝酸钠,和9 mL蒸馏水,超声提取30 min.加入1 mL 106 g/L的亚铁氰化钾,涡旋30 s,加入1 mL 53.5 g/L的硫酸锌,涡旋30 s.室温下反应15 min,滤纸过滤.取200μL滤液加入等体积 200μg/mL TBA室温反应20 min.取200μL反应液加入96孔板中,测定最适检测波长处的吸光值.利用建立的标准曲线计算亚硝酸钠的含量.每份样品平行检测三次.加标的样品的回收率按照公式(3)计算.

(3)
2 结果与讨论
2.1 方法优化
2.1.1 最适检测波长
在300~500 nm波长下分别采集10.0μg/mL NaNO2溶液和200μg/mL TBA溶液以及两者等比混合的反应液的吸收光谱(图2).从图2可以看出,在测定的波长范围内NaNO2溶液的吸光值接近零,NO2-与TBA反应生成的亚硝基硫醇在338 nm处的吸光值最大.同时,在该波长下TBA溶液的吸光值几乎为零.因此,可以选择338 nm作为最适检测波长.

图2 亚硝酸钠、TBA及两者的反应液的在300~500 nm 波长下吸收光谱
2.1.2 TBA浓度的影响
图3给出了10.0μg/mL NaNO2溶液与等体积的不同浓度的TBA溶液(50μg/mL、80μg/mL、100μg/mL、160μg/mL、200μg/mL、300μg/mL、400μg/mL、500μg/mL、1 000μg/mL)反应后的反应液在338 nm的吸光值的测定结果.从图3可以看出,当TBA的浓度低于200μg/mL时,反应液的吸光值随TBA浓度的增加而显著升高(P<0.01).当TBA的浓度继续增加到1 000μg/mL时,TBA溶液的背景吸收显著升高(P<0.01),反应液的吸光值与TBA溶液的背景吸光值同步升高,然而扣除TBA溶液的背景吸收后,反应液的吸光值无显著差异(P>0.05).该结果表明,200μg/mL的TBA既可以保证样品中的亚硝酸根反应完全,同时背景的吸光值接近零,不会对检测产生干扰.因此,测定亚硝酸根的最适TBA浓度为200μg/mL.

图3 不同浓度的TBA及其与亚硝酸钠反应液的吸光值
2.1.3 最适反应pH
利用0.1 mol/L的柠檬酸和0.2 mol/L的磷酸氢二钠配置pH为2.6、3.0、4.0、5.0、6.0、7.0、7.6的缓冲溶液.利用以上缓冲液分别配置200μg/mL TBA溶液.取等体积的10.0μg/mL NaNO2水溶液和TBA溶液充分混合均匀,测定混合液在338 nm下的吸光度值(图4).从图4可以看出,当pH从2.6升高到4.0时,反应液吸光度值呈增加趋势,当pH 继续升高到6.0时,反应液的吸光值随pH的升高而下降,pH值在6.0~7.6之间时,反应液的吸光值几乎为零.因此,该方法的最适检测pH为4.0.
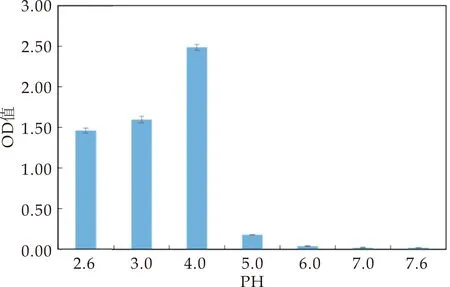
图4 pH对亚硝酸钠和TBA反应的影响
2.1.4 最优反应时间
为确定最优反应时间,试验中10.0μg/mL NaNO2溶液和等体积的200μg/mL TBA溶液分别在室温条件下反应了0、5 min、10 min、20 min、40 min、80 min、100 min.反应结束后,测定了反应液在338 nm处的吸光值(图5).由图5可知,反应时间在0~20 min时,反应液的吸光值迅速增长,反应时间在20~100 min时,反应液的吸光值趋于平稳.因此,可以选择20 min做为最优反应时间.

图5 反应不同时间的亚硝酸钠和TBA的反应液在338 nm处的吸光值
2.2 常见阴离子的影响
在pH4.0的条件下,测定反应体系中分别存在浓度为1 000倍亚硝酸根浓度的硝酸根、硫酸根、碳酸根、碳酸氢根、氯离子、磷酸根、磷酸二氢根、柠檬酸根、醋酸根时,10.0μg/mL NaNO2溶液与等体积的200μg/mL TBA溶液室温反应20 min后的吸光值(图6).图6中误差线为测定值的3%.从图6可以看出,在检测误差不超过3%的条件下,测定的阴离子对亚硝酸根检测几乎无干扰.表明该方法对亚硝酸盐检测的特异性好.而且,单独测定其他离子与TBA的反应液的吸光值发现,反应液吸光值很低(图7),说明该反应对亚硝酸根具有较高的专一性.

图6 常见阴离子对亚硝酸根和TBA反应的影响

图7 亚硝酸根和TBA反应的特异性验证
2.3 标准曲线
测定浓度为0.1~10.0μg/mL NaNO2标准溶液与200μg/mL TBA溶液反应后的反应液在338 nm处的吸光值.以NaNO2的浓度为横坐标,反应液吸光度值为纵坐标,可拟合得到线性方程y=0.294 7x+0.083 2,R2=0.998 2(图8).该结果表明本研究建立的亚硝酸盐检测方法的线性范围比常用的盐酸萘乙二胺方法宽[4],使用更方便.按照公式(1)和(2)分别计算该方法的LOD为0.02μg/mL,LOQ为0.06μg/mL.
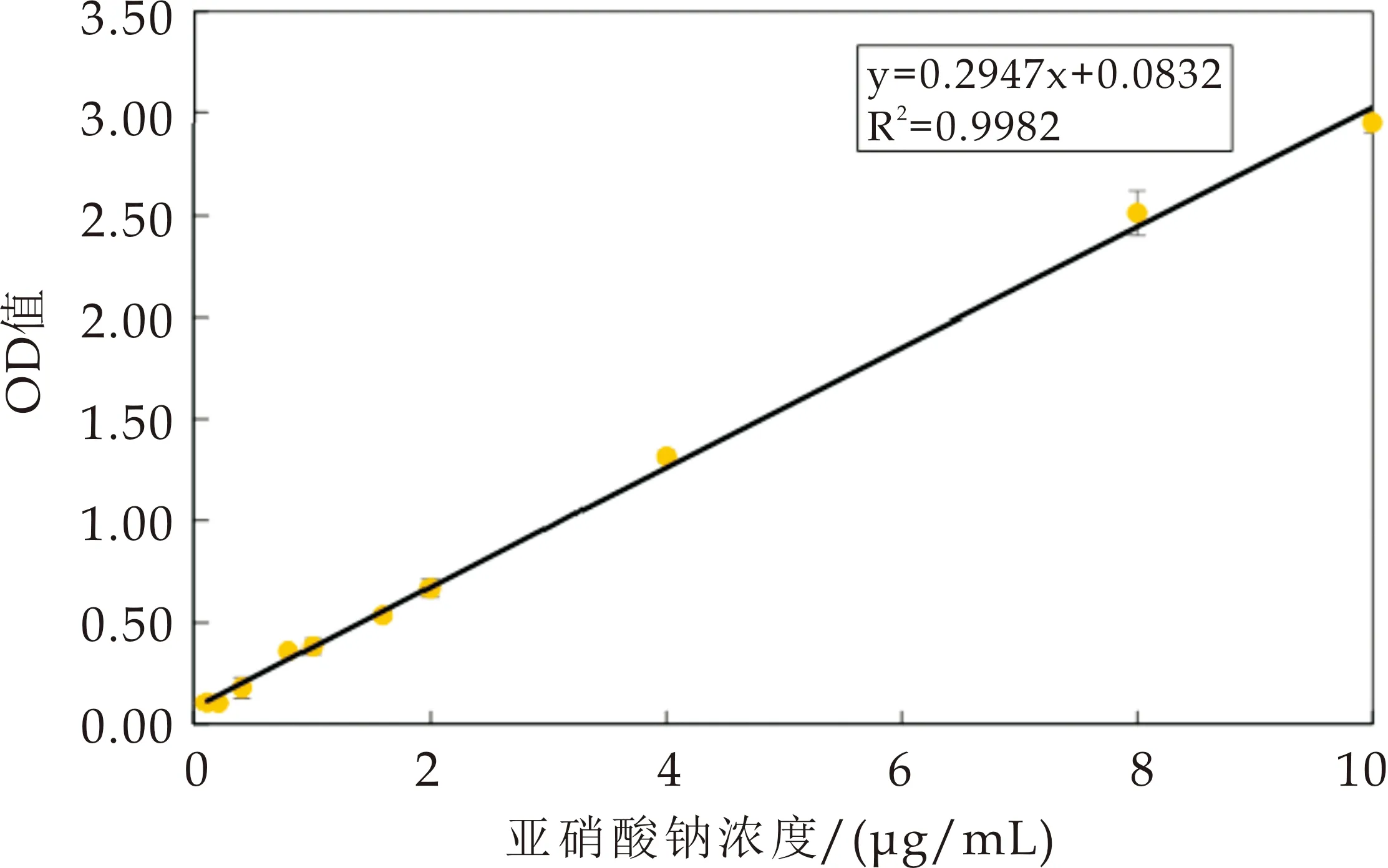
图8 亚硝酸钠检测的标准曲线
2.4 实际样品检测
本试验检测的肉制品为市售的两种不同品牌的火腿样品.测定结果如表1所示.从表1可以看出,该方法的检测结果与国标方法的检测结果具有较高的一致性.利用该方法检测的样品1中亚硝酸钠的含量为5.4μg/mL,样品2中亚硝酸钠含量为4.0μg/mL.两种样品中亚硝酸根含量均小于30 mg/kg,符合国家标准中对火腿类制品亚硝酸根含量的规定.加标回收试验结果显示该方法的回收率为85.0%~94.0%,RSD为1.8%~3.0%,表明该方法的准确性和精密度良好,可以作为一种亚硝酸盐检测的新方法.

表1 两种市售猪肉火腿中亚硝酸钠的检测结果(n=3)
3 结论
本研究以TBA为反应物,通过亚硝酸根-硫醇反应,向亚硝酸根中引入共轭结构,提高亚硝基的紫外吸收值,从而建立了一种灵敏的亚硝酸盐的分光光度检测方法.利用该方法检测亚硝酸盐的最适波长为338 nm,最适pH 4.0,反应时间为20 min,线性范围为0.1~10.0μg/mL,相关系数大于0.99,检出限和定量限分别为0.02μg/mL,和0.06μg/mL.利用该方法检测肉制品中亚硝酸盐的加标回收率为85.0%~94.0%,RSD为1.8%~3.0%.该方法回收率高,准确性好,灵敏度高,操作简便,可以作为肉制品及其他食品中亚硝酸盐检测的一种新方法.

