模拟煤矸石酸溶液制备聚合硫酸铝铁实验研究*
曾德恢 郑光亚 李浩林 刘 奎 海类游 夏举佩 刘成龙
(1.昆明理工大学化学工程学院,650500 昆明;2.宁夏师范学院化学化工学院,756000 宁夏固原)
0 引 言
煤炭开采和洗选过程中会产生大量的煤矸石[1],通常煤矸石的产量为原煤的20%~25%[2],导致其成为我国排放量最大的工业固体废弃物之一。煤矸石中含有大量的铝铁资源,其大量堆存和洗选废水直接排放,不仅占用宝贵的土地资源,而且严重破环生态环境[3]。故以煤矸石为原料制备絮凝剂应用于污水处理,不仅能减轻固体废弃物造成的环境压力,同时也可缓解水资源污染的局势。
无机高分子聚合硫酸铝铁絮凝剂(PAFS)是一种无机高分子复合型絮凝剂,广泛应用于工业、生活等废水的处理。含铝和铁等元素的低质矿物可用作制备PAFS的原料。KONG et al[4]以高铁型煤矸石为原料,在80 ℃,pH值为0.8的条件下聚合8 h制备PAFS,应用于硅藻土模拟废水的处理,去浊率达到98%左右。MA et al[5]以六盘水矿区的煤矸石为原料,在95 ℃,pH值为0.8的条件下聚合7 h制备PAFS,应用于模拟煤泥水的处理,达到污水排放Ⅰ级标准。YANG et al[6]以煤矸石酸浸液为原料,在80 ℃,pH值为0.9的条件下聚合6 h制备高铝型PAFS,应用于模拟废水的处理,去浊率达到98%以上。综上所述,以煤矸石为原料制备絮凝剂并应用于污水处理切实可行,具有较好的水处理效果,但普遍存在耗时长、聚合温度高和pH值低等缺点,不利于工业生产。
为解决以上问题,本实验以煤矸石酸浸液中铝铁物质的量比为参考,并使用分析纯试剂FeSO4·7H2O和Al2(SO4)3·18H2O制备PAFS,探究了质量浓度、温度和pH值等单因素对盐基度的影响,并进行了絮凝剂水处理实验。采用FTIR,SEM和XPS对产品的结构、微观形貌和铁的形态进行了分析,以期为煤矸石的高效利用和洗煤废水的处理提供一定参考。
1 实验部分
1.1 主要试剂和仪器
实验试剂:七水硫酸亚铁、十八水硫酸铝、柠檬酸、碳酸氢钠(均由天津市风船化学试剂科技有限公司生产)和氯酸钠(由成都艾科达化学试剂有限公司生产),均为分析纯;聚合硫酸铁(PFS),由广州看佼蓉环保科技有限公司生产;聚合硫酸铝(PAS),由河南丰泉水处理材料有限公司生产。
实验仪器:WG2-800型浊度计(上海昕瑞仪器仪表有限公司)、FE28型pH计(瑞士,梅特勒-托利多仪器有限公司)、ZNCL-GS190×90磁力搅拌水浴锅(郑州科华仪器设备有限公司)、电热鼓风干燥箱(上海一恒科学仪器有限公司)、RW 20型数显搅拌器(上海翼悾机电有限公司)、VERTEX70型傅立叶变换红外光谱仪(德国,布鲁克公司)、Quanta 200型扫描电子显微镜(美国,FEI公司)、UV-5500PC型紫外可见分光光度计(上海元析仪器有限公司)、K-Alpha+型X-射线光电子能谱仪(美国,赛默飞世尔科技公司)。
1.2 实验方法
1.2.1 聚合硫酸铝铁的制备
表1所示为贵州煤矸石酸浸液的化学组成,其中酸浸液的质量分数为24.33%。

表1 煤矸石酸浸液的化学组成(g·L-1)Table 1 Chemical composition of coal gangue acid leaching solution(g·L-1)
聚合硫酸铝铁的制备包括Fe2+的氧化、铝离子和铁离子水解聚合等主要环节,制备过程如下:由表1可知铝铁物质的量比为2.4,以此为基准准确称取FeSO4·7H2O和Al2(SO4)3·18H2O,总质量为320 g~820 g,配置成1 000 mL的铝铁混合溶液。取100 mL铝铁混合溶液于150 mL锥形瓶中,按Fe2+完全氧化计算加入氯酸钠0.91 g和浓硫酸2.55 g,在30 ℃~80 ℃的水浴锅中进行搅拌实验,10 min后向锥形瓶中缓慢添加碱化剂,调节pH值至1.9~2.3,使铝、铁离子发生水解聚合反应,得到红棕色液体产品,停止加热并缓慢搅拌,熟化40 min。将熟化后的红棕色液体在45 ℃下干燥研磨,得到淡黄色粉末状的自制聚合硫酸铝铁产品。
1.2.2 水处理絮凝沉降实验
煤泥废水取自贵州某公司,测得初始浊度为511 NTU,pH值为7.76。分别于7个400 mL烧杯中加入250 mL煤泥废水,用0.1 mol/L的NaOH溶液调节煤泥废水的pH值至4~10。分别称取5 mg~35 mg淡黄色粉末状的自制聚合硫酸铝铁产品于烧杯中,使用RW 20型数显搅拌器搅拌0.5 min~3.5 min。静置沉降0.5 h~2.5 h后,取距液面1 cm~2 cm处液体使用WG2-800型浊度计测量余浊度。
1.3 分析方法
1.3.1 余浊度的测定方法
首先将WG2-800型浊度计用去离子水调零,再用400 NTU的浊度标准溶液校正,取待测液液面下1 cm~2 cm处的液体测余浊度。
1.3.2 聚合硫酸铝铁盐基度的分析方法
(1) Fe2O3的质量分数测定
本实验中Fe2O3的质量分数测定方法参见GB/T 14591-2016。计算公式如下:
(1)
式中:w1为Fe2O3的质量分数,%;V1为滴定时消耗重铬酸钾标准滴定溶液的体积,mL;M1为Fe2O3的摩尔质量,g/mol(M1=159.70 g/mol);c1为K2Cr2O7标准滴定溶液浓度的准确数值,mol/L;m为试料的质量,g。
(2) Al2O3的质量分数测定
本实验中Al2O3的质量分数的测定步骤按照HG/T 5006-2016进行。计算公式如下:
(2)
式中:w2为Al2O3的质量分数,%;V0为空白实验消耗氯化锌标准滴定溶液的体积,mL;V2为试样消耗氯化锌标准滴定溶液的体积,mL;c2为氯化锌标准滴定溶液的实际浓度,mol/L;M2为Al2O3的摩尔质量,g/mol(M2=101.96 g/mol)。
(3) 盐基度的分析
本实验中盐基度的测定步骤参照HG/T 5006-2016进行,计算公式如下:
(3)

1.3.3 分析表征
将液体产品在45 ℃下干燥、研磨成粉。采用VERTEX70型傅立叶变换红外光谱仪(德国,布鲁克公司)测试样品的红外光谱,KBr-压片法制备样品,扫描范围为4 000 cm-1~400 cm-1,观测各峰的强度并分析引起相应特征峰的因素。采用Quanta 200型扫描电子显微镜在放大2 000倍和1 000倍的条件下观察样品的微观形貌。采用K-Alpha+型X-射线光电子能谱仪分析了样品表面铁价态。
1.4 反应机理
制备PAFS过程中主要发生了亚铁离子的氧化反应、铝铁离子的水解和聚合等反应,其中有关化学反应如式(4)~式(7)所示。

(4)

(5)

(6)

(7)
2 结果与讨论
2.1 制备PAFS絮凝剂单因素实验
2.1.1 铝铁总质量浓度对盐基度的影响
为研究铝铁总质量浓度对聚合物盐基度的影响,在60 ℃的水浴锅中调节pH值至2.25时,考察铝铁总质量浓度为320 g/L~820 g/L时对盐基度的影响(见图1)。由图1可知,随着铝铁总质量浓度增大,PAFS的盐基度逐渐增大。当铝铁总质量浓度小于320 g/L时,碱化剂主要用于中和过量酸,铝盐水解聚合贡献的盐基度较小,主要是铁盐在水解聚合贡献的盐基度。随着铝铁总质量浓度的增大,亚铁氧化消耗的酸增加,碱化剂一部分中和剩余的酸,另一部分用于增大溶液的pH值使铝离子逐渐水解聚合。据文献[7]所知,60 ℃时硫酸亚铁和硫酸铝的溶解度分别为55.1 g和59.2 g,硫酸亚铁的溶解度与温度呈非线性关系,当温度高于64 ℃时,硫酸亚铁的溶解度降低。又根据同离子效应,硫酸铝和硫酸亚铁在硫酸溶液中的溶解度比在水中的溶解度小。当铝铁总质量浓度为820 g/L时,硫酸铝溶液难以稳定存在。因此,铝铁总质量浓度应在320 g/L~820 g/L之间较为适宜。

图1 铝铁总质量浓度对PAFS盐基度的影响Fig.1 Effect of total mass concentration of aluminum and iron on PAFS basicity
2.1.2 pH值对盐基度的影响
为考察pH值对聚合硫酸铝铁盐基度的影响,在60 ℃的水浴锅中铝铁总质量浓度为550 g/L时,考察pH值为1.90~2.30时对盐基度的影响(见图2)。由图2可知,pH值在2.20~2.30得到PAFS的盐基度符合HG/T 5006-2016的要求;当pH值低于2.20时盐基度较低,絮凝效果较差,当pH值达到2.30以上时生成的PAFS难以稳定存在。

图2 pH值对聚合物盐基度的影响Fig.2 Effect of pH value on PAFS basicity
由于PAFS是较浓的无机盐溶液,离子间的静电作用相互影响。常温下Fe3+的浓度为0.1 mol/L时沉淀pH值为2.30,当Fe3+浓度为1 mol/L时沉淀pH值为1.50[8]。根据德拜-休克尔极限公式[9]和离子强度的计算公式[10]可知,一定条件下离子浓度和电荷数越大,离子强度就越大,活度系数就越小。离子的有效浓度相对减小,相应离子的水解pH值升高,表明一定温度下降低溶液浓度能使离子沉淀pH值升高[11]。当pH值低于2.20时,铝和铁主要以单核离子和低聚形态存在,随着pH值继续增大,铝铁逐渐发生水解聚合,形成大分子聚合物;当pH值超过2.30之后,铁的一系列离子会结合游离OH-快速形成Fe(OH)3沉淀。因此,PAFS能够稳定存在于pH值为2.30的溶液中。
2.1.3 温度对盐基度的影响
为考察温度对聚合硫酸铝铁盐基度的影响,在铝铁总质量浓度为550 g/L时调节pH值至2.30,考察温度为30 ℃~80 ℃对盐基度的影响(见图3)。由图3可知,当温度大于60 ℃时,相同时间下Fe2+转化成Fe3+的量越多,Fe3+的浓度增大导致Fe3+的沉淀pH值越低,较容易产生浅黄色不溶物,而此时Al3+几乎不水解聚合。当温度小于60 ℃时,Al3+在低温下聚合程度较弱。因此,PAFS聚合温度选择60 ℃较为适宜。
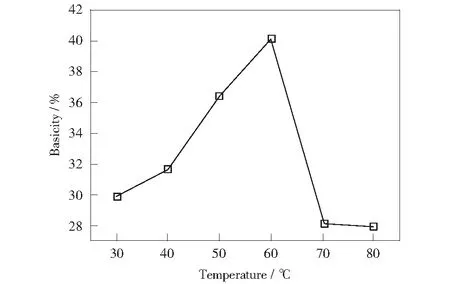
图3 温度对聚合物盐基度的影响Fig.3 Effect of temperature on PAFS basicity
2.2 水处理絮凝实验
2.2.1 絮凝剂投加量对余浊度的影响
为考察絮凝剂投加量对余浊度的影响,调节煤泥废水pH值至7,投加自制聚合硫酸铝铁5 mg~35 mg搅拌1.5 min后,静置沉降0.5 h~2.5 h后测其余浊度,结果如图4所示。由图4可知,随着絮凝剂的投加量增大,余浊度先降低后增加。这是由于絮凝剂凝聚颗粒的Zeta电位值随着投加量的增大呈升高趋势,当投加量达到一定程度时凝聚颗粒的Zeta电位会由负值变为正值。由于胶体颗粒表面所带的负电荷越来越少,胶体颗粒间的斥力也就越来越小,胶体颗粒更容易形成大的絮体而快速沉降。当投加量过大,带正电荷的凝聚微粒的Zeta电位呈上升趋势,进而斥力增加导致余浊度上升。结果表明,煤泥水处理时自制絮凝剂的最佳用量为80 mg/L。

图4 絮凝剂用量对余浊度的影响Fig.4 Effect of flocculant dosage on residual turbidity
2.2.2 煤泥废水pH值对余浊度的影响
为考察煤泥废水pH值对余浊度的影响,调节pH值至4~10,投加自制聚合硫酸铝铁20 mg搅拌1.5 min后,静置沉降0.5 h~2.5 h后测其余浊度,结果如图5所示。由图5可以看出,当时间相同时,随着pH值的增大,余浊度先减小再趋于平稳;pH值在6~8的范围内,沉降0.5 h后余浊度均小于15 NTU,沉降1 h后去除率高达98%;进一步表明自制的聚合硫酸铝铁在絮凝沉降过程中比常规絮凝剂所适应的pH值范围更宽。煤泥废水最佳沉降的pH值范围为6~8。

图5 pH值对余浊度的影响Fig.5 Effect of pH value on residual turbidity
2.2.3 搅拌时间对余浊度的影响
为考察搅拌时间对余浊度的影响,调节pH值至7,投加自制聚合硫酸铝铁20 mg搅拌0.5 min~4.0 min后,静置沉降0.5 h~2.5 h后测其余浊度,结果如图6所示。由图6可知,搅拌时间小于1.5 min时,余浊度下降明显。当搅拌时间大于1.5 min时,随着搅拌时间的增大余浊度缓慢上升。由于短时间的搅拌,药剂混合不充分,絮凝剂发生水解不均匀导致余浊度较高,搅拌时间过长时会将絮凝剂水解团聚形成的絮体再次被打碎,进而使得沉降效果变差;因此,选择适当的搅拌时间有利于沉降过程。在350 r/min下搅拌1.5 min所达到的效果最佳。

图6 搅拌时间对余浊度的影响Fig.6 Effect of stirring time on residual turbidity
2.2.4 与市售絮凝剂对比
在絮凝剂投加量为80 mg/L,pH值为7,搅拌时间为1.5 min的条件下,对比市售絮凝剂(PFS和PAS)与PAFS的水处理效果(见图7)。由图7可知,沉降相同时间PAFS对煤泥废水的余浊度明显低于PFS和PAS对煤泥废水的余浊度。实验过程中也能观察到PAFS的出水色度明显比PFS的出水色度小,絮体大于PAS的絮体,说明自制絮凝剂产品的水处理效果明显优于市售絮凝剂的水处理效果。另外,从制备成本上考虑,Al2(SO4)3·18H2O的市场价比FeSO4·7H2O的市场价高;Al3+和Fe3+浓度相同时,Al3+开始沉淀时的pH值大于Fe3+开始沉淀时的pH值[10],所以相同条件下制备PAS所需碱化剂比制备PFS所需碱化剂多;由式(1)可知,6 mol Fe2+氧化所需氯酸钠仅1 mol,而PAFS较PFS的制备过程中所需氧化剂用量更少。同等条件下制备PAFS过程中所需要的碱化剂用量比PAS的碱化剂用量少,所需要的氧化剂比PFS所需的氧化剂少。从絮凝剂用量及絮凝性能考虑,相同余浊度时PAFS的用量比PAS和PFS的用量少;同时PAFS综合了PFS和PAS的盐基度大、吸附能力及电荷中和能力强、沉降速度快、絮凝效果突出、出水色度低和使用范围广等优点[10],克服了PFS色度大、设备腐蚀作用大和PAS处理废水后铝残余量大等缺点,进一步说明自制絮凝剂产品优于PAS和PFS。

图7 PAFS与PFS和PAS的水处理效果对比Fig.7 Comparison of water treatment effects among PAFS and PFS and PAS
2.3 分析表征
2.3.1 红外光谱特征分析

图8 PAFS的红外光谱Fig.8 FTIR spectrum of PAFS
2.3.2 扫描电镜分析
图9所示为PAFS的微观形貌。由图9可知,PAFS表现出致密的网状结构。据文献[16]表述致密的凝胶网络结构更有利于胶体颗粒的凝聚,絮凝体之间形成与支链结构相对应的桥式聚集。聚合过程中各种形态的聚合体相互连接交错延伸形成紧密的聚合物[12],该结构使其表面积增大,增强了吸附和网捕卷缩凝聚力。

图9 絮凝剂的SEM照片Fig.9 SEM photos of PAFS
2.3.3 X-射线光电子能谱分析
图10为PAFS的XPS和Fe2p谱。其中图10a为产品絮凝剂的XPS总谱,图10b中红色曲线为总谱中分出Fe2p的峰谱,图10b中紫色曲线为拟合残差。由图10b可算出,高结合能端信号强度(I1)与Fe2p峰信号强度(I2)之比为0.89。当比值大于0.65时,Fe以Fe3+的化学态形式存在[17];说明PAFS絮凝剂过程中发生了亚铁离子的氧化反应生成了Fe3+。Fe2p的峰位置在712.12 eV处,根据文献[18]可进一步说明此处峰为Fe3+引起。通过XPS表征分析方法检测出絮凝剂聚合硫酸铝铁颗粒表面Fe以Fe3+的化学态形式存在。

图10 PAFS的XPS和Fe2p谱Fig.10 XPS and Fe2p spectra of PAFSa—XPS;b—Fe2p
3 结 论
1) PAFS的合成条件,铝铁反应总质量浓度为320 g/L~820 g/L,与之相适宜的pH为2.30,实验温度为60 ℃。
2) 将PAFS用于处理煤泥废水的工艺条件:投药量为80 mg/L,350 r/min下搅拌1.5 min,pH值为6~8。在此条件下所得煤泥废水余浊度最低。与市售水处理剂处理煤泥废水做了对比,自制的PAFS效果明显优于市售絮凝剂的效果。
3) 经XPS,FTIR和SEM表征分析可知,PAFS的颗粒表面Fe以Fe3+的化学态形式存在。絮凝剂产品中不仅含有Fe—OH—Fe和Al—OH—Al,而且还含有羟基桥联的铝铁(Fe—OH—Al),表明产品是一种多核羟基的络合物;此外,产品具有致密的网状结构和较大的表面积,进一步表明该产品具有良好的絮凝沉降性能。

