化学核心素养下平衡体系的课堂教学模式探析
程龙兵
一、问题的提出
平衡思想是高中化学核心素养的重要组成部分,沉淀溶解平衡也是化学平衡、离子平衡知识的延伸,学生对沉淀溶解平衡图像的掌握较为困难,难以厘清物质间的相互关系。王磊指出变化观念与平衡思想素养的内涵是能多角度、动态的分析化学变化,依据平衡思想对题目进行编码,筛选出能提现该素养的试题。笔者根据高中多年的教学实践,从不同角度剖析沉淀溶解平衡图像问题,让学生懂得变中不变的辩证思想。
二、沉淀溶解平衡的图像
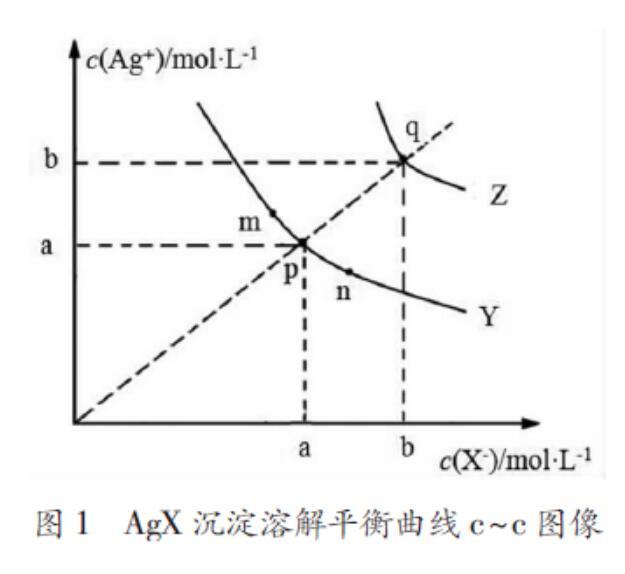
例1.t℃时,卤化银(AgX,X=Cl、Br) 在水中的沉淀溶解平衡曲线如图1所示,已知AgCl、AgBr的Ksp依次减小。下列说法错误的是()
A.图1中Z为t℃温度下AgCl曲线
B.图1中各点对应的Ksp的关系为:Ksp(m)=Ksp(n)=Ksp(p)<Ksp(q)
C.向n点的溶液中加入少量AgNO3固体,溶液组成由n沿npm线向m方向移动
D.p点溶液恒温蒸发可以变成q点
解析:(1)结合题干的信息,抓住Ksp只是温度的函数进行分析,不难得出Y、Z对应的沉淀溶解曲线。
(2)AgX饱和溶液中加入AgNO3固体,此时Qc>Ksp,AgX(s)Ag+ (aq )+X-(aq)向左移动,c(Ag+)·c(X-)仍然是Ksp,溶液组成沿着原曲线向上移动。
(3)饱和溶液恒温蒸发,AgX固体析出,c(Ag+)=c(X-),在图像上表示仍然是p点。通过以上分析,学生对经典的沉淀溶解曲线能够熟练掌握,为其他图像的解决奠定了一定的基础。
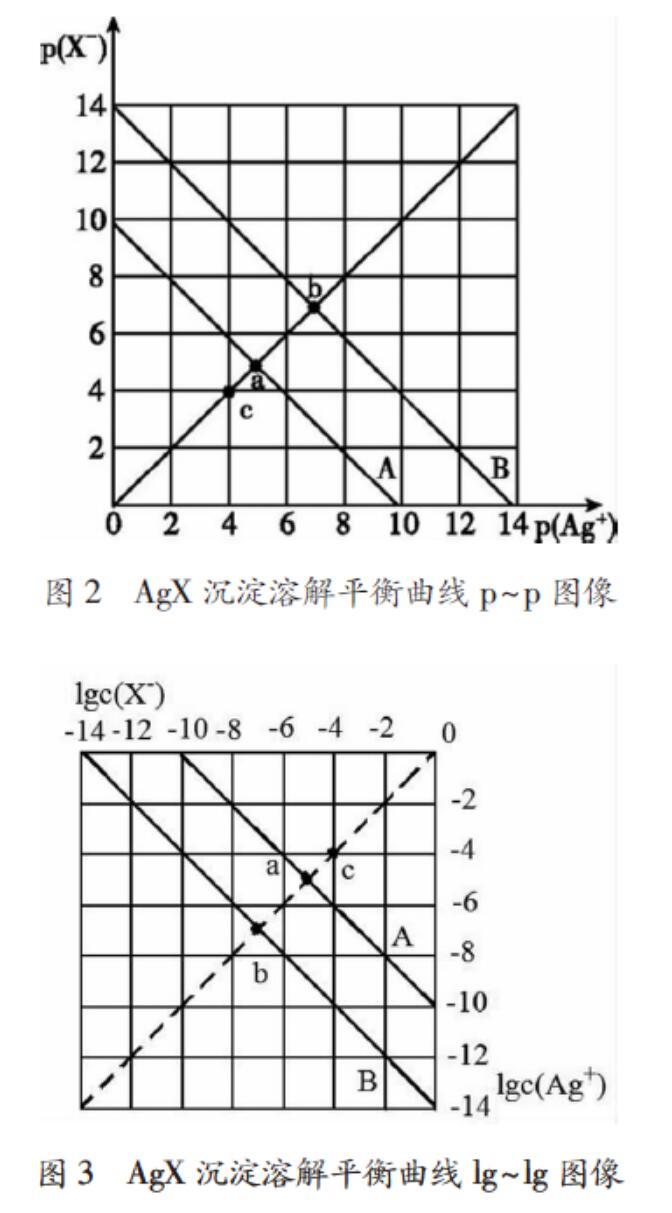
例2.t℃时,卤化银(AgX,X=Cl、Br) 在水中的沉淀溶解平衡曲线如图2所示,已知AgCl、AgBr的Ksp依次减小,且p(Ag+)=-lgc(Ag+),p(X-)=-lgc(X-),利用p(X-)~p(Ag+)的坐标系可表示出AgX的溶度积与溶液中的c(Ag+)和c(X-)的相互关系。下列说法正确的是()
A.t℃时,c点可表示AgCl的不饱和溶液
B.B线表示的是AgCl
C.取a、b两点处溶液等体积混合,维持t℃不变,混合溶液中一定有白色沉淀生成
D.在T℃时,AgCl(s)+Br-(aq) AgBr(s)+Cl-(aq)平衡常数K≈104
解析:(1)结合题干的信息,得出图2中A线表示的是AgCl,B线表示的是AgBr;此时与图1中Z线、Y线分别对应;与图3中A線、B线分别对应;同理图2中的a、b两点与图1中q、p两点分别对应;与图3中a、b两点分别对应。通过不同图像之间的转换,得出对应的关系,使学生对不同图像的相互关系一一理清,能使学生对于沉淀溶解平衡的图像触类旁通。
(2)关于溶液混合问题,分析Qc、Ksp的关系,得出有无沉淀析出。通过数据对比分析、推理等方法得出不同图像间的异同,建立思维模型的认知能力,解决陌生情境下的复杂问题。
三、结语
笔者从常见的沉淀溶解平衡图像进行归纳总结,通过图形转换思想,让学生掌握其中的相互关系,特别在图像的分析上应注意以下两点:
1.解读图像的角度
从曲线上的特殊点(起点、拐点、交点、终点等)、曲线的纵横坐标(图像的类型)及曲线的走势进行分析。微观角度分析溶液中微粒及离子浓度的变化及转化等,从而形成直观的解题的思路。
2.采用数学函数关系,剖析图像信息的规律和本质
借助数学工具,利用函数关系对图像中的数据进行处理,得出自变量、因变量及无关变量之间的关系,同时设置必要的辅助线,进一步加深学生对控制变量的理解,明确不同图像间的联系和解决此类问题的方法。
责任编辑钱昭君
——饱和溶液与不饱和溶液

