源于生活的课前初探
——饱和溶液与不饱和溶液
◎
一、饱和溶液和不饱和溶液
实验1:在室温下,往杯中倒半杯水,挖取一勺食盐放入水中,再用筷子搅拌,观察现象;等溶解后,再加入一勺食盐,搅拌,观察现象;重复上述操作,直至加入最后一勺食盐,用筷子搅拌后仍有白色固体不溶,数一数,你一共加了多少勺食盐? 请记录在表中。继续往杯中再加半杯水,搅拌,观察现象并填写下表。
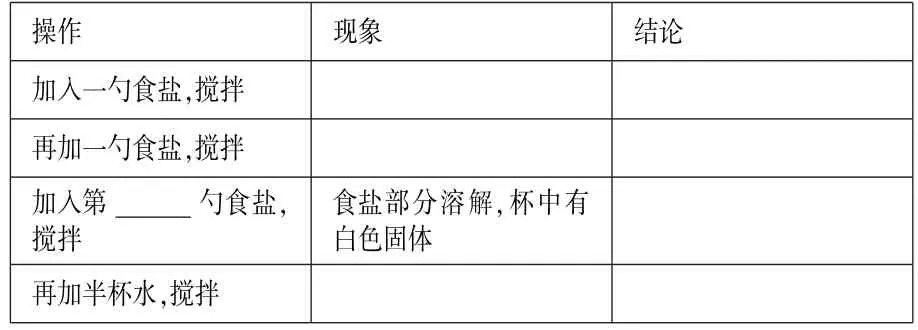
问题与思考:室温下,食盐可否无限制地溶解在一定量的水中?
实验2:在室温下,往杯中加入一定量的水,每次放一颗方糖,直到完全溶解,再加入第二颗。请你数一数,加入第几颗时,方糖不能全部溶解在水中?
往另一杯中加入相同量的热开水,重复上述实验操作,加入与冷水中相同颗数的方糖,观察并记录现象,待热水冷却后,再观察。



仔细观察现象并填写下表。
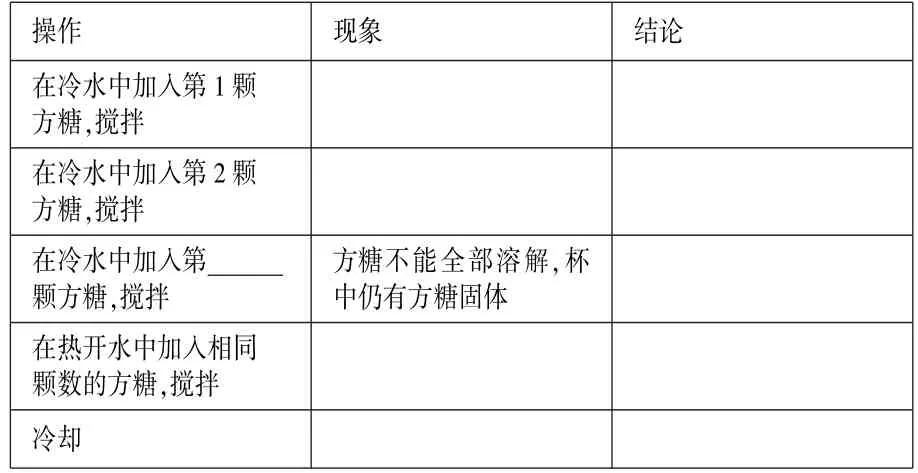
问题与思考
1、在一定温度下,方糖可否无限制地溶解在一定量的水中?
2、杯中水的温度越高,最多能溶解的方糖颗数如何变化?
应急保障是有效开展减灾抢险救援的基础支撑。一些城市缺乏对灾时抢险和平时战备的应急保障要求,尤其是一些北方城市,多年未经历过暴雨洪水考验,防灾减灾意识薄弱,应急抢险队伍、防洪抢险设施和物资储备都有待加强。部分城市防洪应急预案中对通信、信息、供电、运输、物资设备、抢险队伍等的保障措施不够明确,抢险人员和队伍缺乏技术培训和应急演练,严重影响在灾害发生后第一时间进行应急处置。
就像我们饥饿的时候需要吃东西一样,如果还能吃下食物,则说明我们还没吃饱;如果我们再也吃不下食物了,则说明我们已经吃饱了。在一定温度下,向一定量溶剂里加入某种物质,当物质不能继续溶解时,所得到的溶液叫做这种物质的饱和溶液;还能继续溶解该物质的溶液,叫做这种物质的不饱和溶液[1]。
思考与练习
1.根据实验1 现象,填写表格。


2.根据实验2 现象,填写表格。
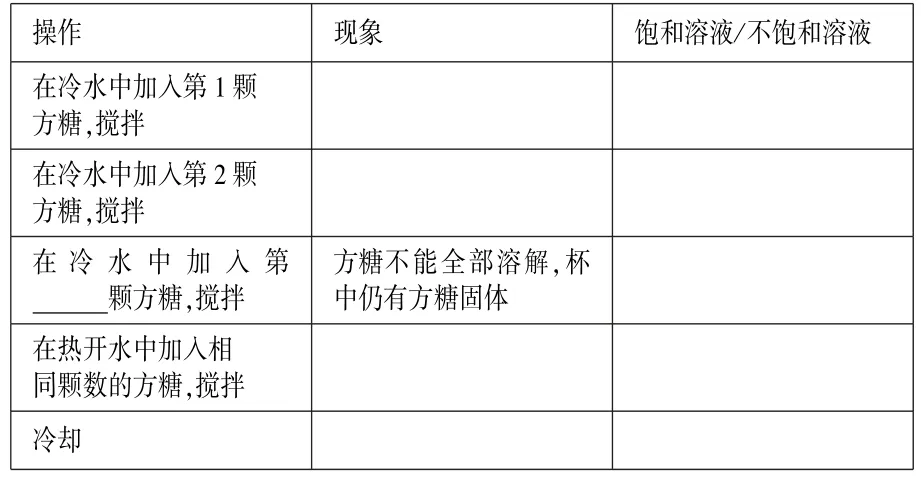
方法指导与学习:
1、通过生活中的小实验,抽象概括出化学概念,既熟悉又容易理解;
2、饱和溶液与不饱和溶液的概念需注意如下要点:①两个限定条件:一定温度,一定量的溶剂(通常为水);②物质在溶剂中能否继续溶解;③得到的溶液为该物质对应的饱和或者不饱和溶液(对象很重要)。
为了帮助学生理解概念中的第三个要点,补充实验3:在饱和的食盐水中加入一小颗方糖,观察方糖的溶解情况。
通过实验可知,饱和食盐水还可以再溶一小颗方糖,所以原来的溶液不是方糖的饱和溶液。也就是说某物质的饱和溶液对于其他物质而言,不一定是其他物质的饱和溶液。所以在提到饱和溶液与不饱和溶液时应注意所溶解的物质,即“这种物质的饱和溶液”或“这种物质的不饱和溶液”[1]。
二、饱和溶液与不饱和溶液的转化
在实验1 中,若食盐能继续溶解,则溶液不饱和;若食盐不能再溶解而有剩余,则溶液达到饱和;再加水,剩余的食盐继续全部溶解,溶液又从饱和变成不饱和。由此可见,饱和溶液与不饱和溶液之间可以相互转化,在某物质的不饱和溶液中继续增加该物质,不饱和溶液可以变成饱和溶液;而在它的饱和溶液中继续加水(溶剂),则饱和溶液可以变成不饱和溶液。
如果不饱和溶液减少水(溶剂),是否可以变成饱和溶液呢? 在我们生活中就有这样的例子,如海水晒盐,就是利用涨潮将部分海水贮存到水池中,待海水澄清后引入到蒸发池,经过风吹日晒,使水分部分蒸发,到一定程度后再将这部分蒸发水分的海水引入结晶池,海水继续被风吹日晒,慢慢由不饱和溶液变成饱和溶液,然后食盐晶体渐渐从海水中析出,得到粗盐[1]。海水晒盐的过程,其实就是通过蒸发水(溶剂),将食盐的不饱和溶液变成饱和溶液。
在实验2 中,加入相同颗数的方糖,在冷水中不能继续溶解而有剩余,此时得到的是饱和溶液,在热开水中方糖全部溶解,溶液是不饱和的;当热水冷却后有方糖固体析出,溶液又从不饱和变成饱和。由此可以得出:一般情况下,某物质的饱和溶液通过升高温度可以变成不饱和溶液,通过降低温度可以由不饱和溶液变成饱和溶液。上述关系总结如下:

课后练习与拓展
1、饱和溶液一定是浓溶液,不饱和溶液一定是稀溶液吗?
2、上网查阅并观看课外趣味实验:热冰实验。
——以硫酸铜饱和溶液析出晶体的计算为例

