猪霍乱沙门菌C500株的检定及安全性评价
王秀丽, 张 媛, 李 建, 辛凌翔, 李俊平, 蒋玉文, 罗玉峰
(中国兽医药品监察所, 北京海淀100081)
猪沙门菌病又称仔猪副伤寒,具有高度适应性和专嗜性,只侵害猪[1]。主要是由猪霍乱沙门菌、猪霍乱沙门菌Kunzendorf变型、猪伤寒沙门菌(S.typhisuis)、猪伤寒沙门菌Voldagsen变型、鼠伤寒沙门菌(S.typhimuriru)、德尔卑沙门菌(S.derby)和肠炎沙门菌等血清型引起。本病常引起较高的死亡率,其中败血型病死率达90%,慢性型病死率达25%~50%,本病传播快,死亡率高[2]。自20世纪60年代以来,仔猪副伤寒活疫苗的研究和应用对本病的预防起到了重要作用。
仔猪副伤寒活疫苗生产用菌株为猪霍乱沙门菌C500株[3],该菌为猪霍乱沙门菌C78-2株(CVCC79102)在含有醋酸铊的培养基中筛选出的弱毒株[4],本研究对该菌种进行了全面检定并对其安全性进行评价。
1 材料与方法
1.1 菌种 猪霍乱沙门菌C500株(CVCC79500,1967年2月23日冻干,F1)、猪霍乱沙门菌C78-2株(CVCC79102,1990年3月16日冻干,F5代)[4],均由中国兽医药品监察所菌种保藏中心提供;仔猪副伤寒活疫苗,批号:201710,由中牧实业股份有限公司江西生物药厂生产。
1.2 培养基及试剂 普通琼脂培养基、普通肉汤培养基、硫盐(TG)、TSB、生理盐水、5% 蔗糖脱脂牛奶、肉肝胃膜消化汤,均购自北京中海生物技术有限公司;细菌生化鉴定试纸条,购自法国生物梅里埃股份有限公司;沙门菌O7因子血清,购自丹麦国家血清研究所(SSI);革兰染色液,购自山东奥博星生物技术有限公司。
1.3 实验动物 SPF级ICR系小鼠、清洁级日本大耳白兔、健康易感断奶仔猪,均购自四川省实验动物专委会养殖场。
1.4 菌种复苏、冻干 用1967年2月23日冻干的猪霍乱款沙门菌C500株(F1代),繁殖并冻干1批菌种,批号:20190122(F2代)。具体繁殖及冻干方法参照猪霍乱沙门菌C78-2株的制备及检定[5]。
1.5 菌种的检定
1.5.1 真空度、纯粹、剩余水分 均按现行《中国兽药典》[6]进行检验。
1.5.2 形态、培养特性、血清学特性和生化特性 按照《中华人民共和国兽用生物制品规程》二〇〇〇版的标准进行检定[3]。
1.5.3 特异性 用接种环取普通琼脂平板上的单菌落接种含1% 醋酸铊的普通肉汤10 mL,37 ℃培养24 h,观察生长情况。
1.5.4 安全性 健康易感断奶仔猪的筛选:取10份 体重15 kg以上健康断奶仔猪的血清,置于56 ℃ 灭能30 min,冷却至室温后,与猪霍乱沙门菌C500抗原做平板凝集试验,其血清与抗原不凝集的猪为健康易感断奶仔猪。
挑取20190122批冻干菌普通琼脂平板上典型的单菌落接种普通琼脂斜面小管,37 ℃培养24 h,将普通琼脂斜面培养物接种于4支中管,37 ℃培养24 h,用普通肉汤将菌苔洗下,充分振荡混匀后对菌液进行计数,将菌液置于2~8 ℃保存,根据计数结果,将置于2~8 ℃保存的菌液稀释至5×108CFU/mL,皮下注射10只小鼠,0.2 mL/只,观察21 d;将菌液稀释至1×1010CFU/mL,皮下注射5只兔子,1 mL/只,观察21 d;将菌液稀释至3×109CFU/mL,静脉注射4头 体重15 kg以上的健康易感断奶仔猪,1 mL/头, 观察30 d[3]。
本试验同时设2个试验组,试验1组:从仔猪副伤寒活疫苗中分离C500株,按照上述方法制备成1×1010CFU/mL, 注射4只家兔,1 mL/只;试验2组: 按《中国兽药典》[6]的规定,将仔猪副伤寒活疫苗稀释至2头份(根据活菌计数的结果,2头份的菌数约为1×1010CFU/mL),注射4只家兔,1 mL/只,均观察21 d。
1.5.5 免疫原性试验 按照安全性试验的方法制备注射菌液,用普通肉汤将菌液稀释至2.5×109CFU/mL, 肌内注射5只体重1.5~2 kg的兔,1 mL/只, 30 d后与条件相同的5只对照兔皮下注射肉肝胃消化汤培养2代的猪霍乱沙门菌C78-2强毒菌液2~4个 最小致死剂量,观察30 d。
最小致死剂量测定:在免疫原性试验攻毒前21 d测毒。将肉肝胃消化汤培养2代的猪霍乱沙门菌C78-2株用肉肝胃消化汤稀释至10、15、20 CFU/mL和25 CFU/mL,各剂量的菌液均皮下注射与免疫原性试验同批次的兔子,观察21 d,记录测毒兔子的死亡情况,对死亡兔进行剖检,记录剖检病变。
2 结果
2.1 真空度、纯粹、剩余水分 冻干的150支菌种按现行《中国兽药典》[6]附录进行纯粹检验,148/150呈白色或粉色或紫色辉光,2支无真空的菌种121 ℃高压30 min处理;随机抽取5支真空度测定良好的菌种进行纯粹检验,5/5纯粹;剩余水分测定结果为0.9%、0.2%、0.3%、0.7%,均小于4.0%。真空度、纯粹、剩余水分测定结果均符合规定。
2.2 形态、培养特性、血清学特性和生化特性 C500株在普通琼脂平板上37 ℃培养20 h,菌落为圆形、边缘整齐、突起、半透明、略湿润的光滑型,革兰阴性小杆菌,普通琼脂平板上的新鲜培养物与沙门菌O7因子血清出现典型的凝集反应(呈片状凝集),均符合《中华人民共和国兽用生物制品规程》[3]的规定。
生化鉴定结果符合细菌分类学中沙门菌的生化特性,但因经过醋酸铊的压力筛选,部分生化特性与其驯化前的菌株C78-2株不一致(表1),说明糖发酵能力较C78-2株有所下降,该结果与仔猪副伤寒活疫苗的研究报告中的描述有差异。
2.3 特异性 猪霍乱沙门菌C500株在含1%的醋酸铊的普通肉汤中均匀混浊生长。将10%的醋酸铊按10%的比例加入普通肉汤时,因蛋白质遇重金属变性形成大量白色沉淀属正常现象,不影响C500株生长。
2.4 安全性 批号为20190122的C500株小鼠安全检验:在接种后21 d内10/10健活,符合质量标准的规定。
兔安全检验初次检验:兔4/5存活,1/5死亡,不符合质量标准的规定;重检:5/5存活,符合质量标准的规定。具体死亡、剖检及细菌分离结果见表2。死亡兔的剖检结果与C500株驯化之前的母株C78-2株一致。试验1组兔4/4存活,注射部位有小结节;试验2组兔1/4死亡,死亡的兔注射部位有2 cm×3 cm的破溃,3/4兔有约4 cm×3 cm×3 cm的肿块。结果表明:疫苗的冻干保护剂对其安全性有影响。
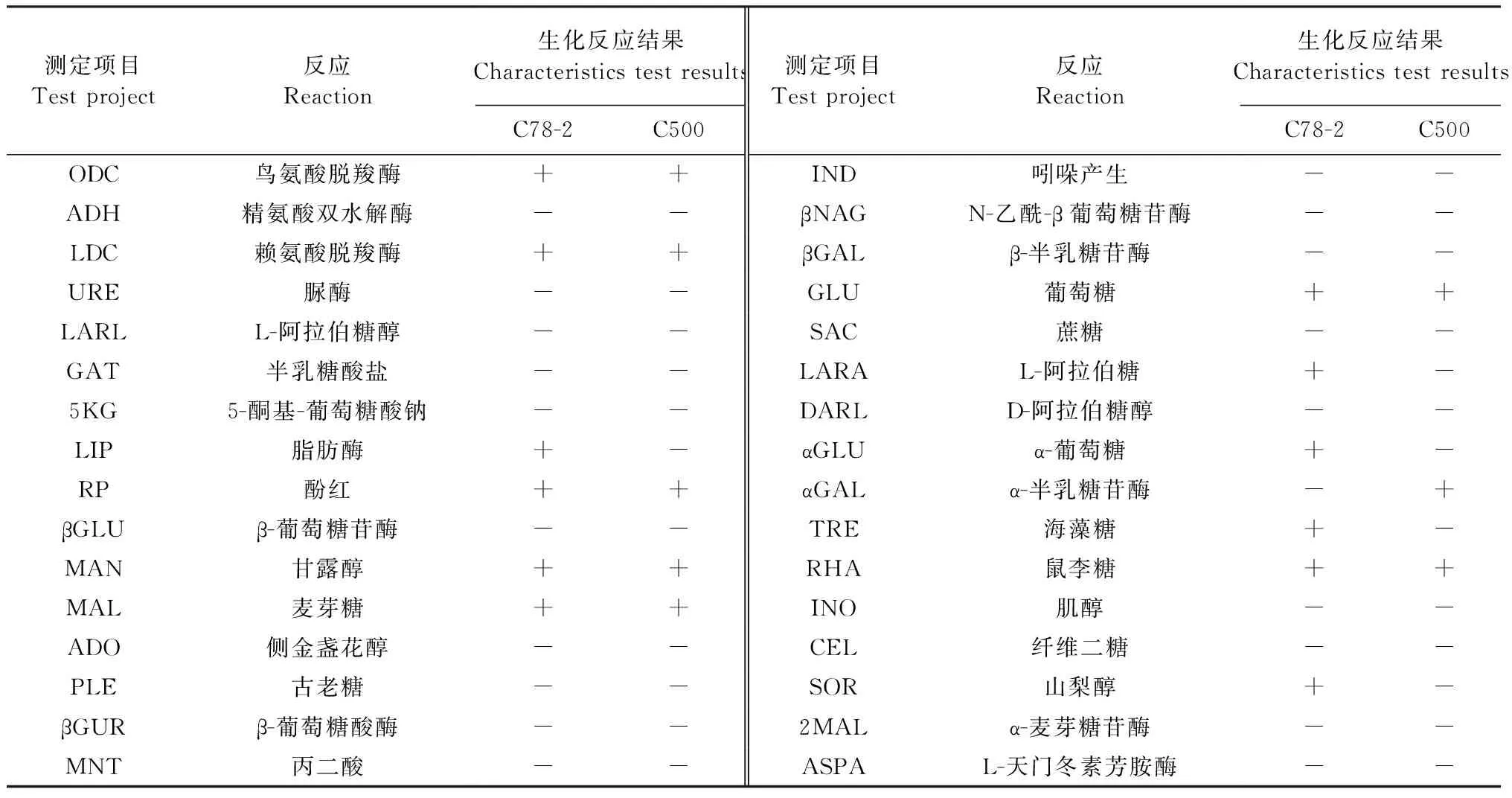
表1 C78-2株与C500株生化特性比较Table 1 Characteristics compare of C78-2 and C500 strain

表2 兔子安全检验结果Table 2 Safety test results on rabbits
猪安全检验初次检验:1/4死亡,死亡猪极其消瘦;剖检结果显示:腹腔有积液,肝脏肿大且表面和背面均可见大量纤维素性渗出和淤血点,胃黏膜脱落,胃壁变薄,弹性差,肠壁黏膜脱落,肠壁变薄,肠系膜与腹腔内脏粘连,脾脏肿大,表面有大量纤维素性渗出;胸腔有大量纤维素性渗出,肺脏出血,胸腔脏器粘连。1/4精神不振,食欲减退,消瘦、跛行、喜卧至卧地不起,后逐渐恢复至可站立,攻毒30 d后剖检,可见胸腔脏器与胸壁严重粘连。2/4精神不振、食欲减退,消瘦。未死亡的猪检验结束后剖检可见胃黏膜脱落,胃壁变薄,弹性差。重检猪与初次检验为同一批,注射时比初次检验大14 d,重检结果为猪4/4存活,精神食欲及增重情况明显差于未免疫猪,安全试验结束后剖检可见胸腔由大量纤维素性渗出,胸腔器官严重粘连,腹腔器官正常。
2.5 免疫原性试验 C78-2株的测毒结果显示,其对兔子的最小致死剂量(MLD)为15 CFU/只,按照质量标准,5只免疫组和5只对照组分别攻C78-2株30 CFU/只(2MLD),30 d后,免疫组5/5保护,对照组5/5死亡,符合质量标准的规定。C78-2株测毒结果见表3,C500株免疫原性试验攻毒保护结果见表4。
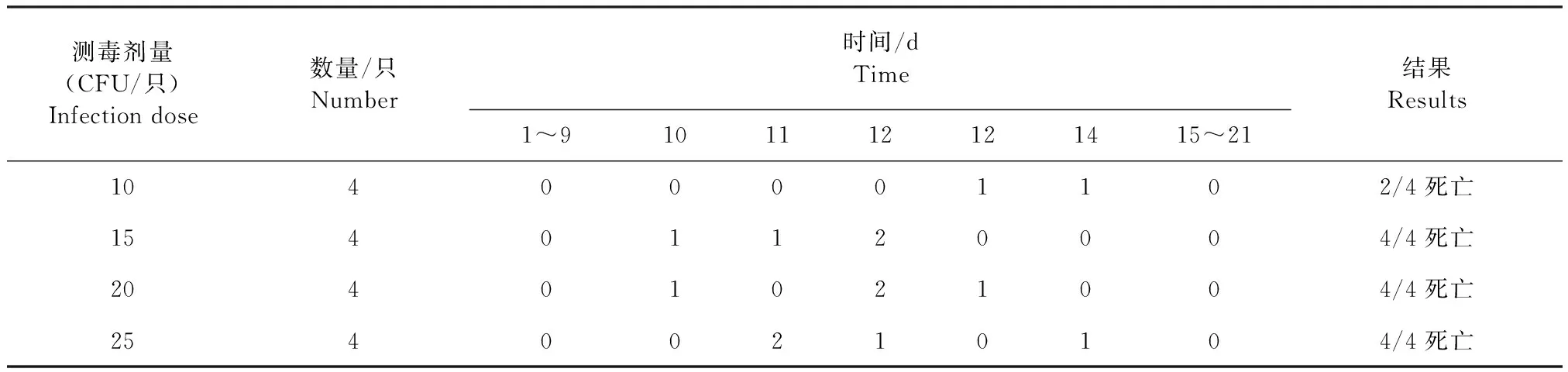
表3 猪霍乱沙门菌C78-2株测毒结果Table 3 Virulence test results of Salmonella choleraesuis,C78-2 strain

表4 免疫原性试验攻毒保护结果Table 4 Immunogenicity test results of challenge protection
3 讨论
20100324批仔猪副伤寒C500株菌种(F3代,中国兽医药品监察所2010年检定冻干),检定记录中显示安全检验初次检验小鼠10/10存活,兔子3/5存活,2/5死亡,重检兔子10/10存活,猪4/4存活。20190122批菌种(F2代),安全检验初次检验小鼠10/10存活,兔子4/5存活,猪3/4存活,重检兔子5/5存活,猪4/4存活。死亡兔和猪的剖检典型病变基本一致,且死亡兔子的病变与其驯化前的母株C78-2株测毒兔的剖检病变完全一致。说明猪霍乱沙门菌C500株的安全性不够好。重检猪与初次检验用猪为同一批次,注射时比初检猪大14 d,与初次检验猪注射相同剂量其健康状况明显优于初次检验猪,经查阅1978年的研究报告汇编,该菌种对于断奶仔猪是安全的,但对哺乳仔猪是有一定毒力。20世纪60-70年代的养殖模式与现在不同,研究报告中断奶仔猪是指56~74日龄,哺乳仔猪为27~45日龄,现在断奶仔猪一般不足25日龄,但增重比在19世纪的养殖模式下快,现在满足质量标准中体重和断奶仔猪要求的猪在之前的定义下依然是哺乳仔猪,这也是导致本次安全检验结果与质量标准不符的主要原因。该结果对于仔猪副伤寒活疫苗的临床应用有重要的指导意义。
仔猪副伤寒活疫苗的成品检验中安全检验无本动物试验,且安全检验仅需用2只兔子进行检验,标准为存活。以往监督检验或复核检验中该产品安全检验的兔子经常出现注射部位破溃的现象,因此,只满足质量标准的规定无法保证该疫苗的安全性。根据近几年对仔猪副伤寒活疫苗监督抽检及复核检验的结果,生产的仔猪副伤寒活疫苗活菌数一般在3.5×109~5.5×109CFU/头份,甚至更高,而该菌种安全检验猪静脉注射3×109CFU/头即可死亡或严重影响其健康状况,因此不能为满足活菌计数的要求盲目增加疫苗活菌数。建议对该产品使用后的安全性进行调研,对该菌种制备疫苗的安全性和最低有效免疫剂量进行评价,结合临床应用情况,修订安全性和活菌计数质量标准。

