钠-葡萄糖共转运蛋白2 抑制剂的心脏和肾脏保护作用及其潜在机制
林毅,彭永德
上海交通大学附属第一人民医院内分泌代谢科,上海 200080
心血管疾病(Cardiovascular Diseases,CVD)是糖尿病患者最常见的死亡原因[1]。研究表明,与非糖尿病患者相比,2 型糖尿病(Type 2 Diabetes Mellitus,T2DM)患者发生心血管(Cardiovascular,CV)事件的风险增加2~3 倍[2],全因死亡率和CV 死亡率也显著增高[3]。糖尿病肾脏疾病(Diabetic Kidney Disease,DKD)是糖尿病主要的微血管并发症之一,可导致终末期肾病(End-stage Renal Disease,ESRD)并增加糖尿病患者的死亡风险[4]。钠-葡萄糖共转运蛋白2 抑制剂(Sodium-glucose Cotransporter 2 Inhibitors,SGLT2i)是一类新型口服降糖药物,通过抑制近端肾小管的SGLT2,减少肾小管对葡萄糖的重吸收,增加尿液中葡萄糖的排泄而发挥降糖作用。除降糖以外,SGLT2i 还能减轻体重、降低血压、降低血尿酸、减少尿蛋白排泄以及降低心血管事件风险并改善肾脏转归等[5],其中SGLT2i 的心、肾保护作用及相关的潜在机制近年来引起了广泛关注并被不断探索,本文将针对这一内容进行综述。
1 SGLT2i 心血管及肾脏获益的临床研究
近年来,一系列探讨SGLT2i 对心血管、肾脏结局影响的研究结果相继揭晓。2015 年公布的首个SGLT2i 的心血管结局研究(Cardiovascular Outcomes Trials,CVOT)EMPA-REG OUTCOME 显示,恩格列净可使合并动脉粥样硬化性心血管疾病(Arteriosclerotic Cardiovascular Disease,ASCVD)的T2DM 患者主要心血管不良事件[(Major Adverse Cardiovascular Events,MACE)心血管死亡、非致死性心肌梗死或非致死性卒中]风险下降14%,CV 死亡风险下降38%,心衰住院(Hospitalization for Heart Failure,hHF)风险下降35%,新发肾病及肾病恶化风险下降39%。2017 年卡格列净的心血管结局研究(CANVAS Program)结果显示,卡格列净可使合并CVD(65.6%)或伴多重CV 危险因素(34.4%)的T2DM 患者MACE 风险下降14%,hHF风险下降33%,肾脏复合终点事件[估算肾小球滤过 率(Estimated Glomerular Filtration Rate,eGFR)持续降低40%、需进行肾脏替代治疗或肾脏性死亡]风险下降40%。2018 年底公布的评估达格列净CV结局的DECLARE-TIMI 58 研究,作为同类研究中纳入人群最广(入组17 160 例患者)且纳入一级预防患者比例最高(40.6%合并ASCVD,59.4%伴多重CV 危险因素)的CVOT,其研究人群特征更加贴近真实世界中T2DM 伴CVD 患者的比例与特点。该研究设置双重主要终点,即“MACE”以及“CV死亡/hHF”,此外还预设了肾脏结局的关键次要复合终点。研究结果显示,与安慰剂相比,达格列净的MACE 结果未达到统计学差异,但显著降低CV死亡/hHF 复合终点达17%,肾脏硬终点事件[eGFR持续降低≥40%至<60 mL/(min·1.73 m2)、新发ESRD 或因肾脏/CVD 导致的死亡]的风险下降47%。随后,在2019 年3 月公布的DECLARETIMI 58 首个预设亚组分析的结果显示,达格列净使既往有心肌梗死病史的T2DM 患者MACE 风险显著下降16%[6]。DECLARE-TIMI 58 的肾脏分析结果也显示,达格列净显著降低肾脏硬终点事件风险,并在伴有微量白蛋白尿和大量白蛋白尿患者中得出一致结果;同时可使eGFR 降低[(持续降低≥40%至<60 mL/(min·1.73 m2)]的风险下降达46%[7],证实达格列净能预防和延缓肾脏疾病的进展。
2019 年4 月,新用SGLT2i 患者心血管疗效比较研究(CVD-REAL)作为首个评估初次使用SGLT2i的T2DM 患者心衰住院和全因死亡风险的大型真实世界研究公布了关于肾脏结局的最新结果。该研究纳入的25 814 例使用SGLT2i(其中57.7%使用达格列净、34%使用恩格列、5.9%使用卡格列净)的患者中超过90%的患者肾功能正常或者轻度受损[eGFR >90和eGFR 60~90 mL/(min·1.73 m2)]。该研究结果证实,SGLT2i 在真实世界广泛人群能够有效延缓eGFR 的下降,显著降低肾脏相关事件风险[降低肾脏复合终点(eGFR 下降50%或发生ESRD)风险达51%,降低ESRD 风险达67%][8],这与既往RCT 的研究结果一致。同期,另一项以肾脏结局为主要终点的CREDENCE 研究结果显示,卡格列净可使研究主要终点(ESRD、血清肌酐倍增、肾脏或心血管死亡)的发生风险降低30%[9]。一项Meta 分析通过对SGLT2i CVOT 的综合分析得出了一致的结果:达格列净、卡格列净和恩格列净具有心、肾安全性获益的类效应[10]。
2019 年9 月,一项探讨SGLT2i 心衰治疗结局的研究DAPA-HF 结果公布,显示在T2DM 与非T2DM 患者中,在标准心衰药物治疗的基础上,达格列净可使射血分数降低的心衰(Heart Failure With Reduced Ejection Fraction,HFrEF)患者心衰恶化或CV 死亡风险下降26%,且能够改善患者的生活质量。
2 SGLT2i 心肾保护作用的潜在机制
2.1 SGLT2i 的心血管获益潜在机制
2.1.1 对心室负荷的作用SGLT2i 的渗透性利尿和排钠作用,可直接减少血容量、降低血压,继而减少心室前、后负荷,改善心衰症状、保护心功能,但SGLT2i 所致的渗透性利尿与传统利尿剂存在根本不同。充血性心力衰竭患者水肿明显,SGLT2i可减少组织间液容量,不会引起代偿性交感神经激活,能够限制血管收缩反应[11],改善血容量。此外,SGLT2i 不会引起电解质紊乱、高尿酸血症或肾血流动力学不良反应。这些区别可能是SGLT2i 和传统利尿剂心血管作用差异的原因。除了对血容量的影响,SGLT2i 还可以改善内皮功能和主动脉硬化指数,并通过激活电压门控钾离子通道和蛋白激酶G 诱导血管舒张,减轻心脏负荷。
2.1.2 对心脏代谢和生物能量的作用在糖尿病和/或心衰的情况下,心脏过度依赖游离脂肪酸作为能量生成的底物,导致游离脂肪酸中间体的累积,增加脂毒性,损害心肌细胞肌浆网钙摄取,促进心脏舒张功能障碍的进展。在高血糖状态下,糖尿病患者心肌摄取的葡萄糖超过其氧化能力,增加心脏负担。T2DM 患者使用SGLT2i 时,能量代谢方式会发生转变,机体脂肪氧化增加,脂肪氧化终产物乙酰辅酶A 会转变为酮体供心肌利用,提高心肌工作效率[12]。也有研究认为,轻度β-羟丁酸升高可减少氧化应激,刺激线粒体生物合成,稳定细胞膜电位,减少心律失常发生[13]。因此,酮体的有效利用可能是SGLT2i 心血管获益的潜在机制之一。
2.1.3 对Na+/H+离子的影响Na+/H+交换器(Sodiumhydrogen Exchanger,NHE)作为一种质膜结合的反载体,在生理条件下对维持细胞内pH 和离子稳态
起着至关重要的作用。糖尿病合并心衰时,心肌NHE1 表达增加,心肌细胞胞质内Na+和Ca2+水平升高,线粒体内Ca2+浓度降低,引起心肌功能障碍。SGLT2i 可抑制心肌NHE1 表达,降低细胞质Na+和Ca2+浓度,升高线粒体内Ca2+水平,逆转造成心衰的电解质异常[14]。由于心肌并无SGLT2 受体的表达,因此SGLT2i 影响心肌细胞NHE 表达的机制尚未明确。此外,NHE3 参与介导肾小管Na+重吸收,而心衰时肾小管NHE3 表达增加。已有研究显示,SGLT2i 可下调近端小管NHE3 活性,促进Na+排出,恢复体内Na+平衡,改善心衰[11]。
2.1.4 对心肌纤维化的作用心肌纤维化在心衰发展过程中发挥重要作用。研究显示,SGLT2i 达格列净可通过RONS/STAT3 信号通路促进M2 型巨噬细胞的活化,减少心肌纤维细胞浸润,从而减缓心肌纤维化进程[15]。在心肌梗死后3 d 的小鼠中使用SGLT2i,可显著提高STAT3 活性、STAT3 核易位、心肌白介素10(Interleukin 10,IL-10)水平和M2型巨噬细胞浸润率。到心肌梗死后第28 d,小鼠心肌成纤维细胞浸润和心肌纤维化显著减少。
2.1.5 对脂肪因子的影响脂肪因子的产生或作用改变是心血管疾病发展和胰岛素抵抗的常见机制,尤其是在肥胖患者中。血管周围和心外膜组织的异位脂肪沉积,改变了脂肪因子在心肌上的旁分泌调节,与心衰的发生有关。临床研究数据显示,SGLT2i 能显著降低血清瘦素和炎性细胞因子IL-6 水平,升高抗炎脂肪因子脂联素水平。另一项临床研究发现,达格列净可降低心外膜脂肪组织的体积,这与心衰发展的进程有关[11]。因此,SGLT2i 可能通过恢复促炎/抗炎脂肪因子之间的平衡,调节钠以及心脏炎症和纤维化的病理生理作用[16]。
2.1.6 对动脉硬化进程的作用动脉硬化是导致心血管疾病的重要危险因素。Chilton 等[17]研究发现T2DM 患者使用恩格列净后可降低脉压差,下调动态动脉硬化指数,这意味着SGLT2i 减轻了动脉硬化。缓解动脉硬化进程也可能是SGLT2i 心血管获益的潜在机制之一。
2.2 SGLT2i 肾脏保护的潜在作用机制
2.2.1 血流动力学假说对于糖尿病患者,高血糖和高血压在肾小球损伤的发病机制中起关键作用,肾小球高滤过是DKD 的危险因素[18]。糖尿病患者近端小管SGLT2 表达上调,肾小管重吸收葡萄糖/Na+增加,使到达致密斑的Na+浓度下降,低Na+进入可减少强效的血管收缩剂腺苷的释放,从而使入球动脉扩张引起肾小球囊内压升高和高滤过。SGLT2i阻断葡萄糖/Na+在近端小管重吸收,提高达到致密斑的Na+浓度,恢复被抑制的管-球反馈,促进入球小动脉收缩,降低肾小球囊内压及减轻高滤过[19,20],发挥肾脏保护作用。SGLT2i 的CVOTs 中,治疗组eGFR 随时间的变化与这一血流动力学假说一致。SGLT2i 治疗的最初几周,eGFR 出现一过性下降,之后eGFR 在几周内趋于回归基线,此后保持稳定。研究结束时,SGLT2i 治疗组eGFR 显著高于安慰剂组。这一现象与肾素-血管紧张素-醛固酮系统(Renin-angiotensin-aldosterone System,RAAS)阻断剂对eGFR 的影响相似。
2.2.2 对肾小管葡萄糖重吸收的作用氧化应激、炎症和纤维化在DKD 的发病机制中发挥着关键作用。肾小管可通过SGLT2 蛋白使葡萄糖的转运增加,可能促进炎症和纤维化,进而引发DKD。体外研究表明,SGLT2i 可在肾小管-间质中改善氧化应激、炎症和纤维化,从而发挥肾脏保护作用[18]。但这些研究数据由于动物模型不同而具有异质性,SGLT2i对肾小管的调控究竟是直接作用还是血液动力学或改善代谢引起的间接作用,目前尚无确切结论。
2.2.3 缺氧假说过量的葡萄糖重吸收会增加近端小管的氧需求,致使肾小管间质缺氧,而肾小管间质缺氧是导致ESRD 的主要原因[21]。间质缺氧使受损肾小管周围的成纤维细胞转分化为肌成纤维细胞,减少红细胞生成素(Erythropoietin,EPO)的产生,导致肾性贫血和肾脏间质纤维化。SGLT2i抑制葡萄糖重吸收,减轻近端小管负担并改善肾小管间质缺氧,通过逆转上述转分化,使成纤维细胞恢复正常的EPO 产生并限制肾纤维化[20]。因此,SGLT2i 可能通过改善肾小管间质缺氧发挥肾脏保护作用[21]。
2.2.4 对肾小囊脏层上皮细胞的作用肾小囊脏层上皮细胞(足细胞)受损在白蛋白尿的发生机制中起关键作用。正常条件下SGLT2 不存在于肾小球内,但可在足细胞中表达。在由牛血清白蛋白(Bovine Serum Albumin,BSA)诱导小鼠蛋白尿的肾小球疾病模型中,SGLT2i 达格列净通过对足细胞的直接作用改善了白蛋白负荷诱导的细胞骨架重塑,从而改善肾小球病变[22]。因此推测,SGLT2i 可减少蛋白尿并改善足细胞的功能障碍或丢失。
2.2.5 对RAAS 信号通路的作用SGLT2i 的渗透性利尿和排钠作用能够激活RAAS[23]。对于使用RAAS 阻断剂的患者,经典的肾素-血管紧张素II-AT1 受体途径被阻断,这时联用SGLT2i 则激活Ang-(1-7)和Ang-(1-9)及AT2 受体信号通路,发挥抗氧化和抗纤维化作用,从而使接受SGLT2i和RAAS 阻断剂联合治疗的患者肾脏获益[20]。
2.3 SGLT2i 的心脏、血管和肾脏保护的可能机制
2019 年Verma 等[24]基于糖尿病的CV 风险和肾脏事件,提出将糖尿病患者的心脏、血管、肾脏比喻成泵、管道及和过滤器,通过这种模拟水动力学的理论,对SGLT2i 的心脏、血管和肾脏作用全面进行了剖析。Zelniker 等[25]基于SGLT2i 的CVOT 荟萃分析提出,T2DM 患者面临泵、管道和过滤器的三重威胁,其证据表明,无论患者是否伴有ASCVD、慢性肾脏病(Chronic Kidney Disease,CKD)或心衰,SGLT2i 均应作为T2DM 患者继二甲双胍之后的一线治疗。这种“泵、管道和过滤器”的概念对SGLT2i 的心、肾保护潜在机制的探讨具有重要意义(图1)。
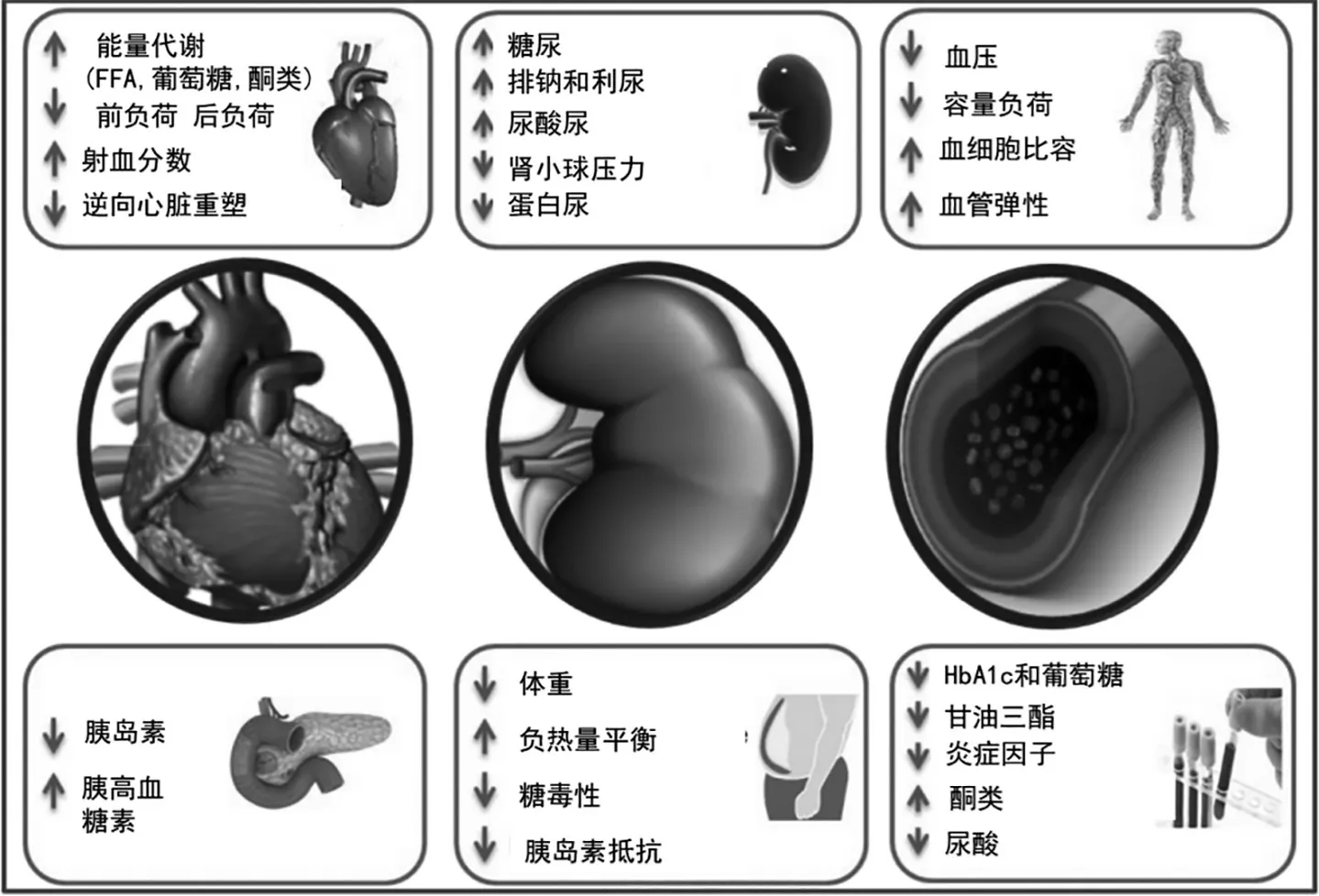
图1 SGLT2i心脏、肾脏和血管保护作用的主要潜在机制
Giugliano 等[26]还在此基础上增加了“水槽”(机体全身)的部分,强调SGLT2i 具有改善泵(减少心衰和主要CV 事件)、管道(减少血管炎症和CV 风险因素)、过滤器(降低肾小球滤过率的下降)和水槽(有益的代谢和血液动力学效应)的功能(图2),而这些效应已远超出其降糖作用的获益。目前已开展了两项在非糖尿病患者中验证SGLT2i 心肾获益的大型临床研究,其中近期已公布结果的DAPA-CKD 研究评估了达格列净对CKD 患者肾脏结局和心血管死亡影响,该研究在疗效和安全性的常规评估中显示达格列净的获益比预期更早出现,证明CKD 患者无论是否合并T2DM,达格列净均可显著降低主要终点事件(eGFR 下降≥50%或发生ESRD 或CV/肾病死亡)的风险(发生率降低39%)[27]。
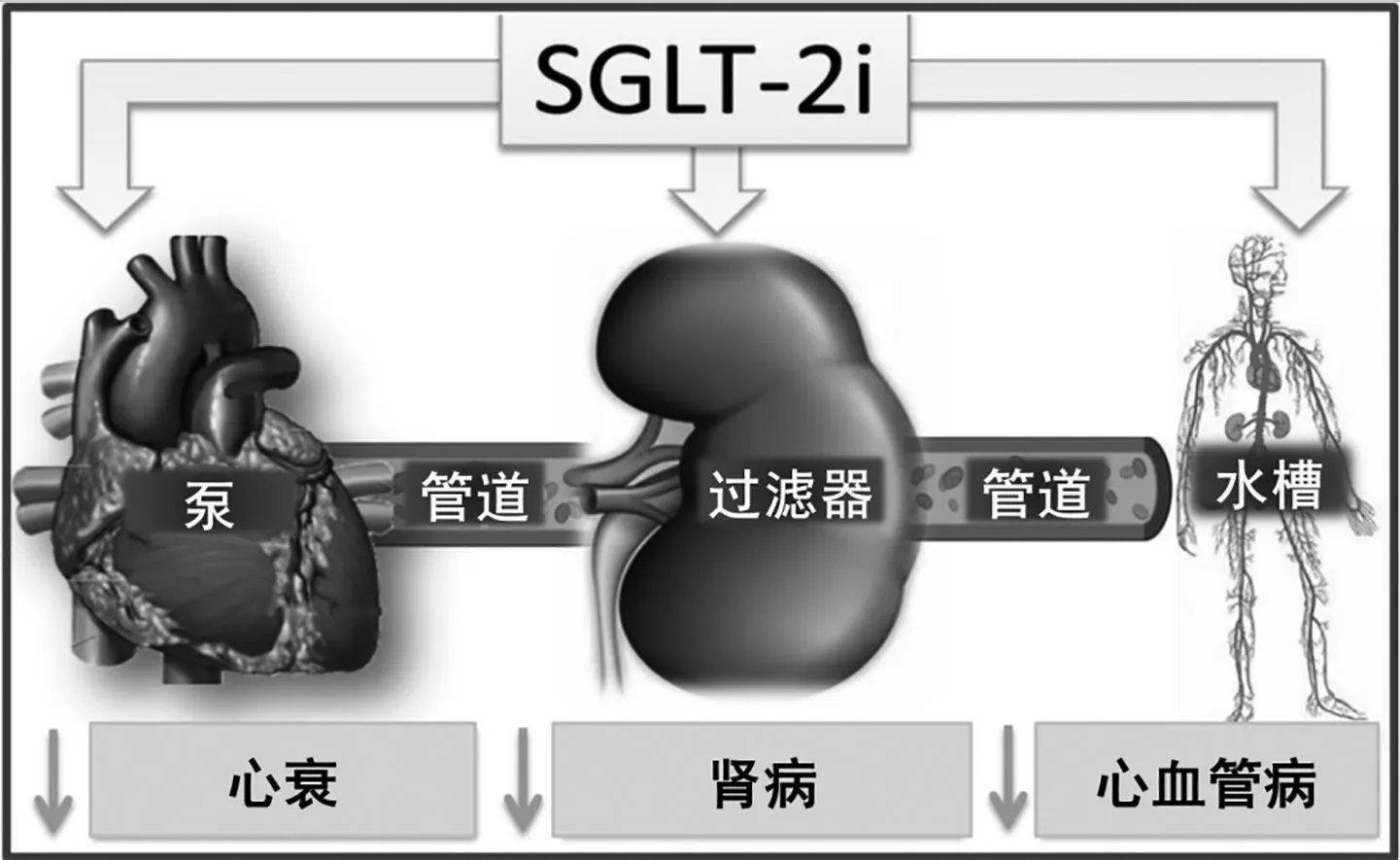
图2 泵(心脏)、管道(血管)、过滤器(肾脏)和水槽(全身)的模拟图
3 结语
降低糖尿病患者心血管风险和肾脏损伤是糖尿病临床管理的关键,需要重视。新型口服降糖药物SGLT2i,降糖疗效与二甲双胍相当,并具有减重、降压和改善代谢的作用,在具有心血管风险和确诊心血管疾病的T2DM 患者中能降低心血管及肾脏事件的发生风险。虽然相关机制尚未完全明确,但现有的研究已经看到了SGLT2i 独特的心肾保护作用。目前SGLT2i 仍有多项心血管和肾脏相关临床、基础研究正在进行,这些数据有望证明SGLT2i 在糖尿病及非糖尿病患者中心血管、肾脏早期保护中的巨大临床价值,也将深化对SGLT2i 的认识,开拓更广阔的临床应用前景,为更多的患者带来获益。

