尖晶石LiMn2O4纳米棒的合成和储锂性能
周钢,陈月皎,范洪波
(1.东莞理工学院生态环境与建筑工程学院,广东东莞,523808;2.中南大学粉末冶金国家重点实验室,湖南长沙,410083)
锂离子电池具有能量密度、功率密度较高,使用寿命长以及环境友好的特点,被广泛应用于电子产品中[1-3],而尖晶石结构的锰酸锂(LiMn2O4)成本低、资源丰富、环境友好,是最具潜力的锂电正极材料之一[4]。LiMn2O4属于AB2O4型化合物,空间群为Fd3m,其中,氧原子呈面心立方最密堆积排布,锂离子占据着1/8的四面体空隙,锰离子交替位于氧原子密堆积的八面体间隙位置[2,5],是一种具有三维通道的嵌入化合物,具有较高的储锂理论容量(148 mA·h/g)。然而和其他电池正极材料相比,其能量密度相对较小,化学稳定性较低,尤其是存在着以下几个问题:1)Mn3+的Jahn-Teller效应,会造成晶格畸变,破坏结构,导致循环性能变差;2)放电末期Mn3+的歧化反应,生成的Mn2+溶于电解液中,造成活性物质减少,降低电池电性能[6-8]。为了改善LiMn2O4的电化学性能,常用的方法有包覆、阳离子掺杂、纳米化尺寸等[4-5,9-14]。目前常见的制备锰酸锂的方法有水热法[11]、模板法[10,15]、固相合成法[16]等。传统的固相法制备的LiMn2O4一般是微米级别,为了合成出纳米尺寸的LiMn2O4,本文作者选用水热法制备的α-MnO2作为前驱体,与LiOH·H2O固相烧结合成纳米棒形貌的LiMn2O4,研究水热反应时间、温度和反应物物质的量比对前驱体α-MnO2形貌结构和性能的影响。
1 实验部分
1.1 正极材料的制备
水热合成α-MnO2,然后将其与LiOH·H2O 在氩气下进行固相烧结制备出纳米棒状结构的锰酸锂。
1.1.1 α-MnO2的制备
α-MnO2的形貌结构主要受到水热反应温度、时间及反应物物质的量比的影响。因此实验设计了反应温度、反应时间、反应物物质的量比3个对照组来探究合成α-MnO2纳米线的最佳实验条件。
水热反应反应方程式为
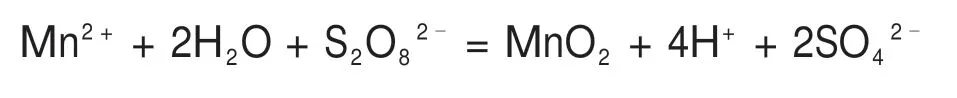
按照物质的量比为1:1:2 将Mn(CH3COO)2·4H2O,(NH4)2S2O8和(NH4)2SO4加入烧杯中,加入60 mL 去离子水,搅拌至完全溶解。将混合均匀的溶液移至100 mL 的反应釜内进行水热反应。反应结束后将获得的α-MnO2分别在去离子水和乙醇溶液中洗涤并干燥(100 ℃,12 h)。
1.1.2 尖晶石LiMn2O4的合成
将α-MnO2纳米线与LiOH·H2O 在管式炉中固相烧结,制备出尖晶石结构锰酸锂纳米棒。
固相烧结反应方程式为
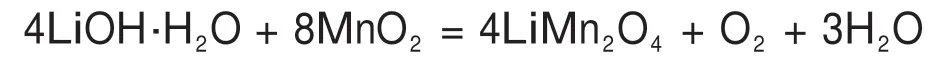
将物质的量比为1:2 的LiOH·H2O 和α-MnO2放入小烧杯,在140 ℃反应12 h,四水乙酸锰、过二硫酸铵、硫酸铵的物质的量比为1:1:4,滴加5 mL无水乙醇,于搅拌器上搅拌至乙醇完全挥发。然后将样品于管式炉中,在480 ℃固相烧结10 h,升温速率为1 ℃/min。
1.2 材料表征
采用场发射扫描电镜(SEM,NOVA NANO SEM230)和透射电子显微镜(TEM,TECNAI G2 F20)分析形貌和结构。采用X 射线衍射分析仪(XRD,日本Rigaku公司)分析材料物相,辐射源采用CuKα(λ=1.54056×10-10m),扫描范围为10°~85°。
1.3 电化学性能测试
按质量比7:2:1 称取制备的LiMn2O4纳米棒、Super-P(导电剂)和PVDF(聚偏氟乙烯,黏结剂)。研磨LiMn2O4和Super-P的混合物,加入溶有PVDF的N-甲基吡咯烷酮(NMP)中,搅拌12 h 后涂于铝箔,在60 ℃下真空干燥12 h,在冲压机上冲成直径为12 mm 的圆形极片并称质量。电池组装在充满氩气的手套箱中进行,水氧质量分数控制在0.5×10-6左右,采用Celgard 2400 作为锂电隔膜,金属锂片作负极,采用高压电解液(碳酸乙烯酯(EC)+碳酸二甲酯(DMC)),组装成CR2025型半电池。
循环性能、倍率性能和充放电曲线在蓝电测试系统(LANHE CT2001A,武汉蓝电电子有限公司生产)上进行,循环伏安曲线(CV)在电化学工作站上以0.1 mV/s速率测试(电压为3.5~4.3 V)。
2 结果与讨论
2.1 不同实验条件对制备α-MnO2的影响
2.1.1 反应时间对合成α-MnO2的影响
固定反应温度(120 ℃)和反应物物质的量比(四水乙酸锰、过二硫酸铵、硫酸铵的物质的量比为1:1:2),设置8组反应时间(4,6,8,10,12,24,36,48 h)进行水热反应。所得产物的SEM形貌图如图1所示。
从图1可以看出,随着水热反应时间的延长,α-MnO2的形貌结构发生较大变化。反应4 h时,大部分α-MnO2以纳米球状形态存在,只有很小一部分为纳米线,说明在此时纳米线已经开始形成。当反应进行到8 h时,已经可以看到大量的线状结构,但是纳米线比较短,说明此时纳米线已经形成,但是还没有长全。反应10~12 h时,可以发现纳米线逐渐变长变细,反应12 h 时,纳米线已经完全长好。当反应时间超过24 h 时,可以发现纳米线变粗,发生团聚。随着反应时间进一步延长到,团聚现象更加严重。由此可知,制备α-MnO2最佳反应时间为12 h。
图2所示为不同反应时间的XRD图谱。从图2可以看出,反应时间为4,6,8,10和12 h的反应产物都能较好地对应α-MnO2的标准PDF卡片,但是在20°~30°之间有许多小杂峰,这些杂峰随着反应时间的增长而逐渐消失,这些杂峰可能是反应的中间产物。当反应进行到12 h 以上时,杂峰已经基本消失。这说明此时反应已经进行完全。因此,选择12 h 作为反应时间可以获得α-MnO2的纯相。另外,随着反应时间的延长,峰强比逐渐提升,说明α-MnO2的结晶度逐渐提升。
2.1.2 反应温度对合成α-MnO2的影响
固定反应时间(12 h)和反应物物质的量比(四水乙酸锰、过二硫酸铵、硫酸铵的物质的量比为1:1:2),设置3 组反应温度(80,140 和180 ℃)进行水热反应,所得产物的SEM形貌图如图3所示。
从图3可看出,水热反应温度为140 ℃时得到的纳米线结构最好,纳米线的长度为1~3 μm,宽度为25~30 nm。当反应温度为80 ℃时,纳米线粗细长度不均匀,较为杂乱,这说明在80 ℃/12 h的条件下,纳米线还没有完全长好。而在反应温度为180 ℃时,纳米线结构已经被破坏,这说明反应时间12 h用180 ℃的反应温度过高。在反应温度为140 ℃时得到的纳米线长径比大,粗细均匀,因此,水热反应的温度应当设定在140 ℃左右。
2.1.3 反应物物质的量比对合成α-MnO2的影响
固定反应时间(12 h)和反应温度(140 ℃),设置四水乙酸锰、过二硫酸铵、硫酸铵的物质的量比分别为1:1:0,1:1:1,1:1:3,1:1:4 共4 组试验,进行水热反应。所得产物的XRD图谱如图4所示。

图1 不同水热反应时间制备的α-MnO2的SEM照片Fig.1 SEM images of α-MnO2 obtained with different reaction time
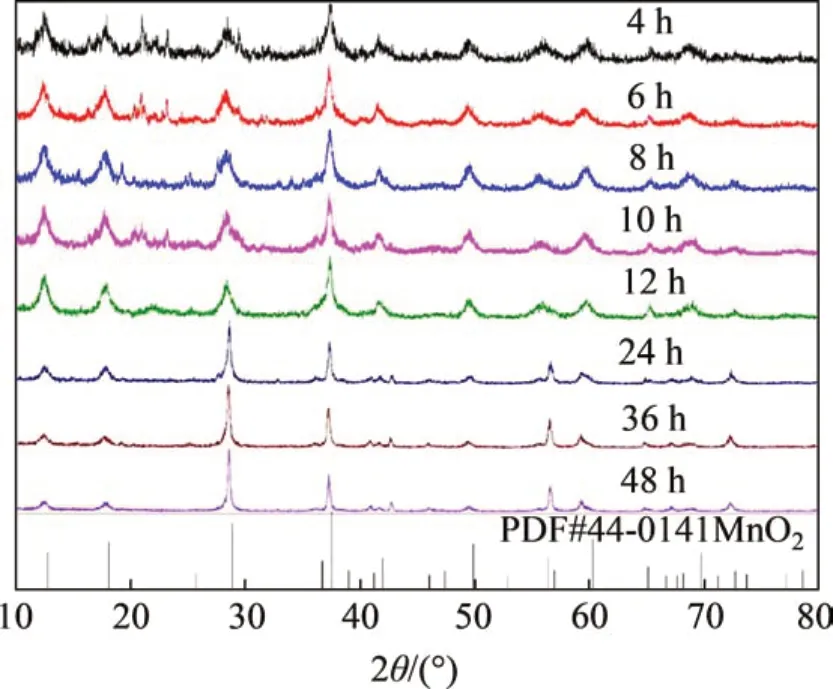
图2 不同水热反应时间的XRD图谱Fig.2 XRD patterns of α-MnO2 obtained with different reaction time
从图4可知,当不加入硫酸铵时(物质的量比为1:1:0),MnO2的晶型为β 型。当加入硫酸铵时,得到了α 晶型的MnO2。α-MnO2是由八面体[MnO6]为基础单元组成的2×2 型晶体,而β-MnO2是由八面体[MnO6]为基础单元组成的1×1型晶体,因此β-MnO2要比α-MnO2更加稳定。当没有外界影响因素的干扰时,α-MnO2会自发地转变为β-MnO2。加入盐就是为了阻止这种相变的发生。当加入了阳离子,如K+,NH4+,H3O+,Ba2+,Na+时,这些阳离子浓度足够大时就会有很大的概率进入到2×2型晶体孔道中,使得α-MnO2相得以稳定存在。另外,阳离子主要是控制MnO2的晶型,而阴离子主要是控制MnO2的形貌。

图3 不同反应温度制备的α-MnO2的SEM照片Fig.3 SEM images of α-MnO2 obtained at different reaction temperatures
图5所示为不同反应物物质的量比的SEM 照片。从图5(a)可以看出:MnO2为纳米棒状结构。阴离子如F-,促使了纳米线结构的形成,其机理如下:由于F-具有很强的电负性,它可以吸附在β-MnO2的(100)及(200)晶面,导致这2 个晶面的生长受阻,从而形成了纳米线状结构。而由于的离子半径较F-的大,因此会优先吸附在Mn2+浓度较低的(100)面,主要抑制了(100)晶面的生长。因此,当阴离子为得到的MnO2为截面为方形的纳米线结构(图5(b)~(d))。另外,由于的离子半径较大,它还会降低离子的扩散速率,使得加入硫酸盐得到的产物比加入其他盐的产物小。从图5还可以发现,四水乙酸锰、过二硫酸铵、硫酸铵的物质的量比为1:1:4 时得到的纳米线结构更好。因此,四水乙酸锰、过二硫酸铵、硫酸铵的最佳物质的量比为1:1:4。
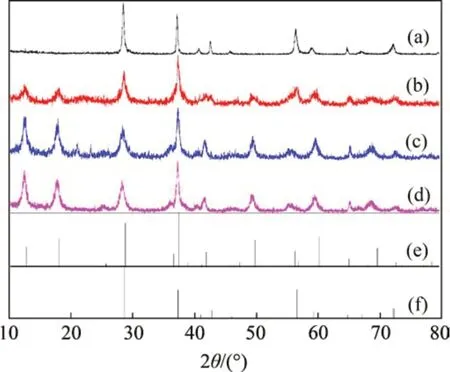
图4 不同硫酸铵比例产物的XRD图谱Fig.4 XRD patterns of products obtained with different ratios of reactants

图5 不同反应物比例的SEM照片Fig.5 SEM images of products obtained with different ratios of reactants
通过设置实验对照组,最终确定了水热温度140 ℃,水热反应时间12 h,四水乙酸锰、过二硫酸铵、硫酸铵的物质的量比1:1:4 时可以得到最佳的α-MnO2纳米线结构。对此条件下合成的α-MnO2纳米线进行TEM表征,如图6所示。
图6(a)中标记的晶面间距为0.690 nm,与标准PDF 卡片的(110)晶面间距相符,即在纳米线生长的过程中,(100)晶面的生长受到限制,晶体延<110>方向生长,与前述的纳米线生长机理“吸附在(100)晶面上限制晶面生长”一致。从图6(b)和(c)可得:纳米线结构直径为10~30 nm,长度为1~2 μm。由图6(d)可见:产物的衍射花样为明锐的衍射亮点,说明α-MnO2结晶性非完美。
2.2 LiMn2O4纳米棒的表征
2.2.1 LiMn2O4的形貌分析
图7所示为制备的LiMn2O4SEM 照片。从图7可以看出,LiMn2O4为纳米棒状结构,较为分散且均匀。纳米棒长1~4 μm,宽约125 nm,比前驱体α-MnO2的宽度大。纳米棒表面有小颗粒,同时还有一些细小的纤维,推测是在烧结过程中纳米线被烧断产生的。
图8所示为LiMn2O4超高分辨率图和选区电子衍射花样。从图8(a)可知,测得晶面间距为0.294 nm,根据标准PDF 卡片PDF#35-0782 得知,尖晶石锰酸锂的(220)晶面间距为0.291 45 nm,因此可以判定此晶面为(220)晶面。从图8(b)可见,衍射花样为明亮的光斑,说明制备的LiMn2O4具有良好的结晶结构。
2.2.2 LiMn2O4的XRD分析
图9所示为LiMn2O4纳米棒的XRD图谱。由图9可知,所有峰均能和标准锰酸锂标准PDF卡片对应,并且没有其他杂峰存在,说明制备出了较纯的尖晶石结构锰酸锂。
2.2.3 LiMn2O4的电化学性能
图10(a)所示为LiMn2O4放电速率1C下循环1圈,50 圈,100 圈,200 圈时的充放电曲线。从图10(a)可以发现2 个明显的在4 V 左右的放电平台,分别代表充放电过程中的2 个相变过程,即LiMn2O4/Li0.5Mn2O4和Li0.5Mn2O4/γ-MnO2。
图10(b)所示为LiMn2O4在3.5~4.3 V 的电压区间内以1C倍率充放电的循环性能,循环圈数为287圈。可见:首圈的充电比容量为119.9 mA·h/g,放电比容量为104.8 mA·h/g。首圈效率为87%。在第一圈结束后,库仑效率快速升至接近100%。首次不可逆容量比例为11%。当循环100圈时,放电比容量为91.8 mA·h/g,容量保持率为87.6%。当循环150 圈时,放电比容量为88.5 mA·h/g,容量保持率为84.4%。当循环圈数到250 圈时,放电比容量为77.2 mA·h/g,容量保持率为73.7%。

图7 尖晶石锰酸锂SEM照片Fig.7 SEM images of spinel LiMn2O4

图8 LiMn2O4 HRTEM照片及选区电子衍射花样Fig.8 HRTEM image and SAED of LiMn2O4

图9 LiMn2O4纳米棒的XRD图谱Fig.9 XRD pattern of LiMn2O4 nanorods
图10(c)所示为LiMn2O4的倍率性能。可见,LiMn2O4在放电速率0.5C和1C时还保持着很好的容量,其中,放电速率1C下,放电结束时还保持着93%的容量,但是当放电速率上升到3C以上时,容量衰减很快。当放电速率3C时,电池保持75%的容量,5C时,保持49%的容量,当放电速率10C和20C时,分别只有30%和13%的容量。这说明制备得到的LiMn2O4纳米棒正极材料无法在超大倍率放电。分析原因可能是在较大倍率的充放电过程中,锂离子来不及进入四面体空位而进入到八面体空位,导致形成了Li2Mn2O4。此时锰离子主要以三价存在,Jahn-Teller效应非常明显,尖晶石锰酸锂的晶体结构发生改变为四方晶系,锂离子的三维扩散通道受到阻碍,导致材料的容量下降。另外,当充放电速率过大时,会导致锰酸锂发生团聚,从而导致锂离子扩散困难,容量下降。
图10(d)所示为LiMn2O4的CV曲线,扫描速度为0.1 mV/s,电压范围为3.5~4.3 V。从图10(d)可见2对非常明显的氧化还原峰,说明锂离子在尖晶石锰酸锂中的嵌入和脱嵌分2步进行。这与放电速率1C时的充放电曲线相符。第一组氧化还原峰在4.05/3.93 V,代表了一半的锂离子从四面体空位嵌入或是脱嵌。第二组氧化还原峰在4.19/4.06 V,代表了另一半的锂离子从四面体空位嵌入或是脱嵌。图中的氧化还原峰都非常尖锐并且分离良好,这说明制备得到的锰酸锂具有良好的结晶度。正极与负极的氧化还原峰的电压差代表了电池的极化程度。电压差(0.12 V)小说明锰酸锂纳米棒具有较小的锂离子迁移阻抗,有利于该材料的倍率放电性能。
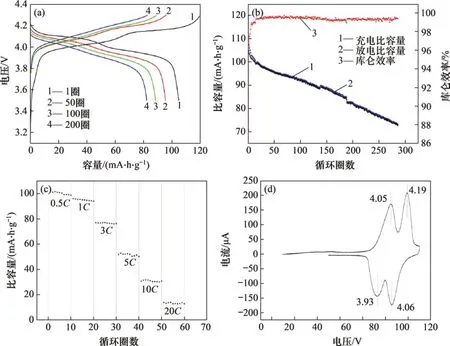
图10 LiMn2O4的电化学性能Fig.10 Electrochemical properties of LiMn2O4
3 结论
1)以水热法合成了α-MnO2纳米线前驱体,最终确定制备α-MnO2纳米线结构的最佳反应条件为水热温度140 ℃,水热反应时间12 h,四水乙酸锰、过二硫酸铵、硫酸铵物质的量比1:1:4。以最佳条件制备的α-MnO2纳米线作为模板,成功地制备了尖晶石结构的LiMn2O4纳米棒。
2)制备的LiMn2O4纳米棒具有较好的结晶性和较大的长径比,有利于缩短Li+扩散距离,可减少循环过程中材料的团聚。
3)制备的LiMn2O4纳米棒在离子迁移过程中具有较低的阻抗和极化,有利于脱嵌锂过程中的电化学动力学,充放电测试过程中表现出的良好的倍率性能和循环性能。

