6种允许总误差对20个生化项目建立个性化质量控制方案的影响*
闫玉珠,王冀邯,赵和平,吕 静
西安交通大学附属红会医院检验科,陕西西安 710054
六西格玛(6σ)是一种高度精炼的管理方法,它克服了管理者对自身质量过于乐观的评估,而且检测过程的性能和风险可以被量化,各质量指标的不良率可转换为σ水平,便于比较[1-3]。6σ允许对整个过程进行全面的质量评估。目前已有一些研究使用σ指标评估了常规化学分析的性能[4-5]。但因为允许总误差(TEa)来源广泛,因此,本研究综合6种TEa来源,分别计算它们对20个项目σ水平分析性能的差异,为临床生化实验室的质量持续改进提供客观证据。
1 资料与方法
1.1一般资料 20种临床常规化学分析指标包括酶、总蛋白(TP)、电解质、脂质。分别为碱性磷酸酶(ALP,速率法/AMP缓冲液)、丙氨酸氨基转移酶(ALT,速率法)、天门冬氨酸氨基转移酶(AST,速率法)、γ-谷氨酰基转移酶(GGT,速率法)、淀粉酶(AMY、酶底物法-麦芽七糖苷)、乳酸脱氢酶(LDH,速率法L-P)、肌酸激酶(CK,速率法)、TP(双缩脲终点法)、清蛋白(ALB,溴甲酚绿法)、总胆红素(TBIL,重氮法)、葡萄糖(GLU,己糖激酶法)、肌酐(CREA,苦味酸法-无空白补偿)、尿酸(UA,尿酸酶比色法)、尿素(UREA,脲酶紫外速率法)、胆固醇(CHOL,胆固醇氧化酶法)、三酰甘油(TG,甘油磷酸氧化酶-过氧化物酶法),钾、钠、氯(K、Na、Cl,离子选择性电极间接法)、钙(Ca,偶氮砷Ⅲ法)。除TG和CHOL来自中国浙江东瓯外,其余均为罗氏原装试剂。
1.2仪器与试剂 德国罗氏cobas 8000全自动生化分析仪,试剂、校准品和质控品为原装试剂(质控品水平1批号:324196;质控品水平2批号2:250280)。除TG和CHOL试剂来自中国浙江东瓯外,其余均为罗氏原装试剂。
1.3数据来源
1.3.1TEa 本研究使用了6种不同的TEa指标来了解TEa对σ指标估计值的影响,TEa选取来源:(1)基于生物学变异(Bio)最低、适中和最佳TEa,可以搜索http://www.westguard.com);(2)TEa选择从1988年的美国临床实验室改进法案修正案(CLIA′88)要求,可以搜索https://www.westgard.com/clia.htm;(3)TEa来自我国行业规范临床生物化学检验常规项目分析质量指标(WS/T403-2012);(4)TEa选自国家胆固醇教育计划(NCEP)[6-7];(5)TEa选自德国RiliBK质控指南(RiliBK 2008);(6)TEa选择来自澳大利亚皇家病理学家学院(RCPA)的质量保证项目[8-9]。在Bio数据中,TEa是由个体内和个体间的Bio得出的,公式如下,其中CV为变异系数,CVI为受试者内Bio,CVG为受试者间Bio,Bias为偏倚[4,10]。
最低:CV<0.75CVI,Bias<0.375(CVI2+CVG2)0.5,TEa<1.65×0.75CVI+0.375(CVI2+CVG2)0.5;
适中:CV<0.5CVI,Bias<0.25(CVI2+CVG2)0.5,TEa<1.65×0.5CVI+0.25(CVI2+CVG2)0.5;
最佳:CV<0.25CVI,Bias<0.125(CVI2+CVG2)0.5,TEa<1.65×0.25CVI+0.125(CVI2+CVG2)0.5
1.3.2不精密度评估 不精密度以CV%表示,由本实验室2019年1—10月间累积的质控数据确定。严格按照文献[11]标准操作规程,进行双水平质量控制。采用Westgard多规则(13s/22s/R4s/41s/8x)[12]进行评判。
1.3.3Bias计算 2019年本实验室参与3次室间质量评价计划。每个项目包含5个水平样本。首先取5个样本的Bias均值,然后取3次Bias均值作为最终Bias(%)。Bias=[(测量值-目标值)/目标值]×100%。
1.4分析性能评估
1.4.1σ计算 按照标准方程计算,标准方程为σ=(TEa-|Bias|)/CV[13]。
1.4.2质量目标指数(QGI) QGI反映了方法的精密度和准确性,可帮助确定质量改进的优先措施。每个测试项目的QGI采用公式QGI=Bias(%)/(1.5×CV)[14]计算。若QGI<0.8,则应先提高精密度。如果QGI>1.2,则应首先提高准确度。若0.8≤QGI≤1.2,则精密度和准确度均需提高。QGI是一个良好的指标,可以用来确定实验室的质量水平没有达到6σ的原因。
1.4.3标准化σ性能验证图 TEa被看作100%,过点(0,100)和(16.67,0)划线,这两个点与6σ线相对应。(0,100)和(20,0)对应于5σ线。(0,100)和(25,0)对应于4σ线。点(0,100)和(33.33,0)对应于3σ线。这4条性能线将图分为5个区域。从左到右5个区域分别是6σ区、5σ~<6σ区、4σ~<5σ区、3σ~<4σ区、<3σ区。然后,标记每个项目的操作点:横坐标是CV/TEa,纵轴是Bias/TEa。
2 结 果
2.16种TEa标准的西格玛指标 6种不同来源的TEa目标值进行的20个项目的σ水平,见表1、2。不同TEa标准下的σ指标对比分析,见表3。Bio(最佳TEa)标准最严格,只有 ALT、GGT、CK、TG 4项超过3σ水平,见图1。RiliBK 2008的 TEa标准最宽松。18个项目中,有17个项目超过了3σ水平,12个项目显示σ>6,见图2。

图1 来自于Bio(最佳TEa)标准化性能验证

图2 来自于RiliBK 2008 TEa标准化性能验证

表1 两个批次使用Bio来源的TEa计算的σ
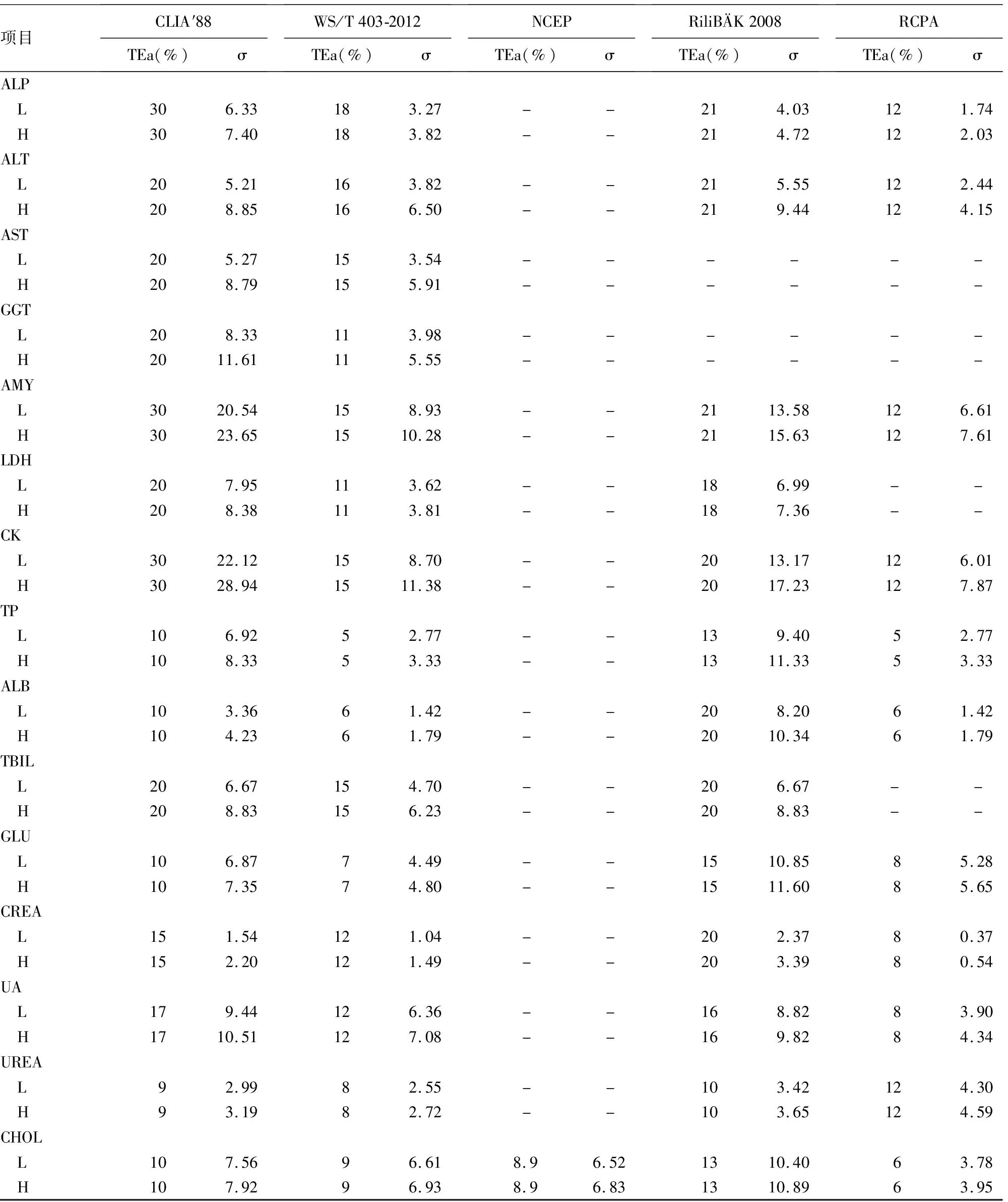
表2 两个批次分别使用5种不同来源的TEa计算的σ

表3 不同TEa的σ指标水平比较[n/n(%)]
2.2质量目标指数以及质控方案 低水平的CV(CVL)高于高水平的CV(CVH),因此,σ指标和QGI由CVL来判断。20项化验的质量指标和质量改进措施见表4。AMY、CK、UA、TG、CHOL超过6σ水平;因此,它们只需要使用13s规则。TBIL、GLU、K、Na显示σWS/T403-2012<5,因此,它们应该遵守13s/22s/R4s/41s规则。剩下的项目没有到达3σ水平,应该遵守最严格的规则。同时,因TBIL、GLU、CREA、UREA、Cl、Ca的QGI<0.8,所以提示精密度需要提高,而0.8 表4 20个生化项目的质量目标指数及质量控制规则 根据1999年国际临床化学联合会和国际标准化组织技术委员会建立的分级系统,基于Bio的质量规范处于2级分级系统,NCEP质量规范处于三级分级系统,CLIA′88为四级分级系统[15-16]。基于Bio的质量规范更客观、更贴近临床需要,是最严格的质量规范。本研究根据Bio(最佳 TEa)标准,只有CK、TG超过6σ,按Bio(适中TEa)标准,GGT、CK、AMY、UA、CHOL、UREA、TG超过6σ标准,而按Bio(最低TEa)标准,19个项目中有12个项目超过6σ标准。HENS等[9]研究表明,Bio(最佳TEa)并不被推荐,因为对许多实验室来说,很难达到此水平。 CLIA′88规范以内部质量评价为基础,具有易理解、易获取的优点。然而,它是基于经验而不是适当的标准。建立评价标准的目的是确定少数未能通过检测的实验室,而不是确定临床要求的质量水平。因此,它可接受的范围相对较广。本研究85%的项目超过3σ,65%的项目超过6σ。例如,按照Bio(最佳 TEa)中TP的σ度量仅为1.3,而根据CLIA′88TEa标准,TP的σ值为6.92,说明TP的TEa太宽,不能按照CLIA′88来计算。NCEP脂质测定标准化专家组对血清总胆固醇(TC)、TG、高密度脂蛋白胆固醇(HDL-C)、低密度脂蛋白胆固醇(LDL-C)等脂质指标的分析提出了质量要求。因此,TC、TG的TEa是从NCEP中选取的。RiliBK 2008和RCPA项目的质量规范也基于Bio。然而,RCPA TEa标准明显比RiliBK 2008 TEa标准更严格。本研究根据RiliBK 2008 TEa 标准,94.4%的实验项目达到了3σ以上,66.7%的实验项目达到了6σ以上。根据RCPA TEa标准,只有50%的实验项目达到了3σ以上,18.8%的实验项目达到了6σ以上。而WS/T 403-2012更加客观、实用,适用于我国的大多数临床实验室的室间质量评价及室内质量控制。 目前,为了更好地评估性能分析,临床实验室可以为每个项目匹配合适的TEa,这样就可以避免由于过于宽泛的标准而得出过于乐观的估计或由于过分严格的标准而加重实验室负担不必要的质量控制。同时,还可以根据不同的测试,采用不同的质量控制程序,以正确地解释其测量程序的准确性和精密度。总的来说,本研究通过对6种来源的TEa计算出的σ进行分析,并结合本实验室实际情况,为更好地利于室内质控和室间质评的发展,每个项目都选择其适合的TEa标准。σ较高便选择略严格标准,σ较低即选择略微宽松的标准。其中TC和CHOL的TEa取自NCEP标准,ALB和Cl的TEa取自 CLIA′88标准,TP的TEa取自Bio(最低TEa),其他项目的TEa来自WS/T 403-2012标准。 在Westgard 多规则下,AMY、CK、UA、TG和CHOL均超过6σ,因此,这些项目只需遵守13s质量控制规则;TBIL、GLU、K和Na并未达到5σ,仍需要遵守13s/22s/R4s/41s规则;剩余项目未达到4σ,所以需要遵守更严格的质量控制规则。同时,ALT、AST、TP、GGT、LDH、ALB、K和Na需要改进精密度和准确度,TBIL、GLU、CREA、UREA、Cl和Ca需要改进精密度。鉴于这些项目中存在的问题,有几个改进计划有待实施。如定期进行维修和校准,加强检查员的技术和理论培训,增强责任感,检查试剂、校准品及质控品是否过期或失效。CREA 的σ仅为2.37,其中可能的原因是目前使用苦味酸法-无空白补偿,无法溯源到国际标准。下一步考虑对肌酐的检测方法进行改进。同时,对离子电极进行定期维护和更换,保证仪器的稳定性可以提高K、Na和Cl的准确度。 综上所述,使用6σ质量管理,全面评价整个实验过程,可帮助临床实验室测试分析系统性能,已经设定的质量目标是否满足要求,以及选择合适的室内质量控制计划为研究者节省大量人力、物力和时间。同时,选择正确的TEa来源和计算正确的σ也很重要。
3 讨 论

