部分脾动脉栓塞术联合内镜治疗门脉高压症合并中重度食管胃静脉曲张破裂出血的疗效分析
徐佰国,王凤梅,韩涛,李隽
食管胃静脉曲张(esophageal and gastric varices,EGV)破裂出血是肝硬化患者最严重的并发症之一,有高病死率、高复发率的特点[1]。食管静脉曲张套扎术(esophageal variceal ligation,EVL)、胃静脉曲张硬化术(gastric variceal sclerotherapy,GVS)治疗已成为防治EGV出血的首选治疗方案[2],但不能降低门静脉压力,需反复治疗,再出血率高。部分脾动脉栓塞术(partial splenic embolization,PSE)是治疗门静脉高压症(portal hypertension,PH)伴脾功能亢进的微创介入治疗方法,不仅可改善脾功能亢进,还有助于降低门静脉压力,现已逐渐取代了脾切除术[3]。本文回顾分析我院2013—2017年应用内镜下EVL/GVS联合PSE及内镜下EVL/GVS治疗肝硬化伴中重度EGV破裂出血患者的疗效、经济性及安全性。
1 对象与方法
1.1 研究对象选择2013年1月—2017年12月于天津医科大学三中心临床学院消化(肝病)科住院的肝硬化合并上胃肠道出血的患者。纳入标准:(1)经实验室检查、胃镜、肝脏B超和(或)腹部CT/MRI诊断为肝硬化PH伴中重度EGV并脾功能亢进患者,内镜下曲张静脉分级参照2016年中华医学会消化病学分会、肝病学分会、内镜学分会食管胃静脉曲张学组制定的分级标准。(2)有明确EGV出血史。(3)生命体征平稳,可耐受胃镜检查者。排除标准:(1)碘过敏患者;严重肝、肾、心、肺功能衰竭者和心、肺、肝、肾功能严重不全不能耐受手术者。(2)依从性差,不能完成内镜下治疗及PSE手术者。将符合上述入组条件的92例中行内镜联合PSE治疗的43例患者作为观察组;同时期符合入组条件、按内镜下食管胃静脉曲张程度匹配的入组的49例患者作为对照组,接受EVL/GVS治疗。
1.2 方法
1.2.1 指标收集收集患者性别、年龄、肝硬化病因、胃镜下曲张静脉程度及分级、治疗方式。2组患者治疗后是否有胃肠道出血,治疗后第1、3、6、12个月复查胃镜结果。
1.2.2 内镜下治疗方法EVL/GVS均采用OLYMPUS GIF-290N型电子胃镜治疗。GVS使用组织胶为α氰基丙酸正丁酯,硬化剂为聚桂醇,使用Wilson cook VIN-21单腔注射针,采用曲张静脉内三明治夹心注射法,单点注射聚桂醇量不超过30 mL,组织胶不超过4.5 mL。EVL使用天津天医公司的6环结扎器,从齿状线开始自下而上呈螺旋式非密集套扎,每次套扎3~18环。PSE在EVL/GVS治疗后3周进行,术前1周予盐酸左氧氟沙星片(0.5 g/次,1次/日)行肠道去污染治疗。采用Seldinger法:局麻下经皮经股动脉插管,插管至脾动脉主干造影,了解脾大小及血管分支、分布情况,确定栓塞范围及所需栓塞材料数量。超选插管至脾下极供血动脉,将所需栓塞材料采用低压流控技术缓慢注入[4]。栓塞完成后退管至脾动脉主干近段再次造影确认栓塞面积。栓塞材料包括三丙烯微球(embosphere)、海藻酸钠微球(KMG)、明胶海绵颗粒(GSF)。栓塞面积控制在40%~60%。术中及术后监测呼吸、血压、脉搏等生命体征变化,术后穿刺部位加压包扎止血6 h,观察穿刺部位有无渗血、血肿,绝对卧床休息12~24 h。
1.2.3 随访2组EGV治疗后1、3、6、12个月复查胃镜。若静脉曲张消失或为轻度则继续随访,无论食管还是胃静脉曲张,若其中之一为中度或重度则再次套扎或硬化治疗,直至静脉曲张均消失或变为轻度,每次治疗后1个月复查胃镜。统计首次EVL/GVS治疗后1、3、6、12个月EGV根治例数、复发例数及再出血例数。统计住院总天数及住院总费用。对比2组治疗1、3、6、12个月EGV的根治率、复发率、术后出血率及至不需要内镜下ELV/GVS治疗,或治疗后12个月内(观察期结束)住院总天数及住院总费用。
1.2.4 疗效判定根治定义为静脉曲张从F2~3变为F0;复发定义为曲张静脉从F0变为F1~F3;若随访期间发生曲张静脉破裂出血则判定为术后出血。治疗≤3个月为短期;治疗>3个月为中远期。
1.3 统计学方法采用SPSS 19.0软件进行数据统计分析。正态分布的计数资料以均数±标准差(±s)表示,非正态分布的采用M(P25,P75)表示。计量资料均数比较采用独立样本t检验或秩和检验。分类变量组间比较用χ2检验。P<0.05为差异有统计学意义。
2 结果
2.1 2组一般情况比较观察组年龄20~77岁,对照组年龄31~75岁,2组性别、年龄、Child-Pugh分级、曲张静脉分级及肝硬化病因构成等方面差异均无统计学意义,见表1。
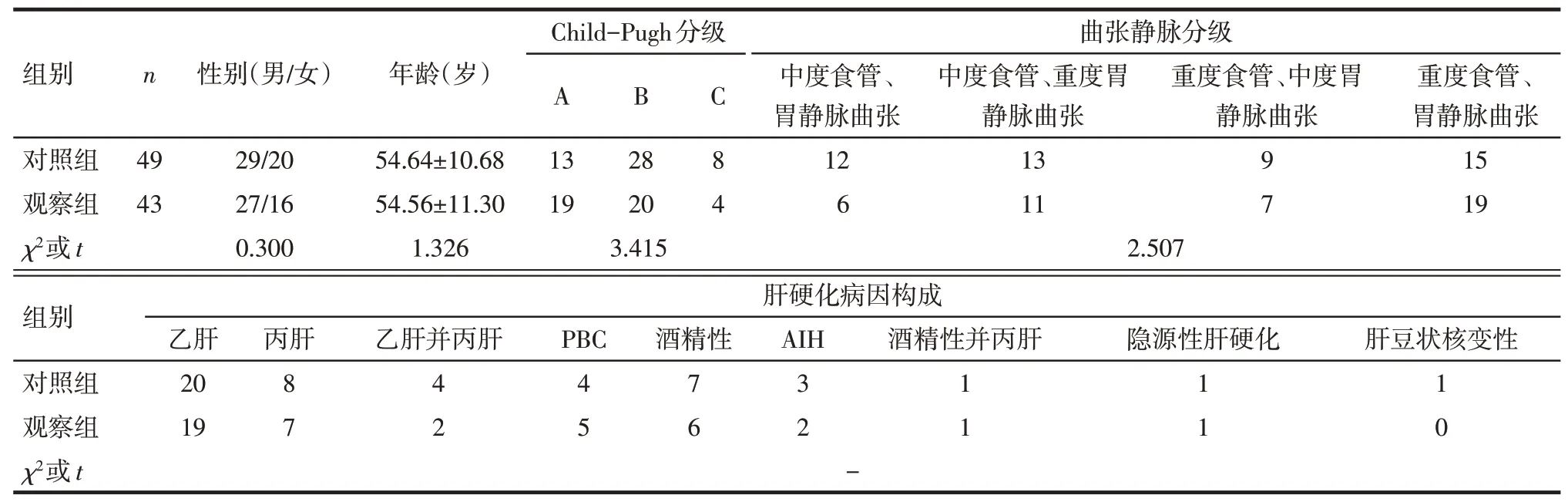
Tab.1 Comparison of general conditions between two groups表1 2组一般情况比较
2.2 2组疗效比较 第1、3个月观察组与对照组在EGV根治率、复发率、再出血率方面差异无统计学意义,第6、12个月观察组EGV根治率显著高于对照组,复发率和再出血率低于对照组。见表2。
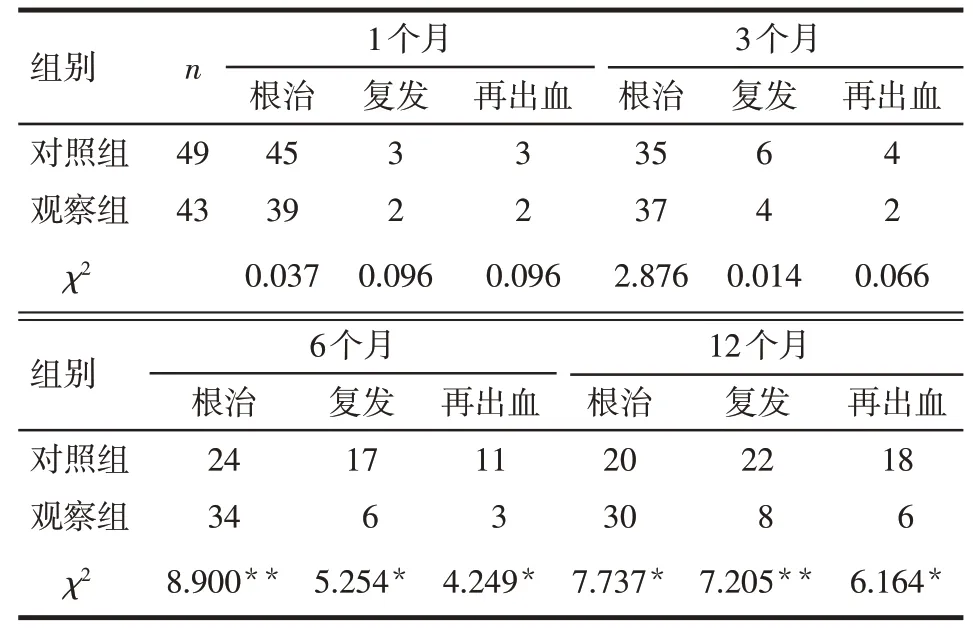
Tab.2 Comparison of efficacy of EVL/GVS combined with PSE and EVL/GVS in the treatment of liver cirrhosis with esophageal and gastric varices表2 EVL/GVS联合PSE与EVL/GVS治疗肝硬化伴食管胃静脉曲张疗效比较
2.3 并发症对照组患者术后有恶心、咽部异物感、轻微咽及胸骨后疼痛、发热、吞咽不畅等并发症,一般3~6 d自行缓解,部分发热患者存在菌血症,需抗生素治疗。观察组患者除上述症状外,还包括腹痛、腹腔积液、腹腔感染、胸腔积液、脾脓肿、脾静脉血栓形成等,见表3。其中急性脾静脉不全血栓形成1例,经皮下序贯口服抗凝药物后控制血栓进展。脾脓肿并持续性腹痛1例,经加强营养支持、强效抗感染等综合治疗后脓肿控制,患者住院治疗40余天出院。
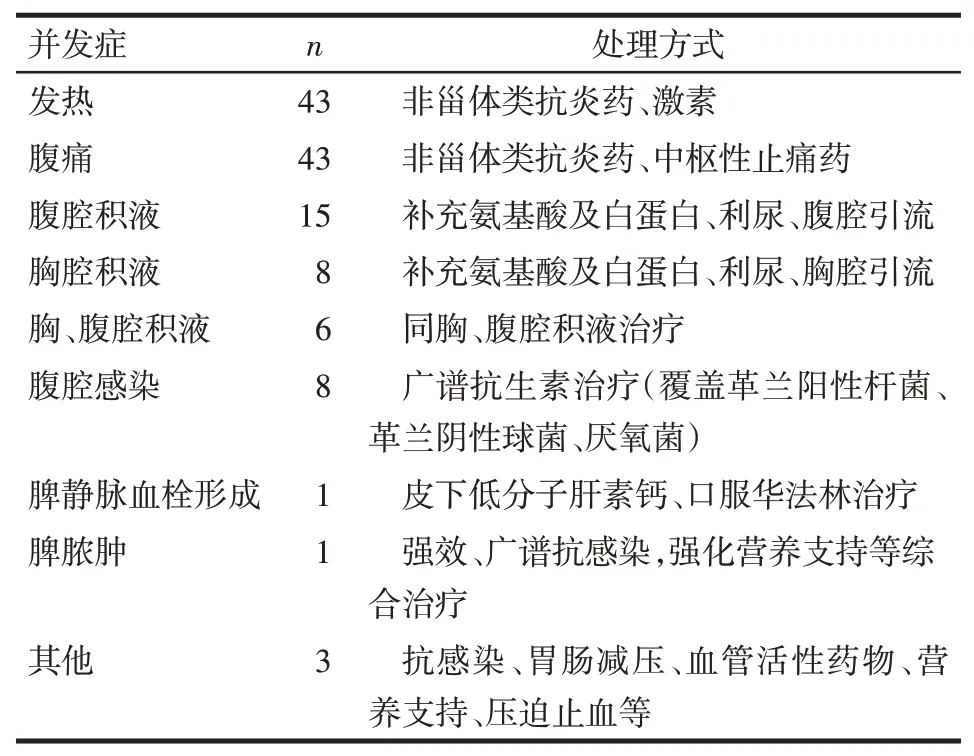
Tab.3 Postoperative complications and treatments of post-PSE in the combined treatment group表3观察组PSE术后并发症及处理方式
2.4 住院时间及总费用EVL/GVS联合PSE治疗累计住院总费用较EVL/GVS组明显降低,住院总天数明显缩短(P<0.01),见表4。

Tab.4 Comparison of total hospital stays and total expenses between the two groups表4 2组住院总天数及总费用比较 M(P25,P75)
3 讨论
3.1 EVL/GVS治疗面临的问题 尽管内镜治疗近十年来在食管胃静脉曲张破裂出血的诊断和治疗中取得了很多进步,但食管胃静脉曲张破裂出血6周内病死率仍高达10%~20%[5],是肝硬化最主要的死因之一。内镜治疗具有创伤小、恢复快等优势,但有高达70%的再出血率及20%~50%的病死率[6]。本研究提示再出血率随时间延长而增加,再出血率的增加往往意味着更高的死亡风险。临床实践中,对内镜治疗的患者往往通过联用药物、缩短复查间隔来降低再出血率,这样会增加治疗费用和住院天数。EVL/GVS仅能治疗黏膜及黏膜下层的曲张静脉而留有深层静脉及侧支循环,不降低门静脉压力,因此EGV复发率高[7],往往需要多次治疗。本研究对EGV患者治疗随访1年,对照组平均住院总天数为43.0 d,平均住院总费用为13.77万元。如何降低EGV复发率及再出血率是内镜治疗面临的挑战。
3.2 EVL/GVS联合PSE治疗的优势EGV是PH的主要表现之一,研究表明脾增大致门脉压进一步升高,使EGV更趋于难治[8]。本研究纳入人群中病因包括病毒性肝炎、自身免疫性、酒精性等常见肝硬化病因,均有门脉高压EGV破裂出血伴不同程度脾功能亢进,降低门静脉压力能更有效地控制EGV程度。目前降低门静脉压力的方式包括外科门体分流术、脾切除术、经颈静脉肝内门体静脉分流术(TIPS)等,均能有效降低门静脉压力[9],仅肝功能良好的患者可耐受。大多数EGV破裂出血患者肝功能较差,外科手术及介入治疗耐受性差。PSE通过栓塞脾动脉分支,减少回流至门静脉的血流量,继而降低门静脉压力,缓解EGV及其他部位静脉曲张出血[10]。有研究提示内镜下治疗联合PSE有助于降低胃静脉曲张(GV)复发率、再出血率及患者病死率[11]。本研究发现2组在短时间内(首次治疗后1~3个月)根治率、复发率、再出血率方面无差异;观察组在中远期(首次治疗后6~12个月)疗效更佳,较对照组有较高的EGV根治率及较低的复发率、再出血率。因此,EVL/GVS联合PSE治疗EGV既可治疗黏膜及黏膜下层静脉曲张,又可能通过缓解PH从而降低内镜下治疗后EGV的复发率和再出血率。PSE既能够保留脾的生理功能,又可缓解PH及脾功能亢进,对不适合TIPS治疗及内镜治疗失败的患者进行PSE治疗,效果明显[12-13]。观察组较对照组明显缩短患者住院总天数及降低住院总费用,减轻患者经济负担,节省医疗资源。
3.3 PSE治疗的并发症及应对策略PSE术后并发症主要有发热、腹痛、腹水、腹腔感染、胸腔积液、脾脓肿、脾静脉血栓形成等,最严重的并发症为脾脓肿。本研究中PSE术后患者普遍出现发热、腹痛,发生率为100%。15例出现腹腔积液,8例出现胸腔积液,腹腔积液合并胸腔积液6例,腹腔感染8例,门静脉不全性血栓1例。其中,最严重并发症为脾脓肿1例,经加强营养支持、强效抗感染等综合治疗后得到控制,患者住院治疗40余天出院,延长了住院时间,明显增加了住院费用。文献报道与PSE并发症严重程度最相关的因素是脾栓塞面积[14],其他因素包括Child-Pugh分级C级以上、总胆红素大于1.4 mg/dL(1 mg/dL=17.1μmol/L)及白蛋白低于28 g/L等[15]。本例脾脓肿发生原因为单次栓塞面积较大(60%)、肝功能差(Child-Pugh C级)、合并糖尿病等。临床中常通过术前优化患者选择、严格掌握适应证、肠道去污染等充分准备,术中分次、少量栓塞治疗[16],术后早期识别高危患者、早期给予强效广谱抗感染治疗及加强营养支持,并发症均可控。
3.4 结论及展望本文结果提示,EVL/GVS联合PSE治疗EGV较单纯EVL/GVS治疗中远期疗效更佳、并发症可控、住院总费用更低,是PH合并EGV较好的综合治疗手段。近年来由于PSE术后并发症的问题,PSE在治疗门脉高压症、脾功能亢进方面的应用有减少的趋势,特别是术后持续性的难以忍受的腹痛,还包括顽固性腹腔感染,甚至致死性脾脓肿的形成。如何更好地预防并减少并发症发生,使该治疗手段继续广泛开展,是临床工作关注的焦点。有学者认为,PSE在食管胃静脉曲张破裂出血中的作用尚未被人们重视,是待被发掘的有效治疗手段[17]。本研究提示优化患者选择、控制栓塞面积、尽早防治并发症是PSE临床顺利开展的关键。

