高考化学试题中工艺流程题的特点分析及解题策略
◇ 山东 张剑锋
工艺流程题是将工业生产中的主要阶段以框图形式抽象出来,以背景的形式出现在试题中,结合中学化学知识步步设问,综合考查学生的基础知识、基本技能、学科思想、学科素养.在高考试卷中占有较大比重,综合性较强,难度大,考生得分往往比较困难.本文结合2020年全国理综卷Ⅰ化学试题加以分析.
1 试题特点
纵观近几年高考试题,工艺流程题主要选择以过渡元素为背景元素,结合物质的制备和分离考查元素化合物性质、平衡移动原理、电解质溶液、电化学、物质分离提纯实验操作、物质循环使用以及有关计算.
2 典例分析
例(2020年全国卷Ⅰ)钒具有广泛用途.黏土钒矿中,钒以+3、+4、+5价的化合物存在,还包括钾、镁的铝硅酸盐以及Si O2、Fe3O4.采用图1所示工艺流程可由黏土钒矿制备NH4VO3.
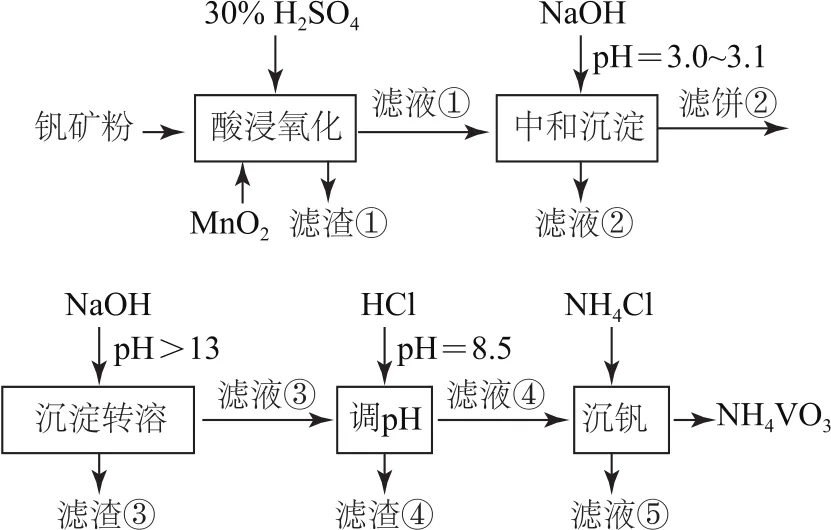
图1
该工艺条件下,溶液中金属离子开始沉淀和完全沉淀的p H如表1所示.
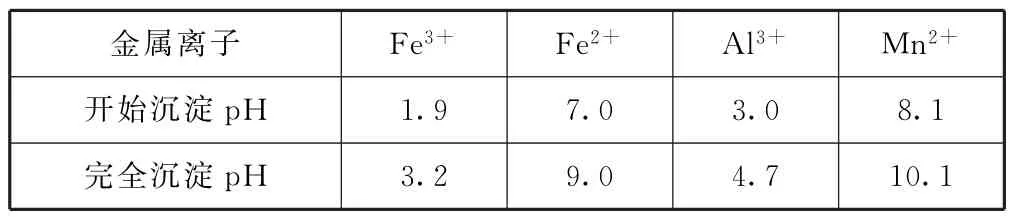
表1
回答下列问题:
(1)“酸浸氧化”需要加热,其原因是________.
(2)“酸浸氧化”中,VO+和 VO2+被氧化成V,同时还有________被氧化.写出VO+转化为V反应的离子方程式________.
(3)“中和沉淀”中,钒水解并沉淀为 V2O5·xH2O,随滤液②可除去金属离子 K+、Mg2+、Na+、________,以及部分的________.
(4)“沉淀转溶”中,V2O5·xH2O 转化为钒酸盐溶解.滤渣③的主要成分是________.
(5)“调p H”中有沉淀生成,生成沉淀反应的化学方程式是________.
(6)“沉钒”中析出NH4VO3晶体时,需要加入过量NH4Cl,其原因是________.
分析比较原料和产品,结合中间流程、表格数据和第(2)(3)(4)问中的相关信息,根据元素守恒和物质转化基本规律,得出钒的变化路径是:钒矿粉先酸溶为VO+和VO2+,后氧化为VO+2,然后“中和沉淀”为V2O5·xH2O,再“沉淀转溶”为 Na VO3,最后“沉钒”为NH4VO3;钾、镁硫酸盐易溶于水,“酸浸氧化”后进入滤液①,再“中和沉淀”后进入滤液②;铝的变化是:铝硅酸盐被硫酸溶解为Al3+,然后进入滤液①,再经Na OH调节p H=3.0~3.1后一部分进入滤液②,一部分变成Al(OH)3进入滤饼②(联系表格信息中Al3+沉淀的p H范围),滤饼②中的Al(OH)3再经过Na OH调节p H>13变为[Al(OH)-4]进入滤液③,最后再经HCl调节p H变成Al(OH)3,进入滤渣④;铁的变化为Fe3O4酸溶为Fe3+和Fe2+,Fe2+再被氧化为Fe3+,经“中和沉淀”一部分生成Fe(OH)3进入滤饼②,一部分进入滤液②(联系表格信息中Fe3+沉淀的p H范围),滤饼②中的Fe(OH)3经过沉淀转溶环节进入滤渣③;Mn的变化为Mn O2被还原为Mn2+,再经Na OH调节p H=3.0~3.1后进入滤液②.
答案(1)加快酸浸和氧化反应速率(促进氧化完全).
(2)Fe2+;
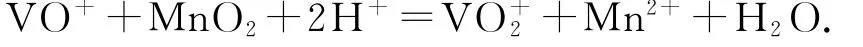
(3)Mn2+;Al3+和Fe3+.
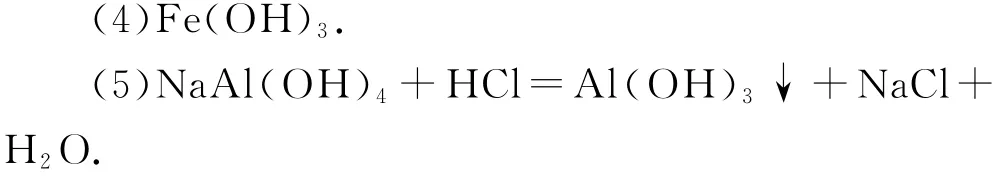
(6)利用同离子效应,促进NH4VO3尽可能析出完全.
点评
该题的难点是物质的转化和推断,在审题中要注意前后联系,可采取先粗读后细读的方式,将附加信息或隐藏在题干或设问中的信息圈画出来,用箭头指向相关环节,进行推理.抓住一种元素进行追踪,可以简化分析问题的复杂性和难度.本题考查的是条件控制,是变化的观念,第(2)问和第(5)问两处考查了方程式的书写,体现的是宏观辨识与微观探析以及符号表达;第(3)(4)问考查物质转化和混合物分离,体现的是变化观念与守恒思想;第(6)问考查平衡原理在物质转化和分离中的应用.氧化还原理论和氢氧化铝的两性是必备知识.该题综合考查考生的综合分析判断能力、信息挖掘和应用能力、阅读理解能力、陌生方程式的书写能力等.
3 思维模型
解题中可以形成如图2所示的思维模型.
1)审题头,明确原料和生产目的.
2)审流程,看箭头,明确反应条件、原理及物质成分的分离、提纯方法的选择.
3)审问题,看考查的是反应方程式的书写,还是平衡原理的应用,或者是物质的判断及相关的计算,然后认真作答.
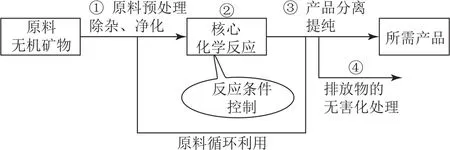
图2
4 高考的命题规律及设问方向
高考工艺流程题常以“以自然资源为原料制备无机物”或“从工业废料中分离提纯无机物”为载体进行考查.
1)无机化学基础知识(物质的类别、名称、元素的化合价、化学式和电子式的规范书写).
2)基本技能(陌生化学方程式、离子方程式、电极反应式的书写、离子交换膜的选择;分离提纯规范操作等).
3)识图能力(物质的转化与跟踪);表格数据的分析能力;图象工艺条件的选择.
4)物质制备及提纯条件的控制(提高反应速率、产率或转化率、产品纯度的措施).
5)基本计算(产品化学式、含量及纯度、氧化还原反应中电子转移数目的计算等).
5 破解策略
5.1 循环物质的确定
1)从流程图上看:箭头回头的是循环物质.
2)从物质的转化上看:在流程中加入的物质,参与反应后续步骤中又会产生(在滤渣或滤液中寻找)的物质是循环物质.
5.2 副产物的判断
1)从流程图上看:支线产品就是副产物.
2)从制备的目的上判断:不是主产品的是副产物.
5.3 滤渣、滤液中成分的确定
要考虑样品中原料和杂质的成分在每一个步骤中与每一种试剂反应的情况:
1)反应过程中哪些物质(离子)消失了(每种沉淀剂沉淀了哪些离子)?
2)所加试剂是否过量或离子间发生化学反应,又产生了哪些新离子?要考虑这些离子间是否会再发生反应.
此外,联系设问回读题目也很重要,有时单独看题干信息,会有好多环节弄不清楚,很容易产生焦躁心理,甚至放弃解题.如果仔细把题目读完,会发现有好多信息蕴藏在设问中,没有这些信息的支持,题目很难读懂,这样就对考生的阅读能力提出了较高要求,这也符合考试大纲中的基本思想,考生要引起足够重视.
当然有时候,对于流程图中个别环节即使没有弄清,一般也不影响设问的作答,在考场上,考生一定不要在此纠结,以免浪费宝贵时间,影响考试时的发挥.
工艺流程题中开始的几个小问题,很多时候与题干信息没有多大联系,可以直接作答,考试中应该先答上,千万不要因为感觉题目过难就全盘放弃.
拓展硼及其化合物在工业、医药、农业等部门有许多用途.某工厂以铁硼精矿(主要成分为B2O3·2 Mg O,还有Si O2、Ca O、Fe O等杂质)制取硼酸、金属镁的工艺流程如图3所示.
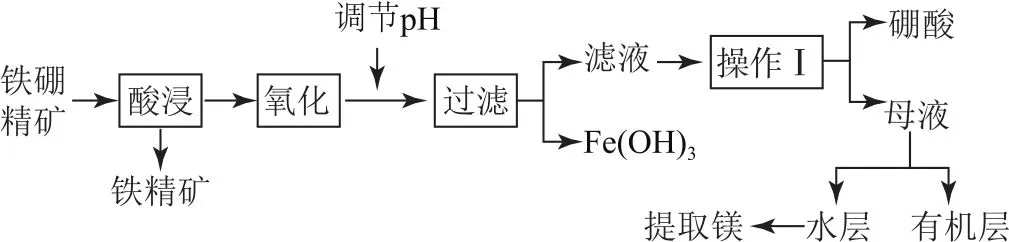
图3
已知:硼酸在不同温度下的溶解度见表1.
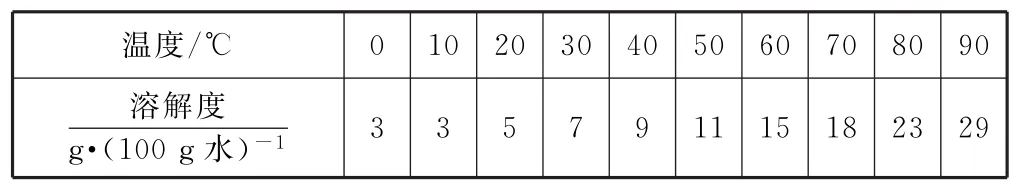
表1
回答下列问题:
(1)使用盐酸酸浸,过程中主要反应的化学方程式为________,为提高浸出速率,可采取的措施有________(写出两条).
(2)酸浸时,温度与硼浸出率的关系如图4所示,则合适的酸浸温度为________.
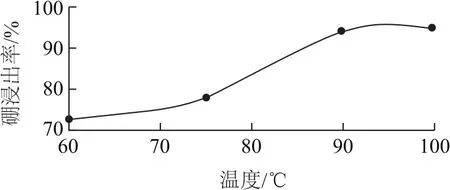
图4
(3)浸出液“氧化”步骤是将溶液中的Fe2+用________试剂氧化为Fe3+,反应的离子方程式为________.
(4)从滤液中获得H3BO3晶体的“操作Ⅰ”具体操作是________.
(5)向滤液中加入有机萃取剂萃取分液,此时硼酸处于________层中(填“有机”或“无机”).实验室模拟“萃取”操作使用的玻璃仪器除烧杯外,另一主要玻璃仪器是________.
(6)某工厂用m1kg的铁硼精矿制备硼酸,得到纯度为99.8%的硼酸m2kg,则铁硼精矿中硼的质量分数是________(列式表达).
分析先看原料和产品,依据元素守恒和对应元素化合物的性质可知,“硼酸”是硼的去向,“提取镁”是镁的去向,“铁精矿”和“Fe(OH)3”是铁的去向,Si O2不溶于酸,去了铁精矿中,“Ca O”溶于盐酸变成了Ca Cl2,与Mg Cl2一起进入“母液”,通过萃取分离.氧化和调p H 是为了将Fe2+氧化为Fe3+再变成Fe(OH)3沉淀除去;第(4)问应“回读”前面“硼酸在不同温度下的溶解度”表格,想到蒸发浓缩、冷却结晶、过滤;结合设问(5)分析有机层中还有一部分H3BO3.
答案(1)B2O3·2 Mg O+4 HCl+H2O=2 H3BO3+2 Mg Cl2;适当增加盐酸浓度、提高反应温度、减小铁硼矿粉粒径、充分搅拌等.
(2)90~95℃(写此范围内的任意温度均可).
(3)H2O2;2 Fe2++H2O2+2 H+=2 Fe3++2 H2O(写氯气也可以得分,2 Fe2++Cl2=2 Fe3++2 Cl-).
(4)蒸发浓缩、冷却结晶、过滤.
(5)有机;分液漏斗.