MRI诊断附睾睾丸结核
闫瑞芳,李学坤,张改云,翟战胜,韩东明
(新乡医学院第一附属医院磁共振科,河南 卫辉 453100)
男性生殖器官结核多见于附睾、睾丸、前列腺和精囊腺,附睾结核最常见。临床常用彩色多普勒超声筛查附睾睾丸病变,但很难鉴别大部分肿块型睾丸结核与非特异性炎性肉芽肿[1-2]。MR弥散加权成像(diffusion weighted imaging, DWI)及动态增强(dynamic contrast enhancement, DCE)成像用于观察附睾睾丸结核的研究尚不多见[3]。本研究回顾性分析15例附睾睾丸结核的MRI表现。
1 资料与方法
1.1 一般资料 回顾性分析2014年9月—2019年3月在新乡医学院第一附属医院经手术或穿刺病理确诊的15例附睾睾丸结核患者(病变组),与10例其他疾病患者(20只正常睾丸,对照组)的MRI进行对照分析。病变组患者年龄20~62岁,中位年龄31.0岁,对照组年龄20~58岁,中位年龄33.5岁;纳入标准:年龄>18岁,因阴囊病变就诊,彩色多普勒超声检查提示附睾或睾丸病变而接受常规MRI、DWI及DCE检查,病理诊断为附睾睾丸结核;排除资料不齐及图像质量不佳者。对照组10例为疑诊骨关节疾病、无阴囊不适而接受盆腔MR平扫+DCE患者,睾丸附睾无异常表现,同意接受全睾丸附睾MR扫描,且未发现相关异常。所有受试者均知情同意。
1.2 仪器与方法 采用GE Signa Hde 1.5T MR检查仪,8通道TORSOPA线圈。平扫采集轴位T1WI、T2WI、DWI及矢状位、冠状位T2WI。快速自旋回波(fast spin echo, FSE)T1WI:TR 580 ms,TE 10.1 ms;快速恢复快速回波(fast recovery fast spin-echo, FRFSE)T2WI:TR 4 380 ms,TE 83.7 ms;层厚6.0 mm,层间距0,矩阵320×224。FOV 38 cm×36 cm×40 cm。
DWI:b值800 s/mm2, TR 4 100 ms,TE 66.9 ms,层厚6.0 mm,矩阵256×256。后处理方法:选择DWI序列,点击FUNCTOOL,进入后处理界面,点击ADC,先调阈值,将最大值设为最右边,调节最小值,保证绿线覆盖全部盆腔组织;系统自动识别或设置b值,点击COMPUTE计算得到ADC图和eADC图。于病变层面选取ROI,完成后处理。病变ROI应仅在同一器官内,且不得超出病变范围。正常睾丸ROI 100~140 mm2,附睾70~100 mm2。
DCE:采用3D LAVA技术,TR 4.7 ms,TE 2.1 ms,层厚4.4 mm,矩阵320×192。先行预扫描,再经静脉以流率2.5 ml/s快速团注Gd-DTPA 30 ml,快速跟进注射生理盐水20 ml,分别于注药后20、50、90 s行矢状位三期DCE扫描,随后行冠状位和轴位扫描。
1.3 图像分析 由工作20年以上的1名副主任医师和1名主任医师共同分析图像,经协商达成一致意见。T1WI、T2WI均以肌肉信号为等信号、皮下脂肪信号为高信号,低于肌肉信号者为低信号。将强化特征分为均匀、不均匀、斑片状、环形、多囊分隔强化等;LAVA预扫描图像对比评价强化程度,以等于预扫描信号为未强化,等于肌肉强化为轻度强化,高于肌肉强化但弱于血管内强化为中等强化,接近血管内强化为显著强化。
1.4 统计学分析 采用SPSS 22.0统计分析软件。计量资料以±s表示,组间比较采用t检验。P<0.05为差异有统计学意义。
2 结果
病变组与对照组患者年龄差异无统计学意义(t=0.091,P=0.928)。病变组患者均以发现附睾肿物、睾丸肿大、阴囊肿块就诊,病程1~13个月;6例伴局部疼痛,12例伴发热,2例可见窦道反复流脓;1例3年前因外伤接受左侧睾丸及附睾切除术。病变组胸部CT显示11例肺部存在结核病灶;15例阴囊彩色多普勒超声均可见异常回声,9例表现为液性暗区回声或低回声团周边见彩色血流信号,考虑结核,6例睾丸内多见低回声团,性质待定;15例结核菌素试验均见直径15~25 mm红肿、硬结。
2.1 平扫MRI 对照组睾丸T1WI呈均匀稍低信号,T2WI呈高信号;附睾T1WI、T2WI均呈不均匀等、稍高信号,T1WI稍高信号呈纡曲管状。病变组睾丸、附睾T1WI以等、低混杂信号为主,附睾病变内均见斑片状高信号;T2WI呈等、稍高及低混杂信号,12例病变内囊变、坏死呈低信号,3例呈高信号;双侧腹股沟区均可见点状、类圆形淋巴结,T1WI呈稍低信号,12例T2WI淋巴结信号不均匀,呈边缘稍高信号、中心稍低信号,3例信号均匀;9例见睾丸鞘膜积液。
2.2 DWI 对照组睾丸呈均匀高信号,附睾呈不均匀低、等信号;共发现6个腹股沟小淋巴结,呈均匀高信号。病变组睾丸、附睾病变均以稍高信号为主,12例病灶内见环形边缘高信号、中心低信号;共发现19个腹股沟淋巴结,14个呈均匀高信号,5个呈边缘环形高信号、中心低信号。病变组睾丸、附睾及腹股沟淋巴结ADC值均小于对照组(P均<0.05),见表1。
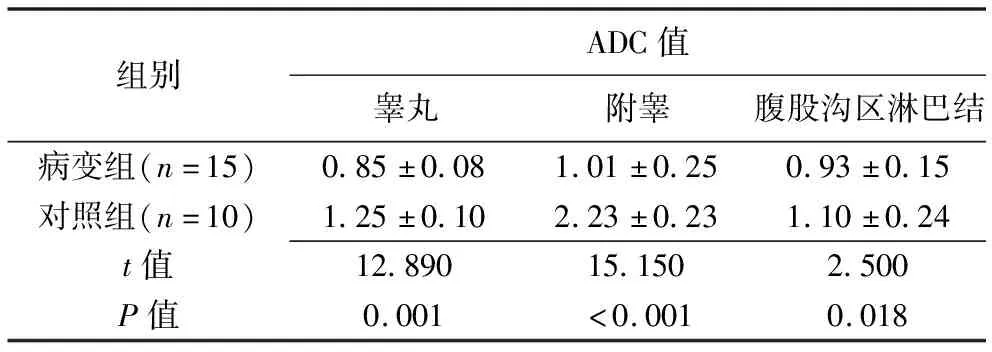
表1 病变组与对照组间睾丸、附睾和腹股沟区淋巴结ADC值比较(×10-3 mm2/s)
2.3 DCE 对照组睾丸呈渐进性轻度均匀强化。病变组睾丸、附睾病变不均匀强化,3例睾丸病变呈多囊间隔强化,12例附睾、睾丸病变呈环形强化,囊壁及间隔厚薄较均匀,壁薄,随时间延长强化更明显;双侧腹股沟区淋巴结增强后呈环形强化,1例增强后输精管壁增厚、强化,2例前列腺内可见斑片状无强化区,1例精囊腺多发环形强化。
病变组MRI诊断结果:2例单侧附睾结核,11例单侧附睾并睾丸结核(图1),1例双侧附睾结核累及双侧输精管、精囊腺、前列腺(图2),1例双侧附睾并睾丸结核累及前列腺;共13个睾丸病变、17个附睾病变,均与病理结果一致,其中13例经手术病理、2例经附睾穿刺病理结果证实;术中见病变附睾睾丸肿大、质硬,呈干酪样坏死改变,伴脓苔及坏死改变;术后病理光镜下可见类上皮细胞、多核巨细胞及干酪样坏死(图1G)。

图1 患者男,27岁,右侧附睾睾丸结核 A~D.分别为轴位MR T1WI(A)、T2WI(B)、增强(C)及DWI(D),右侧附睾见2个脓肿,壁呈等T1等T2信号,腔内呈长T1短T2信号,较小病变内见T1点状稍高信号(箭),增强后呈环形强化,DWI较小脓肿呈环形高信号,中心干酪样坏死呈低信号;E.彩色多普勒超声示右侧睾丸附睾低回声病变,周边可见彩色血流信号;F.大体病理图,右侧睾丸及附睾切面灰红灰白,可见干酪样坏死;G.病理图(HE,×100)

图2 患者男,29岁,双侧附睾结核 A.轴位T1WI示双侧附睾肿大,以等信号为主,内见斑片状高信号;B.T2WI示病变呈不均匀等、高信号;C.矢状位DCE示右侧附睾及精囊腺病变呈多发小环形强化(箭);D.彩色多普勒超声示右侧附睾液性暗区回声
3 讨论
既往认为附睾结核双侧常见,但现在发现很多附睾结核是单侧性的[4],睾丸结核极少见,多由附睾结核直接蔓延。本组15例附睾结核中,12例合并睾丸结核;11例肺部存在结核病灶,考虑血行播散至睾丸、附睾;4例肺部未见结核病灶,考虑原发附睾结核。1例双侧附睾结核累及双侧输精管、精囊腺及前列腺,但未累及睾丸,患者肺部无结核病灶,无肾结核,考虑原发附睾结核逆行感染睾丸。
本组附睾睾丸结核MRI特征如下:①T1WI以等、低信号为主,15例均见斑片状T1高信号,病理为干酪样坏死;②T2WI呈混杂等、高、稍低信号,12例病灶呈T2低信号,病理为干酪样坏死[4-5];③DWI脓肿壁呈高信号,ADC值下降,脓腔呈低信号,与标本干酪样坏死区位置一致[6-7];④典型淋巴结结核DWI呈边缘环形高信号,中心干酪样坏死呈低信号;增强后环形强化可辅助诊断附睾睾丸结核;⑤增强扫描结核脓肿可单发,呈环形强化,也可多发,呈环形、小囊间隔样强化;脓肿壁薄而均匀,随时间延长环形强化更明显,因此DCE更易于诊断结核脓肿。本组1例附睾结核累及精囊腺,呈多发环形强化,较具特征性。
结核发生发展过程中MRI表现不同,与病变内渗出、增殖、坏死及纤维化等病理改变有关。不典型附睾结核需与非特异性附睾炎、肉芽肿病变等相鉴别。早期附睾结核一般无疼痛和发热,无触痛[8],本组80.00%(12/15)附睾结核累及睾丸,13.33%(2/15)双侧发病。非特异性附睾炎常单侧发病,附睾增大,T2WI呈高信号,伴阴囊肿痛,精索增粗,多不累及睾丸[9]。附睾慢性非特异性肉芽肿常急性发病,多单侧发病,体尾部多见,有明显压痛,有时可形成附睾脓肿;彩色多普勒超声于结核脓肿周围发现血流信号对鉴别结核与化脓性脓肿有一定价值[10];脓肿的脓液黏稠,DWI呈高信号,脓肿壁为纤维肉芽组织,呈等、低信号,可与结核脓肿干酪样坏死相鉴别。
睾丸结核需与睾丸肿瘤相鉴别。睾丸肿瘤多为单侧发病,不累及附睾。精原细胞瘤多见于青壮年,多为卵圆形或浅分叶肿块,小者周围可见正常睾丸组织,边界清晰,T1WI呈等稍低信号,T2WI呈均匀低信号;DWI多呈均匀高信号,平均ADC值(0.63±0.12)×10-3mm2/s,增强后轻度强化,内见条带状分隔,并有明显强化[11]。胚胎性癌以20~30岁多见,较小时即可广泛转移;肿瘤体积较大,边界不清,内可见出血钙化纤维化,T1WI呈低等高混杂性,T2WI呈等高混杂信号,增强后明显不均匀强化[12];部分患者血清甲胎蛋白、人绒毛膜促性腺激素升高。淋巴瘤50岁以上多见,可同时或先后双侧发生,病变睾丸弥漫性肿大,T1WI呈等低略高信号,T2WI呈不均匀稍低信号或混杂低信号,增强扫描轻度或显著不均匀强化,可伴鞘膜积液或累及附睾、精索[13]。
综上所述,典型附睾睾丸结核MRI表现具有特征性,结合DWI及DCE可明确诊断;DCE可发现微小病变,准确评估生殖系统结核累及范围。

