肠系膜下动脉分型在腹腔镜直肠癌手术中保留左结肠动脉的应用价值
骆洋 钟鸣,2
全直肠系膜切除(total mesorectal excision,TME)以及规范化的淋巴结清扫是腹腔镜直肠癌手术的金标准,有效降低了患者局部复发率和死亡率,减少围手术期并发症,提高患者术后生活质量和存活率[1-2]。然而,吻合口漏仍然是腹腔镜直肠癌术后最严重和最主要的并发症之一[3];为了增加吻合口血供并降低术后漏的风险,国内外专家在处理肠系膜下动脉(inferior mesenteric artery,IMA)时均选择保留左结肠动脉(left colonic artery,LCA)[4-5]。但是由于IMA的分支变异较大,在保留LCA过程中往往因为各种意外导致IMA出血或者近端肠管下拉困难,增加吻合口张力,而不得不采用转流术来减少吻合口漏所带来的严重并发症[6]; 不但给患者带来了二次手术的危险,也增加了切口疝等术后并发症的风险,严重影响了患者术后生活质量[7]。因此,笔者结合相关报道以及自身临床经验,对腹腔镜直肠癌手术中如何根据IMA分型,精准化保留LCA进行归纳总结。
一、肠系膜下动脉及其周围的解剖结构
IMA是腹主动脉前壁发出的直接分支,其根部约平第3~4腰椎高度,沿腹后壁进入乙状结肠系膜根部,下降至骨盆移行为直肠上动脉(superior rectal artery,SRA),沿途分支包括LCA、乙状结肠动脉(sigmoid colonic artery,SCA),供应横结肠左侧1/3、降结肠、乙状结肠及直肠上2/3的肠管[8-9]。此外,IMA根部周围的自主神经丛主要为上腹下丛(superior hypogastric plexus,SHP);研究表明,无论采取在IMA起点,还是距离起点0.5 cm、1.0 cm、2.0 cm离断IMA,均有可能损伤SHP左侧束[10-13]。
二、腹腔镜直肠癌手术中保留左结肠动脉的意义
腹腔镜直肠癌根治术中IMA的处理主要包括两种方式:高位结扎(IMA根部离断血管)以及低位结扎(保留LCA,在LCA分叉处下方约1 cm~2 cm处离断IMA)(图1)[14]。笔者认为,高位结扎简单易行,提供充足的近端肠管长度进行乙结肠-直肠端端吻合,但近端肠管的血供仅依靠来自中结肠动脉的边缘血管弓,有可能导致吻合口血供不佳[6];而低位结扎IMA,吻合口血供的来源不仅有中结肠动脉,还有左结肠动脉,保证近端肠管有充足的血液供应,为吻合口的生长愈合提供更好的条件,降低了吻合口漏以及吻合口狭窄的风险[4];同时,减少血管根部的一些不必要操作,对上腹下神经及腹主动脉周围神经的保护有着积极的作用[15-16]。因此,在中低位直肠癌手术中外科医师往往选择保留左结肠动脉,但是由于IMA分支变异较大,在手术过程中往往会因为各种意外导致IMA根部及其分支出血(图2),而不得不结扎IMA根部。因此,如何准确寻找LCA以及在保留LCA的同时如何规范化清扫中央组淋巴结(“253组”淋巴结)(图3)[17],这需要年青的外科医师具有扎实的理论基础和技术水平。此外,在保留LCA时发现近端肠管下拉困难,吻合口张力较大,在进行裁剪系膜时,可能会损伤LCA和边缘血管弓,增加了吻合口漏的风险。发生上述风险主要是因为在手术前对IMA分型以及可能存在的变异风险没有充分认识,导致处理血管时各种意外的发生。

图1 肠系膜下动脉两种结扎方式。1A:高位结扎:肠系膜下动脉根部结扎;1B:低位结扎:保留LCA

图2 肠系膜下血管各种意外性出血。2A~2C:肠系膜下动脉根部出血;2D~2E:肠系膜下静脉出血;2F~2H:左结肠动脉根部出血。IMA:肠系膜下动脉,IMV:肠系膜下静脉,LCA:左结肠动脉
三、IMA分型的提出以及在保留左结肠动脉中的指导意义
1997年日本学者Yada等[18]最早根据LCA、SCA以及SRA根部起始点之间的关系,将IMA分为四型(I型~IV型):①Ⅰ型(直乙共干型):LCA首先分出,之后SCA与SRA共干分出;②Ⅱ型(左乙共干型):IMA先分出一支,为LCA与SCA的共干支,SRA为单独一支,接着共干支分为上升的LCA和下降的SCA;③Ⅲ型:LCA、SCA和SRA于IMA处同一点分出(全共干型),然后各自行走于系膜内;④Ⅳ型(无左型):缺少LCA,IMA直接分出SCA和SRA(图4A)。2015年日本学者Murono等[19]通过血管重建对471例患者进行了IMA分型统计,结果发现Ⅲ型患者最多(n=209,44.7%),其次为Ⅰ型患者(n=193,41.2%)和Ⅱ型患者(n=42,9.0%),而Ⅳ型患者最少(n=24,5.1%),这与中山六院黄美近教授研究结果相仿[20]。笔者团队回顾2016年至2018年仁济医院胃肠外科206例直肠癌患者IMA分型,发现Ⅰ型患者最多(n=84,40.77%),其次为Ⅲ型患者(n=51,24.76%)和Ⅱ型患者(n=48,23.30%),Ⅳ型患者例数最少(n=23,11.16%)(图4B),这与黄俊等研究结果类似[21]。此外,IMA分支,特别是LCA与肠系膜下静脉(inferior mesenteric vein,IMV)交错走行,通常越往根部IMV与IMA之间距离越远。解剖关系大致可以分为3种:(1)贴IMV内侧上行;(2)在距离<15 mm的IMV外侧上行;(3)在IMV外侧且远离IMV上行[19]。Al-Asari等[22]在此基础上提出“IMV关键三角”(由IMV、胰腺下缘、LCA组成),在这三角形局域内可能存在连接肠系膜上动脉和左结肠动脉之间的Riolan动脉弓,手术中若LCA处理不当容易损伤该动脉弓,导致远端结肠缺血的可能。笔者认为,手术前对IMA分型进行充足的预判,可减少处理IMA过程中不必要的操作和手术时间,降低意外出血和神经损伤的风险。

图3 保留左结肠动脉的两种方式。3A:保留左结肠动脉,253组淋巴结未清扫;3B:保留左结肠动脉,253组淋巴结规范化清扫。LCA:左结肠动脉
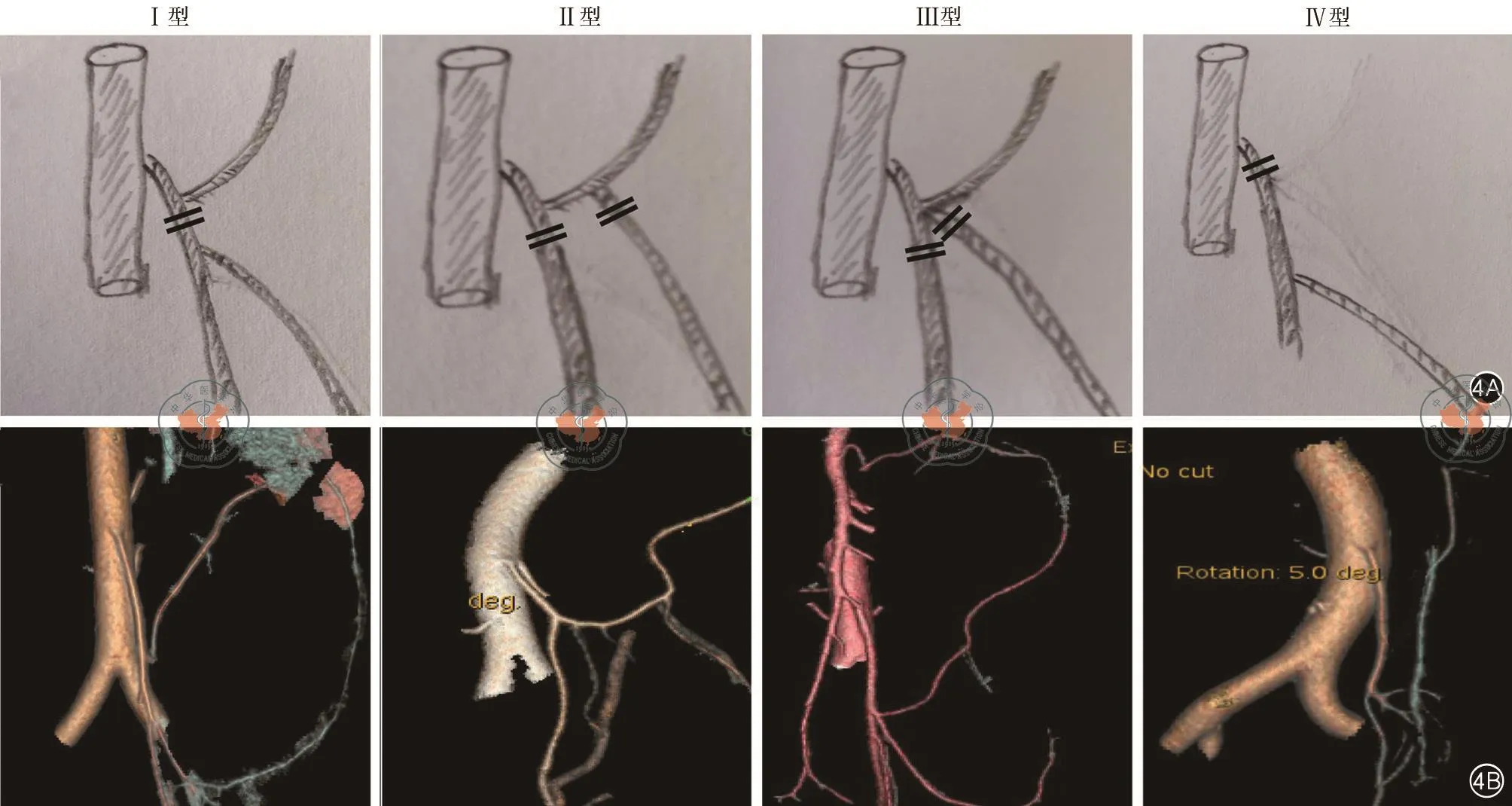
图4 肠系膜下动脉四种分型。4A:IMA四种分型手绘模式图以及保留LCA四种方式;4B:三维血管成像显示的IMA四种分型
研究表明,IMA不同分型会影响术者对血管结扎位置的判断;结扎部位的不同,血管根部淋巴结清扫的难易程度也不尽相同;此外,不同结扎部位与吻合口漏和自主神经功能障碍等术后并发症密切相关[23]。笔者认为腹腔镜直肠癌手术中不能机械地保留LCA,应采取个性化的手术策略,因为IMA根部到LCA起始处之间的血管长度因人而异;分型不同,长度也有可能不同。研究表明,上述血管最短为19 mm,最长为64 mm[24]。课题组通过对183例Ⅰ型~Ⅲ型IMA患者血管重建数据分析,发现IMA根部到LCA起始处之间的血管长度最短为15 mm,最长为70 mm,个体差异较大。因此,需要在手术前通过CT血管重建获得IMA分型,将IMA与LCA以及IMV之间的位置关系有机结合才能真正在手术中对保留LCA的直肠癌根治术有指导意义。例如,CT血管重建显示IMA分型为Ⅳ型,那么术中直接在IMA根部进行结扎,避免较长时间寻找并不存在的LCA,有助于减少手术时间和下腹下神经的损伤。对于Ⅰ型~Ⅲ型IMA,其保留LCA的方式也截然不同,笔者认为,对于Ⅰ型IMA的直肠癌患者,显露LCA起始部时,即可离断IMA,既保留了血供,又减少了不必要的手术时间;对于Ⅱ型IMA,若按照常规方式保留LCA,则容易导致近端肠管下拉困难,增加吻合口张力和吻合口漏的可能;因此,本课题组认为在显露IMA根部后,应进一步显露左乙共干处,离断乙结肠动脉和SRA,这需要有较强的腹腔镜精细操作能力,但容易损伤下腹下神经和肠系膜下静脉;而对于Ⅲ型IMA的患者,则需要显露直左乙共干,并离断乙结肠动脉和SRA,此型手术中应格外仔细,容易导致LCA出血,而不得不放弃低位结扎,降低了吻合口血供(图4)。因此,课题组认为CT血管重建能准确提供IMA分型,甚至可以显示脾曲血管弓的供血血管等相关信息;根据左结肠动脉和肠系膜下静脉走行的相关性,确定D3站淋巴结清扫范围,进而在腹腔镜直肠手术中精准定位LCA起始点,避免相关血管和神经的损伤,保证吻合口血运,减少淋巴结残留。
四、总结展望
目前,国内外专家普遍认为低位直肠癌手术中保留LCA可以增加吻合口血供,但是如何精准化保留LCA尚未达成统一意见。笔者认为,应将“通过CT血管重建技术对IMA进行精准化分型”纳入直肠癌手术的诊疗规范中,这仍需要多中心大样本的前瞻性研究来提供循证医学证据。但是,在精准化保留LCA的同时,应该对D3站淋巴结也进行规范化清扫:(1)头侧:屈氏韧带至肠系膜下动脉根部之间的系膜组织;(2)尾侧:左结肠血管由起始部至与肠系膜下静脉交叉处的区段裸化;(3)内侧:IMA起始部至左结肠血管起始部区段的裸化;(4)外侧:肠系膜下静脉外侧缘。只有在此基础上精准化保留左结肠动脉,才能达到更好的近期疗效和远期疗效(图5)[25]。这样可以在尽可能减少手术带来的损伤的同时,达到肿瘤根治的目的。

图5 253组淋巴结清扫范围。5A:253组淋巴结清扫范围模式图;5B:腹腔镜直肠癌手术中253组淋巴结清扫范围。LCA:左结肠动脉,IMV:肠系膜下静脉,SRA:直肠上动脉,IMA:肠系膜下动脉

