miR-6732-3p对鼻咽癌放射抗拒细胞株CNE-2R放射敏感性的影响
杨晓慧 李开国 朱小东 李龄 杜有芹 杨柳 曲颂
鼻咽癌是一种起源于鼻咽上皮组织的恶性肿瘤[1]。虽然鼻咽癌在全球范围内并不属于常见肿瘤,但我国的鼻咽癌发病率和死亡率均高于世界平均水平,且我国鼻咽癌发病率和死亡率较高的区域主要集中在南方,尤其是两广地区(广西和广东)[2]。放射治疗是鼻咽癌的主要治疗手段及根治性治疗的重要组成部分。然而即使经过积极有效的治疗,仍然约有20%的鼻咽癌患者发生局部肿瘤复发和转移[3]。研究认为放射抗拒是导致鼻咽癌局部复发和转移的主要原因之一[4]。目前有大量研究表明放射抗拒的发生可能与microRNAs的异常表达有关[4-6]。本团队前期研究发现hsa-miR-6732-3p在放射抗拒组和放射敏感组鼻咽癌患者血清中的相对表达量有明显差异,且认为hsa-miR-6732-3p可作为评估鼻咽癌放射敏感性的生物标志物,具有潜在的应用价值[7]。基于本课题组的前期研究结果,为了进一步明确miR-6732-3p表达与鼻咽癌放射敏感性的关系,本研究采用慢病毒转染技术下调鼻咽癌放射抗拒细胞株CNE-2R中miR-6732-3p的表达,探讨沉默miR-6732-3p对CNE-2R细胞增殖、凋亡及放射敏感性的影响。
1 材料与方法
1.1 主要材料与试剂
鼻咽癌低分化细胞株CNE-2购自复旦大学附属肿瘤医院实验中心。鼻咽癌放射抗拒细胞株CNE-2R由本实验室前期在CNE-2细胞基础上通过分次照射的方法诱导构建并保存[8];miR-6732-3p慢病毒表达载体由GenePharma公司合成并构建。胎牛血清和RPMI 1640培养液等试剂均购于美国Gibco公司;1%青霉素、链霉素和胰蛋白酶消化液等试剂均购自中国碧云天公司;RNA抽提试剂Trizol购自美国Invitrogen公司;miRNA First Strand cDNA Synthesis试剂盒、RT-qPCR引物设计合成及2×SG Fast qPCR Master Mix试剂盒由生工生物工程(上海)股份有限公司生产;CCK-8试剂盒购自日本Dojino公司;Annexin V-APC/7-AAD试剂盒购于美国BD公司;4%多聚甲醛固定液和姬姆萨染液购于中国索莱宝公司。
1.2 方法
1.2.1 细胞培养及分组 CNE-2R细胞用含10%胎牛血清、100 U/mL青霉素及100 μg/mL链霉素的RPMI 1640培养基,在5% CO2、37℃恒温细胞培养箱中培养。实验分为正常对照组(CNE-2R)、转染对照组(miR-6732-3p NC)、转染组(miR-6732-3p inhibition)。
1.2.2 慢病毒转染CNE-2R细胞 取对数生长期CNE-2R细胞,以1×105/孔接种于6孔板,待细胞贴壁后加入慢病毒浓缩液,转染12 h后,弃上清,更换培养液。培养72 h后观察细胞荧光强度,检测转染效率。利用嘌呤霉素筛选出转染成功的CNE-2R细胞。
1.2.3 RT-qPCR检测细胞中miR-6732-3p的表达 用Trizol提取细胞总RNA,按miRNA First Strand cDNA Synthesis试剂盒操作步骤逆转录成cDNA。采用2×SG Fast qPCR Master Mix试剂盒和荧光定量PCR仪检测各组Ct值,选择U6作为内参,每个标本重复测量3次,数据采用2-△△Ct法进行分析。
1.2.4 CCK-8法检测细胞增殖能力 参考CCK-8试剂盒说明书操作。取对数生长期细胞,将各组细胞制成单细胞悬液,以 100 μL/孔(2×103个细胞)接种于96孔板中,每组设5个复孔。分别在0 d(细胞贴壁后)、1 d、2 d、3 d、4 d、5 d 检测各组细胞活性,吸出旧培养基,每孔加入100 μL 10%胎牛血清培养基和10 μL CCK-8混合液,继续培养2 h,然后在酶标仪上测定450 nm处的吸光度(OD)值。以各时间点OD值绘制细胞生长曲线。然后,检测三组细胞的放射敏感性,将细胞以2×103/孔的细胞数接种于96孔板中,每组根据不同照射剂量(0 Gy、2 Gy、4 Gy、6 Gy、8 Gy)分成5个亚组,待细胞贴壁后用6 MV-X射线给予相应剂量照射,照射结束继续培养72 h,然后检测各组细胞活性,检测方法同上。以存活分数(survival fraction,SF)评估每组细胞的放射敏感性,SF=ODnGy/OD0Gy。
1.2.5 流式细胞术检测细胞凋亡 按凋亡试剂盒说明书进行。取生长状态良好,细胞融合度约为40%的细胞每组各两瓶,每组各取1瓶接受0 Gy和8 Gy射线照射,继续培养72 h后,收集各组细胞培养液,1 000 r/min离心5 min,弃上清,收集细胞;用胰蛋白酶消化贴壁细胞,收集细胞并转移至相应离心管中,PBS洗涤2次;用0.5 mL 1×Binding Buffer制备单细胞悬液;每管先后加入5 μL Annexin V-APC及5 μL 7-AAD试剂,室温避光孵育15 min,每管加入300 μL Binding Buffer混匀。利用流式细胞仪检测细胞凋亡率。
1.2.6 克隆形成实验检测细胞的存活分数 收集各组细胞并接种于6孔板中,每个剂量设3个复孔。给予贴壁细胞单次射线照射,照射剂量分别为0 Gy、2 Gy、4 Gy、6 Gy、8 Gy,接种细胞数分别对应为 200/孔、200/孔、400/孔、600/孔、800/孔,照射后静止培养 10~14 d。采用4%多聚甲醛固定液固定和姬姆萨染液染色后使用显微镜计数集落数(≥50个细胞数为有效集落)。计算不同剂量照射下的细胞SF值,计算公式如下:克隆形成率(plating efficiency,PE)=克隆数/种植细胞数;SF=PEnGy/PE0Gy,PEnGy代表受照射细胞的PE,PE0Gy代表未受照射细胞的PE。用单击多靶模型拟合剂量-存活曲线,并计算放射生物学参数D0、Dq及SF2。
1.3 统计学方法
采用SPSS 17.0软件进行统计学分析,计量资料以均数±标准差(±s)表示。两组间比较采用独立样本t检验;多组间比较采用单因素方差分析,若组间差异有统计学意义,进一步的多重比较采用LSD-t检验。重复测量数据采用重复测量方差分析进行组间比较,进一步的多重比较采用Bonferroni检验。放射生物学参数和细胞存活曲线使用GraphPad Prism 5拟合。本研究中的各项实验均重复3次。以P<0.05为差异有统计学意义。
2 结果
2.1 miR-6732-3p在CNE-2和CNE-2R细胞中的表达
RT-qPCR检测结果显示,与CNE-2细胞相比,miR-6732-3p在CNE-2R细胞中的表达明显升高(1.00±0.00 vs 2.43±1.22,t=-2.855,P=0.036),见图 1。
2.2 慢病毒转染CNE-2R细胞并验证其表达
慢病毒转染CNE-2R细胞后,在荧光显微镜下均观察到绿色荧光蛋白表达,说明转染成功,见图2A。流式细胞仪检测结果显示,转染对照组和转染组细胞的绿色荧光蛋白阳性率均达到80%以上,见图2B。RT-qPCR检测结果显示,3组细胞中miR-6732-3p的相对表达量比较差异有统计学意义(P=0.001),其中转染组与正常对照组和转染对照组比较差异均有统计学意义(t=12.376,P<0.001;t=4.310,P=0.006),而两对照组间差异无统计学意义(t=0.884,P=0.427),见图3。
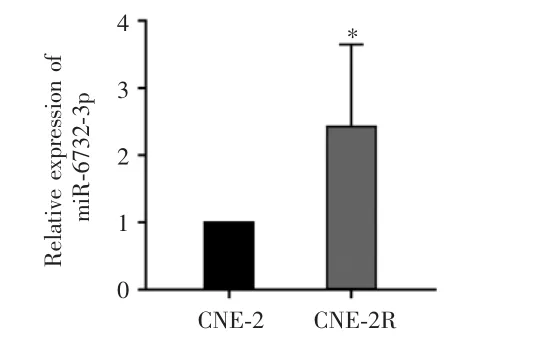
图1 miR-6732-3p在CNE-2和CNE-2R细胞中的表达Fig.1 Expression of miR-6732-3p in CNE-2 and CNE-2R cells
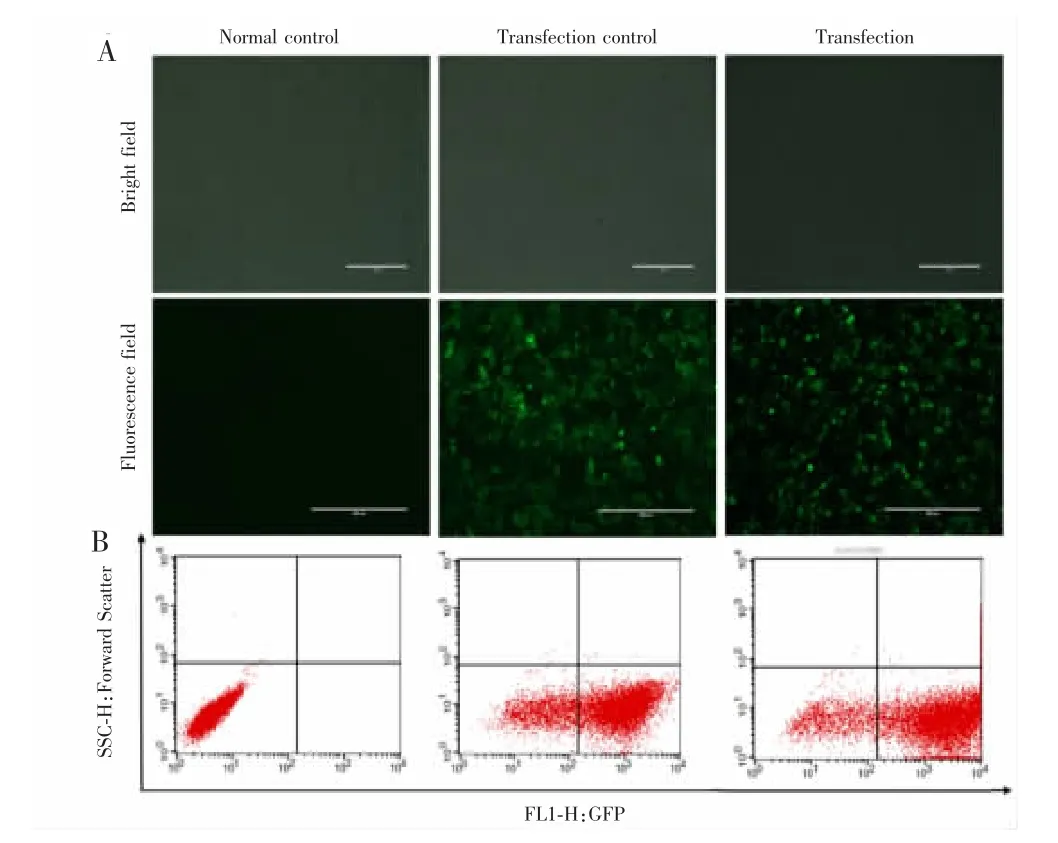
图2 CNE-2R细胞慢病毒转染率Fig.2 Lentivirus infection rates in CNE-2R cell
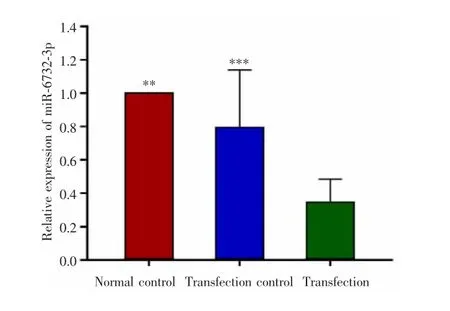
图3 RT-qPCR检测转染后各组细胞中miR-6732-3p的表达Fig.3 Expression of miR-6732-3p in each group cells aftertransfection detected by RT-qPCR
2.3 沉默miR-6732-3p对CNE-2R细胞增殖的影响
CCK-8检测结果显示,三组细胞的增殖能力差异有统计学意义(F=305.373,P<0.001),其中转染组细胞增殖能力均低于正常对照组和转染对照组(P<0.001),且正常对照组和转染对照组的细胞增殖能力差异无统计学意义(P=0.105),见图4A。在不同照射剂量下三组细胞存活分数比较差异有统计学意义(F=50.789,P<0.001),其中在不同照射剂量下转染组细胞存活分数明显小于正常对照组和转染对照组(P<0.001),且两对照组间细胞存活分数比较差异无统计学意义(P=0.192),见图4B。
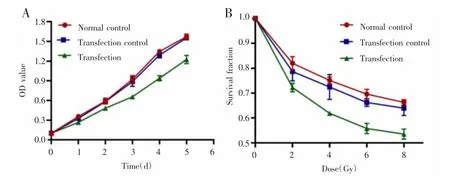
图4 沉默miR-6732-3p对CNE-2R细胞增殖的影响Fig.4 Effects of silencing miR-6732-3p on the proliferation of CNE-2R cells
2.4 沉默miR-6732-3p对CNE-2R细胞凋亡的影响
未照射(0 Gy)时,与对照组相比,转染组细胞凋亡率略增加,其中正常对照组、转染对照组和转染组的细胞凋亡率分别为(3.85±0.54)%,(4.56±0.35)%和(5.69±0.22)%,差异有统计学意义(F=16.714,P=0.004),而正常对照组和转染对照组细胞凋亡率差异无统计学意义(t=-1.907,P=0.129);接受8 Gy剂量照射后,三组细胞凋亡率分别为(7.99±1.06)%、(7.49±3.47)%和(19.74±1.21)%,差异有统计学意义(F=29.581,P=0.001),见图 5。
2.5 沉默miR-6732-3p对CNE-2R细胞放射敏感性的影响
采用不同剂量射线照射后,克隆形成实验结果显示,转染组细胞克隆数均少于正常对照组和转染对照组,见图6A。采用单击多靶模型拟合三组细胞的剂量-存活曲线,结果显示,各照射剂量下,转染组细胞的存活分数均低于正常对照组和转染对照组,三组间比较差异有统计学意义(F=240.256,P<0.001),见图 6B。放射生物学参数中,正常对照组和转染对照组的D0、Dq和SF2值差异无统计学意义(t=-0.025,P=0.981;t=1.423,P=0.228;t=-0.011,P=0.991),但与转染组比较差异均有统计学意义(P<0.05),见图7。克隆形成实验结果提示沉默miR-6732-3p可提高CNE-2R细胞的放射敏感性。
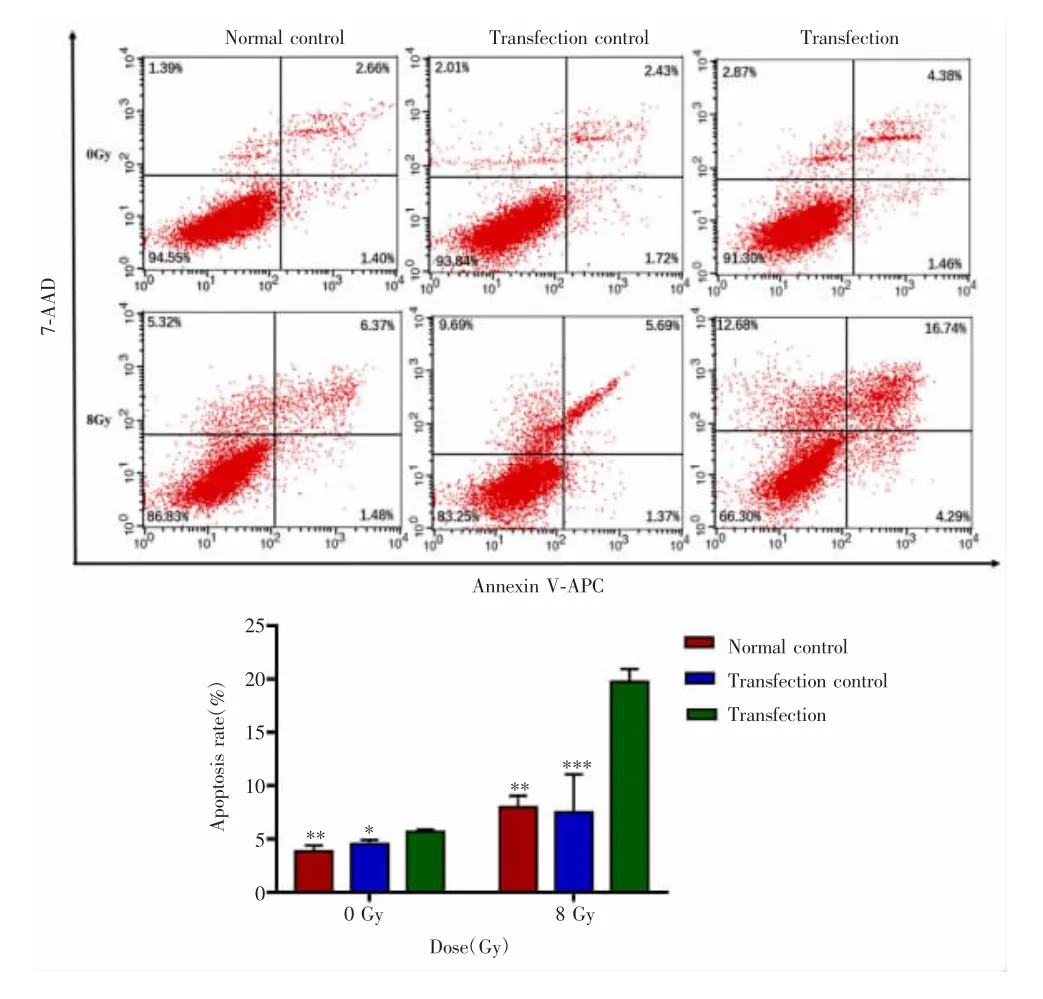
图5 不同处理组细胞接受0 Gy和8 Gy照射后的细胞凋亡率Fig.5 The changes of apoptosis rate in different treatment groups after 0 Gy and 8 Gy irradiation
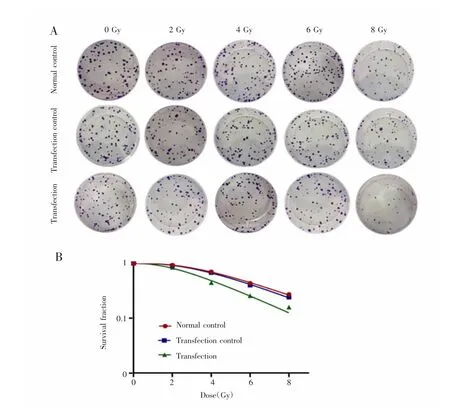
图6 沉默miR-6732-3p对CNE-2R细胞放射敏感性的影响Fig.6 Effects of miR-6732-3p silencing on radio-sensitivity of CNE-2R cells
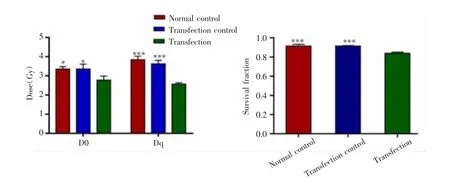
图7 不同处理组细胞单击多靶模型的放射生物参数Fig.7 The radiobiological parameters of single-hit multi-target model in different treatment groups
3 讨论
microRNAs(miRNAs)是一类长 18~25 个核苷酸的非编码单链RNA分子,其作用机制是通过降解靶mRNA或抑制靶mRNA翻译,使基因在转录水平后沉默,从而调节细胞增殖、凋亡、周期和肿瘤血管生成,参与放射抗拒[9]。近年来,越来越多的研究发现miRNAs与鼻咽癌的发生发展存在密切关系[10-12],尤其在miRNAs调节鼻咽癌放射敏感性方面已有较多报道。ZHU等[13]采用高通量测序技术筛选了鼻咽癌细胞株CNE-2和由其诱导构建的放射抗拒细胞株CNE-2-1细胞中的miRNAs,结果发现下调miRNA-21可增强鼻咽癌放射敏感性。同样地,LI等[14]用microRNA基因芯片检测了CNE-2和CNE-2R细胞的miRNAs谱,也发现下调miR-210表达可增强鼻咽癌细胞的辐射敏感性。周苏娜等[15]在放射抗拒的鼻咽癌细胞及临床标本中也发现miRNA-381表达量更高。本团队前期研究中选择鼻咽癌放射抗拒性患者和放射敏感性患者血清作为样本,并利用基因芯片技术成功筛选了血清中miRNAs差异表达谱,发现miR-6732-3p在两组患者血清样本中的表达存在明显差异[7]。根据前期初步实验结果,本研究进一步对CNE-2与CNE-2R细胞中miR-6732-3p的相对表达量进行检测,同样发现miR-6732-3p在两种鼻咽癌细胞中的表达量存在明显差异。
研究发现肿瘤细胞的放射敏感性与细胞乏氧、细胞增殖活性、细胞凋亡及DNA损伤修复密切相关,本质是相关基因在应对射线时的生物反应不同,与放射生物效应过程相关的各种基因变异、基因多态性及表观修饰等均可造成放射敏感性的差异[16]。为了观察miR-6732-3p对鼻咽癌放射敏感性的影响,本研究利用慢病毒转染技术沉默CNE-2R细胞中miR-6732-3p的表达,观察转染前后细胞增殖、凋亡及放射敏感性的变化。通过CCK-8实验检测细胞增殖能力,结果发现下调miR-6732-3p可使CNE-2R细胞增殖受抑制,同时提高了CNE-2R细胞的放射敏感性,因此推测miR-6732-3p可能通过抑制细胞增殖而提高细胞的放射敏感性。
凋亡又称程序性死亡,当细胞受到各种信号刺激后,通过转录凋亡相关基因从而导致细胞自杀死亡的过程。凋亡也是细胞受到辐射后的主要死亡方式。有研究认为肿瘤细胞放射敏感性与放射诱导的细胞凋亡密切相关[17]。本研究流式细胞仪检测结果显示,鼻咽癌细胞在接受0 Gy和8 Gy剂量的射线照射后,转染组细胞凋亡率均较对照组升高,8 Gy剂量照射下细胞凋亡更显著,进一步下调miR-6732-3p发现可增强CNE-2R细胞放疗敏感性,说明miR-6732-3p可能通过调节细胞凋亡而影响鼻咽癌细胞的放射敏感性。细胞剂量-存活曲线是放射生物学中的重要参数,D0为平均致死量,指在存活曲线的直线部分把存活分数从0.1降到0.037或从0.01降到0.0037所需的剂量,反映的是不同或同一细胞对放射敏感性的变化,D0值越小说明细胞对射线越敏感。而Dq为准阈剂量,反映细胞亚致死性损伤修复能力的大小,Dq越小说明细胞修复能力越小,对辐射越敏感。SF2为2 Gy时的存活分数。本研究分析各组细胞单击多靶模型的放射生物参数,结果转染组细胞D0、Dq和SF2值均小于两个对照组,说明miR-6732-3p的表达量高低可影响鼻咽癌细胞的放射敏感性。
综上所述,本研究利用慢病毒转染技术沉默miR-6732-3p可显著提高鼻咽癌CNE-2R细胞的放射敏感性,但是miR-6732-3p调节鼻咽癌放射敏感性的具体机制尚不明确,后续研究将进一步预测其发挥作用的靶基因,并通过细胞和动物实验相结合的方式深入探讨其作用机制,为血清中miR-6732-3p成为鼻咽癌放射敏感性分子标志物提供依据,从而为鼻咽癌放射增敏治疗提供新的治疗靶点。

