甲状腺过氧化物酶抗体光激化学发光间接检测法的建立
金 鑫 陈红霞
(上海大学生命科学学院,上海 200444)
光激化学发光是以纳米级高分子微粒为基础的新一代化学发光技术,在免疫检测中应用前景广阔。具有快速、均相(免冲洗)、高灵敏和操作简单的特点[1]。因其方法的核心特点为均相免冲洗(分离)模式,所以在实际运用中采用夹心法或者竞争法等可一步完成反应。目前还未在光激化学发光平台上有间接法检测的应用。
甲状腺过氧化物酶(thyroid peroxidese,TPO)是一种糖基化血红素蛋白,是甲状腺细胞上的跨膜蛋白,其膜外区的部分酶具有催化活性[2]。甲状腺过氧化物酶抗体(Anti-TPO)的检测始于20世纪80年代,1985年Czarnocka等首先证实纯化的微粒体抗原就是TPO,随后建立了竞争性与非竞争性Anti-TPO免疫分析法(非竞争法多为间接法)[3]。目前Anti-TPO的检测已经成为临床自身诊断免疫性甲状腺疾病,尤其是桥本氏甲状腺病的重要参考指标[4]。检测Anti-TPO的主流方法有酶联免疫分析、化学发光免疫分析、时间分辨荧光免疫分析等[5]。
本研究通过制备免疫复合物IgG的多抗,将发光微粒偶联TPO,生物素标记抗免疫复合物IgG抗体,建立了一步间接法用于检测人血清Anti-TPO浓度的光激化学发光免疫检测分析方法,并进行了该方法的性能评估。该Anti-TPO检测法在Lica平台上实现了间接检测,也对现有的Anti-TPO检测起到了方法学上的补充作用。
1 材料与方法
1.1材料
1.1.1实验材料与试剂 人IgG和BCATM Protein Assay Kit购自赛默飞公司;乙肝核心抗原购自深圳菲鹏公司;重组TPO购自DIARECT AG;Anti-TPO国家标准品购自中国食品药品检定研究院;96孔反应微孔板购自浙江拱东医疗科技有限公司;发光微粒和Lica通用液(链霉亲和素包被的感光微粒)由博阳生物科技(上海)有限公司提供;伯乐质控品购自美国Bio-Rad公司;Biotin-NHS购自Sigma公司。
1.1.2主要仪器 CR21G高速冷冻离心机,自日立公司;Lica 500自动光激化学发光检测仪由嘉兴凯实公司提供;粒径仪Nicomp 370、酶标仪(型号MK3)购自赛默飞公司。
1.2方法
1.2.1人IgG免疫耐受建立 根据文献[6]将100 mg的人IgG溶解于5 ml的生理盐水后与经过抗凝处理的5×109个兔红细胞混合,1 000 r/min离心5 min分离兔红细胞,从而去除能与兔红细胞特异性识别并结合的IgG。将上清液超速离心(15 000 r/min)90 min,取上层1/3的液体,得到处理后的人IgG溶液(去除IgG多聚物,IgG多聚物注射进体内倾向于产生免疫反应而非耐受)。将处理后的人IgG溶液透析至生理盐水,并稀释至10 mg/ml,经兔耳缘静脉注射1 ml人IgG,通常在1周后兔子可以产生免疫耐受,该耐受持续时间可以达到45 d以上,因此选择在免疫2周后使该兔子处于免疫耐受条件下进行后续实验。
1.2.2免疫复合物IgG制备及免疫 用5 ml注射器预先吸取2 ml用于保存红细胞的阿氏液(取20.5 g葡萄糖、8 g柠檬酸钠、0.55 g柠檬酸、4.2 g氯化钠,溶于1 L纯水。将配制好的溶液高压灭菌15 min,冷却后放置于4℃环境内,保存备用),从兔耳缘静脉抽取兔全血2~3 ml并轻轻混匀[7];将抗凝的兔全血转移至15 ml离心管,加满生理盐水混匀后1 000 r/min离心5 min;弃上清,重新加入生理盐水并混匀,1 000 r/min离心5 min,重复上述清洗步骤3遍,得兔红细胞,并计数。取2×109个兔红细胞,加入5 ml正常人血清(预先经凝集反应筛选),混匀后室温反应15 min,混匀;1 000 r/min离心5 min,弃上清;沉淀加生理盐水,混匀,1 000 r/min离心5 min,清洗3遍,加生理盐水至终体积2 ml,免疫复合物IgG制备完成。
在上述经过免疫耐受的兔子背部多点注射兔红细胞免疫复合物IgG,1周后重复以上操作,再次免疫,共免疫4次[8]。
1.2.3抗免疫复合物IgG抗体的分离和纯化 心脏取血,对血清中的抗免疫复合物IgG抗体进行纯化,其原理利用抗免疫复合物IgG抗体可以识别免疫复合物的特点,通过偶联免疫复合物填料的亲和柱将抗免疫复合物IgG抗体进行分离纯化。具体过程是首先制备乙肝核心抗原偶联填料的亲和柱,用乙肝核心抗体阳性血清通过该亲和柱,乙肝核心抗体和乙肝核心抗原会形成免疫反应,使亲和柱表面形成乙肝核心抗原-乙肝核心抗体的免疫复合物,再将需进行纯化的兔血清过此亲和柱,使兔血清中抗免疫复合物IgG抗体识别乙肝核心抗原-乙肝核心抗体的免疫复合物并结合至该亲和柱,用PBS(pH7.4)洗涤,并用0.1 mol/L甘氨酸(pH3.0)缓冲液将形成免疫反应的抗体洗脱。洗脱液用PBS(pH7.4)透析,透析后的洗脱液中会包含乙肝核心抗体(人抗体)及抗免疫复合物IgG抗体(兔抗体)。再将以上透析后的洗脱液经过人体IgG免疫亲和柱(吸附其中的乙肝核心抗体),收集穿透液即为抗免疫复合物IgG抗体,用BCATM Protein Assay Kit检测该抗免疫复合物IgG抗体的蛋白浓度,4℃保存备用。
1.2.4发光微粒偶联TPO 取10 mg粒径为200 nm的发光微粒(微粒表面有活性醛基,浓度为20.5 mg/ml),离心去上清,超声分散至0.1 mol/L、pH8.6的碳酸氢钠缓冲液中,按照发光微粒和蛋白10∶0.1加入TPO(0.1 mg),加入氰基硼氢化钠(NaCNBH3)还原,37℃反应过夜,离心去上清,清洗未结合在发光微粒表面的TPO,离心清洗完成后用PBS将偶联上TPO的发光微粒定容至10 mg/ml,作为发光珠包被浓溶液4℃保存备用。
1.2.5生物素标记抗免疫复合物IgG抗体 取1 mg 的抗免疫复合物IgG抗体,抗体和生物素以1∶30(摩尔比)比例加入生物素(Biotin-NHS),4℃混合反应过夜,用透析的方法去除未结合在蛋白上的生物素,将生物素标记好的抗免疫复合物IgG抗体定容至1 mg/ml,作为生物素标记浓溶液,4℃保存,备用。
1.2.6研制试剂的反应原理 研制试剂包括发光微粒偶联TPO的发光微粒试剂,生物素标记抗免疫复合物IgG抗体的生物素标记试剂辅以链霉亲和素(SA)包被感光微粒的Lica通用液进行检测。当样品中存在Anti-TPO时,加入发光微粒试剂和生物素标记试剂后会形成发光微粒-TPO-Anti-TPO-生物素标记抗免疫复合物IgG抗体的复合体,再加入Lica通用液后,会形成发光微粒-TPO-Anti-TPO-生物素标记抗免疫复合物IgG抗体-SA-感光微粒的复合体。从而使得发光微粒和感光微粒紧密联系,在680 nm激发光下,完成化学发光过程。
1.2.7定标品的制备 用含1%BSA的PBS将Anti-TPO国家标准品进行稀释,配制成0、10、30、120、400、1 400 U/ml的定标品,分装成0.5 ml/管,-20℃保存备用。
1.2.8检测方法 将发光珠包浓溶液用0.02 mol/L HEPES缓冲液(pH8.0,1%BSA)稀释到40 μg/ml,作为发光微粒试剂;将生物素标记浓溶液用0.05 mol/L Tris缓冲液(pH值8.0,0.1%BGG)稀释到1 μg/ml,作为生物素标记试剂。
在96孔反映微孔板中,每孔依次加入定标品或待测样品10 μl、发光微粒试剂50 μl、生物素标记试剂50 μl,然后将微孔板置于LiCA HT光激化学发光检测仪内,第一步温育设定为37℃温育900 s,LiCA通用液加液量设置为175 μl,其后在37℃温育600 s后,进行信号采集及读数。
1.2.9检测方法的评价
1.2.9.1最低检测限 最低检测限是指区别于零点的最低分析物浓度。重复检测20孔定标品1(0 U/ml),计算其RLU均值(AVE)和标准偏差(SD),以AVE+2SD反代入标准曲线,得到的浓度值即为本检测方法的最低检测限。
1.2.9.2回收率 取已知浓度1 000~1 200 U/ml的患者血清样品,对其连续5次对倍稀释,测定每次稀释后的样品浓度,并与其理论浓度进行比较,计算每次稀释的回收率。回收率=(实测值/理论值)×100%
1.2.9.3重复性(精密度) 检测伯乐质控低、中、高3个水平(伯乐质控品批号:Level 1 lot:60201,Level 2 lot:60202,Level 3 lot:60203)的重复性,将伯乐质控低、中、高3个水平各平行做20孔,计算变异系数(CV)。
1.3统计学分析 取117份临床患者血清样本,分别用本研究建立的Anti-TPO检测试剂(光激化学发光法)和贝克曼试剂(化学发光法)进行检测,将两种方法的测值结果进行相关性分析。
2 结果
2.1最低检测限 最低检测限具体计算结果见表1、2,通过总标线计算,最终检测限为0.09 U/ml。
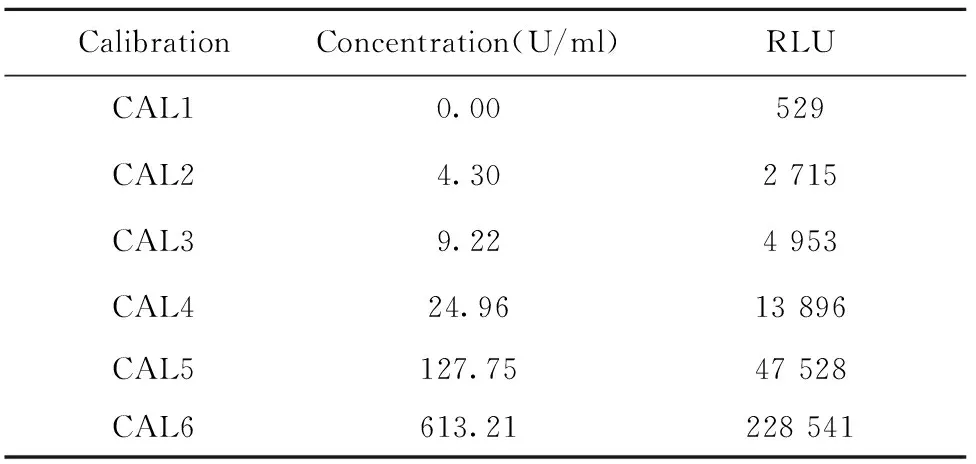
表1 定标曲线Tab.1 Calibration curve
2.2回收率 取已知测值为1 098.25 U/ml的患者血清,将其连续5次对倍稀释,测定每次稀释后的样品值,测定结果如表3,回收率分别为98.86%、98.55%、96.58%、95.10%和92.19%,结果均分布在90%~110%之间,平均回收率为96.26%。
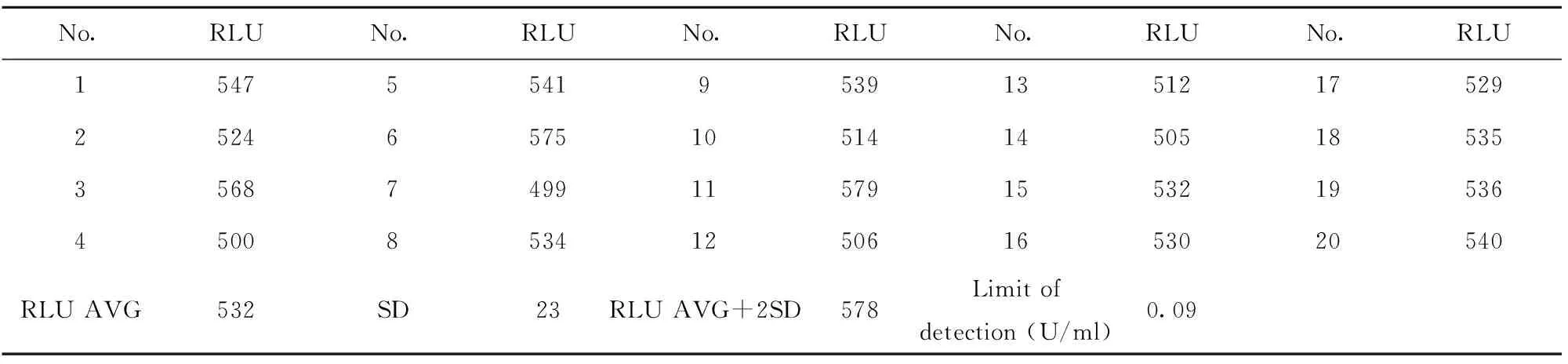
表2 定标品1检测结果Tab.2 Result of calibration 1
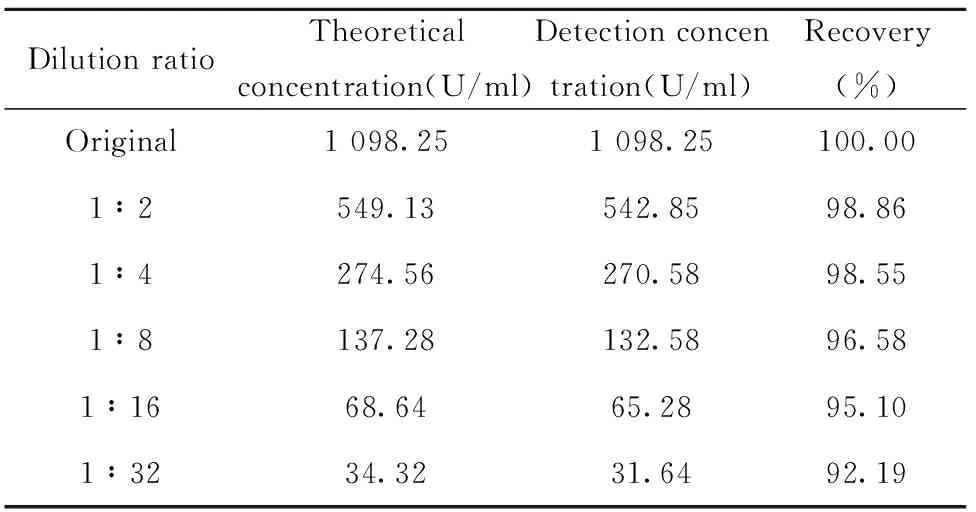
表3 已知Anti-TPO浓度的血清检测回收率Tab.3 Recovery ratio analysis of serum
2.3重复性(精密度) 对伯乐质控品3个浓度水平样品各检测20孔,进行相关的精密度计算,测定结果见表4,可知level 1~3的重复性分别为1.58%、1.97%、1.73%,重复性均小于5%,表现良好。
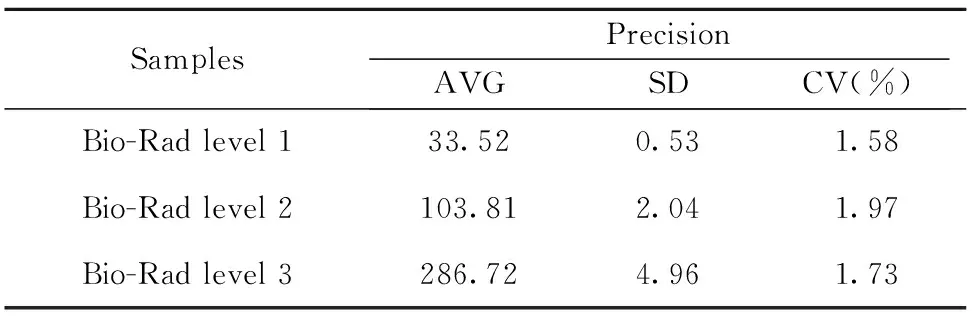
表4 精密度分析Tab.4 Precision analysis
2.4方法学相关性分析 相关性曲线见图1,直线方程为y=1.027x+2.463,相关系数r为0.989,大于0.975,斜率为0.9~1.1,符合要求。实验结果表明,两种检测方法具有较好的相关性。
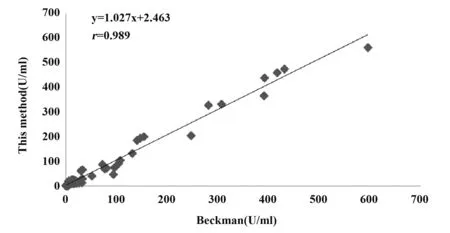
图1 本研究新建方法与贝克曼化学发光法相关性分析Fig.1 Correlation analysis between newly-established method in this study with Beckman test
3 讨论
光激化学发光反应是一种均相免疫反应[9]。在两种微粒表面包被抗原或抗体,通过免疫反应将两种微粒拉近,从而使得单线态氧从感光珠表面传递至发光珠表面,致使发光珠发光。因此,该方法的最大特点就是均相反应无需清洗和分离,但造成了间接法很难在该平台上使用。
传统的间接法检测Anti-TPO,是将TPO抗原进行包被,与样本先进行反应。如果样本中有Anti-TPO,其会与包被抗原进行反应,然后通过洗涤将与包被抗原反应的抗体和未反应的其他抗体进行分离。再加入标记的抗人IgG的二抗,实现对人血清中的Anti-TPO的活性浓度的检测。
本研究通过使用抗免疫复合物抗体作为标记抗体,实现了对TPO及其抗体形成的免疫复合物的特异性识别,从而实现了一步法免清洗的免疫间接法检测,并将其成功应用于Lica平台。
通过最终性能的检测评估,本方法设计的光激化学发光定量检测甲状腺过氧化物酶抗体的方法(间接法原理)与传统化学发光法的相关性较好,最低检测限、回收率和精密度等指标也符合临床需求。
随着免疫检测技术的发展,均相免洗的免疫检测方法的优势会越来越明显,由于均相免洗带来的操作便捷,检测重复性好,灵敏度高等优势正是现在免疫技术的关注焦点[10]。而均相技术在检测抗体时难以使用间接法检测的问题也会限制研发人员对这些技术的应用。通过使用抗免疫复合物抗体,本研究成功地在Lica平台上实现了间接法检测Anti-TPO。同样本研究也可以采取该技术手段在Lica平台上实现类似与Anti-TPO等其他抗体的间接法检测。甚至可以将其推广到其他的均相免洗的免疫检测方法中去。

