脑卒中患者运动功能自动化评定研究进展
刘朗,刘勇国,李巧勤,杨尚明,金荣疆,何霞
1.电子科技大学信息与软件工程学院中医知识与数据工程实验室,四川成都市 610054;2.成都中医药大学养生康复学院,四川成都市 610075;3.四川省八一康复中心,四川成都市610035
脑卒中是世界范围内主要致死性疾病之一[1]。我国40 岁以上人群脑卒中患者达1242万,每年新发患者超过270万,存活人群中超过70%存在不同程度功能障碍[2],包括运动、感觉、认知‑心理、言语和吞咽障碍等[3]。运动功能障碍指患者的肌肉控制、移动能力或活动水平受限或完全丧失,常涉及患者单侧或双侧面部、上肢和下肢,影响超过80%脑卒中患者[4],是脑卒中患者最常见、最严重的功能障碍,严重影响患者的家庭和生活质量[5]。运动康复是降低脑卒中患者致残率最有效的方法,有助于改善患者运动功能,提升独立生活能力,更好回归家庭与社会[6]。脑卒中运动功能康复流程包含问诊与临床检查、评定、治疗及院外康复训练等环节[7]。评定是康复治疗的重要环节,通过评定了解患者功能障碍性质和严重程度,至少在治疗前、中、后期各进行一次[8],根据最新评定结果制定康复治疗目标和治疗方案[9]。
脑卒中运动功能评定涉及运动控制、平衡、步态和关节活动度等方面[10],临床主要通过量表方式进行,常用量表包括Brunnstrom分期、Fugl‑Meyer评定量表(Fugl‑Meyer Assess‑ment,FMA)、Tinetti平衡与步态量表、Berg平衡量表(Berg Bal‑ance Scale,BBS)等[10‑12]。该评定方式存在以下问题:①需专业评定师完成,评定过程耗时长[13‑14];②受评定师主观影响,结果存在个体差异[15‑16];③评定量表选择存在差异和通用性问题[17‑18]。
近来,康复医学正向个性化、精确化、远程化、智能化发展,精准评定是脑卒中康复评定的必然趋势[19]。为弥补传统评定方法不足,方便家庭环境下康复评定开展,融合传感器技术和机器学习实现运动功能自动化评定日益受到重视。传感器用于感知患者运动过程的运动学及电生理学等信息,常用传感器包括惯性测量单元(inertial measurement unit,IMU)、表面肌电图(surface electromyography,sEMG)测试仪和深度传感器等。由于传感器信号存在噪声,需要通过信号预处理,提取均值、方差等时域和频域特征,向量化表示运动强度、范围、频率等信息,构建机器学习模型,自动获得运动功能评定结果(图1)。本文针对脑卒中运动功能评定领域运动控制、平衡、步态、关节活动度(range of motion,ROM)等方面,综述脑卒中运动功能自动化评定的国内外最新研究进展。
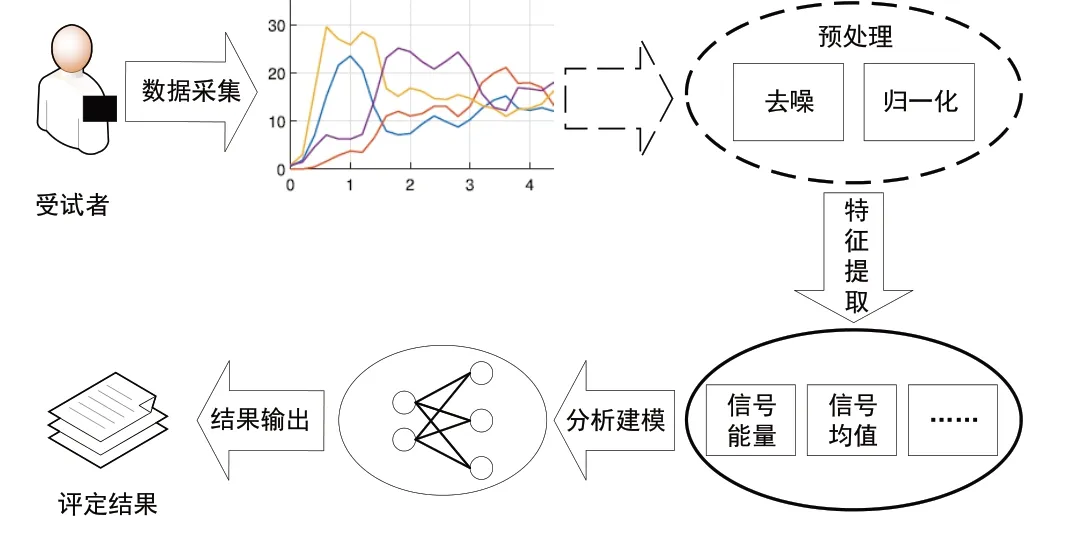
图1 运功功能自动化评定流程
1 运动功能
脑卒中存在不同程度神经系统损伤,导致肌张力升高,引发肢体运动控制功能障碍,常表现为肢体一侧活动范围受限或瘫痪[20]。运动控制功能评定内容包括肌张力、灵活性、稳定性、协调性和运动模式等[21]。引入深度视频、IMU、sEMG 等传感器技术进行客观测量,通过统计分析和机器学习法进行自动化评定,有助于获得客观准确的评定结果。
Zhang 等[17]将IMU 固定于患侧前臂,采集摸肩动作过程中的加速度,使用动态时间规整算法计算患者数据与正常人数据的欧式距离,再输入K 近邻分类器计算上肢Brunnstrom 分期,对21例脑卒中患者试验,该自动化评定准确度82.1%。
Liparulo 等[18]提出基于几何无约束隶属函数的模糊核分类方法,采集三角肌中束单通道sEMG,提取最大振幅、平均振幅等时/频域特征,自动化评定9 例不同程度脑卒中患者Brunnstrom分期,准确率92.47%。
Brunnstrom 分期体系具有评分简单、耗时短、易被患者接受等优点,在临床获得广泛应用[22],但存在敏感性差等不足。FMA 在Brunnstrom 分期基础上对评定任务与评分规则进行细化,提高了信度和敏感性,但也增加了应用难度。Chiang 等[23]采集三角肌前束和中束、肱三头肌长头和外侧头、肱二头肌、背阔肌和肱桡肌sEMG,引入隐马尔可夫模型提取患者运动状态特征,通过多变量自回归模型自动化评定脑卒中患者运动功能,准确率90%。
Yu 等[24]设计远程FMA 自动化评定框架,使用2 个加速度计和7 个柔性传感器捕捉上肢、手腕和手指运动,提取传感器信号的时域特征,利用极限学习机算法对运动数据自动分类并生成评分,24例患者试验结果表明,自动化评定所得结果与传统评定结果的决定系数达0.918。
Lee等[25]构建脑卒中患者上肢FMA 自动化评定系统,使用深度传感器Kinect和力量电阻传感器采集人体关节相对位置和手指抓握力量,将33项上肢评定任务分为5种类型,设计二进制逻辑分类算法以预测患者FMA 评定结果,结果显示,系统能对79%评定任务进行自动化评定,评定时间比传统评定方式减少85%,准确率达92%。
2 平衡功能
平衡与协调功能是人体保持姿势与体位,完成各项日常生活活动的基本保证[26]。脑卒中患者感觉输入、中枢整合、躯干控制等功能受损,影响平衡能力,增加跌倒风险[27‑28]。静态与动态平衡功能的临床评估主要通过仪器和量表完成[29]。专业平衡测试仪器操作复杂,空间环境要求高。基于传感器测量的自动化评定系统可提供客观评定结果,且便于使用。
Similä 等[30]通过腰部绑定三轴加速度计,采集受试者执行3 项BBS 任务过程数据,使用K 近邻算法进行相似性分类,实现BBS 评分,对54 例神经疾病患者、老年人和健康年轻人进行试验,自动评分平均误差4.85分。
Badura 等[31]在患者背部、左右髋与脚踝共5 个位置绑定IMU,采集患者执行14 项BBS 任务的加速度和角速度信号,提取时/频域特征,分别构建Fisher线性判别分析器进行特征降维,再输入多层感知机分类器获得各任务评分,对64 例老年人试验结果表明,BBS自动评分平均误差1.55分。
Bacciu 等[32]使用Wii 平衡板采集患者执行BBS 任务时前后左右四角重力分布数据流,患者无需佩戴附加设备,通过内嵌储备池计算范式的回声状态网络对序列数据进行特征提取,输出层估算BBS 得分,对21 例志愿者进行BBS 自动评分,平均误差3.80分。
3 步态分析
步态异常为脑卒中患者常见功能障碍,是影响日常生活能力和生活质量的主要因素。脑卒中发病6个月后,约50%~80%患者存在不同程度下肢功能障碍和步态异常[33]。步态分析对制定康复治疗方案和评价疗效具有重要参考意义[34]。临床步态分析方法包括主观量表法和定量步态分析。前者通过主观方式评价步行能力,描述步态异常程度;后者需要价格昂贵的专业设备与场地,并且评定时间较长。借助便携传感器和高效数据分析,可快速获得步态参数,为定量步态参数分析提供新思路。
Motiian等[35]提出基于深度传感器Kinect的儿童步态周期自动分割方法,将最大似然估计、均匀尺度估计、非均匀尺度估计和子序列匹配相结合,解决幼儿群体骨骼跟踪数据噪声的高变异性问题,通过2~4 岁健康儿童步态分析,步行阶段分割准确率高于90%。
Zhao 等[36]将IMU 固定于双脚,搭建惯性导航系统进行步态分析,使用不等式约束的零速更新算法辅助惯性导航系统,识别步态周期阶段并计算步态参数,该系统可准确计算步态周期中脚跟着地、站立、脚跟离地和摇摆期时间,有助于医护人员制定治疗计划。
Tunca 等[37]提出一种IMU 步态分析系统,扩展零速更新和卡尔曼滤波算法,提取步幅、节律、周期、姿态时间、摇摆时间、姿态比、速度、最大/最小间隙和转化率等步态指标,对16例健康人和6例神经疾病患者进行分析,该系统获得的步长和摇摆时间与基于红外深度相机三维步态分析结果的相关性系数分别为0.98和1。
Eguchi等[38]结合激光距离传感器(laser range sensor,LRS)和内置压力传感器鞋垫进行步态分析,LRS 用于测量患者步幅、周期和步行速度,鞋垫内置压力传感数据用于计算地面接触力(ground contact force,GCF)和压力中心(center of pressure,CoP),通过直线行走试验,与图像运动捕捉技术相比,下肢运动跟踪精度的均方根误差≤50 mm;与足底力量测量板的CoP 数据相比,X、Y轴坐标CoP轨迹均方根误差分别<16 mm和<5 mm。
4 ROM
ROM 是评定关节运动功能的重要指标[39],系测量大关节在运动状态下的活动角度,条目繁多,传统采用量角器测量,十分费时,重复性差且精确度低,通常最小刻度值为5°[40]。
王杰[41]结合传感器、嵌入式软件、串口通信等技术,使用SCA100T‑D02 倾角传感器研发ROM 评定嵌入式系统计算ROM。将量角尺一条臂固定,旋转绑定有传感器的另一条臂,可实时获取关节角度,经4例受试者重复10次测量,与量角器测量结果相比,平均误差约0.95°。
Lee 等[42]设计无线可穿戴上肢关节ROM 自动化测量系统,使用智能手机收集7 个IMU 的惯性运动数据,选取12 项FMA的评定任务,系统不仅能自动识别所测任务,还可计算关节最大活动角度,与量角器测量结果平均误差0.82°。
葛云等[43‑44]将光学定位设备NDI Polaris Spectra 应用于ROM 测量,将反光小球固定于人体骨性标志点,收集反光小球的三维坐标,使用最小二乘法拟合肢体运动轨迹和轴心,计算关节活动角度,测量平均误差0.313°。
Neto 等[45]利用深度传感器Kinect采集人体深度图像,提取骨骼三维位置信息,计算上肢关节角度,实现动态、非接触式ROM 评估关节,肩外展/内收、肘屈/伸测量结果与量角器法无显著性差异。
5 展望
当前,研究人员将传感器技术与机器学习方法引入脑卒中运动功能自动化评定领域,研究工作仍处于起步阶段,存在以下问题:①传感器单一,而运动控制障碍常表现为身体多部位变化,且不同阶段表现不同[19],单一传感器难以全面准确地反映;②平衡功能自动化评定多关注动态平衡,根据先验知识提取传感器数据时域、频域静态特征,忽略数据动态变化及相互间依赖关系,导致特征提取欠充分,影响评定结果的准确性;③临床步态分析关注患者步态异常特征,而现有步态自动化评定工具主要识别步态行为并估算运动学参数,缺乏步态异常特征分析;④ROM 自动评估由于存在多个关节测量情况,多关节可穿戴式传感器标记困难,深度视频传感器虽受患者干扰低,但存在视频遮挡问题。
针对上述问题,脑卒中运动功能自动化评定可开展以下研究:①多源多模态数据获取,如针对上肢运动控制,除结合人体运动学和机体构造,获取IMU、肌电、握力等传感器数据外,可考虑人口统计学、临床诊断等信息,引入多模态数据融合与特征选择方法开展特征融合与关键属性选取;②设计深度学习模型表示康复多变量时间序列特征,捕获多传感器数据间相互关系和时间维度演化特征;③引入模式挖掘技术开展临床数据与步态异常特征关联分析,辅助医生制定个性化康复治疗方案;④开展基于多源多维深度传感器的运动关节三维空间运动捕捉,避免视频遮挡问题,实现ROM非接触式精准评定。
目前,脑卒中发病日益增加,传统人工评定不能较好满足日益增长的康复需求。运动功能自动化评定通过传感器技术和机器学习方法建立运动功能障碍程度与数据模型的评估关系,经过实验和临床验证,获得较好性能表现。后续脑卒中运动功能自动化评定将在传感器便携性、精准性、易操作性和深度人工智能技术的引入方面深入发展,在改善康复效果、降低医疗成本、减轻医生负担等方面扮演日益重要的角色,促进社区和家庭康复健康发展。

