角层下脓疱性皮病合并结缔组织病二例
刘洋爱 董正邦 王 飞
东南大学附属中大医院皮肤科,南京,210009
临床资料患者1,女,53岁。因“全身反复水疱、脓疱1年余,加重1周”入院。1年前无明显诱因胸背部、双下肢出现红斑,后在红斑基础上出现散在绿豆至黄豆大水疱,并逐渐变为脓疱,伴轻度瘙痒,可自行好转。此后多次反复发作,外用药物效果不佳。1周前患者上述症状再次加重,皮疹以双乳下及双小腿为著。既往有“高血压、2型糖尿病、类风湿关节炎”病史,长期口服甲泼尼龙片8 mg/d+羟氯喹0.2 g/d控制类风湿关节炎病情。
体格检查:心肺腹查体未见明显异常,双侧手关节可见“纽扣花样”畸形,伴活动受限。皮肤科查体:胸背部可见点状色素沉着及叶状鳞屑,双乳下、双小腿可见粟粒至绿豆大脓疱,疱壁松弛,呈弦月状,周围有红晕,尼氏征阴性,部分脓疱破裂愈合后遗留薄痂,口腔、外阴等黏膜未受累(图1)。辅助检查:CRP 8.04 mg/L,血尿粪常规、生化、血沉、凝血功能等未见明显异常。疱液细菌培养阴性。皮损组织病理检查示:角层下脓疱形成,疱内中性粒细胞聚集,表皮稍萎缩,棘层上部细胞明显水肿,可见中性粒细胞移入,真皮上部小血管周围密集的以淋巴细胞和中性粒细胞为主的炎症细胞浸润(图2)。直接免疫荧光检查:IgA(-),IgG(-),IgM(-),C3(-)。结合临床、组织病理及免疫病理结果,诊断为角层下脓疱性皮病。
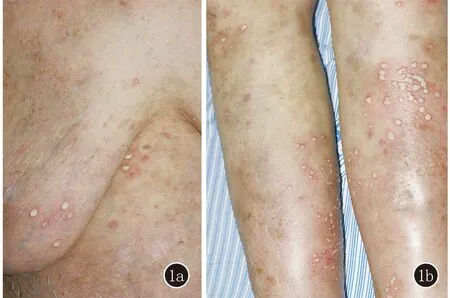
图1 1a:乳房下散在粟粒大脓疱,疱壁松弛呈弦月状,周围皮肤可见脓疱愈合后遗留薄痂;1b:双小腿见密集分布粟粒至绿豆大脓疱,疱壁松弛,周围红晕明显
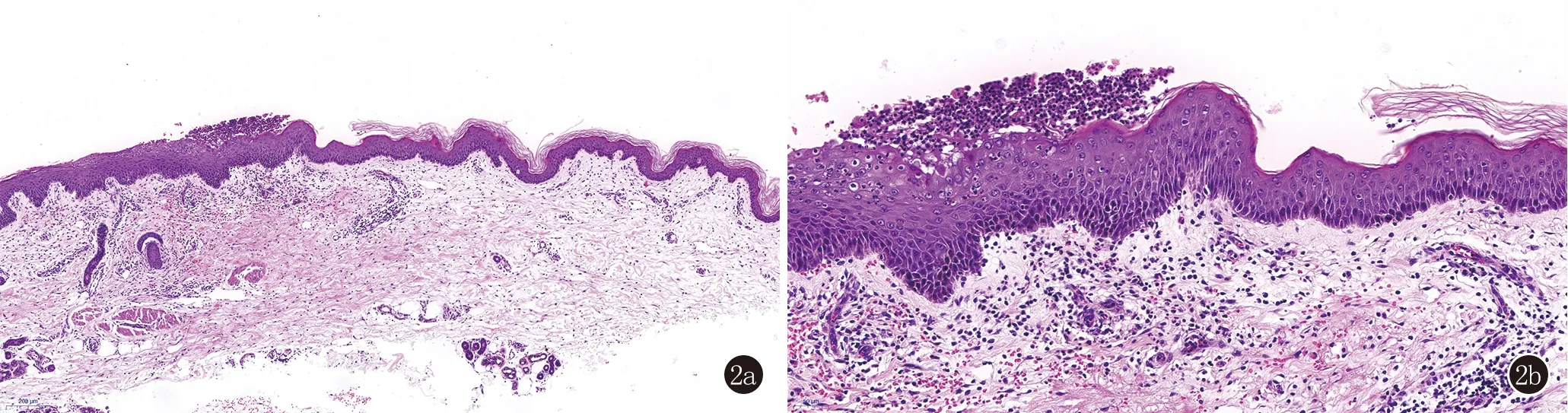
图2 2a、2b:角层下脓疱形成,疱内中性粒细胞聚集,表皮稍萎缩,棘层上部细胞明显水肿,可见中性粒细胞移入,真皮上部小血管周围密集的以淋巴细胞和中性粒细胞为主的炎症细胞浸润(HE,×40;×100)
治疗:予阿维A胶囊20 mg/d口服,8天后无新发水疱,原有皮损全部愈合,遗留点状色素沉着及薄痂(图3)。类风湿关节炎给予甲泼尼龙片8 mg/d+羟氯喹0.2 g/d治疗。
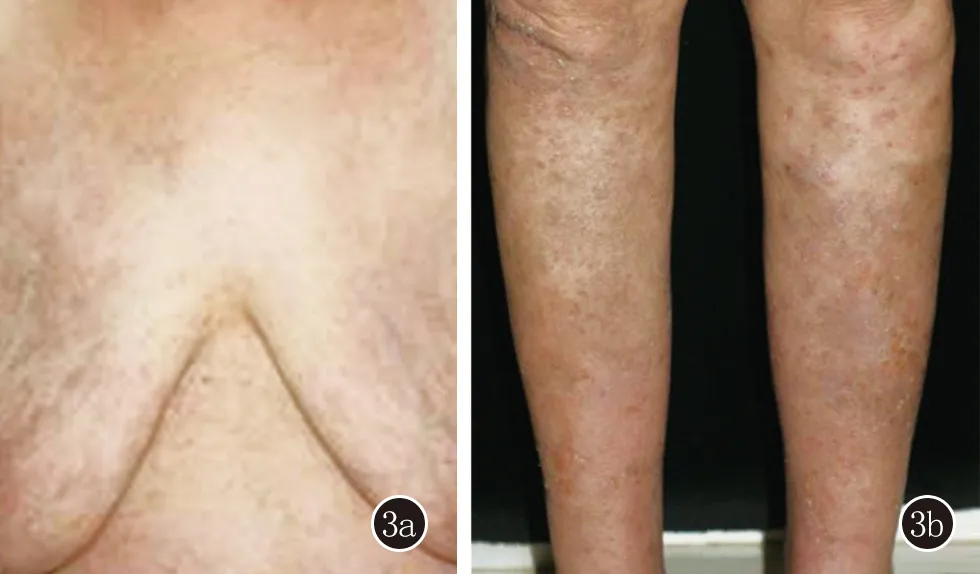
图3 3a、3b:双乳、双小腿皮损全部愈合,遗留点状色素沉着及薄痂
患者2,女,69岁。因“躯干、腋下及会阴部红斑、脓疱伴瘙痒2个月余”入院。2个月前无明显诱因腹部出现红斑,随后红斑上出现散在粟粒大脓疱,伴瘙痒,未处理。后皮损逐渐累及胸背部、双腋下及外阴,外院予“得宝松”肌注、“甲泼尼龙片4 mg/d”及“酮替芬”口服治疗后红斑颜色变浅,水疱数量减少。3天前患者背部、左髂部再次出现新发水疱。既往有“2型糖尿病、自身免疫性肝炎”病史。
体格检查:各系统检查未见明显异常。皮肤科查体:躯干、双腋下及外阴形状不规则暗红斑,融合成片,背部、左髂部红斑基础上可见散在粟粒大脓疱,尼氏征阴性,黏膜未累及(图4)。
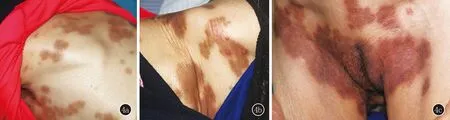
图4 4a~4c:躯干、外阴见形状不规则暗红斑,融合成片,背部及左髂部红斑上散在粟粒大脓疱
辅助检查:ESR 63 mm/h,体液免疫特定蛋白检测IgA 7.79 g/L,余检查血常规、生化、电解质等未见明显异常。眼科检查:BUT右眼3 s, 左眼3 s;泪液分泌试验:右眼5 mm/5 min,左眼1 mm/5 min。唾液腺ECT示:双侧腮腺及颌下腺摄取功能均减退。疱液细菌培养阴性,皮损组织病理检查示:角层下可见一水疱,其内大量中性粒细胞及少量棘刺松解细胞,真皮上部明显水肿,可见大量淋巴细胞、中性粒细胞为主的炎症细胞浸润(图5)。直接免疫荧光检查:IgA(-),IgG(-),IgM(-),C3(-)。结合临床、组织病理及免疫病理结果,诊断为角层下脓疱性皮病。患者有口干、眼干病史多年,外院查抗SSA抗体、抗Ro52抗体阳性,结合入院后眼科相关检查及唾液腺ECT,符合干燥综合症诊断标准。
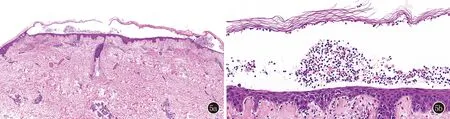
图5 5a、5b:角层下可见一水疱,其内大量中性粒细胞及少量棘刺松解细胞,真皮上部明显水肿,可见大量淋巴细胞、中性粒细胞为主的炎症细胞浸润(HE,×40;×100)
治疗:入院后予甲泼尼龙片16 mg/d,米诺环素50 mg日2次,10天后皮损基本消退,甲泼尼龙片逐渐减量中,随访至今,未复发。
讨论角层下脓疱性皮病(subcorneal pustular dermatosis,SPD)是一种罕见的慢性良性复发性皮肤病,好发于中年女性,皮损表现为正常皮肤或红斑基础上松弛的无菌性脓疱,主要累及躯干及褶皱部位,掌跖及头面部较少受累,但未成年患者头面部累及相对多见[1]。该病一般不侵犯黏膜,多不合并全身症状。目前病因不明,可能与感染、肿瘤、自身免疫紊乱等因素相关,具体发病机制可能涉及TNF-α、Th2。近年来,SPD被发现与TNF-α相关的其他疾病合并出现,如炎症性肠病、类风湿关节炎、坏疽性脓皮病和脓疱型银屑病。大多数SPD患者也被报道血清中IgA升高,与IgA单克隆丙种球蛋白病、多发性骨髓瘤有关,因此在诊断和病程演变过程中应注意排除[2]。另外,国外病理学家多数认为SPD属于一种与病原体感染有关的嗜中性皮病。Bohelay等[3]就曾报道过SPD与肺炎支原体感染有关,他们认为肺炎支原体感染可能是SPD的触发因素,常常因为无明显症状而被忽略,尤其是一些没有合并慢性疾病、不需要系统治疗的儿童或年轻SPD患者,需要高度考虑有无肺炎支原体感染可能。
SPD组织病理特征主要为角质层下的脓疱,疱内较多的中性粒细胞聚集,部分伴有嗜酸粒细胞,棘层松解细胞少见,真皮浅层血管周围可有以中性粒细胞为主的炎性细胞浸润。直接免疫荧光检查抗体阴性。
SPD的鉴别诊断有脓疱型银屑病、IgA天疱疮、落叶型天疱疮、疱疹样皮炎、急性泛发性发疹性脓疱病(AGEP)、脓疱疮等,通过皮损分布特征、病程特点、疱液细菌培养、直接免疫荧光及组织病理检查可鉴别。本文患者1合并有类风湿关节炎,还需要与类风湿性嗜中性皮炎相鉴别,其皮损主要表现为荨麻疹样丘疹、结节,也可出现斑块、红斑基础上的假性水疱,皮损直接免疫荧光检查自身抗体也阴性,但通常随RA病情改善而改善,组织病理最突出的特点是真皮内密集的中性粒细胞浸润,可延伸至皮下脂肪。患者2合并干燥综合症,Tsuruta[4]曾报道同时合并这两种疾病的患者出现过类似Sweet综合症样的环状红斑,应注意鉴别。
治疗上,尽管越来越多对氨苯砜耐药或不能耐受其不良反应的报道,但它仍是SPD的一线治疗方法,口服50~150 mg/d,病情稳定后小剂量维持数周至数年。儿童患者也首选氨苯砜,剂量与成人类似,但更需注意血液系统不良反应[5]。若效果差或出现不良反应,可次选糖皮质激素、阿维A、羟氯喹、PUVA、窄谱UVB、磺胺类药物、TNF-α抑制剂等药物或与氨苯砜联合治疗。Falcone等[6]曾报道使用TNF-α抑制剂己酮可可碱(PTX)成功治疗1例不能耐受氨苯砜不良反应且阿维A、糖皮质激素治疗效果差的患者。国外还有学者使用环孢素控制急性病情,稳定后使用氨苯砜维持治疗成功的报道[7]。
国外陆续有SPD合并类风湿关节炎、系统性红斑狼疮、干燥综合症等结缔组织病的个案报道,本文报道的2例角层下脓疱性皮病合并不同的结缔组织病,进一步佐证了SPD与自身免疫因素存在关联。其中TNF-α被认为是SPD中性粒细胞过度活化的主要趋化因子之一,并且已经在SPD患者的血清和疱液中检测出高水平[9]。而本文患者1合并类风湿关节炎,TNF-α作为类风湿关节炎发病机制的中心环节已得到众多研究的证实,TNF-α抑制剂也广泛用于临床上类风湿关节炎患者;患者2合并的干燥综合症、自身免疫性肝炎,同样通过不同环节最终致使TNF-α高水平。因此推测结缔组织病中免疫异常产生的高水平TNF-α可能是SPD发生的原因之一,但其具体发病机制与结缔组织病之间的联系尚未完全阐明。当然,也有学者认为SPD本身就是类风湿关节炎的皮肤表现之一[10],二者之间的具体关系有待进一步研究。据报道[8],SPD合并结缔组织病有使原有结缔组织病加重恶化的可能,除此之外,在类风湿关节炎患者中,SPD出现在血清阳性(RF阳性)患者中的频率较血清阴性患者略高,治疗方面,兼顾两者治疗对彼此病情均有改善。鉴于氨苯砜的不良反应,其次考虑到国内外均有应用阿维A及四环素成功治疗角层下脓疱性皮病的报道[11,12],本文患者1给予阿维A治疗,1周左右皮损全部愈合,但不排除类风湿关节炎控制病情用药(甲泼尼龙片及羟氯喹)辅助起效,患者2给予甲泼尼龙片及米诺环素治疗,10天后皮损也基本消退。两例患者均未予氨苯砜治疗,但疗效均较好,提示临床医师遇到此类患者可适当考虑选择氨苯砜以外的其他次选用药。

