一种选择性检测肼的近红外荧光增强型探针的合成
崔桂玲, 宋 艳, 胡曰富, 齐庆蓉
(四川大学 华西药学院,四川 成都 610041)
肼作为一种化学物质,由于其碱性和还原性,使其在医药、化学、催化、农业等领域有广泛应用,同时,肼也是一种高能量原料,所以也被应用于航天领域,然而该物质不仅有毒,还有致癌作用,微小量的泄露不仅会造成环境污染,也会对人体的肝、肾、肺、中枢神经、呼吸系统等造成伤害[1-5],因此对于微量肼的检测至关重要。
传统的检测肼的分析方法包括电化学分析法、色谱法和分光光度法,但这些分析方法不仅复杂耗时,而且灵敏度低[6-9]。相比于传统的肼检测方法,荧光分析法具有高灵敏性、高选择性、操作简便、成本低等优点[10-12],因此更受欢迎。文献报道的主要检测肼的基团有乙酰基、4-溴丁酸酯、乙酰丙酸盐、邻苯二甲酰亚胺、醛、丙二腈等,
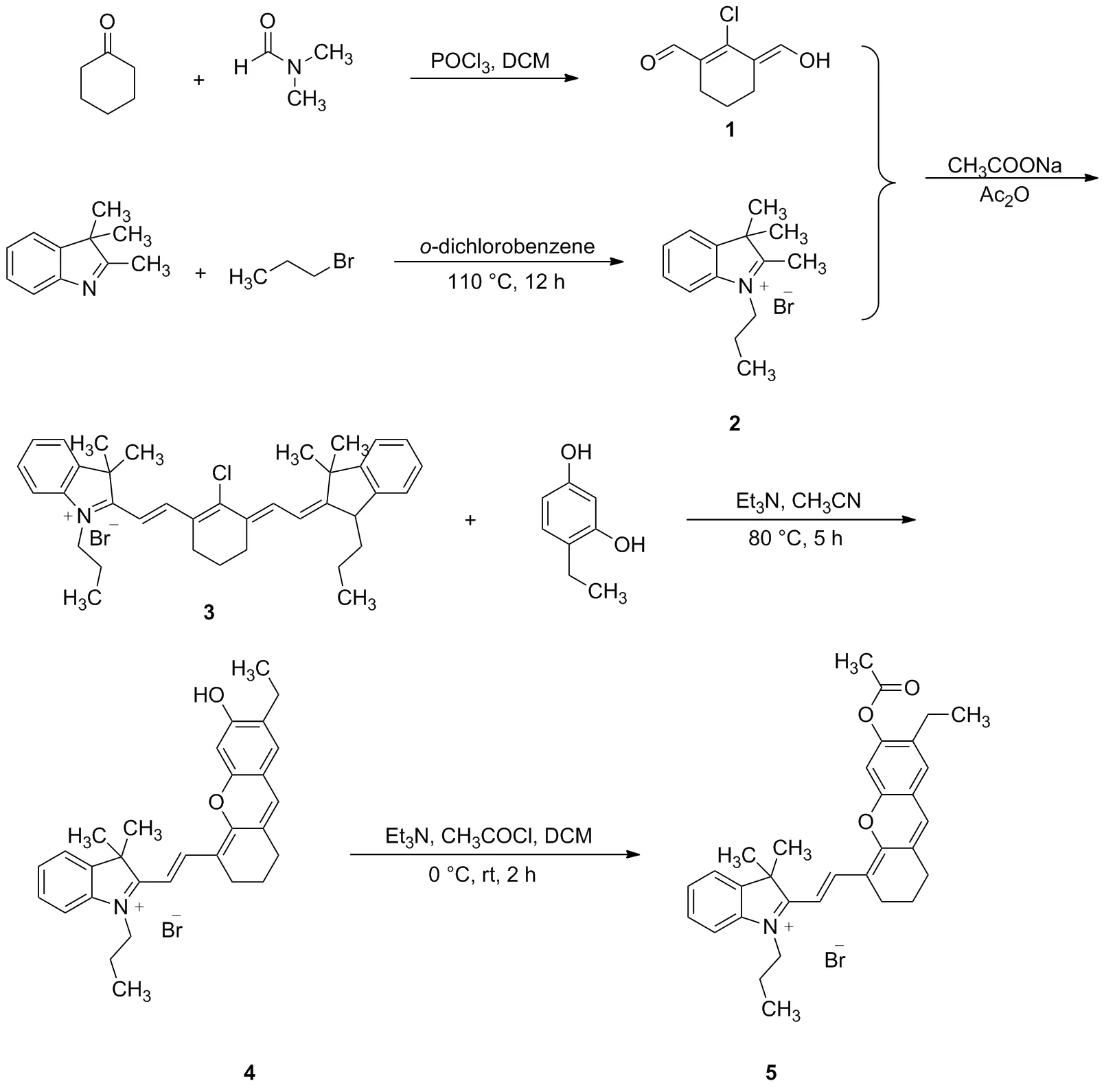
Scheme 1
但大部分探针的最大紫外吸收和发射均位于紫外可见光区,不适合生物成像。因近红外区的光具有较低的背景荧光,较低的光毒性和较深的穿透性[13-14],所以近红外荧光探针更具有应用价值。
2016年,Zhang等[13]发现了用乙酸酯作为识别位点的检测肼的近红外探针,2018年,Lu等[15]报道了用溴丁酸酯作为识别基团的检测肼的近红外探针,这类探针通过一个可以调控的羟基使探针及检测肼后产物的最大发射波长均位于近红外区,具有明显的降低自荧光、低毒性、深度渗透等优点,但两者最大发射波长很接近,难以观察到探针和产物各自荧光变化的线性。2012年,Lin等[16]报道在半花菁类分子(Chart 1)羟基的邻位引入氯原子可以改变半花菁分子的部分光学性质,但类似报道很少。鉴于此本文设计并合成了一个新型的检测肼的荧光探针,并对其进行了光谱分析,研究其对肼的选择性。以2,3,3-三甲基-3H-吲哚与正丙基溴为原料反应合成2,3,3-三甲基-1-丙基-3H-吲哚盐2,继而与2-氯-3-羟次甲基环己烯醛缩合生成2- (2-(2-氯-3-((3,3-二甲基-1-丙基-1,3-二氢-2H-吲哚-2-亚烷基)亚乙基)-1-环己烯-1-)乙烯基)-3,3-二甲基-1-丙基-3H-吲哚盐3,再与4-乙基间苯二酚在三乙胺催化下反应生成2-(2-(7-乙基-6-羟基-2,3-二氢-1H-呫吨-4-)乙烯基)-3,3-二甲基-1-丙基-3H-吲哚盐4,最后与乙酰氯经成酯反应生成半菁类探针2-(2-(7-乙基-6-乙酰氧基-2,3-二氢-1H-呫吨-4-)乙烯基)-3,3-二甲基-1-丙基-3H-吲哚盐5(Chart 2),探针结构经过1H NMR、13C NMR和HR-MS(ESI)表征。
1 实验部分
1.1 仪器与试剂
UV-2450型紫外可见分光光度计;Varian-Unity 400 MHz型核磁共振仪;Waters Q-TOF-Premier型质谱仪;Varian Cary Eclipse Fluoromete型荧光光谱仪。
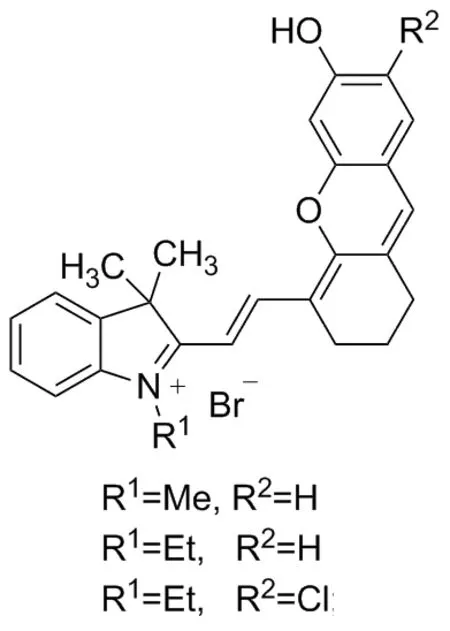
Chart 1
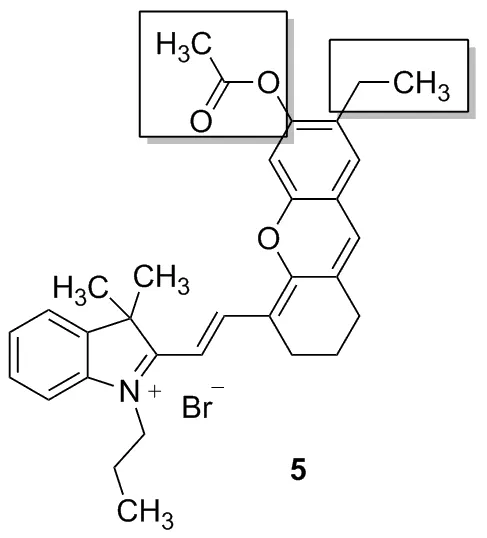
Chart 2
其余所用试剂均为分析纯。
1.2 合成
(1)1的合成[17-18]
在干燥的500 mL三颈瓶中加入N,N-二甲基甲酰胺37.2 g(0.5 mol)和二氯甲烷50 mL, 0 ℃下依次滴加三氯氧磷62.5 g(0.4 mol),环己酮10.0 g(0.1 mol), 80 ℃回流4 h;减压蒸除溶剂,冷却至室温后倾至冰水中,析出大量黄色固体,抽滤,滤饼用冰水洗涤3次,真空干燥,丙酮重结晶后得黄色固体19.0 g,收率51%, m.p.127~128 ℃;1H NMR(DMSO-d6, 400 MHz)δ: 10.84(s, 1H, CHO), 2.53~2.47(m, 1H, CH), 2.36(t,J=6.1 Hz, 4H, CH2), 1.58(p,J=6.3 Hz, 2H, CH2)。
(2)2的合成[17-19]
在干燥的250 mL三颈瓶中加入2,3,3-三甲基-3H-吲哚5.0 g(31.5 mmol)、正丙基溴4.7 g(38.1 mmol)和邻二氯苯15 mL,110 ℃搅拌12 h(TLC检测)。冷却至室温,倾倒入100 mL异丙醚中,大量粘性固体析出,静置,倾倒出上清液,加少量丙酮并搅拌,大量固体析出,抽滤,滤饼用异丙醚洗涤三次,得棕红色固体产物24.5 g。该产品不经纯化直接用于下一步。
(3)3的合成[17-18]
在干燥的100 mL三颈瓶中加入24.5 g(6.0 mmol)、11.9 g(11.0 mmol)、乙酸钠1.8 g(22.2 mmol)和乙酸酐8 mL,于室温搅拌2 h,(TLC检测)。加100 mL异丙醚,有大量绿色固体析出,抽滤,滤饼用异丙醚洗涤,得绿色固体产物36.9 g。该产品不经纯化直接用于下一步。
(4)4的合成[17]
在干燥的100 mL三颈瓶中加入3300.0 mg(49.6 mmol)、 4-乙基间苯二酚100.0 mg (72.4 mmol)、三乙胺270.0 mg(2668.2 mmol)和乙腈8 mL,回流5 h(TLC检测)。冷却至室温,减压蒸除溶剂,残余物经硅胶柱层析(洗脱剂:二氯甲烷/甲醇=100/1~30/1,V/V)纯化得青绿色固体4170.0 mg,收率68%;1H NMR(Methanol-d4, 400 MHz)δ: 8.15(d,J=13.4 Hz, 1H, CH=CH), 7.56(s, 1H, ArH), 7.30(d,J=7.4 Hz, 1H, ArH), 7.20(t,J=7.7 Hz, 1H, ArH), 7.17(s, 1H, ArH), 6.99(t,J=7.3 Hz, 1H, ArH), 6.95(d,J=8.0 Hz, 1H, ArH), 6.41(s, 1H, CH), 5.76(d,J=13.5 Hz, 1H, CH=CH), 3.82(t,J=7.4 Hz, 2H, CH2), 2.66(t,J=6.1 Hz, 2H, CH2), 2.57(t,J=6.7 Hz, 2H, CH2), 2.52(t,J=7.5 Hz, 2H, CH2), 1.82(p,J=6.3 Hz, 2H, CH2), 1.72(p,J=7.4 Hz, 2H, CH2), 1.61(s, 6H, CH3), 1.13(t,J=7.5 Hz, 3H, CH3), 0.94(t,J=7.4 Hz, 3H, CH3); HR-MS(ESI)m/z: Calcd for C30H34NO2Br{[M-Br]+}440.2584, found 440.2578。
(5)5的合成[15-16]
在干燥的25 mL单颈瓶中加入421.9 mg(42.2 nmol)、三乙胺60.0 mg(59.3 nmol)和二氯甲烷25 mL,于冰盐浴中搅拌,缓慢滴加乙酰氯110.0 mg(1.4 mmol)的二氯甲烷溶液2 mL,滴毕,室温搅拌2 h(TLC检测)。减压蒸除溶剂,残余物经硅胶柱层析(洗脱剂:二氯甲烷/甲醇=100/1~30/1,V/V)纯化得青绿色固体5150.0 mg,收率93%;1H NMR(CDCl3, 400 MHz)δ: 8.61(d,J=14.9 Hz, 1H, CH=CH), 7.55~7.37 (m, 4H, ArH), 7.27(s, 1H, ArH), 7.15(s, 1H, ArH), 7.04(s, 1H, CH), 6.70(d,J=14.8 Hz, 1H, CH=CH), 4.58(t,J=7.1 Hz, 2H, CH2), 2.80(t,J=6.1 Hz, 2H, CH2), 2.74(t,J=6.1 Hz, 2H, CH2), 2.58(q,J=7.5 Hz, 2H, CH2), 2.39(s, 3H, CH3), 2.08~1.87(m, 4H, CH2), 1.79(s, 6H, CH3), 1.21(t,J=7.5 Hz, 3H, CH3), 1.08(t,J=7.3 Hz, 3H, CH3);13C NMR(CDCl3, 100 MHz)δ: 178.30, 169.14, 160.27, 151.26, 150.81, 146.14, 142.00, 141.45, 133.86, 131.58, 130.17, 129.34, 127.76, 127.56, 122.52, 119.96, 115.40, 113.36, 109.96, 105.98, 50.91, 47.81, 29.49, 28.24, 24.56, 22.80, 21.59, 21.00, 20.26, 13.97, 11.59; HR-MS(ESI)m/z: Calcd for C32H36NO3Br{[M-Br]+}482.2690, found 482.2693。
2 结果与讨论
2.1 紫外-可见光谱
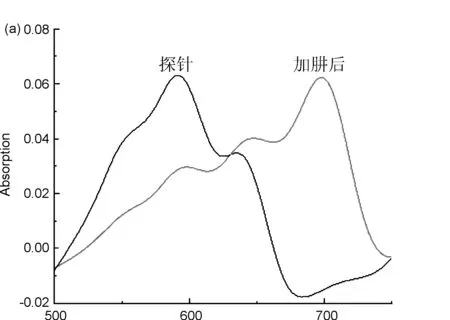
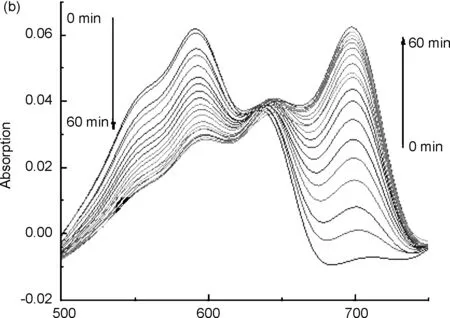
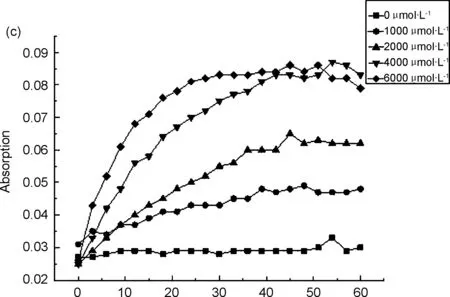
用15% DMSO PBS溶液(pH=7.4)分别配制20 μmol/L的探针5标准溶液和2000 μmol/L的肼溶液,两者等体积混合后,在避光条件下,每三分钟取样进行紫外扫描。由图1a可知,探针5的最大紫外吸收波长为598 nm,与肼反应后生成的产物最大紫外吸收波长为702 nm;由图1b可知,探针与肼反应60 min内,探针最大紫外吸收值逐渐降低,产物最大紫外吸收值逐渐升高,随着反应时间的延长,598 nm处的最大紫外吸收值逐渐降低,702 nm处的最大紫外吸收值逐渐升高,且加肼前后混合液的颜色变化明显,加肼之前为蓝色,加肼反应之后为青绿色,表明探针5能够检测肼;由图1c可以看出,探针与肼的反应时间随着肼浓度的增大而加快。与肼反应之前,探针5的羟基是以乙酸酯的形式存在,羟基氧原子给电子能力降低,最大紫外吸收波长较低,当与肼反应之后,产物主要以氧负离子的形式存在,氧原子给电子能力增强,故最大紫外吸收波长红移[16]。
2.2 荧光发射光谱
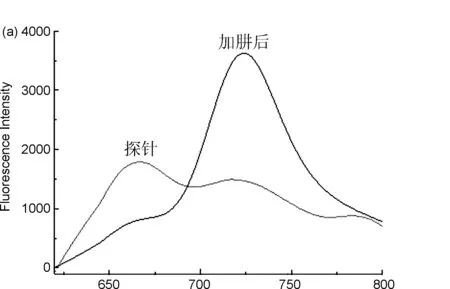
用DMSO配制浓度为640 μmol/L探针标准溶液,用15%DMSO的PBS缓冲溶液(pH=7.4) 将探针5标准溶液稀释成20 μmol/L,分别与不同浓度的肼等体积混合反应,得到荧光发射光谱(图2c)。用598 nm进行激发,可得到探针5的最大发射波长为666 nm,与肼反应之后,产物最大发射波长位于723 nm处(图2a),且产物的荧光强度随着时间的延长大幅度增加,探针的荧光强度缓慢减小(图2b)。
λ/nm
λ/nm
t/min
λ/nm

λ/nm
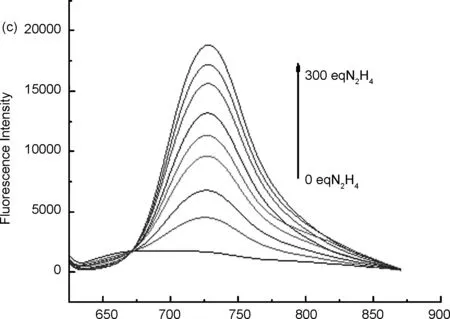
λ/nm图2探针5的荧光发射光谱(a: 加肼前后的变化情况; b: 探针与不同浓度肼混合后在666 nm和723 nm处的荧光强度变化情况; c: 探针对不同浓度肼的荧光强度变化)
根据光诱导电子转移原理(PET),当探针5的识别基团乙酰基处于自由态时,其HOMO轨道上的电子可以向荧光团的HOMO转移,致使荧光团被激发到LOMO轨道上的激发态电子不能返回基态产生荧光或荧光很弱,而乙酰基与肼结合之后,乙酰基的HOMO上的电子无法转移到荧光团的HOMO轨道上,使PET过程无法进行,这时荧光团的激发态电子可以返回基态产生荧光,故产物荧光远强于探针[20]。
2.3 选择性评价
选择性是评价探针的重要指标之一,因此本实验研究了探针5对可能的常见干扰物质 (2-羟基乙基胺、 KCl、 Na2SO4、 CaCl2、 MgSO4、 CuSO4、 ZnSO4、 FeCl3、 FeSO4、 NaBr、 CH3COONa、 K2CO3、 NaH2PO4、 NH4Cl、 NH3.H2O、二乙胺、尿素、硫脲、L-甘氨酸、L-赖氨酸、L-精氨酸、异烟肼和乙酰肼)的响应情况,分别向浓度为20 μmol/L的探针标准溶液中加入等体积的2000 μmol/L的待测物质溶液,室温避光放置48 min后,依次取样进行荧光扫描,结果表明,该探针5对上述物质无明显响应,对肼具有良好的选择性。
本文设计合成了一个可用于检测肼的近红外小分子荧光探针,通过可调控基团羟基,使探针5在与肼反应前后共轭结构发生改变,从而引起荧光强度的变化。探针5最大紫外吸收波长为598 nm,最大荧光发射波长为666 nm,与肼反应后的产物最大紫外吸收波长为702 nm,最大荧光发射波长为723 nm,当肼的浓度在0~1000 μmol/L时,荧光强度与浓度具有良好的线性关系,相关系数R2=0.9919,检测限为2.93 μmol/L。同时,该探针的最大发射波长位于近红外,有利于克服生物体自身荧光的干扰,有望成为一种理想的检测肼的荧光探针。

