局部晚期鼻咽癌放疗结束后影像学残留患者的预后分析*
肖勤,李战战,赵雅洁
(中南大学湘雅医院 1.放射科;2.肿瘤科;3核医学科,湖南 长沙 410008)
鼻咽癌是一类常见的头颈部恶性肿瘤,在中国,以两广(广东省、广西省) 两湖(湖南省、湖北省) 等地为高发区,且以中年男性患者居多[1-2]。到目前为止,放射治疗是鼻咽癌最主要的治疗方式,有研究显示,对于部分患者单纯放疗的局控率可以达到70%~90%[3]。调强适形放射治疗 (intensity modulated radiation therapy, IMRT) 因其可以保护重要组织结构,还能根据肿瘤的形状及体积进行照射,从而提高肿瘤靶区的照射剂量,所以在临床上广泛普及[4-5]。但有研究认为[6],鼻咽癌患者在放疗的早期,肿瘤体积明显缩小,可是到了放疗计划的中后期,因为克隆源性细胞(肿瘤干细胞等) 会出现放疗抵抗,对放疗抵抗的细胞比重逐渐增多,导致治疗结束后的一段时间内仍可见少量残留病灶,这成为鼻咽癌复发或转移的根源。有研究通过回顾性分析196 例无残留和108 例鼻咽部和(或) 颈部淋巴结有残留患者对生存率的影响[7],结果发现放疗后有残留的患者其3、5、10 年生存率均降低;其中仅鼻咽残留者生存率最高,其次为颈淋巴结残留者,两处均有残留者生存率最低;此外,颈淋巴结残留体积越大生存率越低;有残留的患者,其局部复发及远处转移率也明显增加。综上所述,针对鼻咽癌放化疗后残留病灶进一步进行风险分析,不仅是IMRT 后肿瘤残留患者预后评估的重要依据,还关系到制定鼻咽癌患者下一步的治疗计划。
本研究通过回顾性分析局部晚期鼻咽癌患者(74 例) IMRT 结束3~24 个月影像学证实局部残留患者的各项相关因素,寻找鼻咽癌放疗后影像残留与各临床因素之间的关系,并进一步进行预后分析,为放疗后影像学证实有残留的患者制定个体化综合治疗方案提供依据。
1 资料与方法
1.1 研究对象
研究收集了 234 例 2008 年 8 月至 2010 年 1月期间在中南大学湘雅医院肿瘤放疗科IMRT 治疗的鼻咽癌患者。纳入标准:①病理活检明确诊断为鼻咽癌且均行IMRT 治疗;②临床诊断为T3、T4,N 分期不限,且辅助检查证实为M0[美国癌症联合会(AJCC) 第 7 版分期][8];③放疗结束后3~24 个月复查头颈部磁共振证实肿瘤残留,最终共证实74 例鼻咽癌患者存在影像肿瘤残留。排除标准:①证实有远处转移的患者;②有严重内科合并症患者,如器官衰竭、严重感染、心功能障碍、肝肾功能不全、消化道有出血或穿孔倾向等;③精神病患者、家族遗传病患者及妊娠妇女;④在MRI 片上原鼻咽及颈部淋巴结区肿瘤消失并恢复正常解剖结构,增强后无强化。
1.2 治疗方法
①74 例患者均接受6 MV X 射线IMRT 治疗,肿瘤靶区勾画根据国际辐射单位和测量委员会(ICRU) 50 号和 62 号文件报告[9],处方剂量规定如下:鼻咽大体肿瘤体积(GTVnx) 2.0~2.4 Gy/f,共 66.0~79.2 Gy/33 f,5 次/周,颈部转移淋巴结(GTVnd) 1.8 Gy/f,5 次/周,共 69.96 Gy/33 f,肿瘤临床靶区高危区(CTV1) 60.06 Gy/33 f,肿瘤临床靶区低危区(CTV2) 50.96 Gy/28 f;并根据美国肿瘤放射治疗协作组(RTOG) 0225 文件设定危及器官剂量[10]。②化疗:70 例患者均接受以铂类为主的化疗,4 例患者因无法耐受或拒绝化疗等因素未行化疗;③靶向治疗:9 例患者接受表皮生长因子受体(EGFR) 单克隆抗体治疗。
1.3 疗效评价
1.3.1 残留的判断标准 MRI 检查:鼻咽黏膜明显强化且增厚大于1 cm;放疗后颈部淋巴结、咽后淋巴结残留直径分别大于1.0 cm 和0.5 cm 则认为影像残留;周围软组织区放疗后仍可见明显异常信号灶且明显强化则认为影像残留;放疗前副鼻窦无受侵,放疗后出现则考虑炎症。治疗前无侵犯的部位出现强化信号多考虑放疗后炎性反应[11]。
1.3.2 判断复发MRI 标准 放疗结束后复查MRI发现原残留病灶大小、信号强度持续6 个月及以上无明显改变,或原治疗区再次出现异常信号灶并伴有明显强化且经活检证实为相同的病理类型则认为肿瘤复发[12]。
1.4 研究方法
采用回顾性分析,对患者性别、年龄(≤50 岁、>50 岁)、AJCC 第 7 版分期 (Ⅲ期、Ⅳa 期)、GTVnx 残留体积、GTVnd 残留体积、鼻咽大体肿瘤体积及颈部转移淋巴结(GTVnx+nd) 残留体积的分组根据ROC 曲线寻找最优临界值,见图1。其中GTVnx 残留体积的临界值为6.825 mL (曲线下面积 0.665, P=0.019, 差异有统计学意义),GTVnx+nd 残留体积的临界值为11.315 mL (曲线下面积 0.677, P=0.012, 差异有统计学意义),GTVnd 残留体积的临界值为3.360 mL (曲线下面积0.554, P=0.442,差异无统计学意义)。因此,将GTVnx 残留体积按 6.825 mL 分为≤6.825 mL 组、>6.825 mL 组;GTVnx+nd 残留体积按 11.315 mL分为≤11.315 mL 组、>11.315 mL 组;计划鼻咽肿瘤靶区(PGTVnx) 处方总剂量根据中位数74.25 Gy (69.96~80.60 Gy) 分 为 ≤74.25 Gy 组 、>74.25 Gy 组,根据化疗方案及分子靶向治疗等因素进行整理分析。
1.5 随访
从患者确诊时开始直至末次2020 年1 月1 日随访为止,中位随访时间107 个月(12~126 个月),死亡23 例。
1.6 统计学方法
数据处理采用SPSS 23.0 统计软件。计数资料以百分率(%) 表示,比较做χ2检验;Kaplan-Meier 法绘制ROC 曲线;影响因素的分析用多因素一般Cox 回归模型。P<0.05 为差异有统计学意义。

图1 鼻咽癌残留体积的ROC 曲线分析
2 结果
2.1 临床资料
研究对象中男52 例,女22 例;年龄22~77 岁(中位年龄45 岁)。病理类型:低分化鳞癌69 例(93.2%),其他 5 例(6.8%)。依据 AJCC 第 7 版分期,Ⅲ、Ⅳa 期患者比例分别为10 例(14%)、64 例(86%)。①残留部位:在234 例鼻咽癌患者中证实共有74 例患者存在肿瘤残留,本院治疗后鼻咽癌残留率约为31.6%。其中,GTVnx 残留组52 例,按照鼻咽残留部位的不同统计发现,鼻咽癌残留病灶在颅底的发生率最高(43 例,82.7%),其次为咽旁 (16 例, 30.8%)、 鼻咽 (14 例,26.9%) 及副鼻窦(11 例,21.2%);GTVnd 残留组8 例;GTVnx+nd 残留组14 例。②残留体积:GTVnx 残留组残留体积为0.24~51.94 mL;GTVnd残留组残留体积为0.35~15.01 mL;GTVnx+nd 残留组残留体积为0.35~51.94 mL。③残留直径:GTVnd残留组残留直径为6.2~19.0 mm;④残留时间:>6~12 个月的 44 例,>12 个月的 25 例。
2.2 治疗结果
单纯转移10 人、单纯复发13 人、复发+转移4 人、死亡23 人(其中因肿瘤死亡15 例、并发症等原因死亡8 例)。5 年总生存率(OS)、局部无复发生存率(LRFS)、无远处转移生存率(DMFS)分别为70.8%、78.5%、77.5%,见图2。
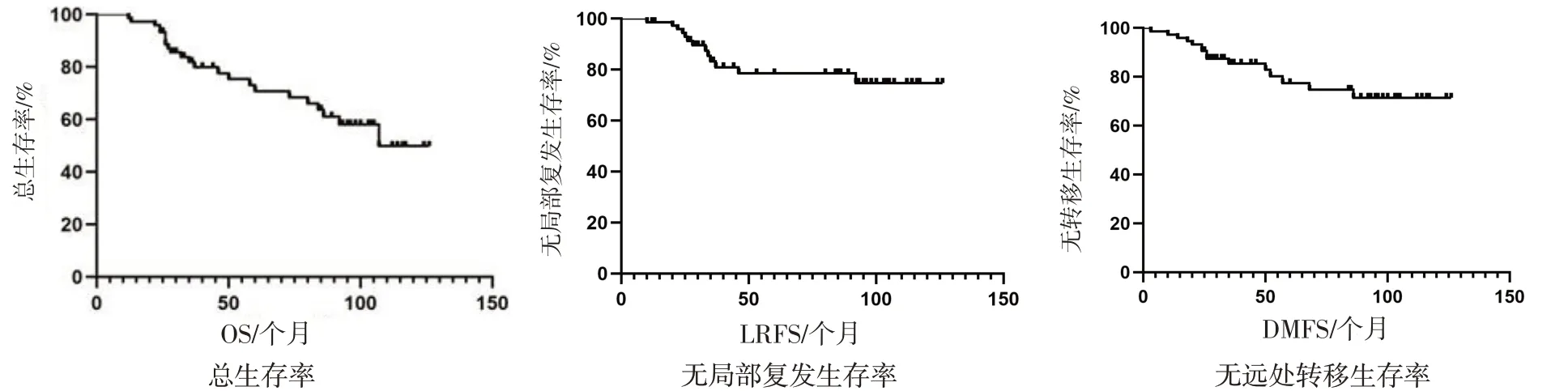
图2 鼻咽癌患者的生存曲线
2.3 单、多因素分析
单因素分析纳入了年龄、性别、AJCC 第7 版分期、残留体积、残留时间、靶区剂量、化疗方案及靶向治疗等因素,结果表明:GTVnx 残留体积、GTVnx+nd 残留体积、AJCC 分期及放疗剂量是影响总生存率的重要因素,前两项还是影响无复发生存率的重要因素,差异均有统计学意义(P<0.05),见表1。多因素采用一般Cox 比例风险回归模型,将上述单因素分析有统计学意义的因素作为自变量,总生存和局部无复发生存分别为因变量,做多因素一般Cox 回归分析,结果发现,AJCC 分期及放疗剂量为影响OS 的预后因素,见表2。GTVnx 残留体积为影响LRFS 的独立预后因素,见表3。
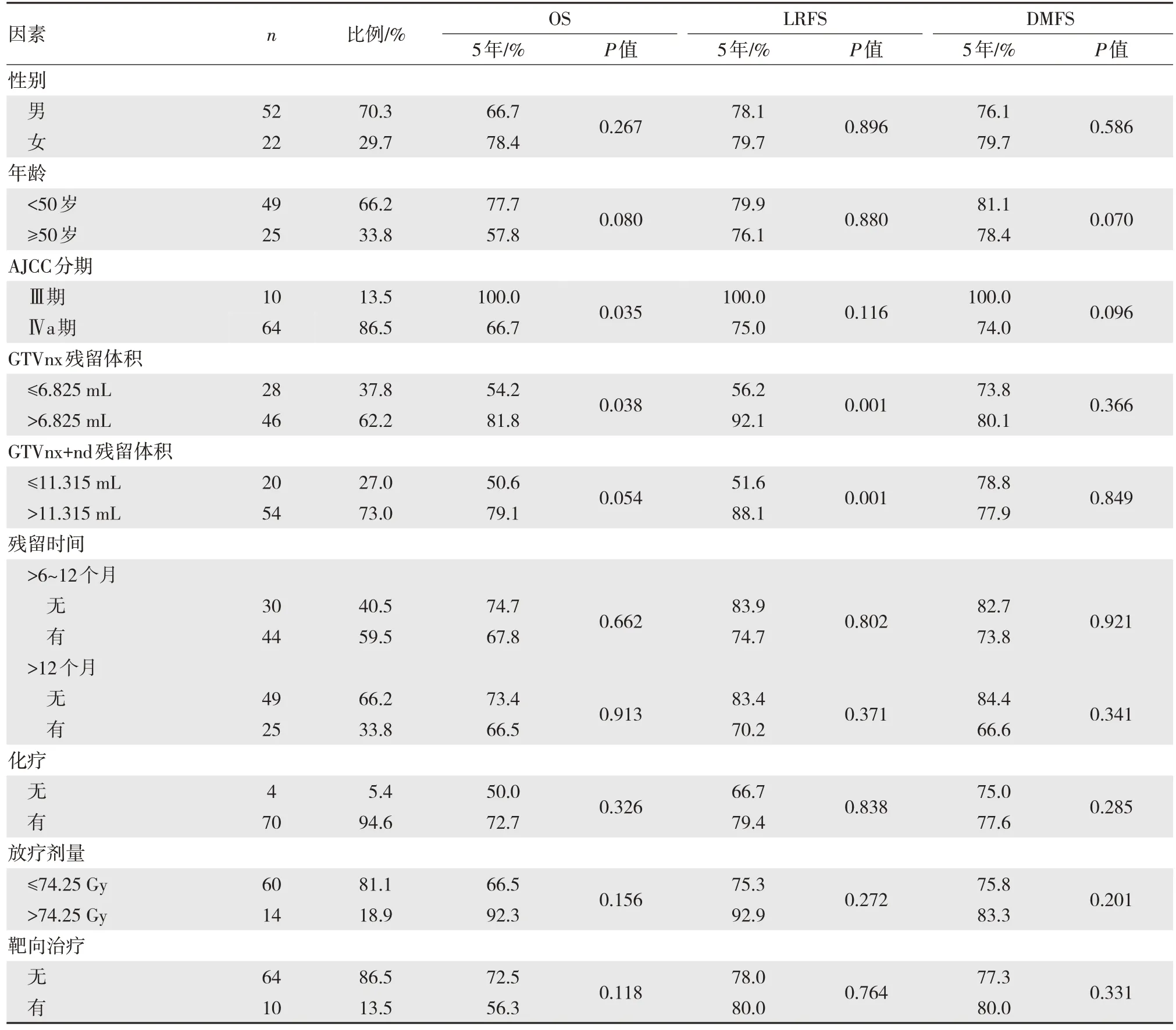
表1 不同因素生存状况的单因素分析

表2 鼻咽癌预后OS 影响因素的多因素一般Cox 回归分析的参数
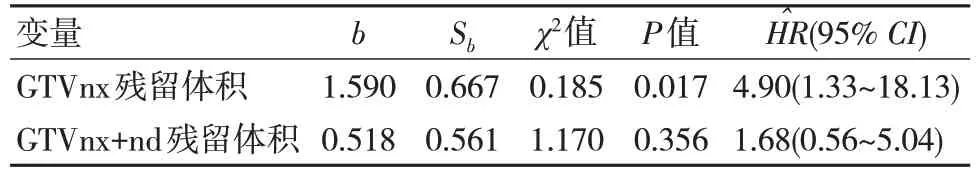
表3 鼻咽癌预后LRFS 影响因素的多因素一般Cox 回归分析的参数
3 讨论
目前,鼻咽癌的治疗仍采用以放射治疗为主的综合治疗方案,虽然近年来调强适形放疗技术水平不断提高,但鼻咽癌患者的局部治疗失败率仍有10%~30%[13]。由于鼻咽部解剖结构较为复杂,相邻危及器官限制了部分部位肿瘤放射治疗剂量,这就增加了肿瘤残留病灶的发生率。对于局部残留的患者,通常选择的补救治疗方式,包括手术、再次放疗、近距离治疗、立体定向光动力放疗和辅助化疗。虽然已有很多研究报道了鼻咽癌残留补救治疗的各种方式[13-14],但目前各学者间仍未达成鼻咽癌局部治疗失败最优补救治疗的共识。
局部治疗失败可以分为局部残留或者局部复发。目前将治疗后原发部位6 个月内仍有病变的病灶被称为残留病灶,而超过6 个月,原发部位再次出现病变且病理类型与首次确诊病理类型相同,则被称为复发病灶。据统计,目前鼻咽癌调强适形放疗后的残留率约为7%~13%[15]。本研究在234 例鼻咽癌患者中证实共有74 例患者存在肿瘤残留,残留率约为31.6%,该结果稍高于前期的其他研究,这是因为本研究所纳入的患者均为Ⅲ、Ⅳa 期,而临床分期越晚,发生残留的风险越高。本研究通过收集放疗后影像学证实有残留的鼻咽癌患者,对影响其肿瘤残留的各项因素进行分析发现,残留时间并不是影响患者各项生存指标的主要因素,分析其原因,笔者认为这可能是由于放射辐射效应具有原发作用和继发作用,辐射生物效应具有一定的时间滞后性,因此部分残留病灶在不经过任何治疗干预的情况下可以在一段时间后完全消退。但笔者的研究却发现鼻咽部残留的体积是影响局部无复发生存率的重要因素,对于单纯鼻咽部残留患者,残留体积≤6.825 mL 的患者无复发生存率明显高于>6.825 mL 的患者。这说明残留体积与肿瘤复发存在着直接关系。这与其他学者的研究结果相一致[3,11,16],LV 等[3]学者研究发现,鼻咽癌残留病灶的局部复发几乎全部发生在GTVnx 和/或GTVnd 范围内,均未超过CTV的范围,这与本研究结果一致,本研究亦发现所有残留病灶均发生在GTV 的范围内;该研究还发现残留患者的临床分期均为Ⅲ~Ⅳa 期,并指出Ⅲ期患者GTVnx 残留体积约为5.60~10.77 cm3,而Ⅳa期患者GTVnx 残留体积高达63.92 cm3,该研究说明对于局部晚期(T3~T4) 的患者,肿瘤T 分期越晚、肿瘤体积越大,其残留率越高,相关的复发风险也越高。这就意味着对于MRI 复查监测时发现影像学残留的患者,及时的补救治疗可以在一定程度上为其带来生存获益。有研究表明[17],鼻咽癌放疗后对局部残留病灶进行放疗补量是有一定获益的,研究分析了50 例局部晚期(原发灶均划分在T3~T4 期) 患者,在配合化疗的同时应用IMRT 提高处方剂量(>76 Gy),其2 年无远处转移率及2 年总生存率均高于未补量组。亦有研究发现[18],咽后淋巴结残留体积大于 13 cc(1 cc=1 cm3)的患者需要进行四周期以上的辅助化疗才能使其总生存获益[19-20]。这些研究均说明对于局部肿瘤残留的患者,放疗补量或辅助治疗可以有效提高患者的局控率及生存率。
目前关于鼻咽癌IMRT 治疗后残留的诊断通常采用影像学的诊断标准[17,21]或鼻咽镜检查[18],一方面是由于放疗后的鼻咽病灶肉眼形态往往变得不典型,这为病理活检带来了困难;另一方面,随着MRI 技术的进展,多项研究指出常规MRI 在鉴别鼻咽癌放疗后肿瘤残留和复发有着重要的参考价值[19-20,22]。英国多学科指南就推荐使用MRI监测鼻咽癌的放疗效果[23]。因此,本研究通过借鉴上述疗后评价方式,以影像学MRI 检查作为鼻咽癌患者治疗后监测局部肿瘤残留及复发的标准,对局部晚期鼻咽癌患者进行预后的疗效评价。近几年,随着分子影像技术的不断发展,18 氟-氟代脱氧葡萄糖-正电子发射计算机断层显像(18-fluorodeoxy glucose positron emission tomography,18FFDG PET) 结合MRI 检查逐渐成为关注的热点,与单纯MRI 相比,FDG 摄取增加可以为分子生物信息改变提供临床依据,有研究表明[24-25],PET/MRI 检查的敏感性较MRI 和PET/CT 均有增高,这三种检查方式的敏感性分别为99.5%、94.2% 和90.9%,并指出PET/MRI 在鉴别原发鼻咽部肿块和转移性咽后淋巴结方面具有较高的特异性,甚至可以及时、准确地发现颅内受侵的病灶,对于治疗后残留病灶也有一定的提示作用。尽管目前美国国立综合癌症网络(National Comprehensive Cancer Network, NCCN) 考虑将推荐 PET/MRI 作为现阶段鼻咽癌患者临床分期最理想的检查方式,甚至称其为 “one-stop” 检查,但由于该项检查成本高、检查时间长、对肺结节检测阳性率低等因素,在临床的使用及推广仍受到阻碍。由于本研究是一个回顾性研究,因此存在一定的局限性。单中心研究的治疗方案往往较为单一,势必会对研究结果造成一定程度的偏移,未来需要纳入更多的研究中心综合分析数据资料;其次是样本量小,由于本研究随访时间长,对部分鼻咽癌患者的信息采集工作带来困难,造成临床资料丢失。
综上所述,肿瘤分期、原发病灶的总处方剂量可以给临床判断有肿瘤残留的局部晚期鼻咽癌患者预后提供一定的参考价值,但也应考虑鼻咽癌放疗后局部残留体积及残留时间等因素,从而更加全面地评估该类患者的预后,并为其个体化治疗提供依据。

