基于潜在类别分析药物不良反应患者的用药特征研究
靳宝芬,高梦倩,蔡永铭
(1.深圳市宝安区福永人民医院,广东 深圳 518103; 2.广东药科大学公共卫生学院,广东 广州 510006; 3.广东药科大学医药信息工程学院,广东 广州 510006)
药物不良反应(adverse drug reactions,ADR)是指质量合格的药品在规定用法、用量下出现的有害的或与用药目的无关的反应[1]。ADR不仅给患者造成巨大的生理、心理伤害,同时也增加了患者的经济负担。随着药物在临床治疗中消耗需求的增长,不良反应率也随之增加[2]。2018年国家药品监督管理局发布的《国家药品不良反应监测年度报告》显示,65岁以上老年患者占总报告的27.7%,静脉注射给药占60%,抗感染药占34.8%[3]。在欧洲,大约5%的住院患者是由ADR引起的,并且欧盟每年有19.7万人死于ADR[4]。为深入了解ADR发生的原因,众多研究进行了ADR相关危险因素的分析,研究表明ADR通常与患者的年龄、性别、饮酒、共患病、联合用药、不适当用药、住院时间和情志等因素相关[5-7]。
目前,研究药物不良反应的方法主要有关联规则挖掘、网络分析、逻辑回归建模和聚类分析等[8]。潜在类别分析(Latent class analysis,LCA)兼具聚类分析与因子分析的功能,不仅可处理分类变量,且能够直接通过概率分布探索分类变量背后的潜在影响因素[9]。本文拟采用LCA识别药物不良反应人群的异质性,从而探索不同人群的用药特征,为临床合理用药提供参考依据。
1 资料与方法
1.1 资料来源
数据来源于深圳某二级甲等综合医疗机构(含21家社康中心)2015年至2018年上报国家不良反应监测系统的1 000例ADR报告。
1.2 收集整理
用SPSS18.0软件对ADR报表中患者的性别、年龄、民族、不良反应类型和结果、药品种类、给药途径等信息进行整理、查重,最终纳入分析594人。按照WHO国际药品监测合作中心关于药品不良反应累及器官/系统分类的相关规范进一步分类和汇总,通过世界卫生组织网站(http://www.whocc.no)上提供的药物ATC(anatomical therapeutic chemical,ATC)编码对ADR涉及药品进行分类统计[10],无ATC编码的药物参考《新编药物学》(第十七版)中的药理学分类方法对药品进行分类[11],共11类。
1.3 统计分析
运用SPSS18.0软件进行描述性分析、χ2检验,用Mplus7.4软件进行潜在类别分析,识别ADR人群的异质性,比较分析各亚类人群用药规律及特点。
Mplus7.4软件构建模型时,本文以新的ADR、严重ADR、出现皮肤及其附件损害、全身性损害、消化系统损害作为外显变量,考虑到性别间的差异性,故将性别作为协变量,建立潜在类别分析模型对ADR患者进行模式识别。为了选择最佳的LCA模型,将潜在类别数从1增加到4,对每个模型进行参数估计,结合模型评价指标,赤池信息量准则(Akaike information criterion,AIC) 、贝叶斯信息准则(Bayesian information criterion,BIC)、aBIC(ajusted Bayesian information criterion,aBIC)、似然比检验(Lo-Mendell-Rubin,LMRT)和熵值( entropy)选择最优模型。前3个指标的数值越小,表示模型拟合的越好,熵值越接近1模型分类越准确,LMRT检验P<0.05时,则表明K个类别的模型显著优于K-1个模型。
2 结果
2.1 基本情况
594名ADR患者中,男性221人,占37.21%;女性373人,占62.79%,发生ADR女性患者多于男性患者;15~44岁的青年患者最多,占74.75%,其次为45岁及以上的中老年人,占19.53%;汉族患者占97.31%;急诊科上报ADR的数量最高(占34.01%),其次是妇产科(占27.95%),再次是内科(占21.72%);按国家药品不良反应报告和监测管理办法规定,药品不良反应分为一般ADR、严重ADR、新的一般ADR和新的严重ADR。发生一般ADR占比最高(占44.11%),新的严重ADR占比最少(占7.24%);594名患者中出现的不良反应最终可被治愈的(占89.90%),好转(占8.76%),未见好转(占0.67%),情况不详者(占0.67%);最易发生不良反应的给药途径是静脉注射(占65.19%);不良反应累及皮肤及其附件损害(占36.20%),其次为消化系统损害和全身性损害(分别占29.63%和26.77%);根据国家药品不良反应监测中心评价分级方法,594名ADR患者中,因果关联性评价为“很可能”347人(占58.42%),“可能”240人(占40.40%),“肯定”7人(占1.18%)。见表1。
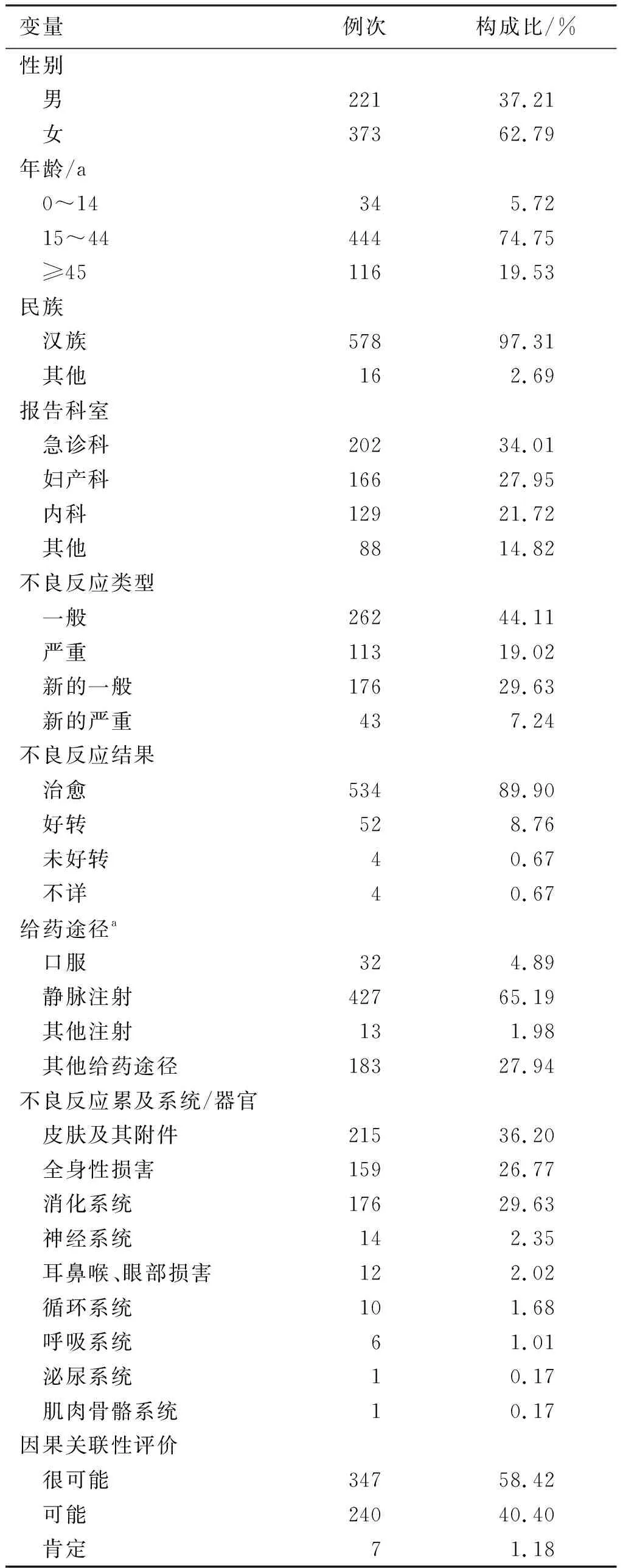
表1 发生ADR患者的基本特征Table 1 Characteristics of patients with ADR
2.2 引发ADR的药品种类
涉及ADR的药品共11类,抗感染类药物所致ADR最多,共294例次(占44.89%);其次是泌尿生殖系统及性激素类药,共157例次(占23.97%);再次是体激素类药,共45例次(占6.87%)。见表2。
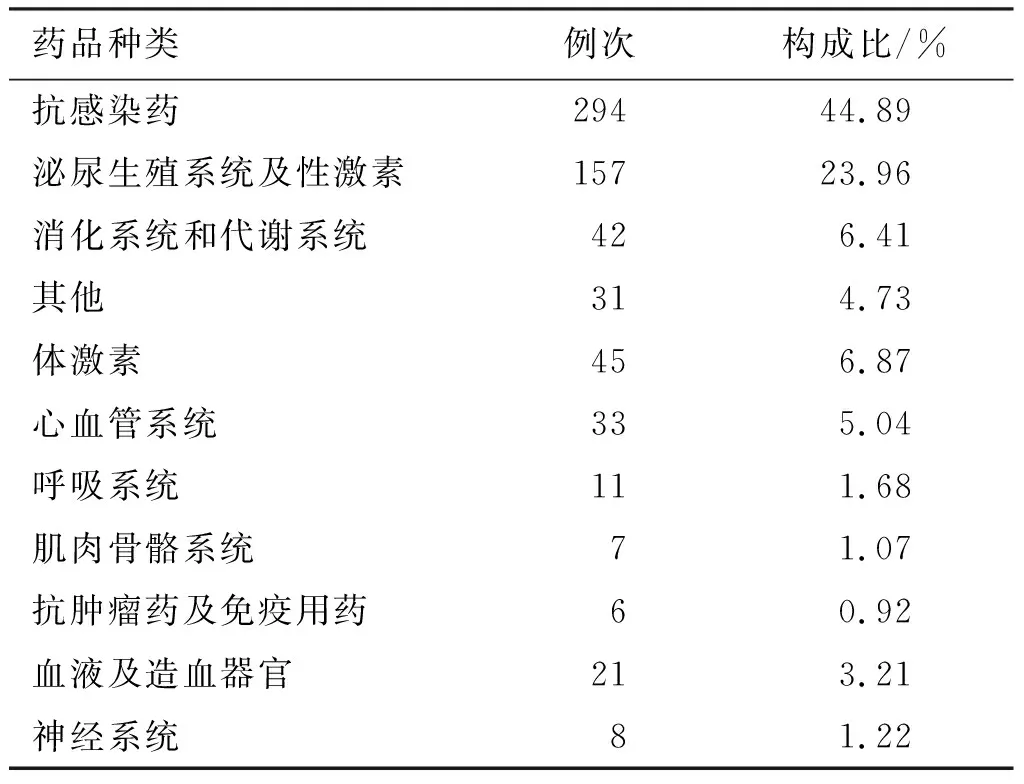
表2 引发ADR的药品种类分布及其构成比Table 2 Distribution and constituent ratio of drugs with ADR
2.3 LCA模型拟合
模型拟合时先将含有1个类别的模型作为基准模型,依次增加潜在类别数至4,从拟合信息可以看出,随着类别数的增加,AIC、BIC、aBIC值变小,结合专业知识,综合考虑熵值和模型的简洁性,最终提示含3个潜在类别的模型为最佳模型。见表3。
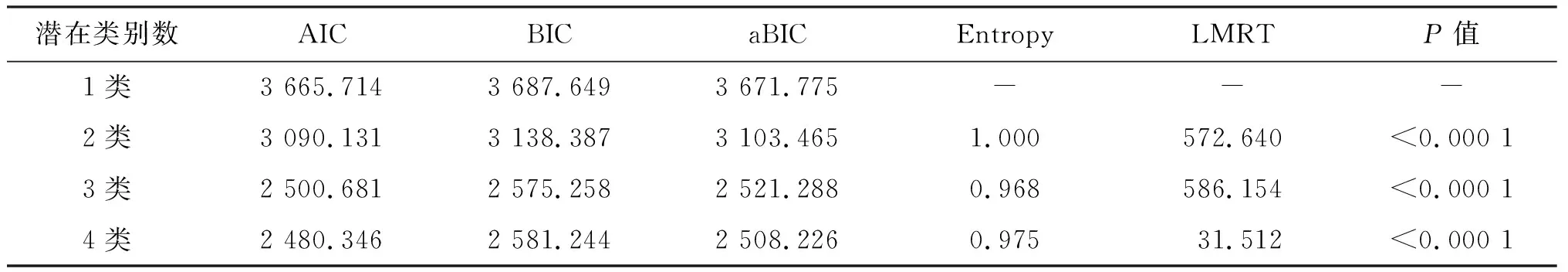
表3 LCA模型拟合统计量结果Table 3 LCA model fitting statistics results
2.4 3个潜在类别的条件概率分布图
由图1可以看出,第1类患者出现“皮肤及其附件损害”的概率为0.9,可将其定义为“皮肤损害的ADR患者”(231人,占38.89%);第2类患者出现“新的ADR”和“全身性损害”的概率均为0.8,其他特征概率较低,可将其定义为“全身损害的ADR患者”(187人,占31.48%);第3类患者出现“严重ADR”和“消化系统损害”的概率均大于0.5,其他特征概率较低,可将其定义为“消化道损害的ADR患者”(176人,占29.63%)。见图1。

图1 3个潜在类别的条件概率分布图Figure 1 1Conditional probability distribution of 3 latent classes
2.5 3类ADR患者的基本特征和用药情况
第1类患者中,上报ADR数量最多的科室是急诊科(占44.16%),其次是内科(占33.77%);主要呈现一般不良反应,不良反应主要累及皮肤及其附件(占93.07%);静脉注射为引发ADR的主要途径(占89.29%),引发ADR的药品种类主要是抗感染类药(占68.25%),其次是心血管系统类药(占9.52%)。
第2类患者中,急诊科上报ADR的数量最多(占50.80%),主要呈现新的一般不良反应,不良反应累及全身(占85.02%);静脉注射为引发ADR的主要途径(占81.61%),引发ADR的药品种类主要是抗感染类药(占50.67%),其次是体激素类药(占12.56%)。
第3类患者以女性为主(占94.32%),主要是严重不良反应,引发ADR的给药途径主要是其他方式,共155例次(占81.61%);不良反应仅对消化系统有损害并不累及其他系统,引发ADR的药品种类主要是泌尿生殖系统及性激素类药物(占83.33%)。见表4。
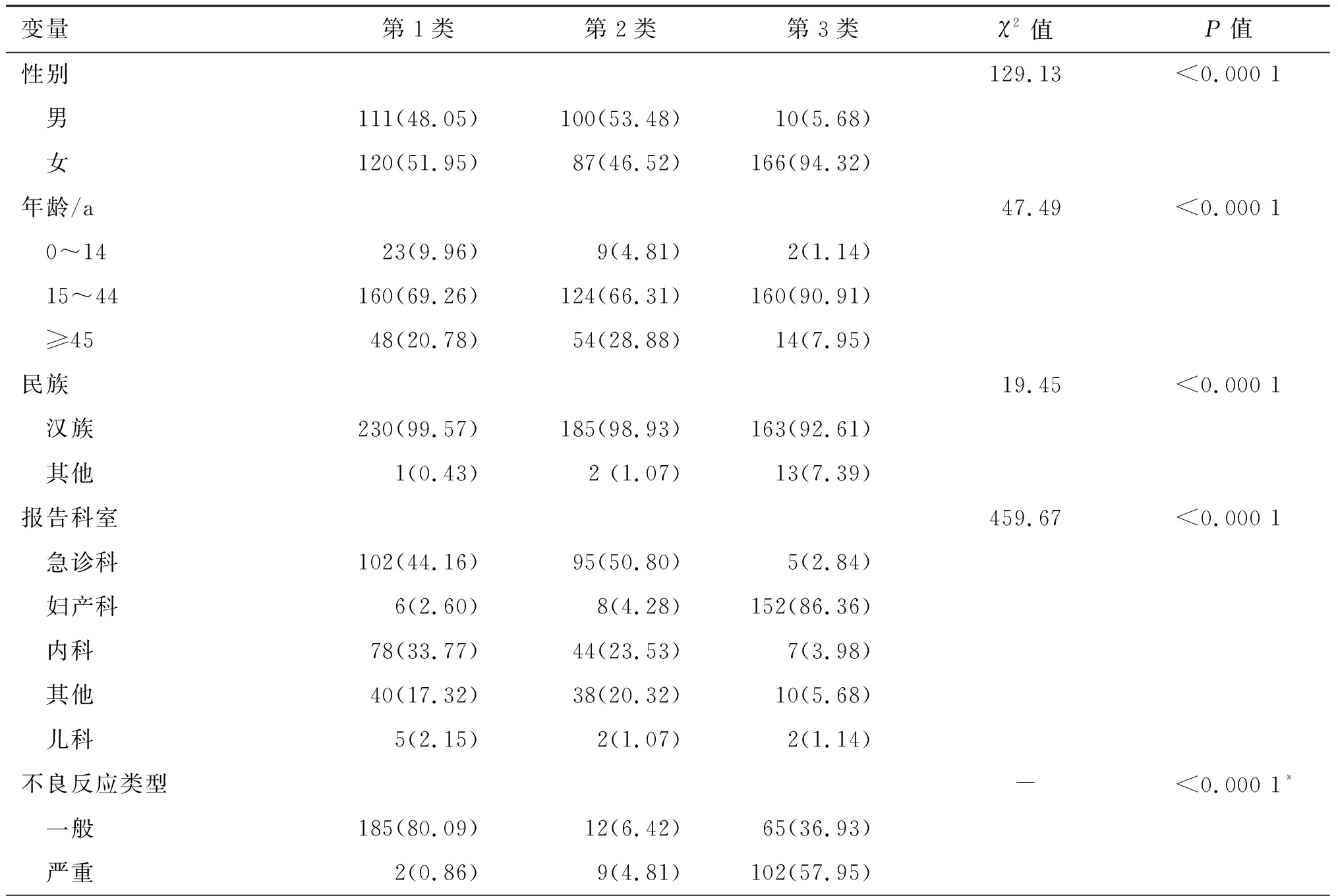
表4 3类患者的基本特征和用药情况Table 4 Characteristics and medications of patients with 3 latent classes [n (%)]
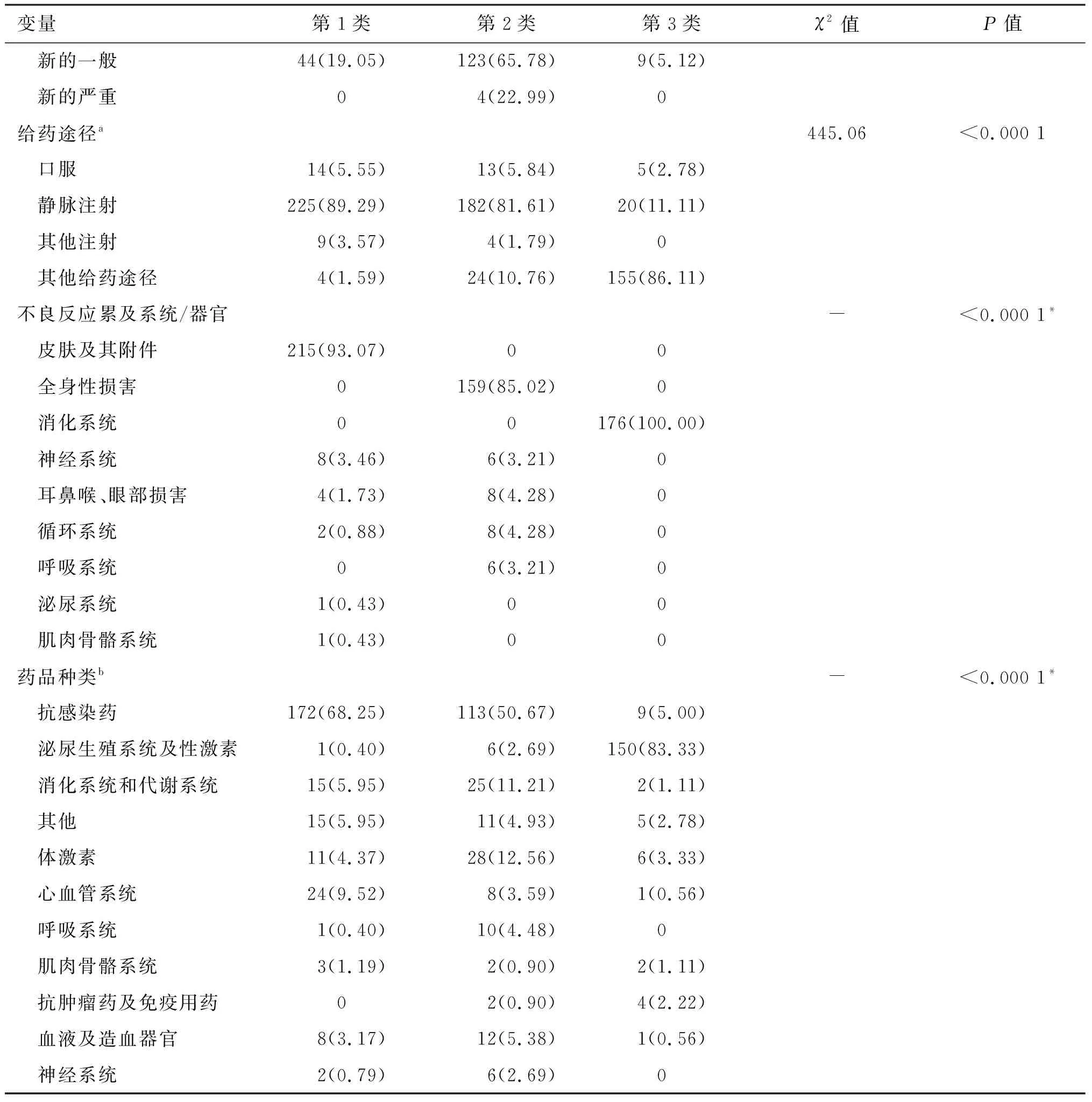
表4 (续)
3 讨论
药物不良反应已成为一个主要的公共卫生问题,不仅给患者带来众多不利影响,同时给社会造成沉重的经济负担[12]。本文采用LCA对深圳某二级甲等综合医疗机构收集的ADR数据进行了分析,识别出药物不良反应群体的异质性,对不同ADR人群的用药规律及特点进行了探索,有助于保障患者用药安全、加快临床药学发展。
本研究发现发生ADR的患者女性多于男性,与我国2018年ADR监测年度报告结果一致[3],考虑到女性在激素水平、基础代谢率、胃肠蠕动等生理和生活行为习惯方面与男性具有差异,使女性更易发生药物不良反应。另外,还发现静脉注射更易引发ADR,主要由于药物可直接经静脉进入血液循环,作用迅速,无肝脏首过效应[13]。在ADR症状体征表现上,绝大多数的不良反应主要累及皮肤及其附件,主要由于皮肤表现较为明显,容易观察,上报率高。本研究中只有0.67%的患者出现的不良反应症状未见好转,绝大多数不良反应经医师减药、停药或对症治疗后可被治愈,这与许多研究结果相一致[14]。ADR涉及的药品种类中抗感染类药位居首位,抗感染药包括抗生素、合成抗菌素、抗真菌药、抗病毒药[15],是临床应用最为广泛的药品类别之一,抗感染药使用不当容易产生耐药性,使得剂量增加,导致ADR发生率升高,因此抗感染药品的使用风险需要重点关注。
根据潜在类别分析的条件概率,本研究将ADR患者分为3类人群,第1类人群大多表现为一般的、不太严重的皮肤症状损害(故称之为“皮肤损害的ADR患者”);第2类人群大多表现为新出现的、较为严重的全身性损害(故称之为“全身损害的ADR患者”);第3类人群大多表现为一般的、严重的消化道损害(故称之为“消化道损害的ADR患者”)。通过数据匹配结合这3类人群的基本特征及用药情况,研究发现第1类患者主要使用了经静脉注射的抗感染类药和心血管系统类药,故不良反应症状多表现为常见的一般的皮肤损害;第2类患者主要使用了经静脉注射的抗感染类药和体激素类药,故不良反应症状多表现为新出现的、较为严重的全身性损害;第3类患者主要使用了经其他方式给药的泌尿生殖系统及性激素类药物,故不良反应症状多表现为一般的、严重的消化道损害。考虑到以上3类人群对ADR的不同特点,本文从公共卫生的角度给予以下建议:针对第1类人群,建议医生在临床用药过程中应尽量选择一些不良反应较少的药物;针对第2类人群,卫生相关部门应严格管理药品的上市,加强对新的不良反应的监测,及时处置不良反应风险预警信号;针对第3类人群,社区应积极开展生殖健康用药安全科普教育,制定个性化给药方案,降低ADR发生的风险,确保患者用药安全。
本研究以一个全新的视角对ADR进行了初步探索,数据来源真实可靠,覆盖了深圳市21家社康中心,医护人员均接受过规范的ADR相关培训,能在第一时间对ADR做出评价,做到了早发现、早应对、早调查、早处置,确保了公众用药安全。但是,本研究还存在以下局限:一、数据仅来源于深圳市某医疗机构,研究结果的外推性难以保证;二、本研究未涉及到ADR患者的受教育情况、个人生活饮食习惯及既往病史等具体情况,而往往这些因素又是ADR的重要影响因素。

