腹部无辅助切口治疗家族性腺瘤性息肉病改良手术方式的初步研究
司呈帅 李东正 杨柳 周欣 朱海涛 关心 仲坚 余东升 蒋谦 王东风
家族性腺瘤性息肉病(familial adenomatous polyposis,FAP)为常染色体显性遗传疾病。FAP表现为结直肠内成百上千的结直肠息肉,大多数息肉直径1 cm ~3 cm,多为无蒂半球形,病变极少累及小肠。如不治疗,几乎所有的患者都会发展成结直肠癌[1]。预防性手术切除病变结直肠为FAP的唯一根治方法。手术方式主要分为两种:全结肠切除术+回肠直肠吻合以及全大肠切除术+回肠肛管吻合[2]。
全结肠切除术需要对直肠残端癌定期复查及进行化学预防。本术式适用于青少年或者老年直肠息肉较少患者。对于手术后患者排便排尿及性功能影响较小。内镜下对于直肠息肉的处理相对困难,尤其是位于低位的直肠息肉。全大肠切除术切除全部结直肠,对患者排便排尿以及性功能影响较大,对青少年患者生活质量影响甚大。
由于FAP患者多较年轻,传统手术以及腹腔镜辅助手术会使患者残留较长的手术切口,影响美观并可能引起相关切口并发症。近几年,经自然腔道取标本手术(natural orifice specimen extraction surgery,NOSES)得到业界的广泛认同,并在腹腔手术中得到快速发展。NOSES手术安全,围手术期并发症及抗肿瘤效果类似传统开腹手术及传统腔镜手术。相比较传统开腹手术及传统腔镜手术,NOSES无胸腹壁辅助切口,美容效果极佳[3];切口相关性疼痛及并发症明显减轻,围手术期止痛药物用量明显减少[4]。经阴道和肛门是结直肠外科NOSES中最主要的两种方式[5-6]。经肛门取标本的方式中,可以分为三种:外翻切除、拉出切除式和切除拖出[5]。
本课题组在结合国内外专家术式的基础上,对NOSES治疗部分FAP患者进行了一定的创新改良。既能针对性处理结直肠几乎全部息肉病变,保留排尿排便和性功能,又能避免腹部手术切口。
资料与方法
一、纳入病例一般情况
纳入2019年6月至2020年3月在江苏省肿瘤医院结直肠中心诊断为FAP的4名患者的病例资料,患者均行改良NOSES术。患者一般情况及术后病理情况见表1。所有患者腺瘤均未发生癌变。入选标准:FAP患者,患者均有相应家族史。肠镜提示无癌变,直肠息肉相对较少;心肺功能耐受腔镜手术;直肠扩张功能正常;肛门收缩功能良好;肿瘤及肠腔直径小于8 cm。排除标准:肿瘤远处转移;直肠低位息肉较多或已癌变;肿瘤及肠腔直径大于8 cm。
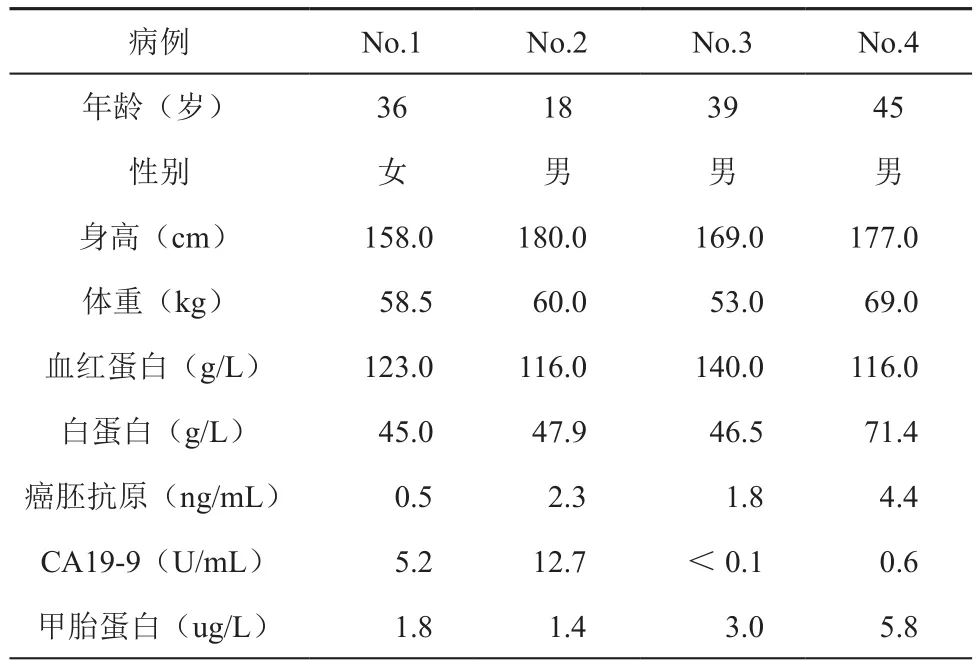
表1 4例FAP患者临床病理特征
二、手术操作步骤
(1)术前准备:术前一天口服聚乙二醇电解质散行肠道准备;(2)游离系膜:全麻成功后取功能截石位,Trocar放置位置(参照术后腹壁图片,图1)。探查腹腔无明显转移后行全结直肠系膜游离。肠系膜上静脉完全暴露后,行中央淋巴结清扫,相应血管结扎,分离;(3)经肛门拉出标本:裸化直肠至肛提肌平面后闭合器离断直肠。充分扩肛之后,大量碘伏水冲洗直肠残端。消毒后打开近端直肠管,置入保护套经直肠断端拉出全大肠(图2)。距离回盲部5 cm离断回肠,在体外于回肠末端置入25 mm DST吻合器钉砧;(4)外翻直肠处理远端直肠息肉:经肛门外翻下段直肠,于体外直视下切除直肠下段及肛管段腺瘤(图3)后,距离肛管上缘1 cm离断闭合肠管。后内翻远端直肠行回肠直肠端端吻合;(5)漏气试验确认吻合质量,随后冲洗腹腔,置入引流管及肛管,关闭Trocar孔。
三、肛门功能及生活质量随访
回顾性统计患者年龄、身高、体重、清扫淋巴结数量,电话随访患者半年内每天排便次数,夜间排便次数(入睡后排便次数),辅助药物治疗排便情况,有无大便失禁等。
结 果
一、术后短期并发症
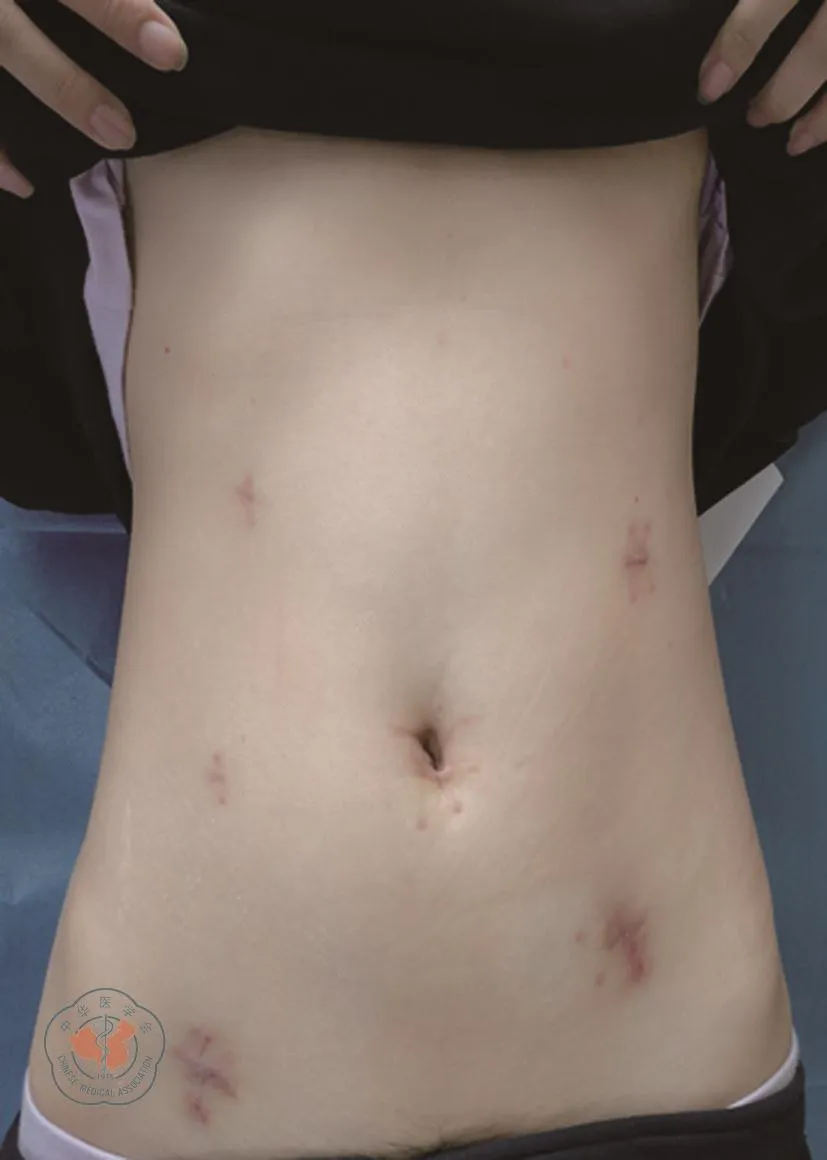
图1 患者术后1个月腹壁恢复情况。可见患者腹壁陈旧性手术瘢痕6处;脐周瘢痕处为观察孔;右上、右下、左下瘢痕处置入12 mm戳卡,左上、左中瘢痕处置入5 mm戳卡;右上左上瘢痕处放置引流管
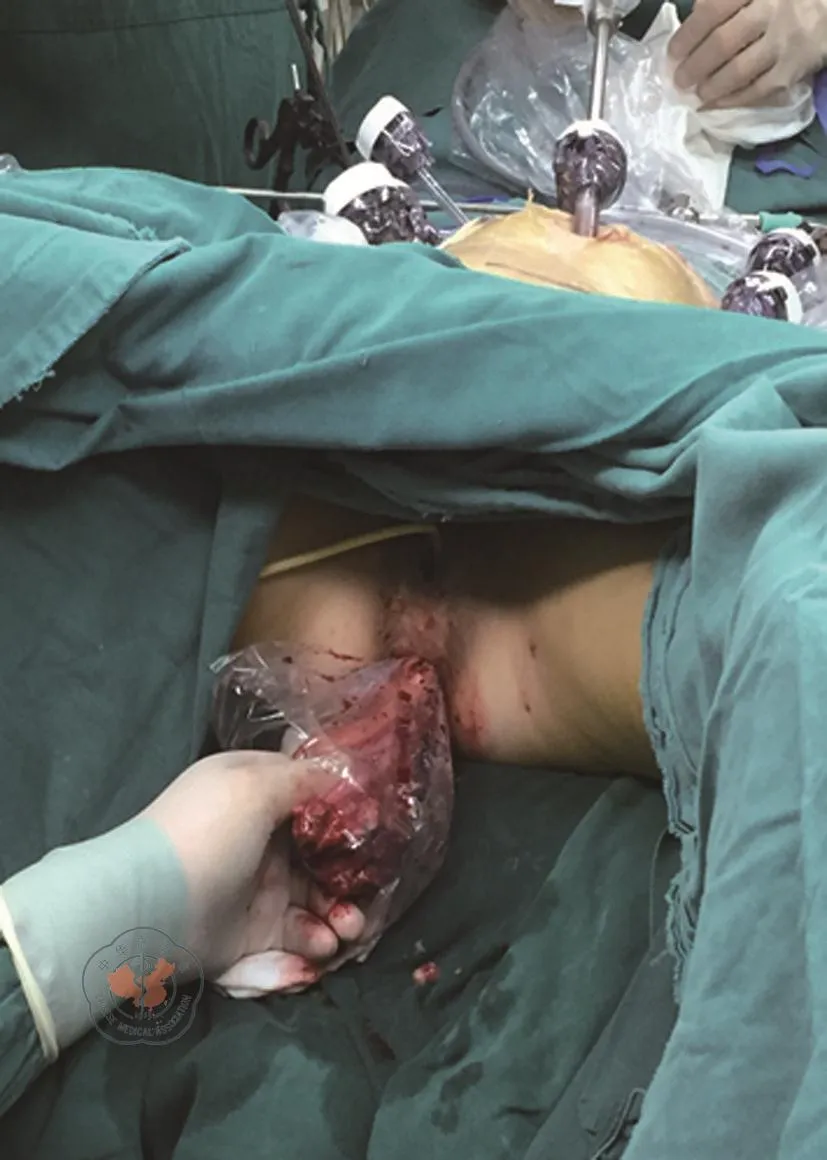
图2 经保护套拖出已游离的结直肠
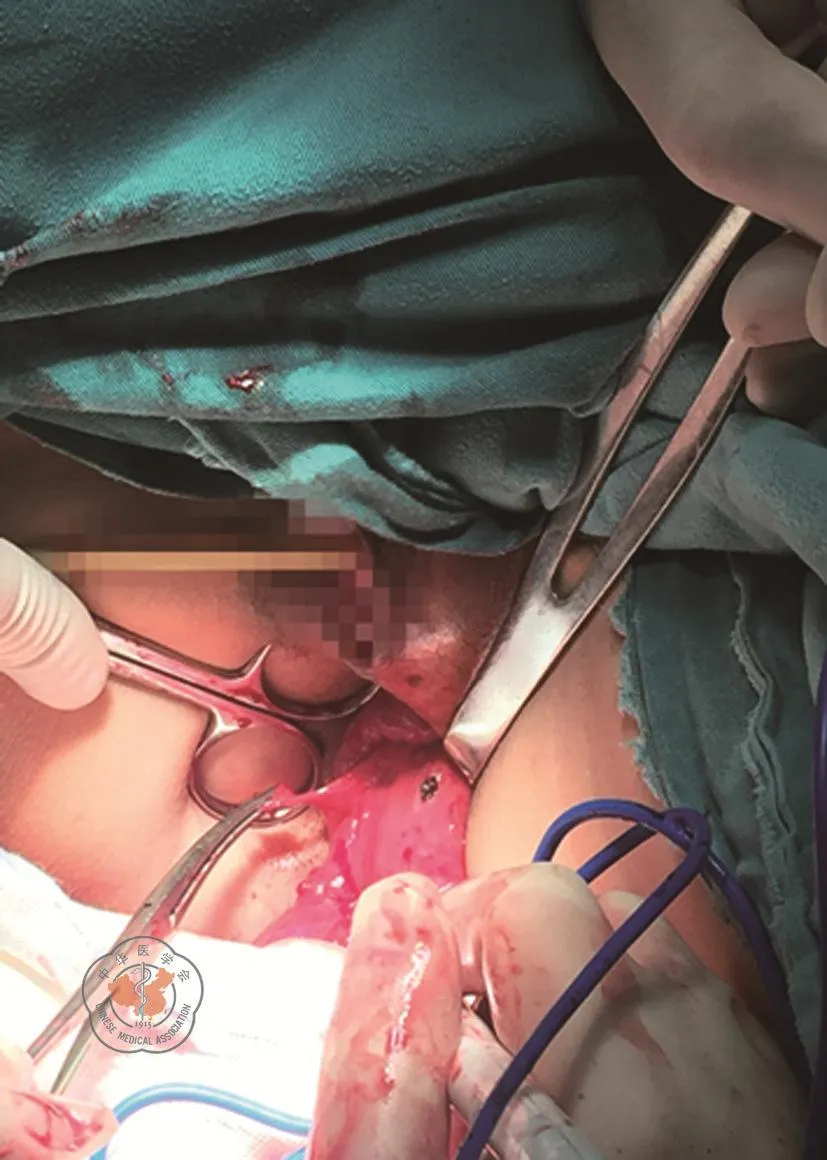
图3 外翻直肠残端,逐步切除直肠残端息肉
所有患者均顺利完成NOSES术,无中转开腹。所有患者术后均无辅助手术切口,且无明显切口瘢痕形成(图1)。随访期内无切口疝发生。患者术后所需的止痛药物相对较少。术后无吻合口漏及其他重大并发症(临床症状阴性,未常规行术后CT检查)。吻合口距肛门的距离分别为8 cm、10 cm、6 cm、8 cm。术后四位患者检查淋巴结数目分别为8、10、14、6枚。
二、排便功能
患者术后排便情况见表2。所有患者均无排便失禁现象。由于纳入病例数目较少,未行统计分析,但可见吻合口距离肛门的距离与排便频率尤其是夜间排便频率有负相关趋向。
讨 论
FAP大多由APC基因的胚系突变引起,该基因位于5q21[7]。APC为抑癌基因,通过与β-actin的结合影响细胞的功能。APC的突变可引起黏膜细胞的增生瘤变,进一步诱发癌变。大多数患者在15岁左右出现结直肠腺瘤,40岁左右出现腺瘤癌变。除结直肠表现外,FAP还有肠外表现:先天性视网膜色素上皮增生、肝脏胚胎细胞瘤、骨瘤、皮肤软组织肿瘤、硬纤维瘤病。同时不同基因型的突变和患者的临床症状与息肉病变程度密切相关。
预防性手术切除为治疗FAP的唯一根治方式。遗传性FAP患者常需要14岁左右开始进行肠镜随访检查。当息肉病变内镜无法控制或者怀疑癌变后,需要进行外科手术干预,行全结直肠切除或者全结肠切除术[8]。随着外科技术的不断进步,手术方式从传统开腹手术,腹腔镜下辅助手术,到NOSES。手术方式都遵守无瘤无菌的原则。手术方式的变革对于腹壁的损伤逐步减轻,降低了术后疼痛及术后切口并发症[8-10]。
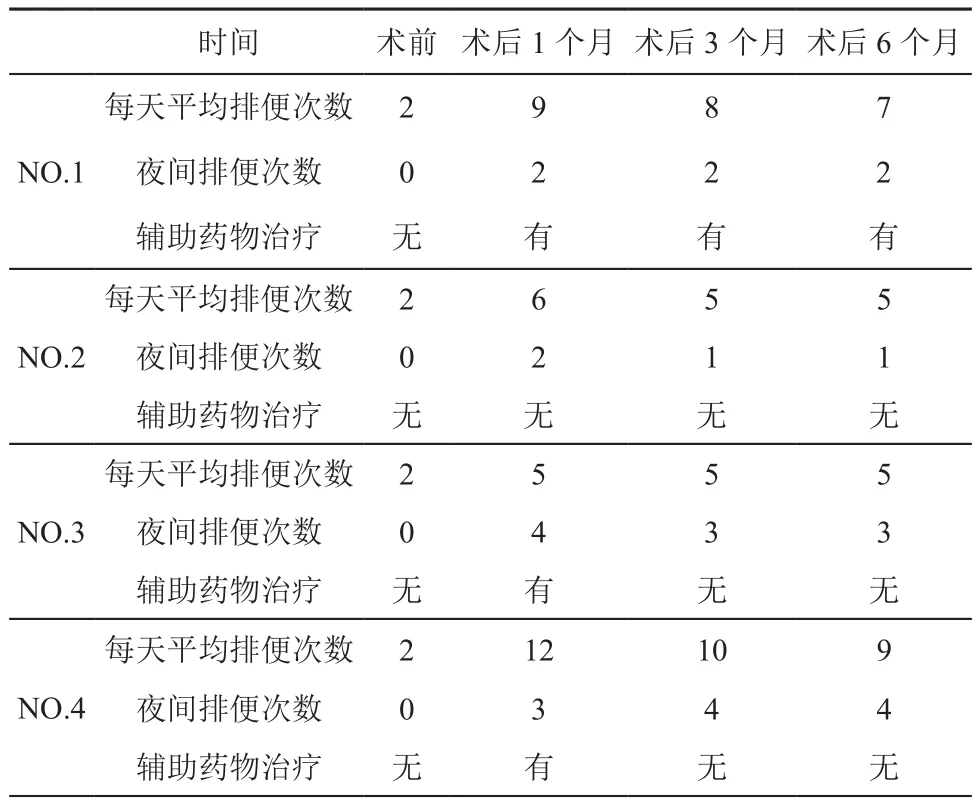
表2 术后排便情况随访
FAP患者多较为年轻,本组病例中患者年龄均低于50岁。对于生活质量要求较高。保留适当的直肠对于术后患者的排尿排便及性功能至关重要。FAP患者中低位直肠息肉内镜下切除较为困难。硬质直肠镜操作又受到操作距离的限制。本改良术式最大的优点是使直肠外翻,在直视下处理直肠息肉。该术式保留了一定长度的直肠,并且避免了直肠周围神经的过度损伤,降低了性功能损伤及排尿功能损伤的可能。但术后仍需口服NSAIDs药物进行化学预防。与此同时,该术式无传统开放手术及腹腔镜辅助手术的切口,从而避免了相关的切口痛、切口感染、切口疝的发生[6]。
结直肠术后排便情况是患者生活质量的重要组成部分。随着保肛率的不断提高,很多直肠尤其是低位直肠癌术后的患者术后腹泻症状严重。有研究表明吻合口距离肛缘的距离、肿瘤的直径是术后排便功能的独立危险因素[11-12]。在我们的研究中,病例纳入数目较少,未能进行统计学分析。但是依然能看出这一趋势。
本研究也有很多局限:随访时间较短,无生存及复发情况统计,纳入病例较少,且为回顾性研究。尚需进一步临床研究证实该手术方式的效果。

