术前胆道引流方式对合并梗阻性黄疸病人胰十二指肠切除术的影响
赵诗葳, 沈子贇, 王建承, 彭承宏, 张 俊, 吴卫泽
(上海交通大学医学院附属瑞金医院外科,胰腺疾病诊疗中心;上海交通大学医学院胰腺疾病研究所,上海 200025)
恶性梗阻性黄疸病人严重情况下会出现凝血功能障碍、肝肾功能不全、内毒素血症等。术后总体并发症发生率及围术期死亡率显著升高[1]。常见的术后并发症包括出血及胰瘘[2]。早期多项回顾性研究表明,术前胆道引流可减少病人行胰十二指肠切除术的术后出血、腹腔感染、术后住院时间等,但不能降低术后死亡的风险[3-5]。然而,目前学界对恶性梗阻性黄疸是否需常规行术前减黄仍有争议。
2019年美国国立综合癌症网络(National Comprehensive Cancer Network,NCCN)发布的《胰腺癌诊治指南》不推荐常规术前胆道引流,但对伴瘙痒症状的重度黄疸或胆道感染者建议行术前胆道引流。引流方式首选内镜逆行胰胆管造影术(endoscopic retrograde cholangiopancreatography,ERCP)胆道支架置入;若ERCP不可行,则可选择经皮肝穿刺胆道引流术(percutaneous transhepatic cholangial drainage,PTCD)[6]。
本研究回顾外科低位恶性梗阻性黄疸行术前胆道引流的病例,比较不同减黄方式的安全性以及对病人行胰十二指肠切除术的影响。
资料与方法
一、临床分组
纳入本中心2012年1月至2019年12月共448例行术前胆道引流的病例,引流后均行胰十二指肠切除术。其中男304例,女144例,平均年龄(63.8±10.4)(25~87)岁。 根据术前最终采取的胆道引流方式分为PTCD组(238例)和ERCP组(210例)(见表1)。ERCP组中,内镜胆道支架置入术(endosopic biliary stenting,EBS)组 101 例,置入的支架均为塑料支架;内镜鼻胆管引流术(endoscopicnasobiliarydrainage,ENBD)组109例 (见表1)。 比较ERCP组与PTCD组的操作失败率及发生的相关围术期并发症。为进一步判断EBS与PTCD产生的影响,比较两组的临床数据。
二、手术方式
所有病人均行胰十二指肠切除术,其中开腹手术376例(ERCP组 191例,PTCD组 185例),机器人手术72例 (ERCP组19例,PTCD组53例)(见表1)。所有病人术中均常规使用预防性抗生素。
三、术后病理检查结果
术后病理检查结果表明,胰腺导管腺癌314例,胰腺神经内分泌肿瘤1例,胆总管恶性肿瘤37例,壶腹部腺癌58例,十二指肠乳头恶性肿瘤38例(见表 1)。

表1 恶性梗阻性黄疸病人的临床特征
四、统计学分析
所有数据用SPSS 22.0软件进行分析。分类变量的比较使用卡方检验或Fisher精确检验。计量资料若为正态分布,则采用t检验,用均值±标准差表示。若为非正态分布,则采用Mann-Whitney检验,用中位和四分位间距(interquartile range,IQR)表示。P<0.05为差异具有统计学意义。
结 果
448例病人中原有220例行ERCP,228例行PTCD。减黄前总胆红素水平中位值为250.1 μmol/L(IQR:188.5~335.2 μmol/L), 术前总胆红素水平中位值为 115.7 μmol/L(IQR:76.7~173.5 μmol/L)。 术前引流中位时间为 8.0 d(IQR:6.0~14.0 d)。 26 例(26/448,5.8%)因操作失败或胆道引流不通畅需再次减黄,其中首次操作为ERCP者18例(18/220,8.2%),首次操作为 PTCD 者 8例(8/228,3.5%),两组差异有统计学意义(P=0.034)。再次减黄的病例中,有11例由ERCP改行PTCD,7例再次尝试ERCP;1例PTCD改行ERCP,7例再次尝试PTCD。共有45例发生减黄操作相关并发症(45/448,10.0%),其中24例为ERCP发生 (24/220,10.9%),21例为PTCD发生(21/228,9.2%),两组差异无统计学意义(P>0.05)。并发症发生包括引流不通畅、引流管脱出、继发胆道感染、败血症、胰腺炎和腹腔出血等(见图1和表2)。
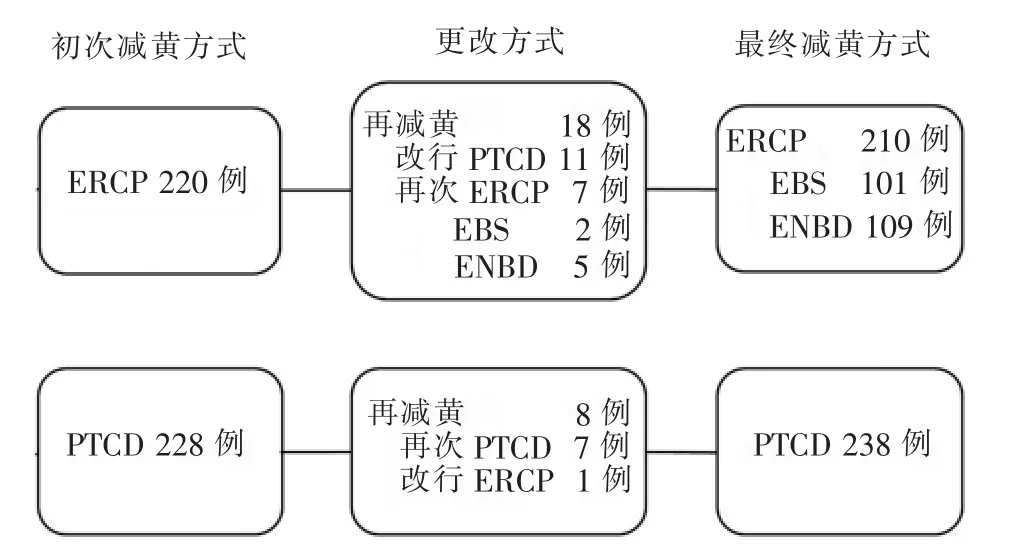
图1 病人首次减黄方式的选择及需再次减黄的情况
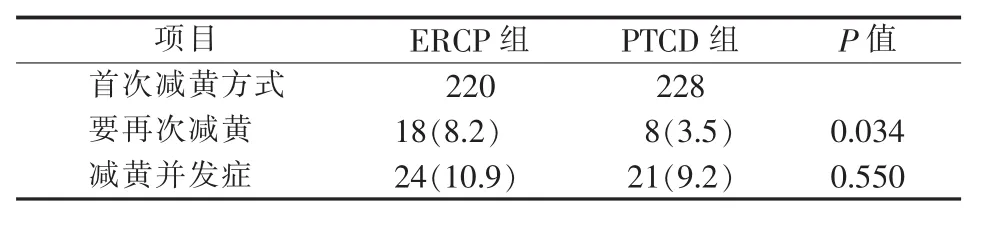
表2 不同减黄方式的失败率及并发症发生率[n(%)]
ERCP组与PTCD组之间的年龄、性别、BMI、基础疾病(包括糖尿病、高血压、心脏病、慢性胰腺炎)等差异均无统计学意义(P>0.05)。两组减黄前的平均血清总胆红素、丙氨酸转氨酶、天冬氨酸转氨酶、总白蛋白、血红蛋白、血小板等差异均无统计学意义(P>0.05)。两组肿瘤直径差异无统计学意义(P>0.05)。两组围术期死亡率和术后总体并发症发生率差异无统计学意义(P>0.05)。ERCP组共16例因术后并发症再次手术,其中腹腔出血11例,胰肠吻合口瘘、胆肠吻合口瘘、胃肠吻合口瘘、腹腔感染和切口裂开各1例。PTCD组共7例再次手术,均为腹腔出血。ERCP组与PTCD组的再次手术发生率的差异具有统计学意义 (7.6%比2.9%,P=0.025)。ERCP组的胰瘘发生率显著高于PTCD组(24.3%比13.9%,P=0.005)。两组其余术后并发症发生包括胆瘘、胃肠吻合口瘘、腹腔感染、腹腔出血、切口感染、胃排空延迟和脏器功能不全等差异均无统计学意义(P>0.05)。两组术后总体并发症差异无统计学意义(P>0.05)。两组中位术后住院时间差异无统计学意义(P>0.05)(见表3)。
进一步亚组分析发现,EBS组与PTCD组年龄、性别、BMI和基础疾病等差异均无统计学意义(P>0.05)。两组减黄前的平均血清总胆红素、丙氨酸转氨酶、天冬氨酸转氨酶、总白蛋白、血红蛋白和血小板差异均无统计学意义(P>0.05)。两组肿瘤直径差异无统计学意义(P>0.05)。两组围术期死亡率差异无统计学意义(P>0.05)。EBS组共8例因术后并发症再次手术,其中腹腔出血6例,胰肠吻合口瘘和切口裂开各1例。EBS组再次手术发生率与PTCD组差异有统计学意义(7.9%比2.9%,P=0.041)。EBS组的胰瘘发生率显著高于PTCD组 (32.7%比13.9%,P<0.001)。两组其余术后并发症发生包括胆瘘、胃肠吻合口瘘、腹腔感染、腹腔出血、切口感染、胃排空延迟和脏器功能不全等差异均无统计学意义(P>0.05)。两组术后总体并发症发生率差异有统计学意义(60.4%比45.8%,P=0.014)。两组中位术后住院时间差异无统计学意义(P>0.05)(见表4)。

表3 ERCP组与PTCD组术后并发症发生比较[n(%)]
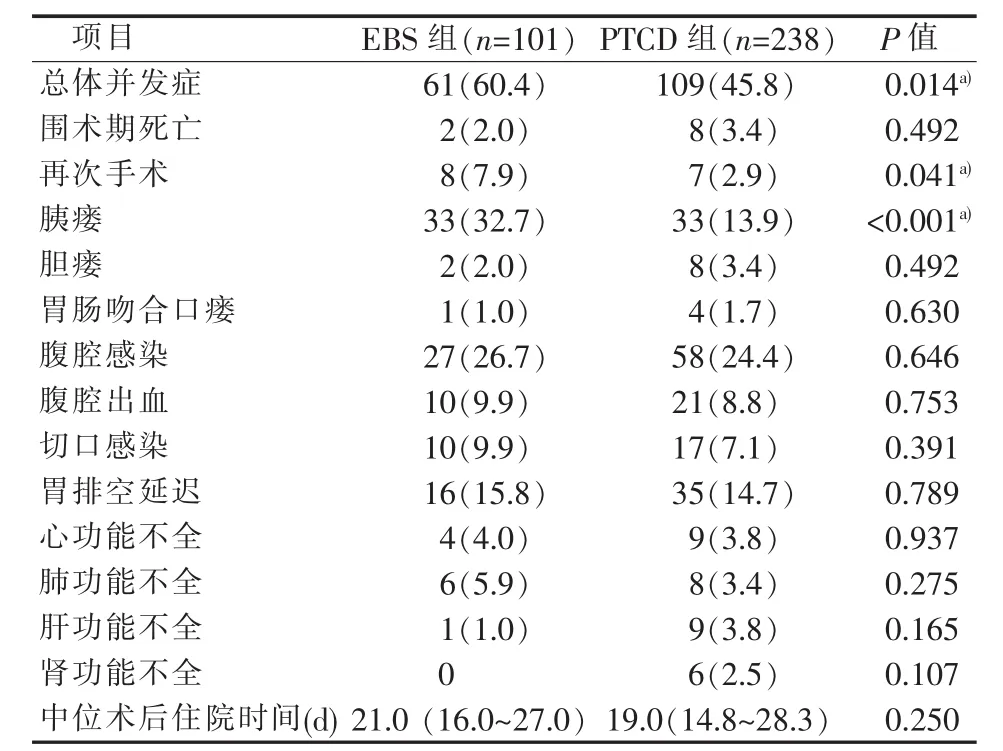
表4 EBS组与PTCD组术后并发症发生比较[n(%)]
讨 论
目前,学界对于低位恶性梗阻性黄疸病人是否需常规行胆道引流以及具体引流方式的选择尚存争议。一项荟萃分析提出,在临床操作中,应根据病人的实际情况、梗阻的位置以及治疗中心的经验来选择胆道引流方式[7]。另一项荟萃分析提出,对于可切除的胰头癌病人,PTCD与EBS两种胆道引流方式对术后并发症发生率无影响[8]。早期多个回顾性研究提示术前胆道引流可减少合并梗阻性黄疸胰十二指肠切除术的术后出血、腹腔感染和术后住院时间等。2010年一项多中心随机对照研究显示,对血清总胆红素水平在40~250 μmol/L的胰头癌病人常规行术前减黄增加术后并发症发生[9]。本中心既往的研究已证实,对于重度黄疸(血清总胆红素>250 μmol/L)的病人,应常规行术前胆道引流[10]。本研究旨在比较不同术前胆道引流方式的安全性以及对病人行胰十二指肠切除术的影响。研究结果推荐PTCD。
首先,PTCD的操作成功率高于ERCP,这点与国际上的观点相似。2014年,一项荟萃分析指出,在治疗恶性梗阻性黄疸时,PTCD的操作成功率高于ERCP,而两者的术后并发症发生率和围术期病死率相仿[11]。分析其原因,这可能与ERCP操作的难度较高相关。ERCP操作成功的要素包括内镜顺利进入十二指肠降段、十二指肠降段的空间足以完成操作以及胆管插管。然而,当胰头癌合并梗阻性黄疸时,易出现十二指肠受压迫或受侵的情况。此时,十二指肠内操作空间小,十二指肠乳头受侵变形,操作难度大大提升。若十二指肠已存在不完全梗阻,即使支架放置成功,仍易出现消化液反流入胆管的情况,易引起胆道感染。国内、外学者均有ERCP失败的经验总结,指出应注意切开后乳头局部的变化、所选附件是否到位以及解剖病理异常等问题。尤其是胆胰管合流异常易导致导管到汇合口,导丝也很难进入胆管。不同的解剖异常应采取不同的应对措施。反复失败的情况下应及时停止操作,行预切开后再寻找适当时机(建议至少4 d后)行ERCP等[12-13]。总之,当肿瘤直径较大、胆管扩张较明显时,ERCP相对易失败,而PTCD相对易成功。以往PTCD均由放射介入科医师在透视下按体表和透视的肝投影进行穿刺,穿刺到位后通过注射造影剂显影管道的走行,以判断显影管道的性质,所以发生胆汁入血引起感染的可能性较高。然而,随着CT检查技术的发展,本中心目前越来越多地使用CT引导下PTCD,穿刺前行CT扫描检查,选定粗细及位置合适的胆管,穿刺过程中反复扫描,引导穿刺针逐步靠近胆管,避开血管穿刺胆道。该方法更准确,操作损伤小。只要病例选择合适 (胆管足够粗),失败率会明显下降。综上所述,对于同等情况的病人,PTCD的成功率相对固定,而顺利完成ERCP取决于多方面的因素,遇到困难时操作者凭经验选用各种插管方式尝试胆管插管,有较多不确定性。
其次,ERCP组总体比PTCD组有更高的再次手术发生率,ERCP组的胰瘘发生率显著高于PTCD组。即使按目前NCCN推荐的EBS方法进行比较,EBS组的术后总体并发症、胰瘘以及再次手术发生率仍均高于PTCD组,与EBS操作需留置胆道支架易引起术区炎症增加相关。一项纳入13项回顾性研究的荟萃分析指出,PTCD在总体术后并发症上优于EBS[14]。2015年,Tsutomu团队一项纳入122例病人的回顾性研究显示,术前行EBS的72例病人术中胆汁培养均为阳性,且该组胰瘘的发生率约36%,与本中心的32.7%相近[15]。
本研究为回顾性研究,存在一定局限性。一直以来,“减黄指征”和“减黄终点”是关注焦点。
一方面,以往普遍认为恶性梗阻性黄疸需常规减黄。但2010年,van der Gaaug等[9]不建议血清总胆红素在40~250 μmol/L之间的胰头癌病人常规术前减黄后,目前我国及欧美国家指南均不建议行常规术前减黄。但临床上部分医师仍倾向于对黄疸较重的病人行术前减黄。本中心既往的研究认为,对于重度黄疸病人,应常规行术前胆道引流[10]。本研究减黄前总胆红素中位值为250.1 μmol/L。
另一方面,术前胆道引流后外科手术的最佳时机也未统一,目前尚缺乏被广泛认可的高级别循证医学证据。本研究病人术前引流中位时间8.0 d,术前总胆红素的中位值为115.7 μmol/L。一项韩国的多中心RCT研究以2周为界,发现胆道引流2周以上的病人,术前胆道引流并发症发生率显著高于少于3周的病人[16]。然而,欧洲一项多中心RCT研究指出,减黄时间不足4周的病人术后严重并发症发生率更高[17]。NCCN指南并未对减黄时间及终点作出明确推荐。有学者认为,不应把血清胆红素的下降作为评价引流效果的唯一指标。若胆道引流过程中,血清胆红素下降较慢,可用白蛋白和酶等其他指标评判肝功能的改善程度,以尽早积极手术[18]。如何平衡减黄时间与疾病进展,将血清总胆红素降至完全正常是否使术后并发症发生及总体预后获益,不同减黄方式是否存在效率的差异以及如何量化该差异,有待进一步研究。不恰当的减黄决定及减黄终点的确认客观上对有关减黄研究结果的意义产生很大的影响。随着减黄指征及减黄终点的更新与统一,将有必要再次就术前胆道引流对手术相关并发症发生及预后的影响进行更深入的研究。
最后,不同胆道引流方式对病人预后的影响也存在差异。2018年,韩国Ahn等[19]纳入80例壶腹癌病人的回顾性研究显示,术前EBS组引流的预后较PTCD组差,且前者术后1年的远处转移率显著高于后者。另有学者提出,对于胆管下段恶性肿瘤,PTCD组的5年生存率显著低于ERCP组,因其增加肝内转移的发生率[20]。可能不同胆道引流方式对不同类型肿瘤的影响不同。这既可能是不同胆道引流方式导致的差异,也可能与肿瘤学特性以及肿瘤所致梗阻特点的差异相关,值得进一步研究。
综上所述,根据本回顾性研究的结果,对于低位恶性梗阻性黄疸病人,在胰十二指肠切除术前使用PTCD方式进行胆道引流,比ERCP方式具有更大的优势。

