单中心奥沙利铂超敏反应的处理及转归真实世界研究*
王闫飞 付巧英 陈晓艳 夏丽娜 刘钟芬 姜丹凤 郑艳群 张红 刘巍
根据2015年中国癌症统计数据,胃癌、结直肠癌发病率分别居中国常见恶性肿瘤第4、5位,而在恶性肿瘤导致的死亡中,胃癌、结直肠癌分别居第3 位和第5 位[1]。奥沙利铂是胃肠道恶性肿瘤晚期一线化疗的基础用药,更是结直肠癌辅助化疗中与氟尿嘧啶类联用的唯一可选的药物。超敏反应(hypersensitivity)是奥沙利铂常见的不良反应,严重者导致过敏性休克,甚至危及生命[2]。研究报道奥沙利铂超敏反应发生率为8.9%~23.5%[3-7],其中约1%可能危及生命[2,8]。奥沙利铂导致的超敏反应常导致化疗中断或方案更换,一般情况下停药后不再次使用,使患者治疗选择严重受限,进而影响患者的预后及生存。
国内外文献常使用“超敏反应”定义奥沙利铂输注过程中出现的输液反应及严重过敏反应,但是其机制并非全部和过敏相关[9]。根据其机制是否和过敏相关,由肥大细胞或嗜碱性粒细胞脱颗粒释放组胺或组胺样物质所引起,可进一步分型为严重过敏反应(anaphylaxis)和标准输液反应(standard infusion reaction)。严重过敏反应临床症状范围涵盖从轻微的荨麻疹、呼吸困难到危及生命的呼吸系统异常、循环衰竭,存在迅速进展、危及生命的危险;过敏性休克仅是严重过敏反应的一部分。
本研究回顾性收集本病区62例奥沙利铂相关超敏反应患者的临床资料,就患者的临床特征、亚型分类、处理和转归情况进行了分析和梳理,旨在为超敏反应的管理提供依据。
1 材料与方法
1.1 临床资料
选取2015年1月至2017年12月北京大学肿瘤医院上报国家药品不良反应(adverse drug reaction,ADR)监测中心的62例奥沙利铂超敏反应的患者,来自7 个临床科室。全部患者经本院病理确诊为恶性肿瘤。综合ADR 记录和住院/门诊病历提取患者信息,包括患者一般资料如性别、年龄、过敏史、体表面积;疾病相关信息包括原发肿瘤部位、肿瘤分期;抗肿瘤治疗情况包括奥沙利铂方案化疗周期数、既往铂类药物治疗史,有无奥沙利铂间歇期、奥沙利铂累积剂量。预处理药物情况;患者超敏反应相关信息包括临床症状及体征、严重程度、治疗情况、转归及后续再用药情况。
1.2 方法
1.2.1 标准输液反应和严重过敏反应的诊断标准 超敏反应定义为不能用已有其他不良反应的药物输注引发的不良反应。按照是否符合过敏反应诊断标准,将超敏反应/输液反应进一步分为标准输液反应和严重过敏反应。
严重过敏反应诊断依据美国过敏、哮喘和免疫学会(AAAAI)在2006年发布的基于症状和体征的临床诊断标准[10],符合下述3 条中的任何1 条,即可诊断严重过敏反应。1)急性起病(几分钟到数小时),累及皮肤和(或)黏膜组织(如全身性荨麻疹、瘙痒、潮红、口唇舌及悬雍垂水肿)。以及下述至少1项:①呼吸系统受累(如呼吸困难、喘息-支气管痉挛、喘鸣、峰流速下降、低氧血症);②血压降低或终末器官功能障碍(如肌张力下降、昏倒、晕厥、失禁)。2)接触可疑变应原后迅速(几分钟到数小时)出现下述至少2 项症状:①皮肤黏膜受累(如全身性荨麻疹、瘙痒-潮红、口唇舌及悬雍垂水肿);②呼吸系统受累(如呼吸困难、喘息-支气管痉挛、喘鸣、峰流速下降、低氧血症);③血压降低或相关症状(如肌张力下降、昏倒、晕厥、失禁);④持续的胃肠道症状(如痉挛性腹痛、呕吐)。3)暴露于已知变应原后(几分钟到数小时)出现血压降低:①婴儿和儿童:收缩压减低(依年龄各异:1~12个月为<70 mmHg;1~10岁为<[70 mmHg+(2×年龄);11~17 岁为<90 mmHg]或收缩压下降>30%;②成人:收缩压低于90 mmHg 或较基线水平下降>30%。
1.2.2 标准输液反应及严重过敏反应严重程度评价标准 根据美国国家癌症研究所(national cancer institute,NCI)常见不良事件评价标准(common terminology criteria for adverse events,CTCAE)5.0版进行评估。标准输液反应的评估:1级:反应短暂且轻微,无需中断输液,无需治疗;2级:需要治疗或需要中断输液,但对症治疗(如抗组胺药、非甾体抗炎药、阿片类麻醉药、静脉输液)后迅速缓解,需要不长于24 h的预处理用药;3级:症状持续时间长(如对症治疗疗效不迅速和/或短暂中断输液),初始症状改善后又复发,需要住院治疗的其他后遗症;4级:危及生命,需要紧急治疗;5级:死亡。严重过敏反应的评估:1~2级:无;3级有症状的支气管痉挛伴有或不伴有荨麻疹;需要肠外治疗;过敏反应相关性水肿或血管性水肿;低血压。4级:危及生命,需要紧急治疗。5级:死亡。
由于CTCAE 5.0 标准对严重过敏反应的严重程度区分度较弱,另依据《严重过敏反应急救指南》推荐[11]进行分级。标准如下:Ⅰ级:只有皮肤黏膜系统症状和胃肠系统症状,血流动力学稳定,呼吸系统功能稳定;Ⅱ级:出现明显呼吸系统症状或血压下降;呼吸系统症状包括胸闷、气短、呼吸困难、喘鸣、支气管痉挛、发绀、呼气流量峰值下降、血氧不足等。血压下降:成人收缩压80~90 mmHg 或比基础值下降30%~40%;婴儿和儿童血压,年龄<1 岁的收缩压<70 mmHg;1~10 岁的收缩压<70 mmHg+2×年龄;11~17 岁的收缩压<90 mmHg 或比基础值下降30%~40%。Ⅲ级:出现神志不清、嗜睡、意识丧失、严重的支气管痉挛和/或喉头水肿、发绀、重度血压下降(收缩压<80 mmHg或比基础值下降>40%)、大小便失禁等任一症状。Ⅳ级:发生心跳和/或呼吸骤停。
1.3 统计学分析
采用SPSS 19.0软件进行统计学分析。正态分布变量采用表示,非正态分布变量采用中位数及上下四分位数表示。符合正态分布且具有方差齐性的定量数据比较采用独立样本t检验,不符合正态分布的定量数据比较采用Kruskal-Wallis H检验,无序分类资料比较采用χ2检验或Fisher 检验,有序分类资料比较采用秩和检验。以P<0.05为差异具有统计学意义。
2 结果
2.1 患者一般临床特征
62例患者的平均年龄为(52.9±11.3)岁,其中男性32例(51.6%)、女性30例(48.4%),男女比例1.07:1。1例(1.6%)患者既往存在药物过敏史,为青霉素及碘造影剂过敏。所有患者既往均未接受过其他铂类药物治疗。
所有患者均接受奥沙利铂为基础的化疗方案,其中XELOX 方案治疗49例(79.0%),SOX 方案治疗10例(16.1%),mFOLFOX6 方案治疗3例(4.8%)。在治疗上,辅助化疗患者42例(67.7%),新辅助治疗患者1例(1.6%),姑息化疗患者17例(27.4%),Ⅳ期根治性切除术后2例(3.2%)。
患者发生输液反应时奥沙利铂中位治疗周期为6(4~7.25)个周期,中位累积剂量为456.9(263.5~651.0)mg/m2。19例(30.6%)患者存在无奥沙利铂间隔期,间隔原因10例(52.6%)为术后辅助化疗后复发转移行姑息化疗,5例(26.3%)为新辅助化疗后手术期间停用奥沙利铂,2例(10.5%)为多线姑息化疗,既往奥沙利铂方案化疗进展后再次使用,1例(5.3%)为姑息化疗stop-and-go 疗法,1例(5.3%)为异时性结肠双原发癌既往行含奥沙利铂方案辅助化疗。
37例(59.7%)患者在输注奥沙利铂前使用了糖皮质激素预处理,目的包括预处理或止吐。其中24例(63.2%)使用甲泼尼龙,14例(36.8%)使用地塞米松,换算为等效氢化可的松剂量250(200~400)mg。无患者应用抗组胺药物预处理。
2.2 超敏反应的分型及严重程度
41例(66.1%)患者诊断为标准输液反应,21例(33.0%)诊断为严重过敏反应,不同亚型超敏反应间患者一般情况无显著性差异(表1)。
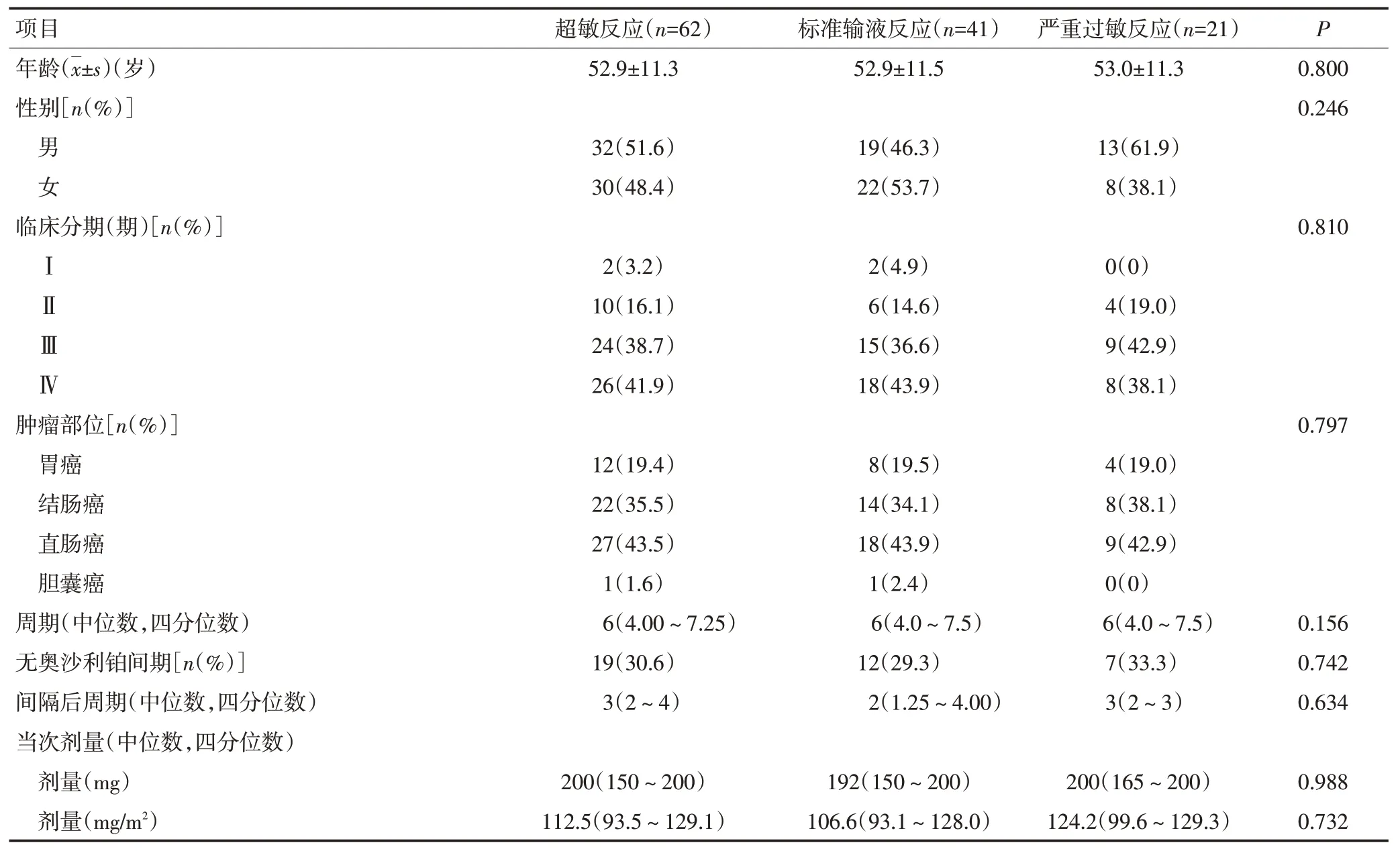
表1 不同亚型超敏反应患者的临床特征
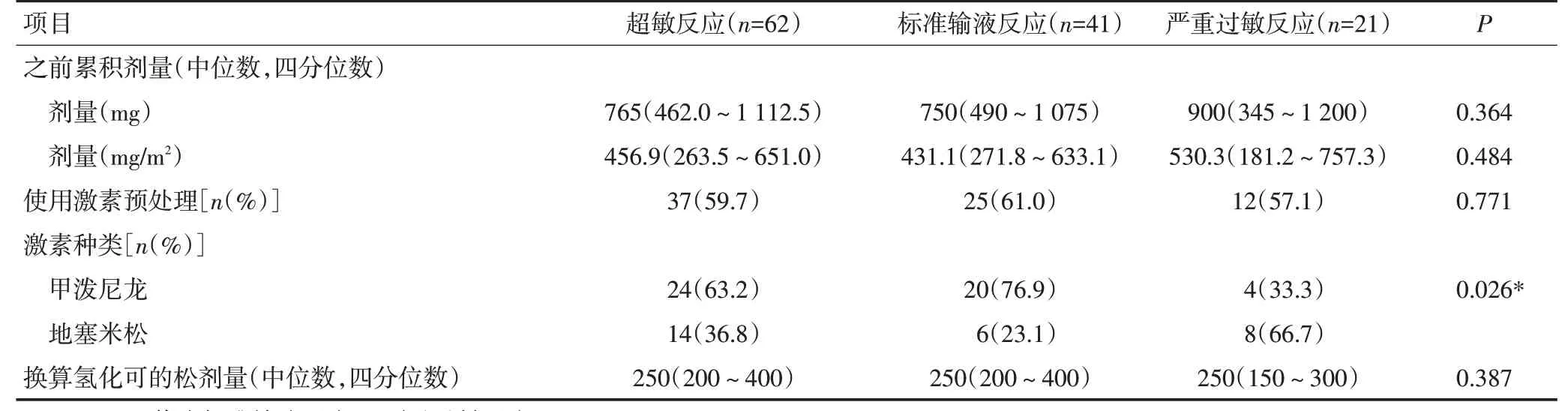
表1 不同亚型超敏反应患者的临床特征 (续表1)
标准输液反应患者中,CTCAE 5.0严重程度分级2级33例(80.5%),3级8例(19.5%),无1级、4级、5级患者。
严重过敏反应患者中,CTCAE 5.0分级3级18例(85.7%),4级3例(14.3%),无5级患者;《严重过敏反应急救指南》分级标准Ⅰ级4例(19.0%),Ⅱ级12例(57.1%),Ⅲ级5例(23.8%),无Ⅳ级患者。
2.3 不同亚型超敏反应的临床症状与体征
两种亚型超敏反应的临床症状及体征发生率见表2。与标准输液反应患者相比,严重过敏反应患者出现皮肤潮红(38.1%vs.14.6%,P=0.037)、支气管痉挛(9.5%vs. 0,P=0.045)、血压下降(23.8%vs. 0,P=0.003)、冷 汗(52.4%vs. 22.0%,P=0.015)、呕 吐(33.3%vs. 7.3%,P=0.023)、恶心(23.8%vs. 2.4%,P=0.037)、头晕(28.6%vs.0,P=0.002)的发生率更高。
2.4 超敏反应的处理与转归
47例(75.8%)患者的超敏反应发生在输注过程中,15例(24.2%)患者发生于奥沙利铂输注完成后,出现超敏反应症状距离开始输注中位时间为85(30~140)min(表2)。所有患者均采取暂停用药、更换输液器的处理。治疗方面,无患者使用肾上腺素;47例(75.8%)使用糖皮质激素治疗,等效氢化可的松中位剂量250(200~400)mg。19例(30.6%)患者使用抗组胺治疗,21例(33.9%)患者进行吸氧治疗,4例(6.4%)患者进行快速补液治疗。经过上述处理,所有患者症状均缓解,无死亡病例。出现症状到症状完全缓解中位时间为35(30~65)min,缓解最快者10 min,最慢者162 min(表3)。
2.5 发生超敏反应后再用药情况
2.5.1 当次化疗周期中再用药情况 对于超敏反应出现于奥沙利铂输注过程中的47例患者中,16例患者在症状完全缓解后尝试了继续输注,其中1例患者再次出现超敏反应,停止当次奥沙利铂输注,15例患者当次输注顺利完成,未再出现超敏反应。
2.5.2 后续化疗再用药情况 62例患者在发生超敏反应后无人进行奥沙利铂皮试或药物脱敏流程。后续化疗再用药情况见图1。
41例标准输液反应患者中,22例进行了再次用药。再次用药前13例患者输注糖皮质激素剂量同前,7例患者输注奥沙利铂前加用了糖皮质激素,2例患者加用了苯海拉明预处理,2例患者未进行预处理;所有患者均进行了减慢输液速度的处理。
按不同严重程度分级划分,33例2级标准输液反应患者中2例因治疗计划完成停药,2例后续治疗情况不详,其余患者中58.6%(17/29)进行了再次用药。17例接受再次用药的2级标准输液反应患者中,12例(70.6%)未再出现超敏反应;4例(23.5%)患者出现标准输液反应,其中3级3例,均终止治疗,2级1例,后续尝试了再次用药,未出现超敏反应;1例(5.9%)患者出现过敏性休克,后续终止治疗。8例3级标准输液反应患者中5例(62.5%)进行了再次用药,均未出现输液反应。
21例严重过敏反应患者中,4例进行了再次用药。再次用药前1例预处理方案同前,2例未使用预处理药物,1例增加了糖皮质激素剂量;所有患者均进行了减慢输液速度的处理。
按不同严重程度分级划分,18例3级严重过敏反应患者中4例(22.2%)进行了再次用药,均未出现超敏反应。3例4级严重过敏反应患者均未进行再次用药。
首次发生超敏反应后患者再次治疗周期数如图2所示,中位再治疗周期为2(1~4)个。仅4例首次再用药时因再次出现超敏反应停药,1例再用药第5个周期时因过敏性休克停药,其余患者均按计划完成治疗。
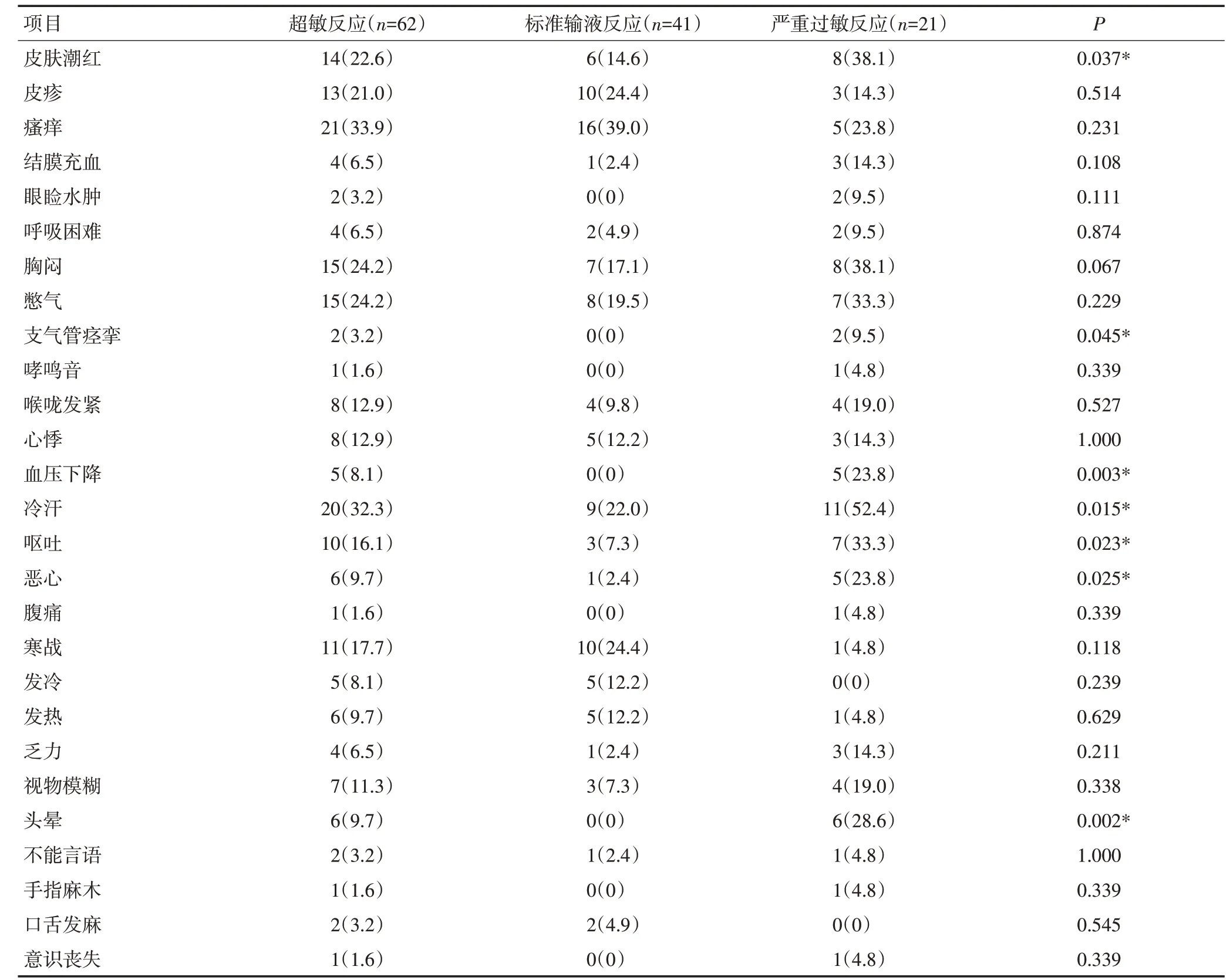
表2 不同亚型超敏反应的临床症状及体征 n(%)
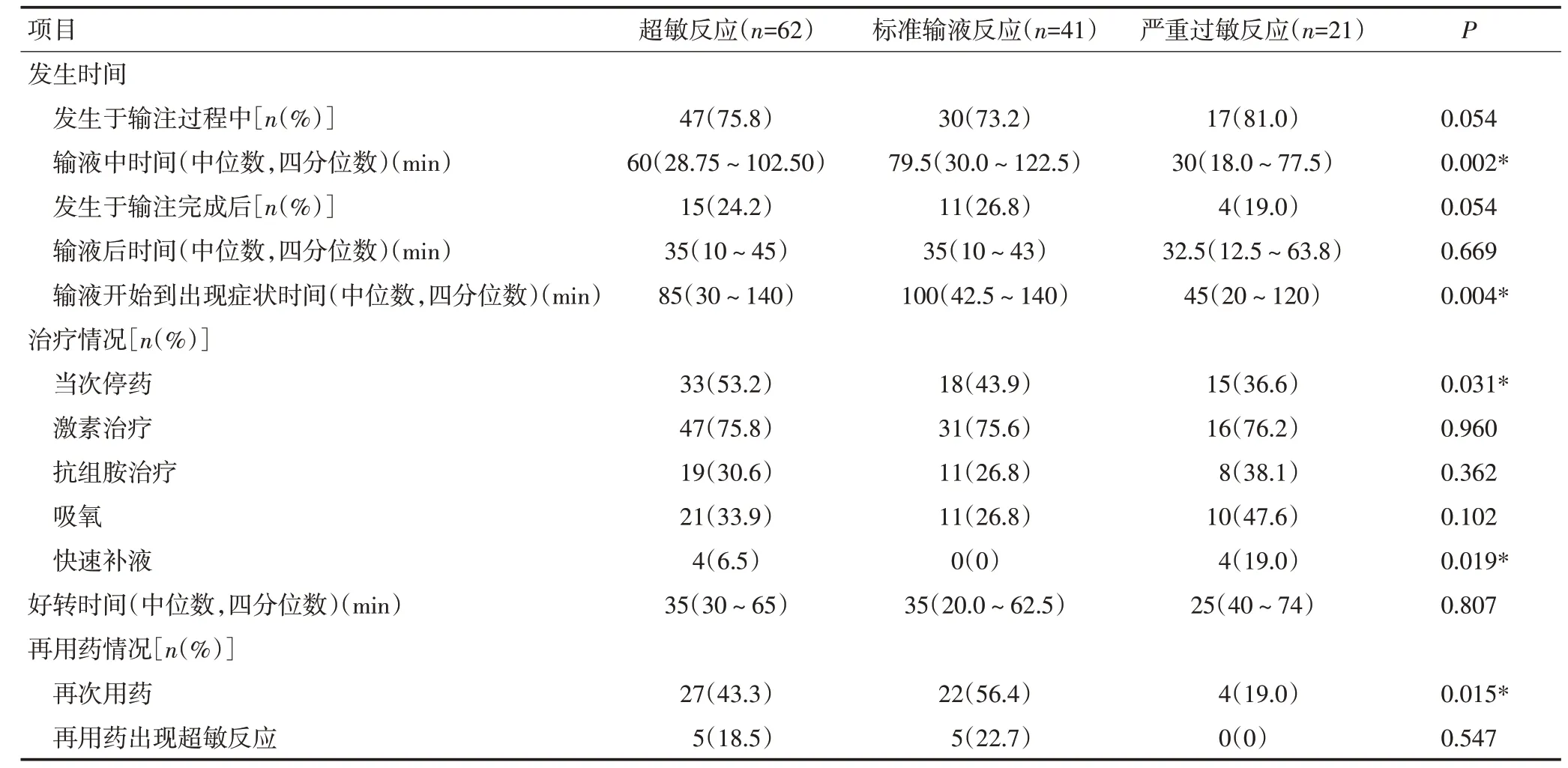
表3 不同亚型超敏反应的发生时间、治疗、转归及再用药情况
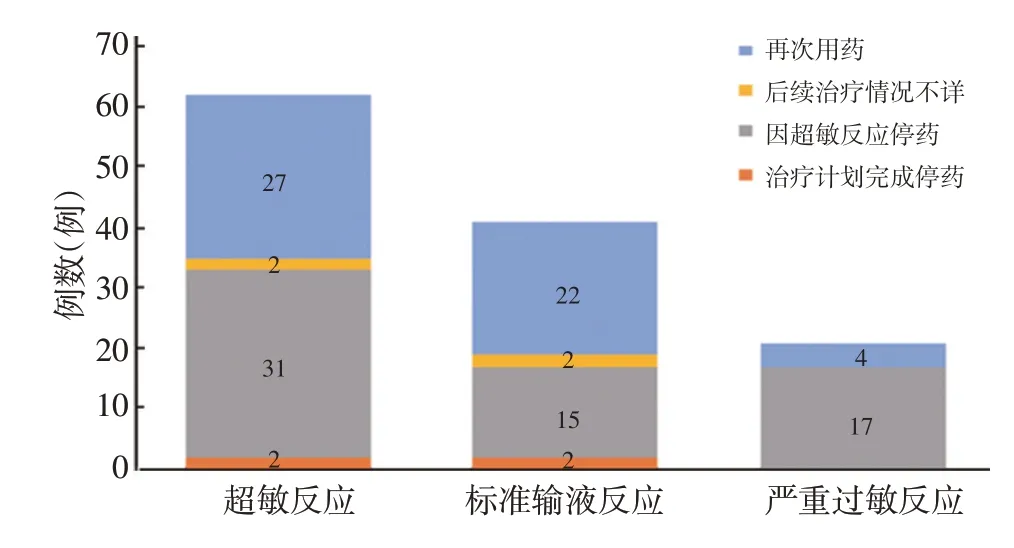
图1 发生超敏反应后后续治疗情况
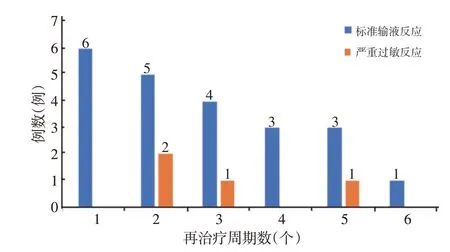
图2 首次发生超敏反应后再治疗周期数
3 讨论
超敏反应常见的症状包括潮红、瘙痒、心率及血压改变、呼吸困难或胸部不适、背痛或腹痛、发热和/或寒战、恶心、呕吐和(或)腹泻、皮疹、喉头发紧、缺氧、抽搐、头晕和(或)晕厥;就症状谱来说,标准输液反应和严重过敏反应症状谱无明显区别。但本研究中,与标准输液反应患者相比,严重过敏反应患者出现皮肤潮红、支气管痉挛、血压下降、冷汗、呕吐、恶心、头晕的发生率更高,提示当患者一旦出现上述症状时,即使临床症状体征暂不足以诊断为严重过敏反应,也应高度警惕严重过敏反应的可能,及时处理以避免症状迅速恶化。
目前国际通用的严重过敏反应标准为临床标准,主要依据为临床症状、体征及出现症状体征的时间特点。单纯依靠临床症状诊断严重过敏反应可能存在一定局限性,如奥沙利铂属于中度致吐风险化疗药物,对于部分合并危险因素的患者为高度致吐风险,当预防性止吐治疗不足时极易出现恶心、呕吐症状,当患者因标准输液反应导致皮疹时,两种症状同时存在会被误诊为严重过敏反应,导致不必要的停药。本研究中1例患者症状仅符合2级标准输液反应,再次用药时却出现过敏性休克;而4例符合严重过敏反应诊断的患者未经脱敏治疗再次用药并未发生超敏反应。这提示临床应注重收集完整症状体征,做好鉴别诊断;此外,有必要通过客观指标检测对考虑严重过敏反应的患者进行进一步评估,如皮试、血类胰蛋白酶检测、特异性IgE检测等[12]。
目前尚无降低奥沙利铂超敏反应的标准预处理方案。一项回顾性队列研究显示,使用地塞米松20 mg+口服苯海拉明50 mg+法莫替丁20 mg 对比使用地塞米松8mg 进行预处理,超敏反应发生率明显降低(7%vs.20%,P=0.0153),且延长了可耐受治疗周期[13]。日本一项前瞻性多中心单臂Ⅱ期临床试验在奥沙利铂化疗前予以地塞米松6.6 mg预处理,之后使用地塞米松6.6 mg联合奥沙利铂输注,超敏反应发生率为4.1%(3/73),均仅表现为皮肤反应。我国一项回顾性研究使用5 mg 低剂量地塞米松进行预处理,超敏反应发生率为4.9%[14]。为了减轻糖皮质激素的不良反应,理想的方式是根据高危因素筛选发生超敏反应高风险的患者,对这些患者针对性地采取预处理措施。但遗憾的是,有研究显示,奥沙利铂超敏反应的危险因素重复性差,无法根据临床特点进行评估[3];而皮肤试验等客观指标用于指导预处理上存在争议[15-16]。尽管关于预处理的最佳药物种类、剂量均有待证实,但支持在奥沙利铂输注前常规使用糖皮质激素进行预处理,以降低超敏反应发生率,避免化疗中断。
严重过敏反应发展迅速,且发展越快提示病情重且危及生命[17],因此对于出现严重过敏反应表现或3 级标准输液反应的患者,推荐立即停药,治疗首选肾上腺素治疗[18]。目前尚缺少针对肾上腺素使用的最佳循证医学证据,而受伦理限制,针对使用肾上腺素的随机、安慰剂对照临床试验无法开展[19];但已有在循证医学证据下,推荐使用肾上腺素作为初始治疗的证据强于初始使用组胺H1受体抑制剂、H2受体抑制剂或糖皮质激素[20-22]。既往研究显示,肾上腺素的延迟使用与严重过敏反应所致死亡相关[19,23]。肾上腺素治疗严重过敏反应患者无绝对禁忌,对于老年患者和既往有心血管病史的患者,使用肾上腺素的获益超过风险[18,24]。肾上腺素的使用方法为0.01 mg/kg,大腿前外侧肌肉注射。肌肉注射肾上腺素安全性好,可能的不良反应包括轻度、一过性的皮肤苍白、震颤、心悸、头痛等[18]。本研究中严重过敏反应患者均未使用肾上腺素,包括出现过敏性休克的患者,提示临床对于肾上腺素一线地位认识不足。英国一项回顾性研究[23]收集了164例全身性过敏反应所致死亡的病例,其中医源性全身性过敏反应占50%左右;在医源性全身性过敏反应导致死亡的患者中,出现症状到呼吸心脏骤停的中位时间仅为5 min。仅62%死亡患者在治疗中使用了肾上腺素,而在心脏骤停前使用的仅占14%。因此,亟需加强肿瘤科医生对严重过敏规范治疗的培训,解决肾上腺素的使用率不足的问题。
出现超敏反应后能否继续用药是临床医生关心的问题。Thomas 等[25]回顾已有文献,提出轻到中度过敏及输液反应的患者在进行激素和组胺受体拮抗剂预处理后可以安全地进行再次用药,而对于发生3级标准输液反应或符合严重过敏反应特点的患者不推荐通过预处理再次用药,需要进行脱敏治疗。本研究31例需要后续继续治疗的2级标准输液反应患者中,仅54.8%(17/31)进行了再次用药,再次用药的患者中70.6%未出现输液反应,与既往文献一致[6]。提示当前临床医师对于奥沙利铂的停药指征掌握欠严格,通过对超敏反应进行准确的分型和严重程度分级可以降低奥沙利铂由于超敏反应导致的停药率。
本研究的主要局限性在于为回顾性研究,临床资料尤其是过敏反应的症状、体征收集存在遗漏可能;但是本研究选择上报ADR中心的病例,均客观记录了患者的临床症状、体征、处理及转归等情况,通过查阅后续住院及门诊病历了解再次用药情况,记录较为全面,弥补了回顾性的不足。
综上所述,当前临床医师对标准输液反应及严重过敏反应分型、严重程度分级认识较弱,对严重过敏反应处理中肾上腺素一线使用意识不足。在明确临床诊断分型标准的基础上开展皮试、血清学评估、脱敏治疗可减少奥沙利铂停药,为患者带来更多获益。

