超声诊断联合扩展性无创产前检测在孕期胎儿染色体疾病筛查中的应用
代鹏 赵干业 时盼来 孔祥东
郑州大学第一附属医院遗传与产前诊断中心(郑州450046)
染色体异常导致的疾病尚无有效的治疗手段,通过筛查和产前诊断及早识别胎儿染色体异常对降低出生缺陷、提高人口健康、避免孕妇身心伤害、减轻家庭及社会经济负担尤为重要[1]。超声检查作为一种无创产前筛查与诊断手段,能够在孕早中期发现胎儿严重结构异常或软指标阳性,被广泛用于临床,但其指标阳性几率大,指标阳性孕妇是否行穿刺术尚存争议[2]。近年来,无创产前检测(noninvasive prenatal testing,NIPT)以无创、安全等优点得到了广泛的临床应用,缓解了产前诊断压力[3]。该技术主要通过采集孕妇外周血游离DNA 检测胎儿染色体疾病,对胎儿本身没有伤害,快速获取结果[4]。但最近研究[5]显示NIPT 大约检测到23%与染色体异常相关的疾病,67%临床表型相关的染色体异常被忽略。更有研究[6]表明,15 767 例智力障碍/发育迟滞等先天异常的患病儿童中,约7.2%的患儿可能由<10 Mb的基因组拷贝数变异(copy number variations,CNVs)引起。基因组CNVs 能够导致染色体微缺失/微重复综合征(microdeletion/microduplication syndrome,MMS),且其发病率与孕妇年龄无关,对于40 岁以下孕妇,染色体MMS 的发生比唐氏综合征更常见[7]。因此,NIPT 进一步扩展到了CNVs 的额外分析[8-9]。研究显示,染色体MMS 与胎儿超声结构畸形和软指标阳性密切相关[10-11],常规超声检查可发现胎儿结构畸形和软指标阳性[12]。但扩展性NIPT(NIPT-plus)是否可以作为超声诊断异常的一线筛查手段未见相关文献报道。因此,本研究旨在探讨NIPT-plus 在超声诊断提示胎儿结构异常或软指标阳性的临床应用价值。
1 资料与方法
1.1 一般资料回顾性分析2018年9月至2019年10月因超声检查提示胎儿结构异常或软指标阳性于我中心行NIPT-plus 筛查的1 487 例不同孕期的孕妇。孕妇年龄19~42 岁,平均年龄28.6 岁,孕周为(12~32+5)周,平均孕周为(21.9±2.7)周,行超声检查的时间为12 周,即颈项透明层(nuchal translucency,NT)检查及后期各个阶段的超声检查。双胎孕妇48 例,试管婴儿孕妇58 例。NIPT-plus 筛查高风险孕妇要求在我中心行穿刺-染色体核型分析或全基因组拷贝数变异分析排除胎儿染色体异常,并随访妊娠结局。孕妇排除接受细胞治疗者、肿瘤患者和一年内异体输血者。本研究获得医院医学伦理委员会批准(2018-016),所有孕妇均签署知情同意书。
1.2 方法
1.2.1 超声检查采用GE Voluson E8 或Prosound a7 超声仪,经腹二维和三维探头,频率分别为1~5 MHz 和5~9 MHz。孕11~14 周查NT 厚度、胸腹脏器、脊柱、颜面、头颅等实质性脏器,并测量胎心、羊水深度、股骨、肱骨、腹围以及双顶径、头围、静脉导管及脐血管等。若发现异常的行NIPT-plus检测,并于孕中晚期行胎儿Ⅱ、Ⅲ级或胎儿心脏产前超声筛查,按照产前诊断超声指南,依次观察胎儿结构和软指标有无异常。
1.2.2 NIPT-plus 检测采血前详细咨询既往病史、生育史、遗传病史、孕期用药情况、有毒物品和放射性物品接触情况及夫妻双方染色体核型等基本信息,并签署知情同意书。采集孕妇外周血10 mL 保存在无创专用采血管;提取母体血浆游离DNA(cell-free DNA,cfDNA),使用10 ng cfDNA 构建文库,建库过程无需PCR 扩增。文库定量后,在基因测序仪(Nextseq CN500,美国)进行高通量测序,生成约20 M 45 bp(37 bp+8 bp index),通过提高测序深度和加强算法,实现染色体非整倍体和CNV 分析,并设置超纯水代替的空白对照,21-三体、18-三体和13-三体样本作为阳性对照,结果采用Z值风险评分。如果NIPT-plus 结果正常,继续定期超声检查。
1.2.3 侵入性产前诊断NIPT-plus 提示高风险孕妇行侵入性产前诊断。常规消毒后,在超声引导下行绒毛穿刺术取10~15 mg 绒毛或羊膜腔穿刺术抽取羊水20 mL。CNV-seq 分析:提取样本基因组DNA 1~1.5 μg;将DNA 打断、扩增,构建基因组文库;利用NEXTseq CN500 测序平台测序,使用Burrows-Wheeler 算法将所有测序序列与hg19 基因组进行比对分析和分析数据。染色体核型分析:将羊水细胞1 600 rpm 离心10 min,在沉淀物加入羊水培养基转移到细胞培养瓶,放置于37 ℃、5%CO2的培养箱培养7 d,更换培养液后继续培养至10~12 d 观察羊水细胞生长状态。生长良好的细胞加入秋水仙素,经37 ℃低渗、固定、制片、烤片、胰酶消化、G 显带,利用蔡司MetaSystems Ikaros 染色体核型分析系统采集与分析染色体中期分裂相。核型按照人类细胞遗传学国际命名体制ISCN2016 进行描述与诊断。
1.2.4 随访对所有孕妇,在孕晚期或新生儿出生后进行随访。
2 结果
2.1 染色体异常胎儿检出情况本研究利用NIPT-plus 检测了胎儿常见常染色体和性染色体非整倍体、相对高发的>3 Mb 大小并位于特定症候群相关染色体片段位置的微缺失疾病和>10 Mb的染色体大片段缺失/重复综合征等在内的大约100 种胎儿染色体异常疾病。1 487 例超声异常孕妇接受NIPT-plus 筛查后,共检出85 例为NIPT-plus高风险,检出率为5.72%(85/1 487),其中73 例高风险孕妇行侵入性产前诊断,确诊36例胎儿为染色体非整倍体或MMS,阳性预测值(positive predictive values,PPVs)为49.32%(36/73)。3 例双胎孕妇的NIPT-plus 结果为高风险(6.25%,3/48),3 例试管婴儿孕妇的NIPT-plus 结果为高风险(5.17%,3/58)。见表1。
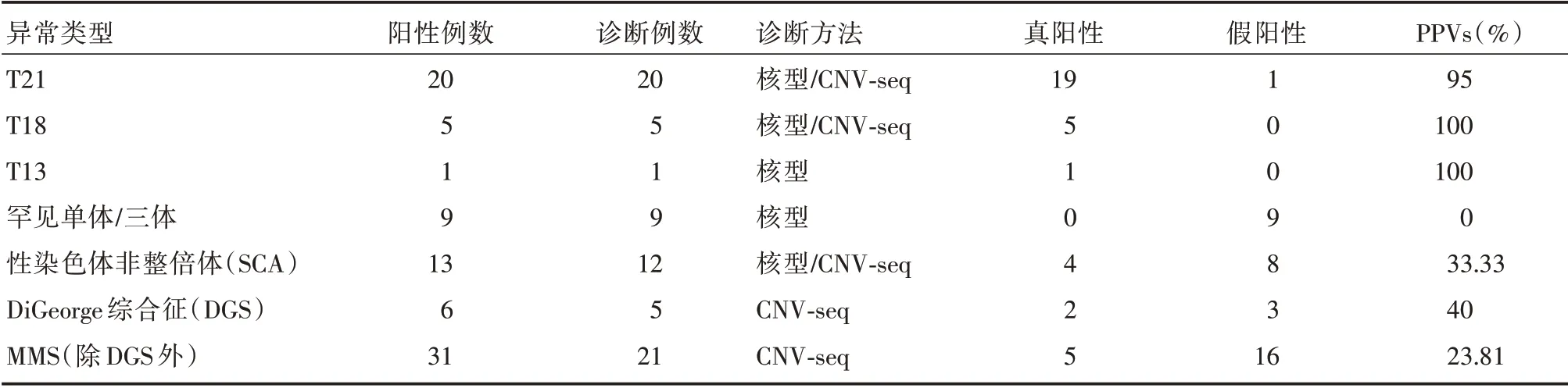
表1 超声异常孕妇行NIPT-plus 及侵入性产前诊断结果Tab.1 NIPT-plus and invasive prenatal diagnosis results of pregnant women with abnormal ultrasound例
21-三体、18-三体、13-三体和罕见单体/三体高风险孕妇行侵入性产前诊断结果为阳性的行终止妊娠,假阳性的继续妊娠。13 例NIPT-plus 提示SCA 高风险孕妇,随访得知其中1 例孕妇因超声显示胎儿心脏血管异常行NIPT-plus 检查高风险后未行侵入性产前诊断,孕妇孕晚期定期行超声和其他相关检查,胎儿心脏血管发育恢复正常且未发现任何异常继续妊娠,出生后各项指标都正常。6 例NIPT-plus 提示DGS 高风险孕妇,随访得知其中1 例孕妇因超声显示胎儿室间隔缺损行NIPT-plus 高风险后未行侵入性产前诊断而继续妊娠,胎儿出生后各项指标都正常。31 例NIPT-plus提示MMS 高风险孕妇,随访得知10 例孕妇未行产前诊断,其中3 例孕妇直接行终止妊娠,7 例孕妇在孕中晚期定期行超声和其他相关检查未发现其他异常进而继续妊娠,且婴儿出生后各项指标正常。此外,MMS 高风险孕妇行侵入性产前诊断发现部分胎儿染色体MMS 遗传父母,因此在遗传咨询中发现确诊为阳性MMS 的胎儿,建议父母行CNV-seq 检测以便鉴定胎儿MMS 来源父母遗传还是新发突变,有利于判定MMS 的致病性。NIPTplus 对罕见三体/单体的PPVs 为0,提示需要提高生物信息学算法和扩大样本量验证NIPT-plus 对罕见三体/单体的检测能力,更要求检测机构提高实验质控和报告审核以及临床医生的遗传咨询能力,减少孕妇不必要的心理负担。
2.2 NIPT-plus对临床超声异常分布的检出率根据超声诊断常见的结构异常或软指标阳性,1 487例孕妇超声异常分布见表2。NIPT-plus 对超声胎儿结构异常或软指标的检出率不同,其中心脏发育其他异常、肾盂分离、室间隔缺损、NT 增厚、单脐动脉和鼻异常等检出率最高。按PPVs 指标来看,鼻异常、囊性肿瘤、NT 增厚、肠管回声增强和心脏发育其他异常的PPVs 高于超声诊断提示其他胎儿结构异常或软指标阳性见表2。
2.3 随访结果12 例NIPT-plus 提示高风险孕妇因担心穿刺存在风险拒绝产前诊断,其中6 例定期产检监测胎儿发育情况,且出生正常,3 例后期超声检查发现胎儿严重结构畸形选择终止妊娠,3 例继续妊娠。73 例孕妇行侵入性产前诊断,37 例为假阳性,胎儿顺利分娩,新生儿各项指标正常;36 例确诊孕妇中,19 例21-三体、5 例18-三体、2 例性染色体非整倍体和2 例MMS 的孕妇选择终止妊娠,其他确诊孕妇选择继续妊娠或已顺利分娩。
对NIPT-plus 提示低风险孕妇建议遗传咨询,并孕期定期超声检查密切监测胎儿发育情况,如超声发现胎儿出现严重结构畸形或软指标阳性,建议孕妇进一步行有创性产前诊断,最大程度减少假阴性病例的出生。1 402 例NIPT-plus 低风险孕妇中,电话随访有效者1 279 例(随访91.2%),其中482 例胎儿顺利分娩,且新生儿体检各项指标正常,784 例胎儿后期超声检测指标逐渐恢复正常且处于妊娠状态,13 例胎儿结构异常或胎死宫内引产,但实验室诊断结果为染色体正常。截至2020年2月未发现已出生的新生儿异常。
3 讨论
染色体病和染色体MMS 是严重出生缺陷的主要原因,我国每年出生此类患儿近30 万,给家庭、社会和国家带来沉重负担[13]。染色体MMS 常见的临床表现包括生长发育迟缓、智力障碍、自闭症、多发畸形和功能障碍等[14-15]。因此,产前筛查与诊断是防控这类疾病的最有效途径。研究显示,胎儿鼻骨异常或缺失等微小畸形均与染色体MMS常密切相关[16],所以对超声诊断结构异常或软指标阳性的胎儿进行产前检查具有重要的临床意义[17-18]。NIPT的出现提高了筛查的准确性,减少了孕妇不必要的穿刺术和心理负担以及出生缺陷的发生,但常规NIPT只筛查21、18和13-三体综合征,仅占染色体疾病的20%左右,剩余的大部分染色体异常综合征被忽视,特别CNVs[5-6]。LEFKOWITZ等[19]从1 210 例孕妇中发现240 例胎儿超声异常行NIPT,其中34 例(14.2%,34/240)胎儿为21-三体综合征,6 例(2.5%,6/240)胎儿为18-三体综合征,10例(4.2%,10/240)胎儿为13-三体综合征,16 例(6.7%,16/240)胎儿为性染色体非整倍体异常,22例(9.2%,22/240)胎儿为染色体拷贝数变异,超声异常在所有孕妇行NIPT 的检出率为7.3%(88/1 210)。LIANG 等[20]对94 085 名单胎妊娠女性的胎儿异常进行前瞻性研究,评估NIPT-Plus 在染色体非整倍体和全基因组MMS 检测中的临床表现,共发现1 128 例(1.2%)具有临床意义的胎儿染色体异常,包括965 例染色体非整倍体(1.026%)和163 例(0.174%)MMS,且具有较好的PPVs,因此作者建议将NIPT-plus 作为临床一线妊娠筛查技术。本研究分析了1 487 例因超声异常孕妇行NIPT-plus筛查结果,共发现85 例孕妇胎儿筛查结果为高风险,检出率为5.72%,包括35 例常染色非整倍体,13 例性染色体非整倍体和37 例MMS。但本研究只分析了超声异常孕妇的NIPT-plus 结果,未在超声检测正常或未行超声检测的病例中进行NIPTplus 检测分析。
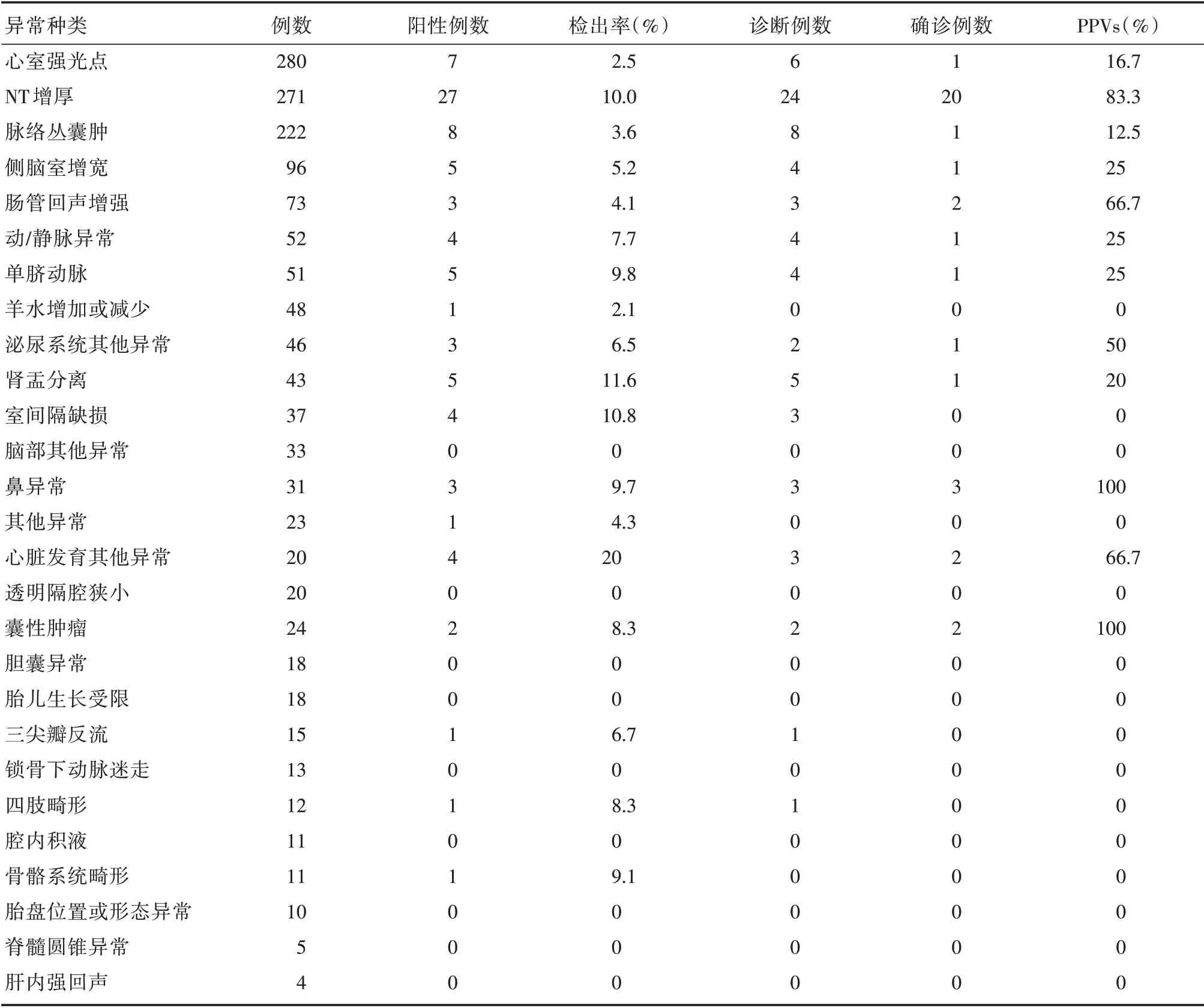
表2 超声异常的临床分布及NIPT-plus 筛查阳性例数和PPVsTab.2 Clinical distribution of ultrasound abnormalities and the positive number of NIPT-plus screening and PPVs例
NIPT-plus 不仅可以检测常见的染色体非整倍性,还可检测罕见的常染色体非整倍体[21]。然而,本研究中,NIPT-plus 筛查高风险的罕见三体/单体经侵入性产前诊断均为假阳性,增加了侵入性操作。LIANG 等[20]从94 085 例单胎妊娠女性的胎儿异常中发现49 例非常见常染色体非整倍体,其中35例为假阳性,PPVs较低。FIORENTINO等[22]研究12 114 例孕妇行NIPT 检测,17 例为常染色体罕见三体,其中10 例进行了侵入性产前诊断,确诊3 例胎儿为限制性胎盘嵌合,未行侵入性产前诊断1 例后期诊断为15 号染色体的UPD(uniparental disomy,单亲二倍体),罕见三体的PPVs 也较低。因此,NIPT-plus 确定的大多数罕见三体/单体高风险的孕妇可能不需要进行侵入性产前诊断,否则增加了过度诊断的风险,但此类数据也许具有重要的临床意义,有助于改善妊娠管理。FIORENTINO等[22]研究显示NIPT-plus 提示罕见三体高风险的胎儿可能存在限制性胎盘嵌合或UPD 风险,需要进行连续超声检查以监测胎儿的生长发育,排除宫内生长受限。
鉴于以上分析,NIPT-plus 是否推荐为超声诊断异常孕妇的一线筛查手段需要进一步扩大样本量验证。但根据相关文献和本研究结果,笔者建议将NIPT-plus 作为超声诊断异常孕妇进行产前筛查的备选技术。对NIPT-plus 低风险的孕妇后期定期行超声诊断等相关检查,监测胎儿发育情况。对NIPT-plus 高风险的孕妇建议羊水穿刺行胎儿染色体核型或全基因组拷贝数变异检测,降低先天性缺陷儿的出生。

