以硫酸氧钛为钛源制备二氧化钛粒子
龚之宝,韩迈,孙伟振,马占华,李青松
(中国石油大学(华东)重质油国家重点实验室,山东 青岛 266580)
二氧化钛是现今无机材料研究的热点,因为其具有着一些显著的优点而被逐渐用于众多领域,如其具有耐酸碱、耐高温高压、抗菌抗污染以及具有宽禁带宽度和光催化性能等特点[1-4],致其逐渐被广泛用于无机陶瓷膜材料,光催化降解燃料和催化剂,化妆品,传感等领域[5-9]。
二氧化钛应用在不同领域时制备上也会有一定的区别,比如利用其催化性能时若高温煅烧就可能影响比表面积以及酸性位[10],多孔材料的制备时往往会加入各种模板剂[11],无机膜的应用也多会加入一些表面活性剂等对粒径进行控制[12],不同的制备方法得到的粒子存在差异。不仅如此,不同钛源制得的粒子同样存在差异。制备二氧化钛的原料主要是钛的有机盐和钛的无机盐两大类。第1类主要有钛酸四正丁酯、钛酸四乙酯;第2类有四氯化钛、硫酸氧钛和硫酸钛等[13-16]。钛的有机盐类水解制备已有较多文献介绍,本文以更为廉价的硫酸氧钛为钛源制备二氧化钛粒子,综述了各种主要制备方法以及国内外对该粒子制备的研究进展同时针对国内实际情况对该领域的研究提出了建议和展望。
1 水热法
水热法的基本步骤是将硫酸氧钛溶液(或硫酸氧钛固体颗粒)与水放在一起,加入到反应釜中,通过控制一定的温度生成二氧化钛的前驱体氢氧化氧钛[TiO(OH)2,亦称偏钛酸],继续延长反应时间使偏钛酸向二氧化钛颗粒转变[17-18]。但这个过程可以不仅仅只是加入硫酸氧氧钛和水,可以加入碱性溶液(如氨水、氢氧化钠溶液)加速生成偏钛酸,加入表面活性剂抑制粒子团聚等[19-20]。同时这个过程可以分成两步,一步是沉淀过程,另一步是水热反应过程,即将硫酸氧钛溶液加入氨水或者加热生成偏钛酸之后再移入到水热反应釜进行反应[21]。第1步:
TiOSO4+H2O = TiO(OH)2↓+ H2SO4
或者:
TiOSO4+NH3·H2O=TiO(OH)2↓+(NH4)2SO4
第2步:
TiO(OH)2= TiO2+H2O
分步过程可以大大提高二氧化钛粒子的纯度,因为过程中不可避免的生产干扰粒子,如SO42-,第一步生产的沉淀经过水洗过滤之后可以得到纯净的偏钛酸,这样生成的二氧化钛粒子也极为纯净。在这里如果没有使用氨水作为沉淀剂而是直接通过调节温度反应的话,反应时间会有较大幅度的延长。水热法明显的特点是可以取消后期的晶化处理过程,因为一般情况下水解或者溶胶等得到的粒子往往处理不定型状态,但是水热法的过程往往是伴随着高温高压条件使得得到的粒子具有温度的晶型结构,故也称之为一步合成法。可以看出此方法重点并非沉淀过程,而是后续的水热反应过程。
陈贝等[17]以TiOSO4为原料,利用氨水调节pH,在180 ℃下反应12 h,得到平均粒径为137 nm锐钛矿二氧化钛粒子。值得一提的是其在制备过程中进行了La掺杂之后粒径得到了明显的降低,达到73 nm。张一兵等[19]在探究二氧化钛的光催化性能时同样利用水热法制备得到了粒径相对均一的二氧化钛粒子,并利用FeCl3·6H2O进行了Fe3+发现有利于提高其催化性能。郭琼等[21]以同样的方法制得TiO2粒子后探究了水钛摩尔比以及光照等众多影响光催化性能的因素,并优化得到最佳条件。
2 沉淀法
沉淀法的重点是放在沉淀过程上,而后续的处理往往大相径庭,都是将得到的沉淀洗涤过滤出去杂离子后在一定温度下焙烧得到二氧化钛粒子。该操作过程并不复杂,即向硫酸氧钛溶液中加入沉淀剂通过控制反应温度来控制生成的沉淀[22-23],根据沉淀过程的不同也可以将沉淀法分为直接沉淀法和均匀沉淀法两种,如加入氨水进行的沉淀就是直接沉淀,而加入碳酰胺然后生成氨水的过程即为均匀沉淀[24-25]。以加入碳酰胺为例,其过程主要可分为三步:
CO(NH2)2+3H2O →2NH3· H2O+CO
TiOSO4+ NH3·H2O→
TiO(OH)2+(NH4)2SO4
TiO(OH)2→ TiO2+H2O
沉淀法比较明显的优势在于能够在短时间内生成大量粒子并且粒度较为均一,同时相对于均匀沉淀法而言,因为控制了尿素的水解温度进而控制了硫酸氧钛的沉淀过程,使得过程中粒子的生成和核的生长速率得到了很好的控制,这就在一定程度了控制了粒子的粒径,成功避免了一次粒子和二次粒子的结合[26]。在这里可以明显看出均匀沉淀反应的要点在于控制升温的时间使碳酰胺的分解得到控制,如果没有程序升温的过程则很难做到均匀沉淀。需要指出的是沉淀法的原料除了可以是硫酸氧钛之外也可以是偏钛酸,当使用偏钛酸时其原理依然是生产硫酸氧钛再沉淀的过程[27]。
均匀沉淀法的用途较为广泛,如在直接催化剂方面,Ye Jiang等[25]采用均匀沉淀法制备得到Ce-Mo-Ti混合氧化物催化剂并发现该催化剂在250~450 ℃温度范围内展现出良好的SCR活性。
梁进闯[23]在制备二氧化钛纳米晶的过程中同样采用了均匀沉淀法,其使用硝酸铕对纳米晶进行了Eu3+掺杂后在600 ℃下焙烧4 h,得到平均粒径在50.12 nm的锐钛矿二氧化钛,多方面实验证明,在进行其他粒子掺杂,可以减少沉淀过程制得的粒子粒径。徐春宏等[28]在制备复合材料时,同样用到以硫酸氧钛为钛源的均匀沉淀法,其以膨胀珍珠岩作为载体,对其进行二氧化钛颗粒负载作为催化剂进行光催化降解实验研究。其制备得到的粒子比表面积最小可达到3.59 m2/g,粒子粒径可控制在10~20 nm。郑典模等[29]系统的对影响均匀沉淀法制得粒子的粒径因素进行了探究,包括溶液浓度、温度以及pH等。
3 胶溶法
胶溶法也称为胶溶萃取法或萃取法或萃取精馏法,因为这个过程包括有沉淀过程、胶溶过程、萃取过程以及精馏过程。该过程相对于其他方法要更为复杂,但复杂过程带来的是更优质的TiO2粒子,其优势主要可分为两点:一是粒子的纯度更高,因为采用硫酸氧钛作为钛源时往往都含有较高的杂质,不仅仅是沉淀过程产生的SO2-和NH+,硫酸氧钛的制备往往采用钛精矿为原料,利用硫酸法钛白工艺制备得到[30],钛精矿中含有大量Fe元素,还有少量P、S、Ca、Mg等,后续的萃取过程能除去99%的杂质离子。第二个是偏钛酸的胶溶过程在一定程度上可以通过控制溶胶的状态,减少粒子间的聚合,从而减小粒子的粒径,如加入表面活性剂和少量电解质等。此外,胶溶过程同样对二氧化钛进行其他粒子的负载[31]。主要步骤如下:
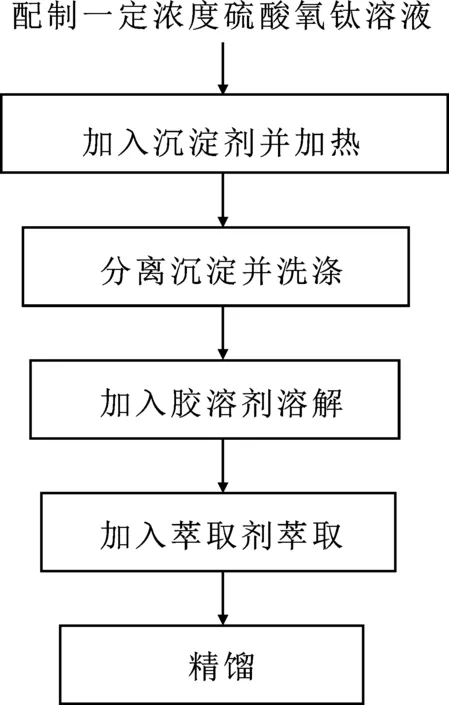
图1 胶溶法制备二氧化钛步骤Fig.1 Steps of preparing titanium dioxide by peptization
精馏的过程不仅可以提纯制备得到的粒子,同时可以对有机溶剂进行回收,该过程萃取剂的选择多为有机溶剂,如甲苯、二甲苯以及丙酮等,精馏过程对萃取剂进行回收以便循环利用。胶溶过程常需抑制粒子间的团聚而加入表面活性剂(如十二烷基苯磺酸钠),利用其位阻效应降低粒径[32]。
胶溶法因为过程复杂所以研究的并不多,加上现今不断对硫酸氧钛的生产工艺进行优化,使得到的TiSO4纯度更高、杂质更少,以至于此方法缺点更加明显。
4 水解法
水解法在一定程度上与直接沉淀法有些类似,其过程主要是让硫酸氧钛与水发生水解反应生成沉淀。硫酸氧钛本身是可以溶解在水中的,所以可以配制成硫酸氧钛水溶液,但在室温情况下溶解在水里的硫酸氧钛并不会与水发生水解反应,这时候在硫酸氧钛的存在形式主要是硫酸根离子和钛氧根离子。但是加热的情况下,钛氧根离子(TiO+)会结合水电离的氢氧根粒子形成沉淀。其水解方程式如下:
H2O → H++OH-
TiO++ 2 OH-→ TiO(OH)2
总:TiOSO4+2 H2O = TiO(OH)2↓+ H2SO4
该过程水解温度在50 ℃以上为宜,该水解过程是吸热反应,所以继续升高温度会加速沉淀的生成[33]。此外,在一些研究中对加入盐溶液以促进沉淀生成的硫酸氧钛的间接水解过程也被称为水解反应。从上述方程可以看出,依靠水的电离毕竟有限,且需要长时间的反应,所以向溶液中加入OH-往往会加速这一过程的进行[34]。Wahyuningsih等[35]利用硫酸氧钛水解法制备了二氧化钛粒子,并探究了溶液浓度酸碱度等对粒子粒度的影响,同时对粒子进行了一系列表征,并展现出了良好的性质。Zeng等[36]同样利用水解法研究了其制备过程,这是该团队更细致的通过表征测试等方法,研究了水解过程中粒子的晶体结构形态以及尺寸变化和原因解释等。
5 展望与建议
作为无机多功能材料的代表,二氧化钛的研究与应用得到了国内以及世界各国的重视,小到日常用品大到国防科技等领域都在逐渐出现它的身影,二氧化钛的应用更是成为了一个国家科技发展的标志。因此,对二氧化钛的制备研究是基础性要求,更高的是对二氧化钛的应用以及根据具体的应用来改进制备的过程,不同的制备方法得到的粒子形态结构包括性质都是有区别的,这在文首已经提及,重点关注其微观性能和纳米性能,这将是该材料发挥作用的重大突破点。

